深圳市卫健委特聘岗人才
南方医科大学医学博士
中国抗癌协会肿瘤分子医学委员会
肿瘤标志物专委会会员
广东省抗癌协会-会员
深圳市医学会肿瘤分会青年专委会-委员
致力于鼻咽癌、乳腺癌的临床诊疗及科研工作,参与3项国家自然科学基金面上项目,1项深圳市面上项目,参编专著3部。
ASCO 解读文献
ASCO摘要解读
Sequential chemoradiotherapy versus induction chemotherapy plus concurrent chemoradiotherapy for locoregionally advanced nasopharyngeal carcinoma: A multicenter, open-label, non-inferiority, randomised, phase 3 trial.
序贯放化疗对比诱导化疗联合同步放化疗治疗局部晚期鼻咽癌:一项多中心、开放标签、非劣效性、随机Ⅲ期临床试验。
研究背景
诱导化疗(IC)联合同步放化疗(CCRT)因良好的疾病控制率,一直被视为局部晚期鼻咽癌(LA-NPC)的标准治疗方案,远处转移仍是导致其治疗失败的主要原因。其中顺铂同步化疗的方案不仅患者耐受性差,且在预防疾病远处转移方面效果有限。鉴于目前的治疗手段中调强放疗(IMRT)可提升疾病局控率,放疗前/后的化疗可降低远处转移风险。那么,在局部晚期鼻咽癌治疗中,探索序贯放化疗(SCRT)能否作为IC+CCRT方案的替代模式则具有重要的理论依据和临床价值。
研究方法
本研究为一项开放标签、Ⅲ期、非劣效性临床试验,于2018年1月至2021年9月在中国6家中心开展。入组鼻咽癌患者年龄介于18-65岁,分期为T1-4、N2-3或T3-4、N0-1、M0。按1:1比例随机分配至:SCRT组:2周期GP方案诱导化疗(吉西他滨1000 mg/m² d1,8 + 顺铂25 mg/m² d1-3,q21d)+ IMRT,序贯2周期相同方案辅助化疗(AC);IC+CCRT组:2周期GP方案诱导化疗后,序贯IMRT联合每周同步顺铂化疗(30 mg/m²)。主要研究终点为3年无失败生存(FFS),非劣效界值设定为绝对差异10%(HR<1.6),次要终点为放疗期间发生≥3级急性黏膜炎事件。疗效与安全性分析分别基于意向治疗(ITT)人群和安全性人群。
研究结果
共420例患者随机分组(SCRT组210例,IC+CCRT组210例),中位随访47.0个月(IQR 35.0-57.8)。3年FFS:SCRT组84.0% vs. IC+CCRT组79.8%(log-rank 0.344),HR 0.804(95% CI 0.510-1.266),绝对差异4.2%(95% CI,−3.2%-11.6%),达到非劣效标准。其余数据中,3年总生存率(OS):97.4% vs. 94.5%(HR 0.413, 95% CI 0.159-1.076, P=0.061);3年局部区域控制率:91.7% vs. 88.8%(HR 0.767, 95% CI 0.420-1.401, P=0.386);3年远处转移无生存率(DMFS):93.6% vs. 91.5%(HR 0.756, 95% CI 0.376-1.520, P=0.430),两组间均无显著性差异。安全性:SCRT组因省略同步化疗,≥3级急性非血液学不良事件率(急性黏膜炎29.0% vs. 41.9%, P<0.001;恶心9.5% vs. 18.1%, P=0.011;呕吐3.8% vs. 9.5%, P=0.019)显著降低;但SCRT组因辅助化疗增加,≥3级血液学毒性(血小板减少、白细胞减少)发生率更高。
研究结论
对于局部晚期鼻咽癌,SCRT可作为IC+CCRT的替代方案,其在3年FFS方面不劣于IC+CCRT,且放疗期间严重非血液学毒性事件发生率更低,尤其适用于无法耐受同步化疗的患者。
解读
研究亮点与突破
(1)“去同步化疗”策略的里程碑意义:SCRT首次挑战IC+CCRT标准
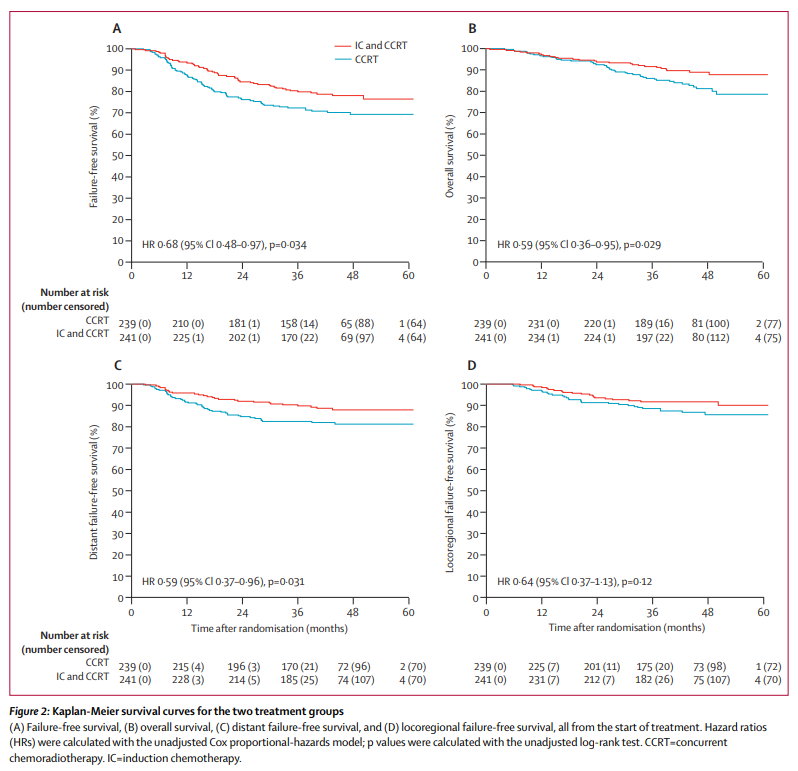
传统观点认为,放疗同步化疗是局部晚期鼻咽癌生存获益的基石。该研究首次通过Ⅲ期临床试验证实,序贯放化疗(SCRT)在3年无失败生存(FFS)方面不劣于标准治疗方案(IC+CCRT),绝对差异达4.2%(84.0% vs 79.8%),HR=0.804(95% CI:0.510-1.266),跨越非劣效界值(HR<1.6)。这一结果与既往(Sun Y等2016年的Ⅲ期试验(1))研究形成鲜明对比:后者显示TPF诱导+CCRT较CCRT单用显著提升FFS(HR 0.68)。本研究通过科学的试验设计和严谨的研究方法,证明了在不进行同步化疗的情况下,序贯放化疗同样能够取得不劣于传统方案的治疗效果,这为局部晚期鼻咽癌的治疗理念带来了新的变革,为未来的治疗策略优化提供了重要的参考和方向。
(2)毒性谱的“跷跷板效应”:血液学vs.非血液学毒性的权衡
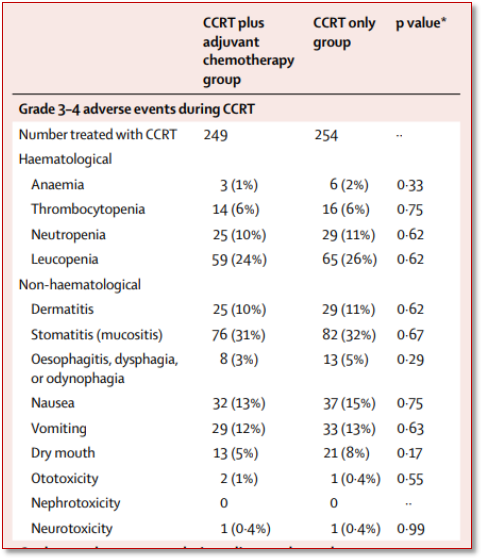
既往研究(如Chen L等2012年的CCRT+AC试验(2))揭示了顺铂同步化疗的急性黏膜炎风险:3-4级口腔黏膜炎发生率高达32%;顺铂肾毒性及消化道反应常导致患者治疗中断,超三分之一患者无法按计划完成足量化疗(3)。本研究结果提示:SCRT组因辅助化疗增加,≥3级血小板减少(18.1% vs. 9.5%)和白细胞减少(22.4% vs. 14.3%)发生率显著升高。而非血液学毒性(黏膜炎、恶心、呕吐)事件发生率显著降低,且降幅(12.9%~5.7%)远超血液学毒性事件的增幅(8.6%~8.1%)。SCRT通过“强化诱导+辅助化疗”替代同步化疗,在保证生存率的同时,将≥3级黏膜炎发生率从41.9%降至29.0%(P<0.001),为无法耐受同步化疗的患者提供了首个Ⅲ级证据支持的替代方案。受此启发,毒性评价及管理需从既往的“单一维度”转向未来“多维平衡”。对于老年、多发合并症、无法耐受同步化疗的患者,SCRT的可耐受性优势(非血液学毒性降低)可能抵消血液学毒性事件增加的不良影响(4),且血液学毒性事件可通过G-CSF等方案预防管理,为个体化治疗决策提供了新的依据。
(3)降低远处转移的“核心逻辑”:同步化疗的边际效应是否被高估
传统观点认为同步化疗通过放射增敏降低肿瘤远处转移率。但本研究显示:SCRT组3年无远处转移生存率(DMFS)达93.6%,高于IC+CCRT组的91.5%(HR=0.756);SCRT组3年总生存率(OS)为97.4% vs IC+CCRT组94.5%(P=0.061)。提示省略同步化疗并未导致远处转移率提高,推测其原因:当诱导化疗(如GP或TPF)达到足够的治疗强度,或者随着单纯放疗局控率的进一步提高,同步化疗对控制远处转移的贡献可能被逐渐稀释。
研究局限性
(1)随访时间有限,长期疗效待验证
中位随访时间47个月,相较于鼻咽癌复发高峰期(3-5年)仍稍显不足,延长随访至5年以上以评估SCRT对远期生存的影响将更具价值。
(2)人群覆盖偏差,高危亚组证据缺失
该研究排除T4或N3期超高危患者(仅纳入T1-4 N2-3或T3-4 N0-1),而此类患者恰是远处转移风险最高群体(转移率>30%)。
(3)机制探索不足,未解析免疫微环境影响
放疗同步顺铂化疗可能通过释放肿瘤抗原增强抗肿瘤免疫,研究未评估SCRT方案是否可能削弱此效应,亦未分析PD-L1表达或肿瘤浸润淋巴细胞等免疫指标与预后间的相关性。
总结
本研究为局部晚期鼻咽癌的个体化治疗开辟了新路径,尤其为老年、体弱或同步化疗禁忌的患者提供了首个Ⅲ级证据支持的“去同步化疗”的标准方案,同时提出了新的观点:
(1)同步化疗并非局部晚期鼻咽癌生存获益的唯一通路:诱导/辅助化疗可替代;
(2)毒性管理需多维度综合评估:血液学毒性可预防管理,非血液学毒性更影响患者的治疗完成度及生活质量;
(3)控制远处转移的核心因素再评价:诱导化疗强度及同步化疗孰轻孰重。
未来研究方向展望:
(1)优化诱导/辅助方案(如联合免疫治疗)
近年多项研究探索免疫治疗在鼻咽癌中的价值,形成对传统化疗方案的挑战或补充:如DIAMOND研究(马骏院士,2025 ASCO)(5):采用特瑞普利单抗全程治疗并省略同步顺铂化疗,3年FFS率达88.3%,且≥3级呕吐发生率从59.8%降至26.2%(P<0.001),实现“减毒不减效”。
(2)探索生物标志物(如EBV-DNA动态监测)指导的精准治疗策略:寻找SCRT最佳获益者探索生物标志物导向的治疗方案制定:包括EBV DNA动态监测、PD-L1表达水平(如CPS评分)、肿瘤突变负荷(TMB)等。
李先明教授 深圳市人民医院
该研究为一项多中心、开放标签、非劣效性、随机Ⅲ期临床试验,旨在探索序贯放化疗(SCRT)能否替代诱导化疗联合同步放化疗(IC+CCRT)这一局部晚期鼻咽癌经典治疗方案。唐子博博士的解读从不同治疗模式的疗效对比、毒性权衡、远处转移控制率等多个维度进行了深入探讨,精准挖掘出该研究的亮点与价值,同时,还对研究存在的局限性以及未来发展方向做了准确的总结及合理的推测。唐子博博士的解读内容全面、逻辑清晰、论据充分、观点鲜明,充分体现了他对本专业领域的深刻理解与思考,为读者带来了一定的启发。
【温馨提示】:如果您觉得唐子博医生解读的好,请在下方为他点赞并将文章分享给更多的同道!当然,您也可以在下方留下您的个人见解哦!
1.Sun Y, Li WF, Chen NY, Zhang N, Hu GQ, Xie FY, et al. Induction chemotherapy plus concurrent chemoradiotherapy versus concurrent chemoradiotherapy alone in locoregionally advanced nasopharyngeal carcinoma: a phase 3, multicentre, randomised controlled trial. The Lancet Oncology. 2016;17(11):1509-20.
2. Chen L, Hu CS, Chen XZ, Hu GQ, Cheng ZB, Sun Y, et al. Concurrent chemoradiotherapy plus adjuvant chemotherapy versus concurrent chemoradiotherapy alone in patients with locoregionally advanced nasopharyngeal carcinoma: a phase 3 multicentre randomised controlled trial. The Lancet Oncology. 2012;13(2):163-71.
3. Wang C, Wang F, Min X, Zhang Q, Shen LJ, Jiang Y, et al. Toxicities of chemoradiotherapy and radiotherapy in nasopharyngeal carcinoma: an updated meta-analysis. The Journal of international medical research. 2019;47(7):2832-47.
4. 刘晓梅, 李智慧, 蒋朝阳, 周代君, 钱小梅, 李东. 诱导化疗治疗≥60岁老年局部晚期鼻咽癌患者的疗效:一项单中心回顾性研究 %J 肿瘤预防与治疗 %J Journal of Cancer Control and Treatment. 2024;37(10):853-64.
5. Xu C, Zhou GQ, Li WF, Hu DS, Chen XZ, Lin SJ, et al. Nivolumab combined with induction chemotherapy and radiotherapy in nasopharyngeal carcinoma: A multicenter phase 2 PLATINUM trial. Cancer cell. 2025;43(5):925-36.e4.











 苏公网安备32059002004080号
苏公网安备32059002004080号


