山东省青年医务工作者协会乳腺肿瘤多学科诊疗分会委员
山东省抗癌协会肿瘤靶向治疗分会委员
主持项目:山东省自然科学基金(青年项目):2025.01-2027.12,线粒体动力学及线粒体自噬促进三阴性乳腺癌新辅助化疗联合免疫治疗耐药的机制及调控增敏可能性的研究,主持,在研。
发表多篇论文专著
ASCO 解读文献
Abstract 编号:515
达尔西利联合内分泌治疗辅助治疗HR+/HER2 -早期乳腺癌:随机,III期,DAWNA-A研究
Dalpiciclib (Dalp) plus endocrine therapy (ET) as adjuvant treatment for HR+/HER2– early breast cancer (BC): The randomized, phase 3, DAWNA-A trial.
研究背景
CDK4/6抑制剂联合内分泌治疗(ET)作为晚期HR+HER2-乳腺癌一线标准治疗方案已经广泛普及,然而这一方案对于局部晚期或早期乳腺癌患者的疗效证据仍在不断的探索中。达尔西利(Dalp)是一种强效 CDK4/6 抑制剂,已证实联合内分泌治疗(ET)用于 HR+/HER2- 晚期乳腺癌(BC)可显著改善无疾病进展生存期(PFS)。因此为了进一步证明Dalp联合ET在局部晚期或早期乳腺癌中的疗效,我们设计了一项针对早期高复发风险的HR+/HER2-乳腺癌的三期双盲临床试验,并在此发表首次临时分析的结果。
研究方法
DAWNA-A是一项双盲、安慰剂对照的三期临床实验。本研究纳入了年龄18至75岁,II-III期、HR+/HER2- BC女性患者,这些患者已完成局部治疗,并经病理学证实同侧腋窝淋巴结受累。患者按1:1的比例随机分配接受口服达尔西利(Dalp,125 mg,每日一次;服药3周/停药1周,疗程2年)+ ET(来曲唑2.5 mg/阿那曲唑1 mg/他莫昔芬10 mg/托瑞米芬60 mg,每日一次,疗程5年)或安慰剂+ ET。绝经前/围绝经期患者接受LHRH激动剂治疗(围绝经期用药由研究者决定)。实验的分层因素包括绝经状态(绝经前/绝经期 vs 绝经后)、临床分期(II vs III)、受累淋巴结数量(<4 vs ≥4)以及辅助化疗(是 vs 否)。主要终点是无浸润性疾病生存期 (iDFS),次要重点为无病生存期(DFS)、无缘出疾病生存期(DDFS)等,实验设计如下图: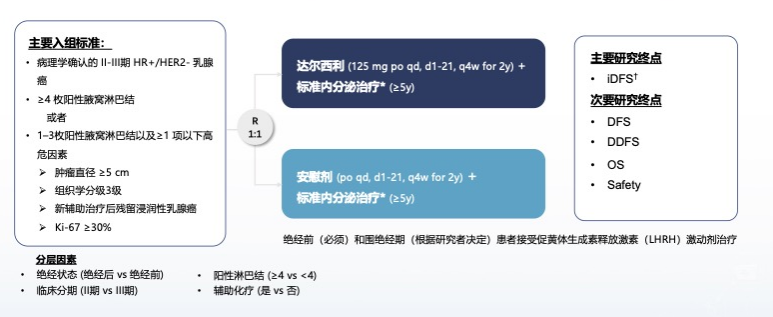
研究结果
2021 年 4 月 30 日至 2024 年 7 月 19 日期间,5274 名患者被随机分配为两组(Dalp,n=2640;安慰剂,n=2634)。截至数据截止,中位随访时间为 20.3 个月(范围 0.0-41.9)。与安慰剂 + ET 相比,Dalp + ET 显着延长了 iDFS(HR 0.56,95% CI 0.43-0.71;p <0.0001);Dalp 的 iDFS 获益在分层因素和其他基线亚组中基本一致。DFS 和远处 DFS (DDFS) 也优于安慰剂 + ET。TRAE 导致 Dalp 组 2.1% 的治疗患者停用 Dalp,安慰剂组 0.8% 的治疗患者停用安慰剂。 Tr-SAE 发生率分别为 3.7% 和 1.5%。无 TRAE 导致的死亡病例。
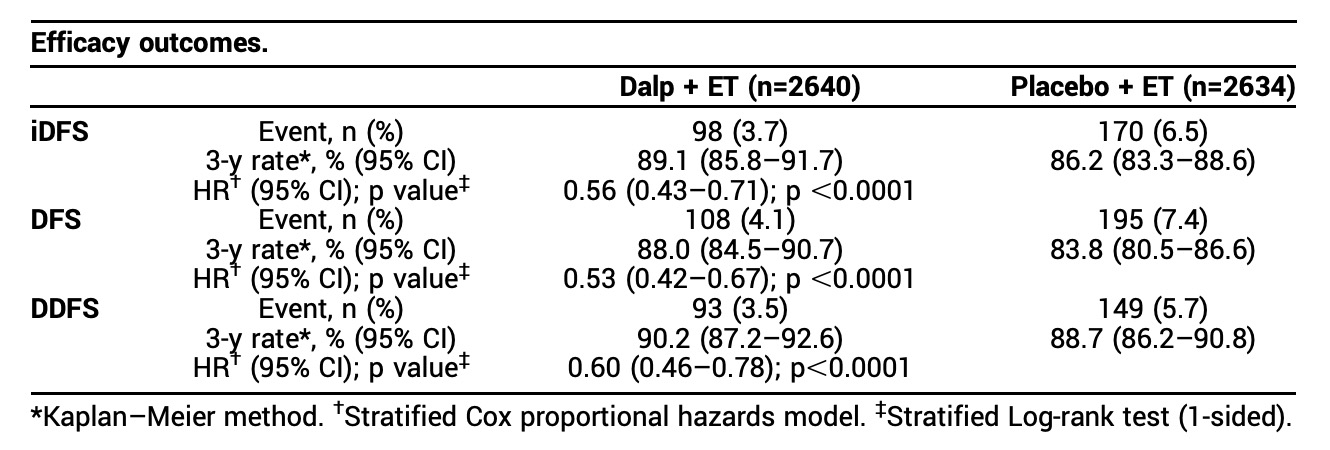
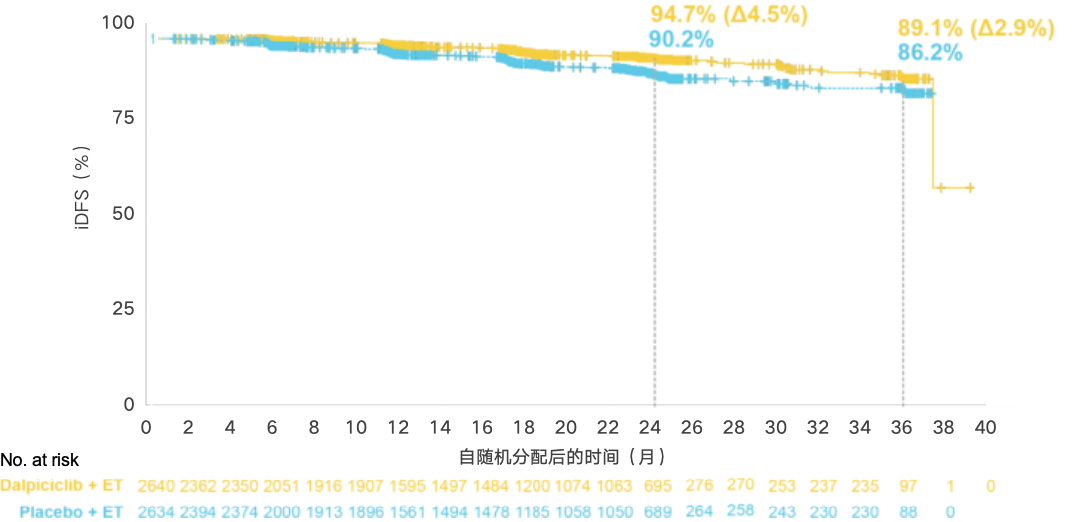
研究结论
在首次中期分析中,III期DAWNA-A研究达到主要终点:与安慰剂+内分泌治疗(ET)相比,达尔西利+ET显著改善iDFS,安全性可控。
解读
HR+/HER2–早期乳腺癌的的风险与机遇
乳腺癌已成为全球女性发病率最高的癌症,其中HR+/HER2–乳腺癌是最常见的乳腺癌亚型,约占70%[1]。如何实现避免复发,实现治愈并保证良好的生活治疗,是早期乳腺癌追求的目标。然而在中国早期乳腺癌中II至III期比例高,且发病年龄高于其他国家地区[1]。有研究通过二十年的随访证实,HR+/HER2–乳腺癌,无论分期如何,20年的复发风险可持续存在,并随着淋巴结的分期程度,风险持续增加[2]。因此在如此庞大的发病基数、较早的发病年龄与长期的复发风险并存的情况下,除了适量的化疗、放疗及基础的内分泌治疗之外,如何降低患者短期及长期复发风险需要进一步探索。
内分泌治疗是HR+/HER2–乳腺癌的重要基石,从选择性雌激素受体调节剂(SERMs)开始到芳香化酶抑制剂(AI),内分泌治疗贯彻了HR+/HER2–早期乳腺癌治疗的半个世纪,联合手术、化疗、放疗一直是近20年来HR+/HER2–早期乳腺癌的主要治疗历程。然而对于完善治疗的接受ET治疗5年的早期乳腺癌患者,初诊II期及III期的10年乳腺癌复发率仍可高达24%及41%[3]。为了进一步提高患者的生存质量降低复发风险,国内外针对如何精准瞄控高复发风险人群进行内分泌治疗的延长及辅助强化进行了多方位的探索。2023年ST Gallen国际乳腺癌会议对于复发风险因素的定义达成了共识,结合国内外共识及Monarch E、NATALEE等研究,国内指南提出了高、中、低复发风险的患者分层,2025年NCCN乳腺癌指南提出高复发风险条件包括:所有淋巴结阳性;N0且T3-4;N0且T2,但合并高位复发因素(G3,或G2伴Ki-67≥20%,或G2伴基因组高风险)。各大指南均对高、中复发风险的人群增加了CDK4/6i的治疗推荐。
DAWNA-A的解读与对比
CDK4/6i作为针对HR+/HER2–乳腺癌的靶向药物,它的加入一定程度改变了内分泌治疗的格局,它通过阻断肿瘤细胞G1至Sqi2从而使其无法增殖,联合内分泌治疗的雌孕激素的获取受阻达到抗肿瘤的目的[4]。CDK4/6i+ET的晚期一线治疗临床研究已发现CDK4/6i与AI或氟维司群联合治疗均有显著的生存获益。然而对于早期乳腺癌来说,PENELOPE-B及PALLAS均未得到派柏西利有效的得力证据。monarchE入组了II-III期的高危患者(≥4个淋巴结阳性;1-3个淋巴结阳性伴T≥5cm, G3, Ki67≥20%)。NATALEE的入组条件较为宽泛,为广泛的II-III期,不论淋巴结状态如何,对于IIA期T2N0疾病标准为(2级且Ki-67≥20%或高基因组风险;3级),并将用药时间延长至了3年,证明了N0及N1的患者有相似的复发风险,并将N0人群的复发风险降低了33.4%[5]。
DAWNA-A的研究入组标准与MonarchE较为相似,增加了进行新辅助治疗后完成手术的患者人群,聚焦于新辅助治疗不敏感的患者。同时将药物使用剂量减至125mg,保证在缺少肿瘤负荷的条件下保持疗效并提高患者的耐受性。与众不同的是,DAWNA-A的入组标准将Ki67 提升至30%, 2024年中国抗癌协会乳腺癌诊治指南与规范提示可采用20%~30%作为判断Ki-67增殖指数高低的界值[6]。近期研究均证明了30%的cut-off值具有更高的敏感度,有助于此项研究结果的可比性及一致性[7]。实验计划入组5220例患者,入组100%中国人群,相比MonarchE与NATALEE,入组了跟多绝经前与围绝经期、N2及以上的患者,更符合中国国情。2年中期分析获得了IDFS 4.5%的绝对获益(HR=0.56, 95% CI 0.43–0.71, p<0.0001),各分层结果基本一致,DFS与DDFS的2年绝对改善为5.2%(HR= 0.53, 95% CI 0.42–0.67, p<0.0001) 及3.8%( HR= 0.60, 95% CI 0.46–0.78, p<0.0001)。Dalp的主要药物不良事件为血液学毒性,相对可控,对肝脏的毒性相对其他CDK4/6i较小。
作为仅入组中国患者的临床试验,针对中国国情及患者病情特点,药物研发及临床试验的结果具有绝对的优势及目标性。中期实验结果也表现出较好的效果和可控的安全性。但与已经完成的MonarchE与NATALEE的实验相比也存在一些可以思考的地方,NATALEE更宽泛的入组要求为更多患者的辅助强化治疗选择提供了理论依据,并针对部分临床中风险未行化疗的人群提供了辅助强化内分泌治疗的选择。MonarchE作为最早开始并获得可靠结果的临床试验,并最早获批早期高危乳腺癌的适应症,DAWNA-A在一定程度上学习了入组经验并根据中国国情及国际最新研究结果进行了改变。尤其是增加了进行新辅助治疗的患者,不仅仅是新辅助化疗的患者,部分行新辅助内分泌治疗的患者术后的Dalp的辅助强化的增加了我们为患者的远期生存获益的效果的期待。初步结果已经展露了头角,但尚不够充分,比如,实验初始入组是进行了分层,各亚组的结果并未完全展现;排除了N0的患者包括T3N0及T4N0这部分高复发风险的患者,与实际临床辅助强化用药目的存在偏离等。
总结
总之,作为继Monarch E及NATALEE后拥有阳性结果的的针对早期乳腺癌辅助强化治疗的CDK4/6i,将会为未来国内患者用药提供了新选择,期待后续更全面的研究结果。同时通过对三个临床实验的对比,各种药物不同的入组要求及分层因素也决定了未来临床工作中对于患者类群的选择,我们需要更多的考量因素。
【温馨提示】:如果您觉得王月辰医生解读的好,请在下方为她点赞并将文章分享给更多的同道!当然,您也可以在下方留下您的个人见解哦!
[1]LI J, ZHOU J, WANG H, et al. Trends in Disparities and Transitions of Treatment in Patients With Early Breast Cancer in China and the US, 2011 to 2021 [J]. JAMA Network Open, 2023, 6(6): e2321388-e.
[2] PAN H, GRAY R, BRAYBROOKE J, et al. 20-Year Risks of Breast-Cancer Recurrence after Stopping Endocrine Therapy at 5 Years [J]. New England Journal of Medicine, 2017, 377(19): 1836-46.
[3] LANDIN J A V, MARCUS. The {San} {Antonio} {Breast} {Cancer} {Conference} 2022: An {Overview} [J]. healthbook TIMES Oncology Hematology, 2023, 15: 80—3.
[4] PORTMAN N, ALEXANDROU S, CARSON E, et al. Overcoming CDK4/6 inhibitor resistance in ER-positive breast cancer [J]. Endocrine-Related Cancer, 2019, 26(1): R15-R30.
[5] FASCHING P A, STROYAKOVSKIY D, YARDLEY D, et al. LBA13 Adjuvant ribociclib (RIB) plus nonsteroidal aromatase inhibitor (NSAI) in patients (Pts) with HR+/HER2− early breast cancer (EBC): 4-year outcomes from the NATALEE trial [J]. Annals of Oncology, 2024, 35: S1207.
[6] 中国抗癌协会乳腺癌专业委员会 中. 中国抗癌协会乳腺癌诊治指南与规范(2024年版) [J]. 中国癌症杂志, 2023, 33.
[7] WONGMANEERUNG P, CHITAPANARUX I, TRAISATHIT P, et al. The association between Ki-67 expression and survival in breast cancer subtypes: a cross-sectional study of Ki-67 cut-point in northern Thailand [J]. BMC Cancer, 2025, 25(1): 346.











 苏公网安备32059002004080号
苏公网安备32059002004080号


