肺外神经内分泌癌(epNEC)是一类罕见的、发生在肺外的高级别、分化差的神经内分泌肿瘤,最常见于消化道[1],异质性高。患者确诊时往往已处于晚期,铂类为基础的化疗通常是这些患者的一线治疗选择,平均生存不到12个月[2-5]。目前,epNEC面临巨大的未满足治疗需求,生存状况亟待改善。
在2025年美国临床肿瘤学会(ASCO)年会上,评估靶向DLL3的IgG样T细胞衔接器(TcE)obrixtamig的首项人体试验更新了其在epNEC患者中的研究数据。此次更新基于DLL3表达情况,对疗效及安全性结果进行了分析,并以口头报告的形式重磅发布。研究发现,DLL3高表达epNEC患者确认的客观缓解率(ORR)达40%,疾病控制率(DCR)达67%,中位缓解持续时间(DoR)达7.9个月[6]。Obrixtamig为epNEC患者带来新的治疗希望。本文特邀山东大学齐鲁医院郝静教授深度解析epNEC治疗困境,深入探讨obrixtamig治疗epNEC的应用价值和前景,以飨读者。
专家介绍
郝静 教授
医学博士
山东大学齐鲁医院肿瘤内科主任医师 副主任
丹麦奥胡斯大学临床实验肿瘤学系访问学者
加拿大安大略省癌症研究院访问学者
中国抗癌协会神经内分泌肿瘤专委会常委
中国医疗保健国际交流促进会神经内分泌肿瘤分会副主任委员
CSCO 胰腺癌专委会委员
CSCO 神经内分泌肿瘤专委会委员
山东省医师协会神经内分泌肿瘤专委会 主任委员
山东生物医学工程少见肿瘤转化医学专委会主任委员
山东省研究型医院协会肺癌转化医学专委会副主任委员
山东抗癌协会女医师分会副主任委员
山东省罕见疾病防治协会少见肿瘤分会副主任委员
山东省公共卫生协会消化道肿瘤防治委员会副主任委员
山东省抗癌协会肺癌专业委员会常委
险象环生,epNEC患者存在巨大未满足治疗需求
神经内分泌肿瘤(NEN)是一类起源于肽能神经元和神经内分泌细胞,具有神经内分泌分化并表达神经内分泌标记物的少见肿瘤[7]。根据肿瘤分化程度,NEN可分为分化良好生长缓慢的神经内分泌瘤(NET)和分化差恶性程度高的神经内分泌癌(NEC)[7]。NEC是NEN中最具侵袭性的亚型[2],可发生于多种器官,约91%原发于肺部,epNEC在整体NEC中占比约9%[1],可以说是“罕见中的罕见”。SEER数据库分析显示,epNEC最常见于胃肠胰(GEP),约占37.4%,泌尿生殖系统(GU)约占17%,妇科系统(GY)约占10%,未知原发部位(CUP)约占28.2%[1,8]。
在治疗策略方面,epNEC的一线标准治疗以铂类为基础的化疗为主,如EP/EC、IP方案[9]等。而二线及后线治疗尚缺乏标准治疗方案,临床上仍以化疗为主,如白蛋白结合紫杉醇、伊立替康脂质体等,客观缓解率(ORR)约0~25%[10],中位总生存期(OS)不足1年[11]。除dMMR/MSI-H患者外,免疫检查点抑制剂疗效有限[12],且缺乏疗效预测标记物。因此,如何突破epNEC的治疗瓶颈是亟待解决的临床难题。
突破桎梏,Obrixtamig单药治疗epNEC初显成效
Notch 通路是一种高度保守的细胞信号通路,与恶性转化、细胞增殖、细胞周期停滞和凋亡、上皮间质转化以及神经内分泌分化抑制有关。Delta样配体 3 (DLL3) 是Notch受体的抑制性配体,通过抑制Notch信号传导,参与NEC的发生和发展,在多种具有神经内分泌特征的肿瘤中特异性表达[13-15]。大约80%的epNEC肿瘤细胞表面表达DLL3,其中胃肠胰NEC、宫颈NEC以及小细胞膀胱癌的DLL3表达率分别达76.9%、81%以及68%[13-15]。然而,DLL3在健康成人组织细胞表面几乎没有表达[13,15]。基于DLL3在epNEC中的特异性表达及临床关联性,其成为了epNEC治疗的潜在靶点。
近年来,靶向DLL3的TcE成为NEC领域内的研发热点,其中obrixtamig是首个公布epNEC临床研究数据的DLL3 TcE类药物,其可通过同时靶向肿瘤细胞表面的DLL3和T细胞表面的CD3分子,介导细胞毒性T细胞对DLL3表达阳性肿瘤的精准杀伤[16]。
1438.1研究(NCT04429087)是一项正在进行的I期、首次人体、开放标签、剂量递增临床试验,研究obrixtamig单药用于二线或后线治疗DLL3表达阳性的局部晚期/转移性肺内和肺外NEC[6,16,17]。在2024年欧洲神经内分泌肿瘤学会(ENETS)大会上,该试验更新了其在epNEC患者中的研究结果,截至2023年11月17日,在剂量水平≥90μg/kg时,53例epNEC患者接受obrixtamig治疗的整体ORR为26%,疾病控制率(DCR)为45%。不同部位的epNEC均展现出较好疗效,obrixtamig在胃肠道NEC(GI-NEC)、GU-NEC、以及未知原发部位的NEC的ORR分别为22%、40%、以及17%[17]。安全性方面,obrixtamig在临床有效剂量水平下,安全性是可接受和可控的。细胞因子释放综合征(CRS)绝大多数为1~2级,发生在初次给药期间,并可通过标准支持治疗进行管理[17]。此项研究结果的发布为obrixtamig在epNEC中的后续探索带来了信心,表明obrixtamig有潜力成为epNEC患者的一种有效治疗选择。
粲然可观,Obrixtamig单药治疗epNEC最新数据亮相2025 ASCO
今年的ASCO大会进一步报告了obrixtamig单药用于epNEC二线及以后治疗的最新数据,本次分析评估了obrixtamig在DLL3高表达与低表达的epNEC患者中的疗效和安全性[6]。
研究方法
Obrixtamig采用4种剂量递增方案(R)静脉注射给药:RA(固定剂量,每三周一次);RB1(固定剂量,每周一次);RB2(阶梯给药,随后每周一次)和RB3(阶梯给药,随后每周一次,持续3周,随后每三周一次),直至病情进展或出现不可接受的毒性。疗效评估采用RECIST v1.1标准,通过ORR和DCR进行评估。会议报告了RB2或RB3两组接受obrixtamig治疗的患者结果(图1),根据DLL3表达水平分为DLL3高表达组和DLL3低表达组,其中DLL3高表达组阈值定义为使用实验性DLL3抗体(SP347,罗氏诊断)染色呈中等至强阳性的肿瘤细胞比例≥50%(图2)[6]。
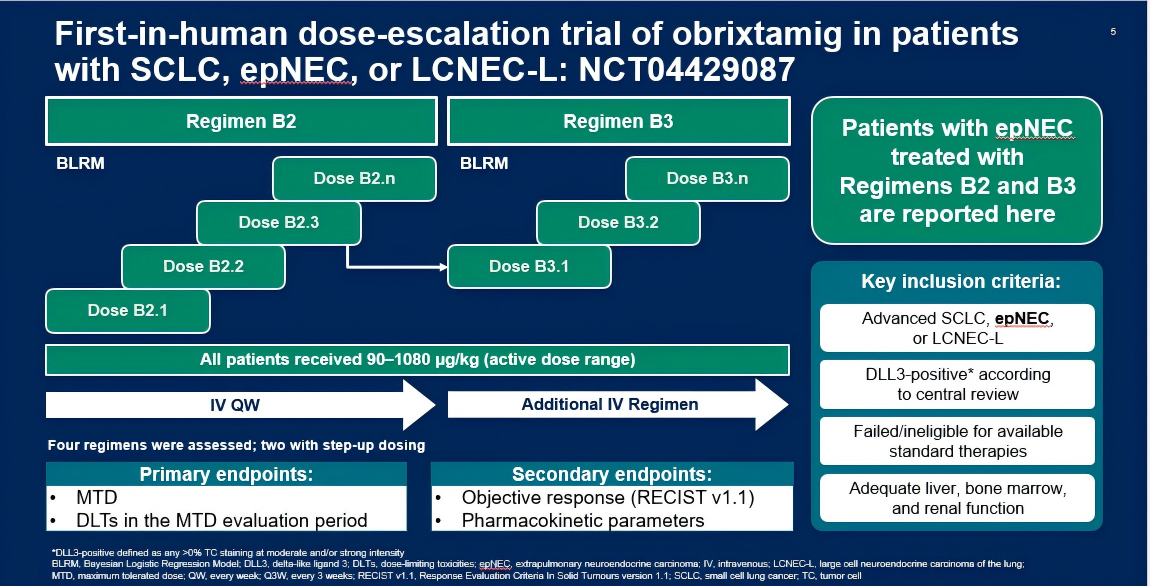
图1. 研究设计
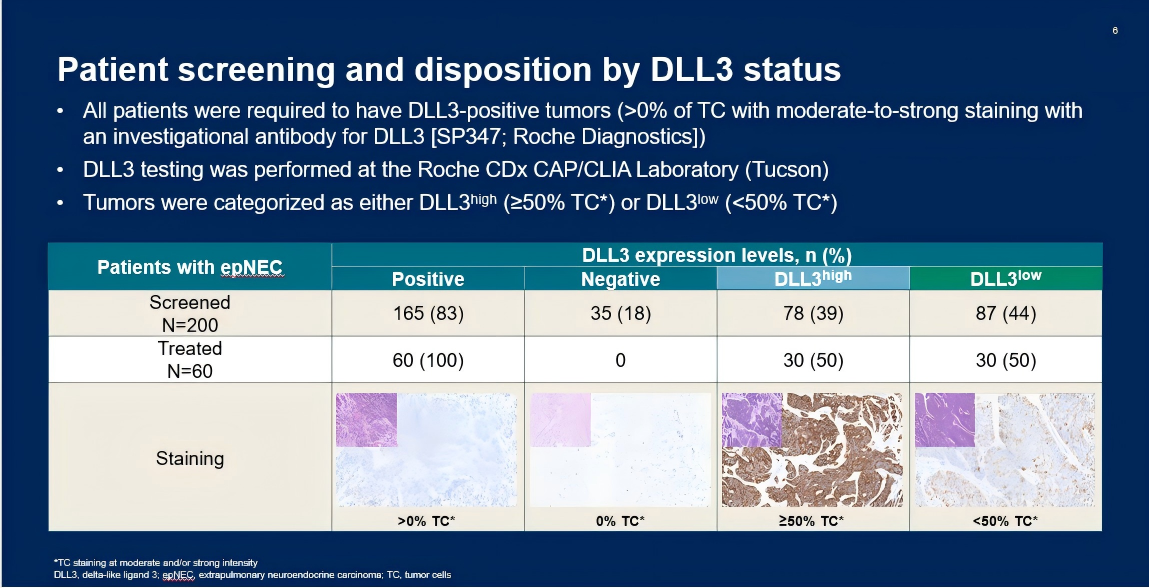
图2. 根据 DLL3 表达水平进行患者筛查和处置
研究结果
截至2024年6月21日,共纳入60例epNEC患者(GI:53.3%,GU:33.3%,其他/未知原发部位:13.3%);DLL3高表达组和DLL3低表达组各30例。所有患者均接受过既往全身治疗;30%的DLL3高表达患者和50%的DLL3低表达患者接受过二线以上治疗[6]。
研究结果显示,接受obrixtamig治疗后,DLL3高表达组的ORR、DCR和DoR均高于DLL3低表达组,其中DLL3高表达组确认的ORR可达40%,DCR达67%,中位DoR达7.9个月(图3、图4)。且无论epNEC原发肿瘤部位如何,DLL3高表达患者的缓解率均令人鼓舞,其中DLL3高表达的GI和GU NEC患者确认的ORR分别为43%和50%[6]。
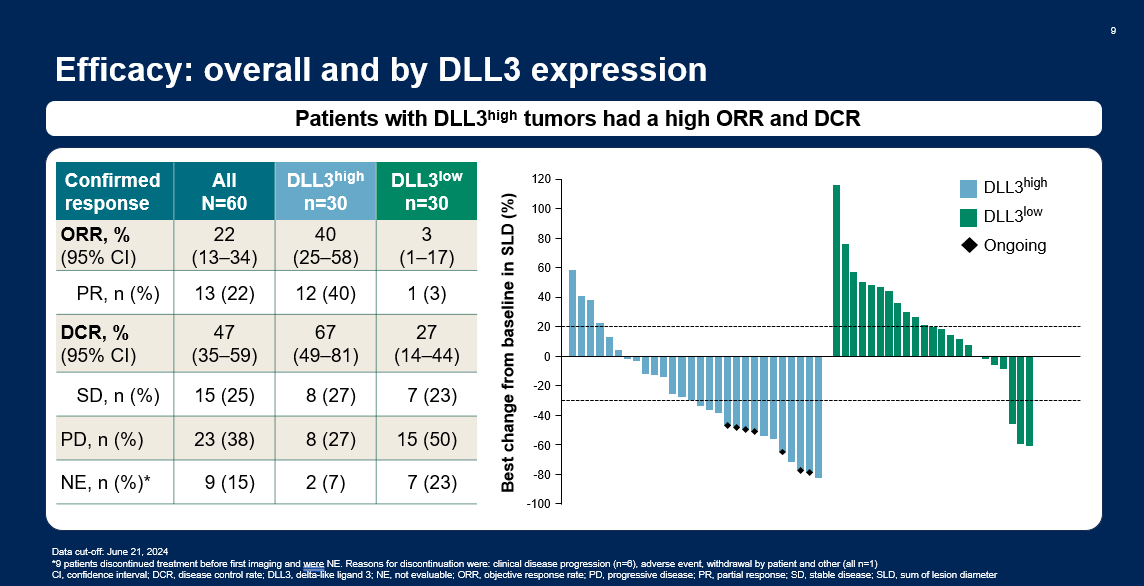
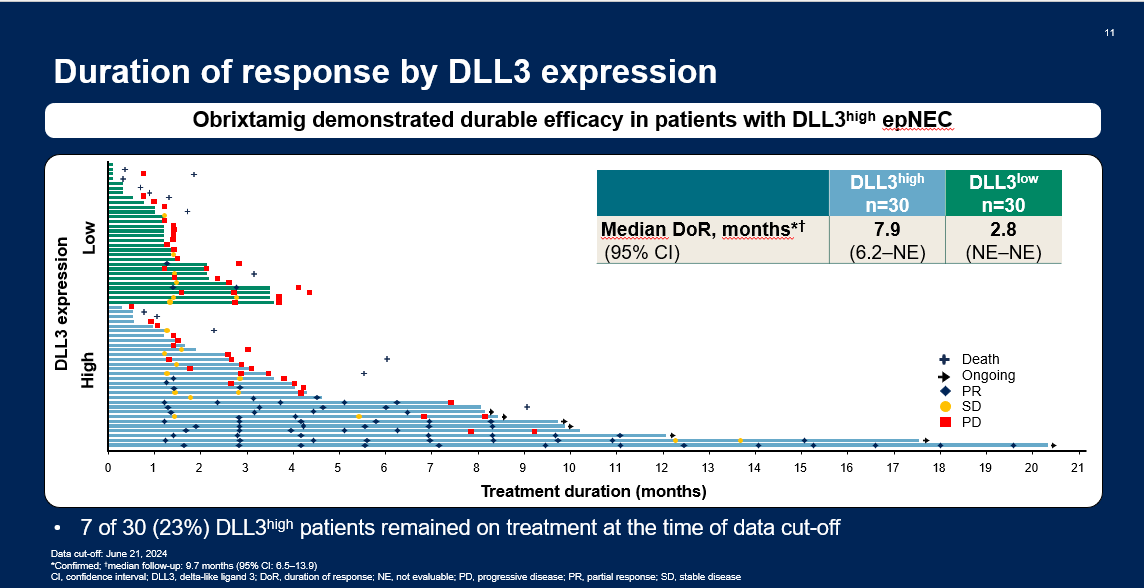
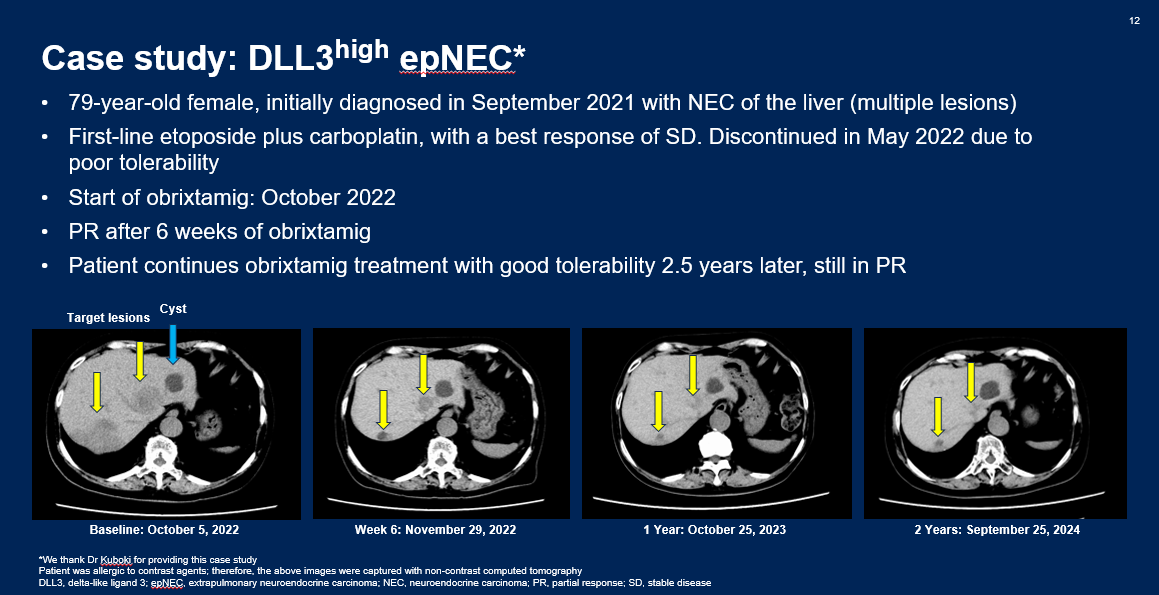
在本次数据更新中,研究者还公布了一例obrixtamig治疗DLL3高表达肝脏NEC病例。该高龄女性患者因难以耐受依托泊苷+卡铂一线治疗而停药,后接受obrixtamig二线治疗。用药6周后,患者即达到了肿瘤部分缓解(PR),且持续治疗并保持PR达2.5年,耐受性良好(图5)[6]。
在安全性方面,obrixtamig治疗的整体安全性可控。所有epNEC患者治疗相关不良事件(TRAE)发生率为95%,其中大多为1-2级,≥3级TRAE发生率仅为22%。CRS发生率(总体/≥3级)为65%/3%,潜在神经系统不良事件(包括免疫效应细胞相关神经毒性综合征,ICANS)的发生率(总体/≥3级)为13%/5%。DLL3高表达组与DLL3低表达组安全性特征相似[6]。
综上,迄今为止,这项研究报告了靶向DLL3的TcE药物在epNEC患者中最大规模的前瞻性数据集,obrixtamig在所有epNEC患者中显示出可控的安全性。对于DLL3高表达的经多线治疗的epNEC患者,obrixtamig单药治疗显示出令人鼓舞和持久的反应,ORR可达40.0%,中位DoR达7.9个月,支持其在该亚组中的进一步开发[6]。一项正在进行的II期试验(DAREON-5)正在评估obrixtamig对复发/难治性DLL3高表达epNEC患者的治疗效果,研究结果值得期待。
结语
epNEC作为一种罕见的高侵袭性异质性恶性肿瘤,目前的治疗选择非常有限,生存状态亟待改善。DLL3靶点的发现和初步探索成果无疑为epNEC患者带来了新的希望。Obrixtamig作为首个公布epNEC临床研究数据的DLL3 TcE药物,在本次ASCO大会中公布的obrixtamig单药用于DLL3高表达epNEC二线及以后治疗的研究成果振奋人心,提示DLL3靶点可能具有潜在疗效预测功能,也预示着obrixtamig有望成为未来epNEC二线及以后治疗的新选择。相信随着研究的不断深入,obrixtamig的临床价值能够得到更为充分的验证,为epNEC患者带来更精准且有效的治疗选择,开启epNEC治疗新篇章。
1. Dasari Arvind, et al. Comparative study of lung and extrapulmonary poorly differentiated neuroendocrine carcinomas: A SEER database analysis of 162,983 cases .Cancer, 2018, 124: 807-815.
2. Frizziero M, et al. Is the Morphological Subtype of Extra-Pulmonary Neuroendocrine Carcinoma Clinically Relevant? Cancers (Basel). 2021 Aug 18;13(16):4152.
3. Volante M, et al. Extrapulmonary neuroendocrine small and large cell carcinomas: a review of controversial diagnostic and therapeutic issues. Hum Pathol. 2014 Apr;45(4):665-73.
4. European Neuroendocrine Tumor Society (ENETS) 2023 guidance paper for digestive neuroendocrine carcinoma. J Neuroendocrinol. 2023 Mar;35(3): e13249.
5. NCCN. Neuroendocrine and Adrenal Tumors. 2025 version 2.
6. Jaume Capdevila, et al. Efficacy and safety of the DLL3/CD3 T-cell engager obrixtamig in patients with extrapulmonary neuroendocrine carcinomas with high or low DLL3 expression: Results from an ongoing phase I trial. 2025 ASCO abstract #3004.
7. 中国抗癌协会神经内分泌肿瘤专业委员会, 等. 中国抗癌协会神经内分泌肿瘤诊治指南(2025年版) CHINA ONCOLOGY 2025 Vol.35 No.1.
8. Stumpo S, et al. Extrapulmonary Neuroendocrine Carcinomas: Current Management and Future Perspectives. J Clin Med. 2023 Dec 15;12(24):7715.
9. 中国临床肿瘤学会(CSCO). 神经内分泌肿瘤诊疗指南2024版.
10. Weaver JMJ, et al. Selection of Chemotherapy in Advanced Poorly Differentiated Extra-Pulmonary Neuroendocrine Carcinoma. Cancers (Basel). 2023;15(20):4951.
11. McGarrah PW, et al. Efficacy of Second-Line Chemotherapy in Extrapulmonary Neuroendocrine Carcinoma. Pancreas. 2020;49(4):529-533.
12. Bongiovanni A, et al. Activity and Safety of Immune Checkpoint Inhibitors in Neuroendocrine Neoplasms: A Systematic Review and Meta-Analysis. Pharmaceuticals (Basel). 2021 May 17;14(5):476.
13. Yao J, et al. DLL3 as an Emerging Target for the Treatment of Neuroendocrine Neoplasms. Oncologist. 2022 Nov 3;27(11):940-951.
14. Liverani Chiara, et al. Diagnostic and Predictive Role of DLL3 Expression in Gastroenteropancreatic Neuroendocrine Neoplasms .Endocr Pathol, 2021, 32: 309-317.
15. Peddio A, et al. DLL3 as a potential diagnostic and therapeutic target in neuroendocrine neoplasms: A narrative review. Crit Rev Oncol Hematol. 2024 Dec;204:104524.
16. Wermke M, et al. Phase I trial of the DLL3/CD3 bispecific T-cell engager BI 764532 in DLL3-positive small-cell lung cancer and neuroendocrine carcinomas. Future Oncol. 2022 Aug;18(24):2639-2649.
17. Jaume Capdevila, et al. Updated data from a Phase I trial of the DLL3/CD3 IgG-like T-cell engager BI 764532 in patients with DLL3-positive tumours: focus on extrapulmonary neuroendocrine carcinomas. 2024 ENETS abstract #28781.
审批号:SC-CN-16887,有效期至:6/16/2026
排版编辑:肿瘤资讯-Delia











 苏公网安备32059002004080号
苏公网安备32059002004080号


