胰腺癌领域不断突破,共护胰腺癌患者生存希望。
胰腺癌具有“三高三低”的特点,即发病率高、复发转移率高、死亡率高,早期诊断率低、治疗有效率低、5年生存率低,是公认的“癌中之王”,一直以来是恶性肿瘤领域亟待突破的治疗难题。近年来,多项胰腺癌相关研究不断突破,为胰腺癌患者带来生存新希望。正值“世界癌症日”到来之际,本文特别邀请了中山大学附属第一医院副院长、胆胰外科学科带头人殷晓煜教授就胰腺癌领域相关治疗进展进行盘点,同时,从临床实际治疗角度出发,为广大胰腺癌患者树立抗癌信心。
困难重重,胰腺癌患者生存预后亟待改善
殷晓煜教授就胰腺癌疾病特点和目前诊疗现状进行了阐述:“近年来,胰腺癌的发病率在国内外均呈明显的上升趋势。中国国家癌症中心2021年统计数据显示,胰腺癌位居我国男性恶性肿瘤发病率的第7位,女性第11位,占恶性肿瘤相关死亡率的第6位[1]。胰腺癌恶性程度高,它起病隐匿、进展快,80%~85%的胰腺癌患者就诊时已为局部进展或有远处转移而无法进行手术切除;此外,胰腺癌预后极差,转移性胰腺癌的中位生存期不足12个月,5年生存率不足3%[2-3],化疗是此类患者的主要治疗方式。对于局部进展期/转移性胰腺癌患者,目前一线标准治疗方案主要有AG方案即白蛋白紫杉醇+吉西他滨,与FOLFIRINOX方案即奥沙利铂+伊立替康+5-氟尿嘧啶/亚叶酸,但其生存获益远不能满足临床治疗需求。”
“胰腺癌是治疗极为困难的一种恶性肿瘤。虽然近年来免疫治疗在许多恶性肿瘤的治疗中疗效显著,但胰腺癌一直被认为是免疫治疗中的‘冷肿瘤’,免疫检查点抑制剂难以在胰腺癌治疗中发挥疗效。在分子靶向治疗方面,虽然PARP抑制剂在BRCA胚系变异、Sotorasib(也称AMG510)在KRAS G12C突变、尼妥珠单抗在KRAS野生型等胰腺癌的精准靶向治疗中取得了新进展,但获益人群仅占极少的一部分,靶向治疗和免疫治疗难以给广大胰腺癌患者带来生存获益。总体而言,胰腺癌对胰腺外科及肿瘤内科医生来讲依然是一个巨大的挑战。”
荟萃之声,盘点胰腺癌领域治疗进展
随着新药的不断研发和临床研究的深入开展,胰腺癌领域近年来也取得了一定的进展和突破,殷晓煜教授就近1年来胰腺癌在靶向治疗、免疫治疗、晚期一线及二线化疗方案进展和围手术期治疗进展进行了相关盘点与总结。
靶向治疗领域相关进展
殷晓煜教授解读了2022 ASCO上由秦叔逵教授牵头的一项治疗KRAS野生型胰腺癌的NOTABLE Ⅲ期研究——尼妥珠单抗联合吉西他滨对比吉西他滨单药治疗KRAS野生型的局部晚期或转移性胰腺癌的研究[4]。“研究结果提示尼妥珠单抗联合吉西他滨可显著提高KRAS野生型局部晚期或转移性胰腺癌患者的总生存期(OS)和无进展生存期(PFS),安全性与对照组相似,为KRAS野生型胰腺癌患者提供了治疗新选择。”
在该研究中,共有92名中国患者被随机分配到尼妥珠单抗+吉西他滨组(n=46)或安慰剂+吉西他滨组(n=46)。
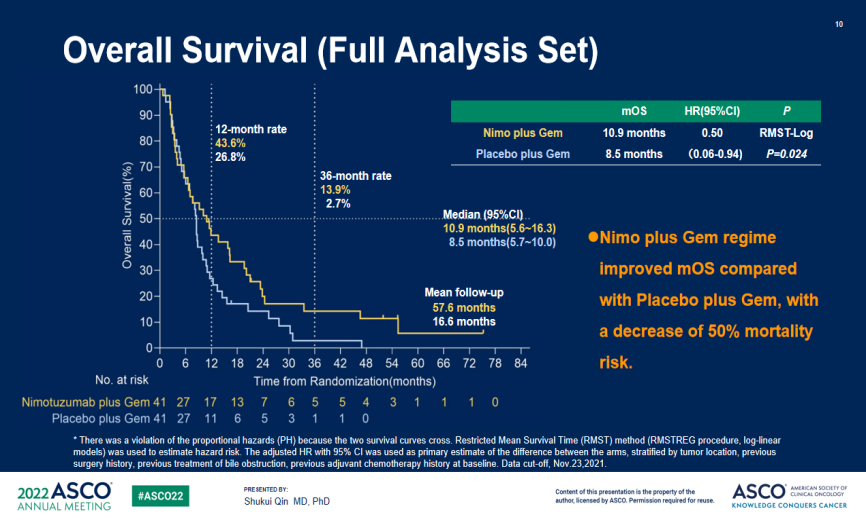
在完整分析集(n=82)中,尼妥珠单抗+吉西他滨组的中位OS显著延长(10.9个月vs 8.5个月,HR=0.50,95%CI:0.06~0.94,p=0.024)。
尼妥珠单抗+吉西他滨组的一年生存率为43.6%,安慰剂+吉西他滨组为26.8%,3年生存率分别为13.9%和2.7%。
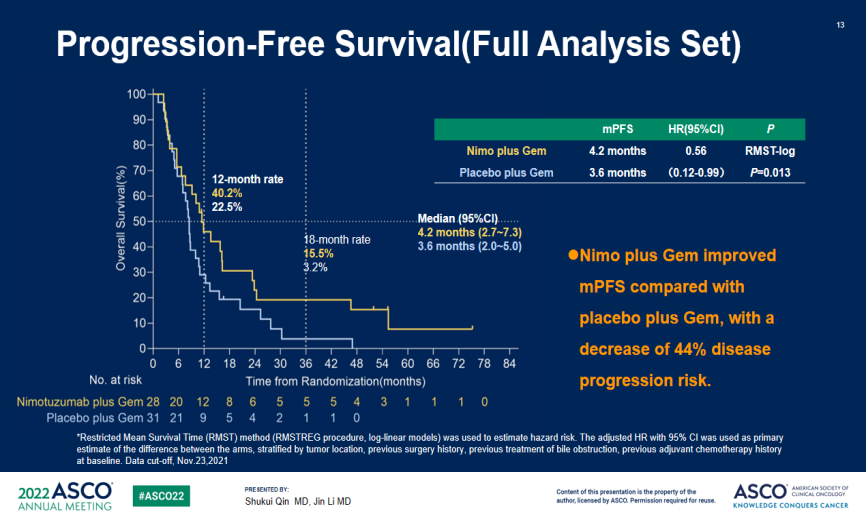
尼妥珠单抗+吉西他滨组的中位PFS显著延长(4.2个月vs 3.6个月,HR=0.56 ,95%CI 0.12-0.99,P=0.013)。
另外,殷晓煜教授还对2022年ASCO GI中一项KRAS G12C突变的Ⅰ/Ⅱ期CodeBreak 100研究[5]进行了相关解读:“目前85%~90%的胰腺癌患者存在KRAS突变,其中G12C约占这类突变的1%-2%,也一直被学界公认为‘不可成药靶点’。该研究结果显示,在38例接受过至少一种全身治疗的KRAS G12C突变的晚期胰腺癌患者中,Sotorasib的客观有效率(ORR)为21.1%,疾病控制率(DCR)为84.2%,中位缓解持续时间(DoR)为5.7个月,中位PFS为4.0个月,中位OS为6.9个月。Sotorasib打破了KRAS不可成药的困境,对胰腺癌靶向治疗产生了重大意义,为部分胰腺癌患者带来了生存新希望。”
免疫治疗领域相关进展
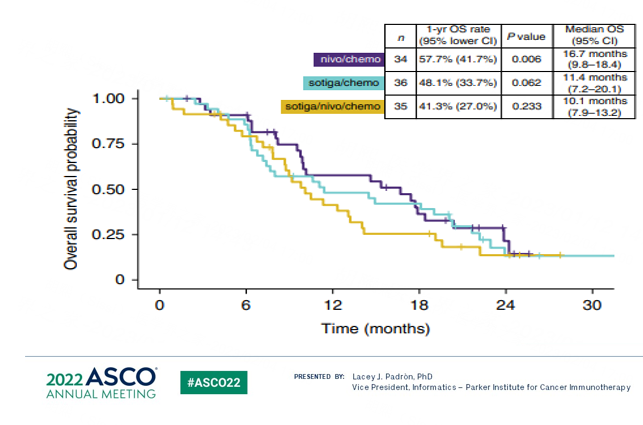
殷晓煜教授为我们解读2022年免疫治疗在胰腺癌领域进展的相关研究,2022 ASCO上一项免疫联合化疗的的相关研究[6]中,纳入了34例转移性胰腺癌患者进行纳武利尤单抗联合吉西他滨+白蛋白紫杉醇(GnP)一线治疗。研究结果显示,免疫联合化疗组一年OS率达57.7%,显著高于单用传统化疗的35%(p=0.006);中位OS为16.7个月(95%CI:9.8-18.4);中位PFS为6.4个月(95%CI:5.2-8.8);ORR为50%(95%CI:32-68);DCR为74%(95%CI:56-87);中位DOR为7.4个月(95%CI:2.1-NE)。”
殷晓煜教授指出在另一项2022 ASCO GI上公布的免疫联合化疗CISPD3研究[7]中,“信迪利单抗联合改良FOLFIRINOX(mFFX)方案对比mFFX方案治疗中国转移性和复发性胰腺癌患者,研究结果提示信迪利单抗联合mFFX显著改善晚期胰腺癌患者的ORR(50% vs 23.9%,p=0.010),但OS和PFS未获益。”
化疗方案相关进展
化疗目前仍是胰腺癌治疗的基石,殷晓煜教授重点介绍了在最新ASCO GI上公布的达到主要研究终点的Ⅲ期NAPOLI-3研究[8]以及在不可切除局部晚期胰腺癌围手术期治疗中取得突破性进展的CONKO-007 Ⅲ期研究[9]。同时,其解读了另一项晚期二线化疗方案相关研究。
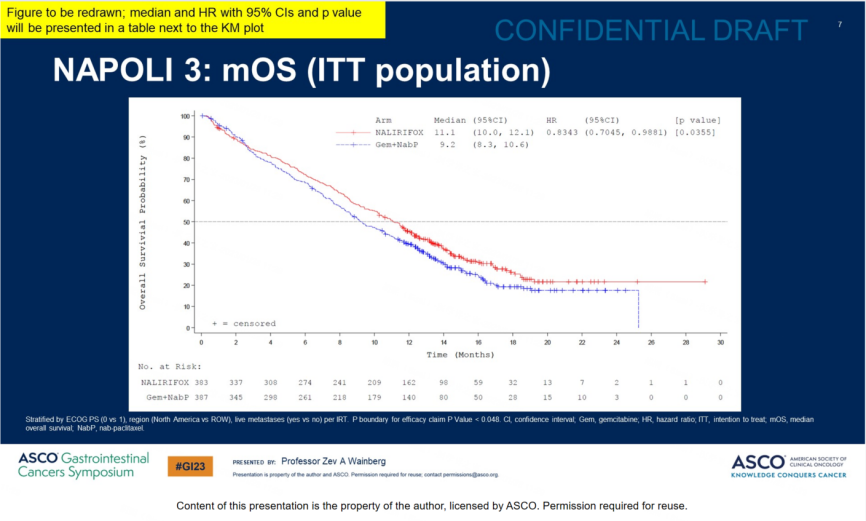
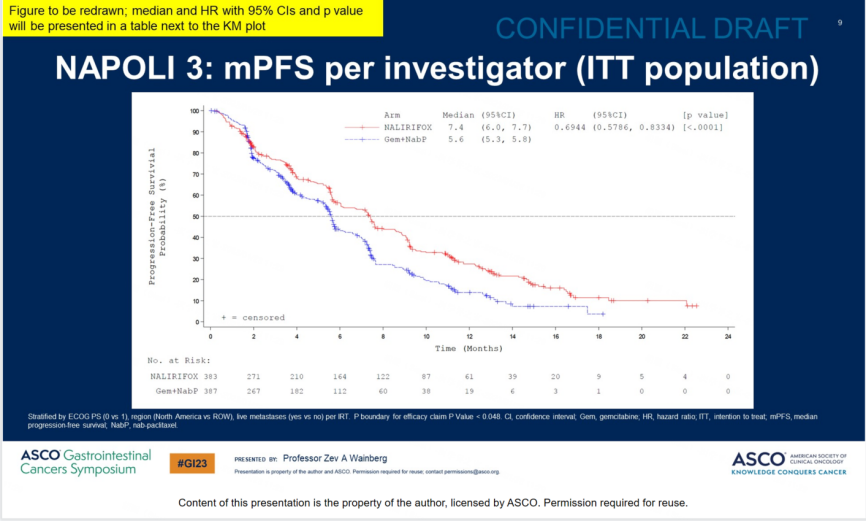
殷晓煜教授解读了2023 ASCO GI上公布的NAPOLI-3研究结果:“该随机Ⅲ期临床研究对比了伊立替康脂质体+5-FU/LV+奥沙利铂三药化疗方案(NALIRIFOX)与AG方案在转移性胰腺导管腺癌(mPDAC)中的一线治疗效果,研究共纳入770例转移性胰腺导管腺癌患者,其中383例患者分配至NALIRIFOX组,387例患者分配至AG组接受治疗。结果显示,NALIRIFOX组的中位OS及中位PFS均较AG组显著提高。”
NALIRIFOX组中位OS较AG组显著延长1.9个月(11.1个月vs 9.2个月),降低16%死亡风险(HR=0.84 [95%CI:0.71–0.99];p=0.04)。
NALIRIFOX组中位PFS较AG组显著延长1.8个月(7.4个月vs 5.6个月),降低30%疾病进展风险(HR=0.70 [95CI:0.59–0.84];p=0.0001)。
NALIRIFOX组的ORR为41.8%(95%CI:36.8-46.9),而AG组为36.2%(95%CI:31.4-41.2)。
在一项二线治疗化疗方案研究中,吉西他滨联合紫杉醇(GEMPAX)对比吉西他滨单药(GEM)治疗FOLFIRINOX治疗失败或不耐受的转移性胰腺导管腺癌的随机Ⅲ期研究[10]结果显示GEMPAX方案相较于GEM单药治疗,改善了中位PFS(3.1个月vs 2.0个月,HR=0.64,p=0.008)和ORR(19% vs 5%),中位OS未获益(6.4个月vs 5.9个月,p=0.4095)。临床上我们经常将AG和FOLFIRINOX方案互为一二线方案对胰腺癌患者进行治疗,已有研究表明该方案可提高化疗的有效率及转化成功率,期待更多大样本的二线及后线相关研究探讨出有效治疗方案来改善晚期胰腺癌患者的远期生存获益。
在围手术期治疗中,一项CONKO-007 Ⅲ期研究[9]评估了诱导化疗后序贯放化疗与单独化疗治疗不可切除局部晚期胰腺癌的疗效与安全性。结果显示,诱导化疗后增加放疗可显著提高环周切缘(CRM)阴性率以及病理完全缓解(pCR)率;并且与CRM阳性的R0切除、R1切除以及未手术切除的患者相比,CRM阴性的R0切除的患者预后有显著改善。该研究中CRM阴性的患者其5年生存率为35.9%,R0切除的患者其5年生存率为27.3%。殷晓煜教授表示:“该研究也显示出放射治疗的作用,相信综合治疗模式将会成为局晚期胰腺癌治疗新的研究方向,为不可手术的胰腺癌患者带来手术机会和生存获益。”
未来展望,胰腺癌研究热点及方向
近年来胰腺癌领域在靶向治疗、免疫治疗、晚期一线、二线化疗治疗和围手术期治疗上都有不小的突破,但胰腺癌仍存在着巨大的未被满足的临床需求。对于后续研究热点及方向,殷晓煜教授认为:“基于分子分型,在可行靶点上进行精准靶向药物治疗的探索和突破。在胰腺癌治疗领域,已经获批适应症的相关靶点有dMMR、BRCA和NTRK等;还有BRAF、ALK、HER2、KRAS G12C等靶点已有相关靶向药物,但尚未在胰腺癌领域获批,刚刚我们也提到了KRAS G12C在胰腺癌领域的Ⅰ/Ⅱ期研究进展,表明KRAS已不再是既往认为的不可进行靶向治疗的基因,同时针对KRAS G12D、G12V突变的靶向药物的前期临床研究正在如火如荼地开展中,同时期待后续能够挖掘更多潜在靶点,为更多胰腺癌患者带来临床治疗新思路。”
同时胰腺癌属于冷肿瘤,对于此类冷肿瘤,殷晓煜教授指出:“将肿瘤由‘冷’转‘热’,发挥免疫治疗疗效仍是胰腺癌未来探索的方向和热点,可以通过深入研究胰腺癌微环境特征、寻找生物标志物来筛选免疫治疗敏感人群、寻找新药物降低胰腺癌纤维化进而改善免疫抑制状态等方式来提高免疫疗效。目前已有几项小样本的Ⅰ/Ⅱ期研究已表明免疫联合化疗具有协同增效的作用。”
对于目前的CAR-T细胞疗法、肿瘤疫苗等新型疗法,殷晓煜教授表示“其在部分癌种治疗中已展现出极具期待的前景,但该疗法在胰腺癌领域中的应用尚处于研究阶段,值得期待。但从治疗机理上看,仍有待解决上述的将胰腺癌由‘冷’转‘热’的难题,CAR-T细胞疗法才能看到曙光。”
医患携手,共同战胜“癌中之王”
正值“世界癌症日”,殷晓煜教授也为广大胰腺癌患者送上鼓励及树立抗癌信心:“首先,胰腺癌患者在疾病治疗过程中要树立正确、科学的治疗观念进行抗癌治疗,过程中保持乐观的心态和信心。在临床工作中,我们经常看到患者还没有被癌症打倒,就已经被焦虑、抑郁、恐惧和绝望等不良情绪打败了。不良的情绪会使人体免疫系统明显减弱甚至崩溃,已经被多篇论文证实与癌症患者生存期及预后呈负相关,极大地影响肿瘤的治疗和恢复,这是很可惜的。因此,对患者来讲,在面对胰腺癌这一可怕的疾病时要努力做自己情绪的主人,及时找家属、心理医生及临床医生抒发情绪,或者通过兴趣爱好,如听音乐、看电影、有氧运动等方式疏解负面情绪。此外,在治疗及随访过程中,患者要学会与医生及家属沟通交流,充分了解治疗方案的不良反应及其应对措施,在相互信任的基础上积极配合医生的治疗,共同面对疾病、治疗与康复过程。”
“其次,虽然胰腺癌的恶性程度比较高、治疗难度大,但胰腺癌近年来的生存获益有了重大突破,在前10年五年生存率小于5%,而近5年已经突破了10%[11]。在胰腺癌的治疗上,不止患者在努力,包括医护人员、研究人员、科学家等都在致力于寻找更优的治疗药物、治疗方案来改善患者的生存获益,提高晚期患者的生活质量。前面也介绍了胰腺癌相关的治疗进展,相信后续在药物治疗方案上能在胰腺癌领域将有更多的创新和突破。”
最后,殷晓煜教授表示:“临床医生会在最大程度上通过规范化、全程化的患者管理,在多学科团队管理下为患者选择合适的治疗手段,即使无法延长患者的生存时间,也可更注重提高晚期胰腺癌患者的生活质量。无论晚期胰腺癌患者的生命长度如何,希望医护和患者、家属共同携手一同去关心晚期胰腺癌患者,正如特鲁多医生的名言‘有时去治愈,常常去帮助,总是去安慰。’真正让患者感受到医生和家属对于患者治疗的关心和支持。在此也呼吁广大胰腺癌患者相信自己、相信医生,共同携手,一同抗击胰腺癌,早日战胜疾病。”
专家简介
二级教授、一级主任医师、博士生导师
中山大学附属第一医院副院长、胆胰外科学科带头人
中国抗癌协会神经内分泌肿瘤专业委员会 副主任委员
中国抗癌协会胆道肿瘤专业委员会 常委
中华医学会外科学分会胰腺外科学组 委员
中国医师协会胰腺病学专业委员会 常委
国际肝胆胰协会中国分会胆道肿瘤专业委员会 副主任委员
中国研究型医院协会数字医学临床外科专业委员会 副主任委员
中国研究型医院协会胰腺病学专业委员会 常委
中国研究型医院协会术后快速康复委员会、智能医学委员会 常委
广东省医学会外科学分会 副主任委员
广东省医疗行业协会肝胆胰外科管理分会 主任委员
广东省抗癌协会胆道肿瘤专业委员会 主任委员
广东省医师协会胰腺病学分会 副主任委员
广东省抗癌协会胰腺癌专业委员会 副主任委员
[1]胰腺癌诊疗指南(2022年版)[J].临床肝胆病杂志,2022,38(05):1006-1030.
[2]American Cancer Society. Cancer Facts & Figures 2022. Atlanta, Ga: American Cancer Society; 2022.
[3]Ruhl JL, Callaghan C, Hurlbut, A, Ries LAG, Adamo P, Dickie L, Schussler N (eds.) Summary Stage 2018: Codes and Coding Instructions, National Cancer Institute, Bethesda, MD, 2018.
[4]Shukui Qin, et al. Nimotuzumab combined with gemcitabine versus gemcitabine in K-RAS wild-type locally advanced or metastatic pancreatic cancer: A prospective, randomized-controlled, double-blinded, multicenter, and phase III clinical trial. 2022 ASCO Abstract LBA4011.
[5]John H Strickler, et al. First data for sotorasib in patients with pancreatic cancer with KRAS p.G12C mutation: A phase I/II study evaluating efficacy and safety.2022ASCO GI Abstract 360490.
[6]Padrón LJ, Maurer DM, O'Hara MH,et al. Sotigalimab and/or nivolumab with chemotherapy in first-line metastatic pancreatic cancer: clinical and immunologic analyses from the randomized phase 2 PRINCE trial. Nat Med. 2022 Jun;28(6):1167-1177.
[7]Qihan Fu, et al. Randomized phase III study of sintilimab in combination with modified folfrinox versus folfrinox alone in patients with metastatic and recurrent pancreatic cancer in China: The CISPD3 trial.2022 ASCO GI Abstract 560.
[8]Zev A. Wainberg, et al. NAPOLI-3: A randomized, open-label phase 3 study of liposomal irinotecan + 5-fluorouracil/leucovorin + oxaliplatin (NALIRIFOX) versus nab-paclitaxel + gemcitabine in treatment-na¨ıve patients with metastatic pancreatic ductal adenocarcinoma (mPDAC).2023 ASCO GI Abstract LBA661.
[9]Rainer Fietkau, et al.Randomized phase III trial of induction chemotherapy followed by chemoradiotherapy or chemotherapy alone for nonresectable locally advanced pancreatic cancer: First results of the CONKO-007 trial.2022 ASCO GI Abstract 4008.
[10]Christelle de la Fouchardiere, et al. Evaluation of gemcitabine and paclitaxel versus gemcitabine alone after FOLFIRINOX failure or intolerance in metastatic pancreatic ductal adenocarcinoma: Results of the randomized phase III PRODIGE 65 - UCGI 36 - GEMPAX UNICANCER study.2022 ESMO Abstract LBA60.
[11]Bhagat, V.H., Shahid, H., Sarkar, A., Tyberg, A., & Kahaleh, M. (2020). Su1161 TRENDS IN 5-YEAR SURVIVAL RATES OF PANCREATIC CANCER: WHERE ARE WE NOW? Gastroenterology, 158.
排版编辑:肿瘤资讯-展思懿











 苏公网安备32059002004080号
苏公网安备32059002004080号


