近年来,肿瘤个体化治疗通过疾病靶点的基因检测信息结合循证医学,为患者提供了更精准的治疗方案,已经成为现代医学发展的趋势。BRCA1/2基因作为乳腺癌和卵巢癌等相关肿瘤的风险评估及治疗决策的关键生物标志物,在个体化治疗中发挥了重要作用。PARP抑制剂尤其是奥拉帕利的应用,为BRCA突变的乳腺癌患者带来了新的治疗选择。本期特邀辽宁省肿瘤医院张强教授针对BRCA突变在乳腺癌个体化治疗中的意义及奥拉帕利的治疗获益进行深入探讨,以飨读者。
BRCA突变影响DNA修复机制
乳腺癌易感基因(BRCA)包括 BRCA1和 BRCA2,是重要的抑癌基因,其编码产物参与 DNA 损伤同源性重组修复 (HRR)。BRCA1/2 基因突变会导致同源重组缺陷 (HRD),使得基因组不稳定性显著增加。BRCAm 分为两种类型:1)胚系突变(gBRCAm), 是指来源于精子或卵母细胞的生殖细胞突变,导致机体所有细胞都携带有突变基因,可遗传给后代;2)体细胞突变(sBRCAm),是指发生于肿瘤细胞中的 BRCA 基因突变,为非遗传性突变。
BRCA1/2基因突变状态在相关肿瘤(卵巢癌、乳腺癌、胰腺癌、前列腺癌等)的遗传风险评估、治疗选择、预后判断等方面都具有重要意义 。 研究显示,携带 BRCA 突变的健康女性乳腺癌发生风险较普通人群提高5倍。BRCA1 突变常见于三阴性乳腺癌,而 BRCA2 突变则多发生在激素受体阳性亚型中。BRCA1/2 基因是评估乳腺癌、卵巢癌和其他相关肿瘤发病风险的重要生物标志物,也是影响患者个体化治疗方案选择的生物标志物。因此,BRCA1/2基因检测有助于协助制定精准诊疗方案。NCCN指南[1]也推荐对于确诊时年龄≤50岁,有高风险家族史、TNBC以及晚期乳腺癌和早期高危HER2阴性乳腺癌符合PARPi用药适应症的患者进行BRCA检测。

BRCA1/2 基因突变状态与聚二磷酸腺苷核糖聚合酶(PARP)抑制剂疗效密切相关。近年来,FDA及NMPA已陆续批准多种 PARP抑制剂用于多种实体肿瘤的治疗。
PARP抑制剂的合成致死机制
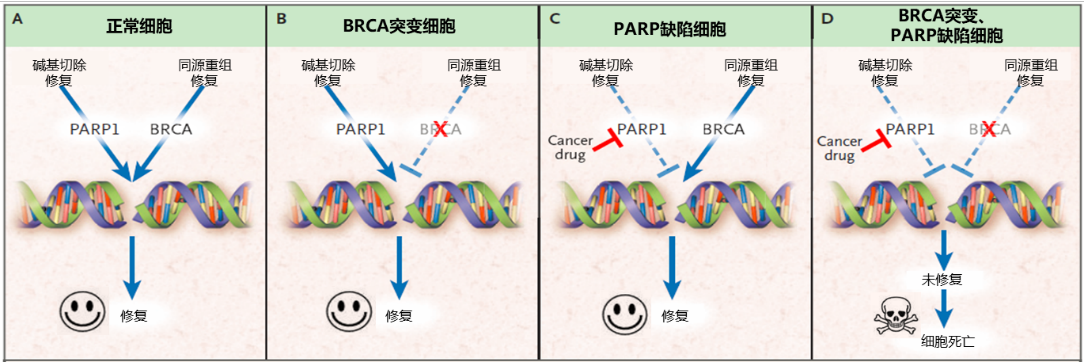
研究表明,在BRCA1/2突变型乳腺癌患者中,联合应用PARP抑制剂能达到“合成致死”的疗效。这个概念首次由1946年遗传学家 Theodosius Dobzhansky提出,当两个非致死基因突变单独发生时,细胞并不发生损伤或死亡;而两个非致死基因突变同时发生时,就可以引起细胞死亡,即存在杀死效应。Helleday又提出了PARP抑制剂在BRCA基因突变细胞的“合成致死”模型, 主要通过DNA损伤修复通路发挥作用。
正常情况下,人体细胞产生的大量 DNA 单链断裂可通过 PARP 介导的碱基切除修复 (BER)途径修复。DNA双链断裂的主要修复途径为非同源末端连接(NHEJ)修复和同源重组修复,前者速度快,但是会发生修复错误,导致基因组不稳定性;后者精确度高,修复后的 DNA 具有高保真性。PARP抑制剂利用“合成致死”机制杀伤肿瘤细胞:通过抑制 PARP 酶催化活性和 PARP 捕获,使 DNA 单链断裂无法修复并大量堆积,进而产生大量的 DNA 双链损伤; 当细胞存在BRCA1/2基因突变时,DNA双链断裂无法修复或者依赖容易错配的NHEJ途径修复,二者作用叠加,增加细胞死亡。即“合成致死”效应,这也是PARP抑制剂治疗BRCA1/2突变乳腺癌的主要机制。
奥拉帕利在BRCA突变乳腺癌
个体化治疗中的应用
奥拉帕利是首个应用于临床的口服PARP抑制剂,临床试验发现奥拉帕利在BRCA 突变的患者中表现出持久的抗肿瘤活性。
奥拉帕利用于早期乳腺癌(新)辅助治疗
II期GeparOLA 研究[2]纳入102例伴有同源重组缺陷的HER2阴性乳腺癌患者,所有患者随机分配,接受奥拉帕利联合紫杉醇或卡铂联合紫杉醇的新辅助治疗方案,12 周治疗后,两组均序贯 4 个疗程的阿霉素+环磷酰胺(EC)化疗方案再进行手术,结果发现:奥拉帕利组的 pCR 为 55.1%, 高于卡铂组的 48.6%,但差异无统计学意义。该研究对BRCA突变亚组分析时发现,BRCAm 患者的两组 pCR 相当 ( 60% vs. 60%)。
OlympiA Ⅲ期临床试验[3]共纳入1836例gBRCA1/2突变伴高危因素的HER2阴性早期乳腺癌患者,按照1∶1随机分配至奥拉帕利组和安慰剂组,用药时长1年。结果显示,奥拉帕利和安慰剂组的3年无浸润性疾病生存(iDFS)率分别为85.9% 和77.1%,降低疾病复发、新发肿瘤或死亡的风险42%(HR=0.58,99.5%CI:0.41~0.82,P < 0.01);3年无远处疾病生存期(DDFS)率分别为87.5%和80.4%,降低远处疾病复发或死亡风险43%(HR=0.57,99.5%CI:0.39~0.83,P < 0.01)。两组4年OS率分别为89.8% vs 86.4%(HR=0.68;P=0.01),奥拉帕利降低了32%的死亡风险[4]。
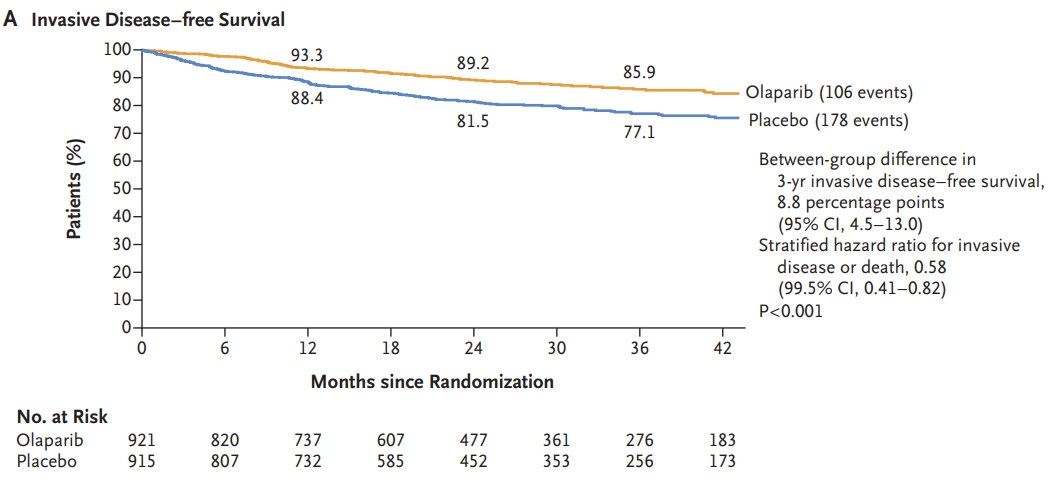

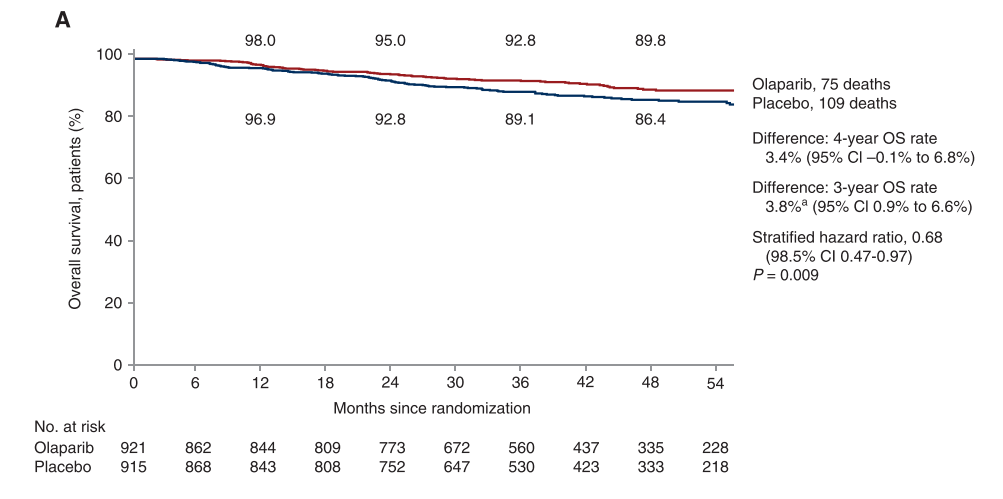
基于OlympiA Ⅲ期研究结果,NCCN指南推荐对于携带gBRCA1/2突变的复发高危三阴性乳腺癌和含紫杉与蒽环类药物新辅助化疗后未达pCR的HER2阴性患者优选奥拉帕利辅助强化治疗。
奥拉帕利单药治疗gBRCA突变转移性乳腺癌
OlympiAD Ⅲ期临床试验[5]共纳入302例BRCA1/2突变且HER2阴性转移性乳腺癌患者,按照2∶1的比例随机分配至奥拉帕利组或医师选择的标准化疗方案组。研究结果发现,奥拉帕利组的中位 PFS 显著优于 TPC 组(7.0 个月 vs. 4.2 个月HR=0.58, P<0.001),奥拉帕利组和 TPC组的ORR分别为 59.9%和28.8%,奥拉帕利组3级及以上不良事件发生率为36.6%,TPC 组为 50.5%,因不良反应停药率分别为4.9% 和 7.7%;亚洲患者的疗效、安全性和耐受性与全球数据基本一致[6];值得注意的是,部分初治的晚期患者,一线使用奥拉帕利的 OS 有明显获益(22.6 个月 vs.14.7 个月, HR=0.51, P=0.02)[7]。
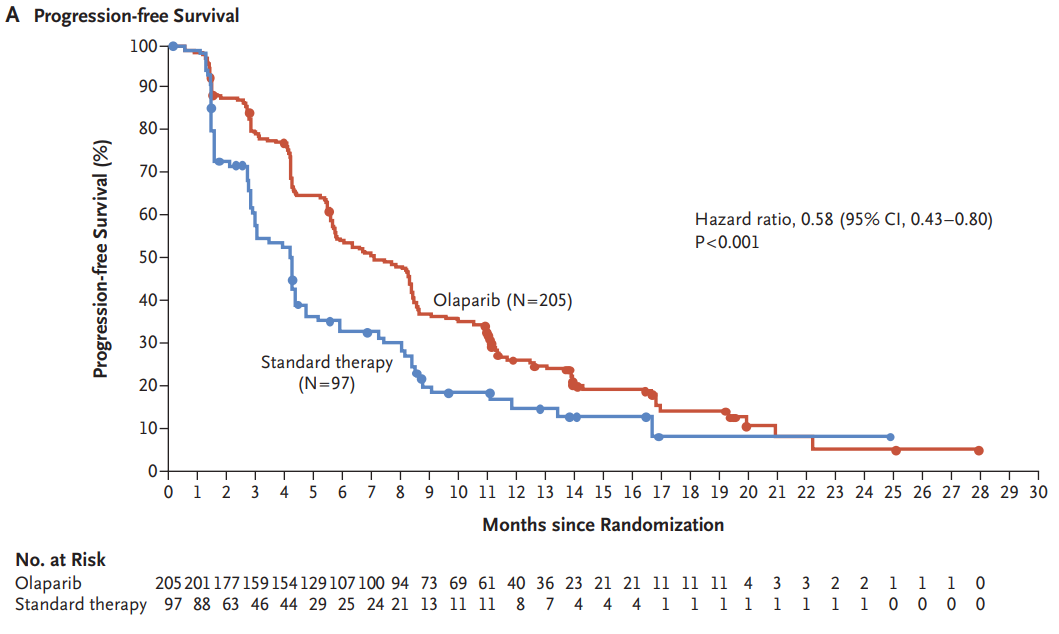
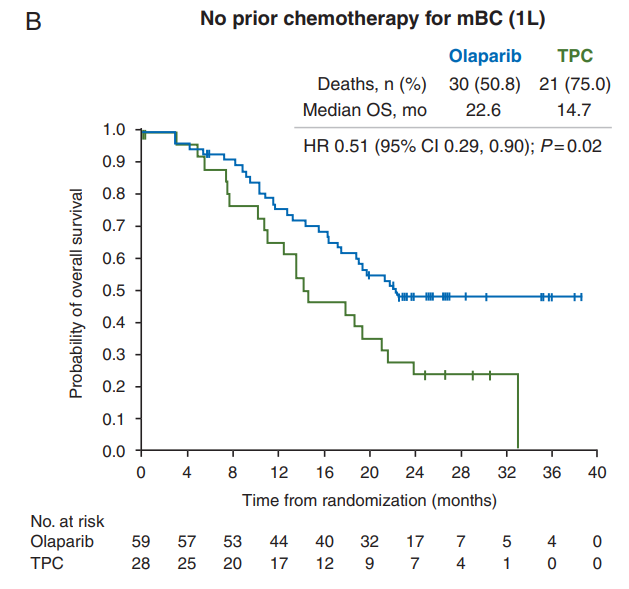
基于 OlympiAD 研究,2018 年FDA批准了奥拉帕利用于携带 gBRCAm 的 HER2 阴性转移性乳腺癌的治疗,也是第一个获批用于乳腺癌治疗的PARP抑制剂。
LUCY Ⅲb期研究共纳入252例BRCA1/2突变、HER2阴性转移性乳腺癌患者,给予奥拉帕利治疗(中位总疗程7.9个月),中期研究结果显示,中位PFS为8.1个月(95%CI:6.93~8.67),临床缓解率(CRR)为48.6%[8]。该研究入组人群与OlympiAD入组人群基线特征相似,几乎所有患者都接受了蒽环和紫杉药物治疗。结果显示,LUCY研究与OlympiAD研究中患者获益一致,该研究进一步支持奥拉帕利在真实世界gBRCAm HER2阴性转移性乳腺癌患者的临床疗效。
奥拉帕利联合免疫治疗gBRCA转移性乳腺癌
I/II期MEDIOLA研究[9]进一步探索gBRCA1/2突变患者PARPi联合ICIs的疗效。该研究共纳入34例HER2阴性BRCA1/2突变的转移性乳腺癌患者,给予奥拉帕利治疗1个月后再加用度伐利尤单抗,结果显示:奥拉帕利联合度伐利尤单抗12周ORR高达63.3%,既往未接受或仅接受一线化疗的患者12周ORR为70%。发生缓解的患者表现出持久的获益,中位缓解持续时间(DOR)为9.2个月,中位PFS和OS分别为8.2个月(95%CI:4.6~11.8)和21.5个月(95%CI:14.4~25.5)。
II期DOLAF 研究[10]旨在探索奥拉帕利、度伐利尤单抗和氟维司群联合治疗HRR 缺陷或微卫星不稳定性 (MSI) 的晚期ER阳性、HER2阴性转移性乳腺癌患者的疗效。研究结果显示:在中位随访时间24.6个月时,154例可评估患者的24周PFSR达到66.7%,而gBRCAm患者组的24周PFSR更高,为76.3%。全人群和gBRCAm患者的中位PFS分别为9.3个月、12.6个月。全人群的ORR为41%,中位OS为30个月。
未来展望
BRCA基因突变的发现不仅为乳腺癌患者带来了个体化治疗的希望,也为治疗策略的优化提供了新的思路。未来,BRCA突变检测将更多地用于风险评估、早期诊断,渗透到从新辅助治疗、手术方案选择、术后放化疗到靶向用药的全程个体化治疗体系。奥拉帕利作为用于BRCA突变乳腺癌的PARP抑制剂,通过“合成致死”机制显著提高了患者的生存率和治疗效果。随着未来更多研究的开展,PARP抑制剂有望在更多肿瘤类型及治疗阶段中发挥重要作用,为精准医疗的推进贡献力量。
专家介绍
辽宁省肿瘤医院乳腺外科四病区主任
大连理工大学、中国医科大学及大连医科大学肿瘤外科研究生导师
辽宁省“百千万人才”工程百层次人才
北京癌症防治学会乳腺癌个体化诊疗及MDT专业委员会候任主委
中国抗癌协会乳腺肿瘤整合康复委员会副主任委员
第十届中国抗癌协会乳腺癌专业委员会常委
中国临床肿瘤学会乳腺癌专家委员会委员
中华医学会肿瘤分会乳腺癌学组委员
中国医师协会肿瘤分会乳腺癌学组委员
先后在MD.Anderson癌症中心及欧洲肿瘤研究所(IEO)的乳腺科进修学习
[1]NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®) for Genetic/Familial High-Risk Assessment: Breast, Ovarian, and Pancreatic V.5.2024.
[2]Fasching PA, et al. Ann Oncol, 2021, 32(1):49-57.
[3]Tutt ANJ, et al. N Engl J Med, 2021, 384(25): 2394-2405.
[4]Geyer CE Jr, et al. Ann Oncol 2022;33:1250–1268.
[5]Robson M, et al. N Engl J Med, 2017, 377(6):523-533.
[6]Im SA, et al. Sci Rep, 2020, 10(1):8753.
[7]Robson ME, et al. Ann Oncol, 2019, 30(4):558-566.
[8]Gelmon KA, et al. Eur J Cancer, 2021, 152: 68-77.
[9]Domchek SM, et al. Lancet Oncol, 2020, 21(9): 1155-1164.
[10]Séverine Guiu,, et al. 2024 ESMO BC abstract 179O
排版编辑:肿瘤资讯-yu











 苏公网安备32059002004080号
苏公网安备32059002004080号


