2024年9月13日至9月17日,欧洲肿瘤内科学会(ESMO)年会在西班牙巴塞罗那盛大召开。作为全球最具知名度的肿瘤学盛会之一,此次ESMO年会中报告了多项肝癌领域的最新临床与基础研究进展,涵盖免疫治疗、靶向治疗、精准检测以及新型药物等。本期GI有约,我们特邀肝癌领域专家,来自西安国际医学中心医院消化病院的韩国宏教授和来自中国医科大学附属第一医院的邵海波教授,基于ESMO前沿进展成果,述评他们对靶免联合局部治疗肝细胞癌(HCC)的新策略和思考。
韩国宏教授、邵海波教授采访视频
专家介绍
消化病医院执行院长、主任医师、教授、博士生导师
国际门静脉高压最权威Baveno Ⅶ 专家组成员、科学委员会委员
亚太原发性肝癌理事会理事(APPLE Council Member)
中国抗癌协会第九届理事会理事
中国非公立医疗机构协会介入医学分会会长
中国抗癌协会-中西医整合肝癌专委会主委和肿瘤肝病学专委会副主委
中国研究型医院学会-介入专委会副主委
卫健委原发性肝癌诊疗指南专委会介入治疗组副组长
(2011版、2017版、2019版、2022版和2024版)
2023年入选全球2%顶尖科学家、2021年入选全球学者库
2020-2023年连续3年入选“ 中国高被引学者 ”
2020年中国消化病领域学术影响力排名TOP 100 中位列第六
2017年以第一完成人获军队科技进步一等奖
2016年作为主要成员获国家科学进步奖创新团队奖
2011年以来作为第一或通讯作者在Nat Rev Gastro Hepatol、Ann Oncol、Lancet Gastro Hepatol、Gastroenterology、J Hepatol、Gut、Radiology等权威杂志发表SCI同行评议论文162篇。他引8000余次,H指数48。
专家介绍
介入治疗科主任、教授、主任医师、博士生导师
中华医学会放射学分会介入学组委员
中国医师协会介入医师分会委员
中国抗癌协会肿瘤介入学委员会常务委员
中国抗癌协会肿瘤微创治疗委员会常务委员
中国临床肿瘤学会(CSCO)放射介入治疗专委会常务委员
中国医药教育协会介入微创治疗专委会常务委员
辽宁省医学会介入医学分会副主任委员
沈阳市医学会肿瘤介入学分会副主任委员
韩教授您好,系统治疗联合TACE、手术等局部治疗目前在临床应用广泛,但已公布结果的III期研究非常有限。LEAP-012在本次ESMO大会的Practice-Changing Trials专场中以LBA的形式公布了数据,大家都非常关注。您能第一时间为我们简要介绍该研究的结果并分享看法吗?
LEAP-012研究PFS获得阳性结果,靶免+TACE三联方案成为中期HCC潜在新方案
韩国宏教授:众所周知,中国是肝癌大国,几乎每年全球新发肝癌患者有一半在中国。肝癌的治疗一直是临床上亟待解决的重要难题,存在大量未满足的临床需求。随着晚期肝癌系统治疗方法的不断出现和获批,我们现在拥有了免疫治疗和靶向治疗的选择。此次公布的LEAP-012研究[1],也为中期肝癌提供了一种有价值的治疗选择,即靶免联合局部治疗方案。
自系统治疗在晚期肝癌一线治疗中获批以来,学者和临床医生们一直在思考如何将系统治疗结合到中期肝癌的标准治疗中,即所谓的经肝动脉化疗栓塞(TACE),以提升TACE治疗的疗效。LEAP-012研究正是基于这样的设计理念。
LEAP-012是一项随机、双盲、安慰剂对照的III期临床研究,旨在评估TACE联合仑伐替尼和帕博利珠单抗的治疗效果。研究最终共入组了480例患者,其中中国贡献了208例。入组的患者均确认为不适合根治性治疗,无门静脉癌栓形成,无转移,Child-Pugh A级且体能状态良好。研究最终按1:1随机分配至试验组或对照组,试验组采用TACE联合仑伐替尼和帕博利珠单抗,对照组采用TACE联合仑伐替尼和帕博利珠单抗的双药安慰剂。无进展生存期(PFS)和总生存期(OS)是研究的主要终点,并根据肝功能和肿瘤负荷等因素进行分层。
值得一提的是,这项研究的肿瘤负荷分层采用了我们团队牵头全国24家中心制定的“Six-and-twelve”标准。该标准根据肿瘤数量和最大肿瘤直径的总和将患者分为低负荷(≤6)、中负荷(6-12)和高负荷(>12)三组,有助于更精准地评估不同肿瘤负荷患者的治疗效果。
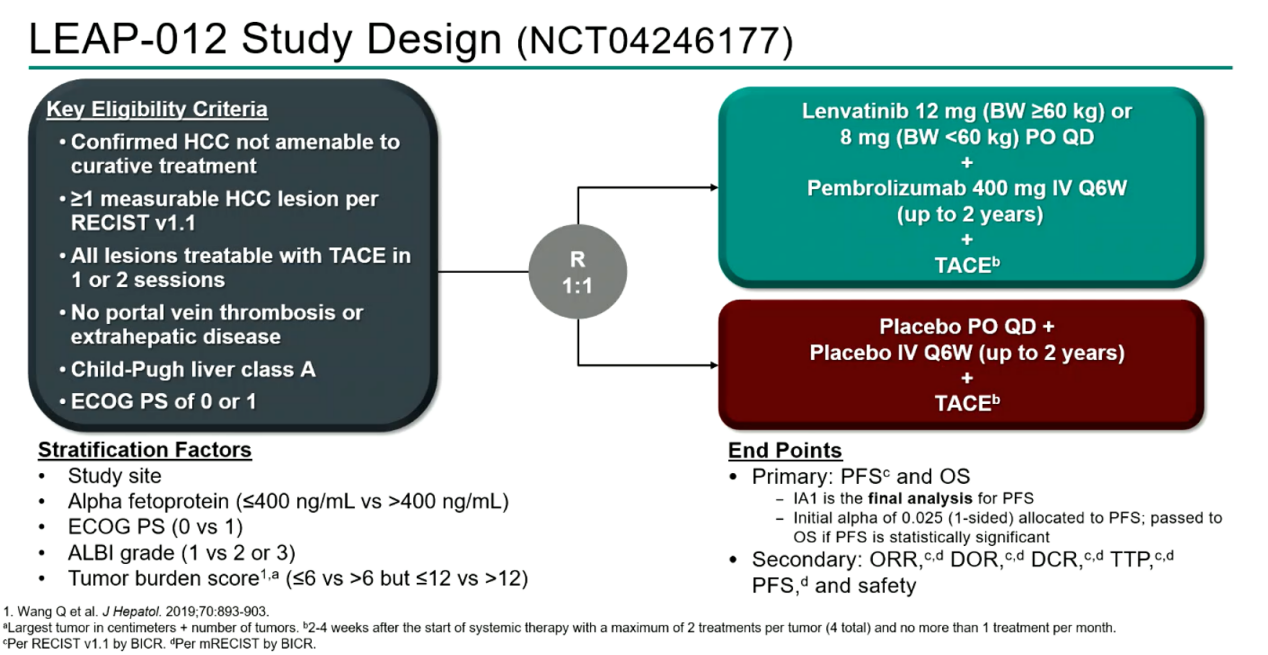 图 LEAP-012研究设计
图 LEAP-012研究设计
研究结果显示,对比单纯TACE治疗,仑伐替尼及帕博利珠单抗联合TACE可显著改善患者的中位PFS,从10个月延长至14.6个月,降低了患者疾病进展或死亡的风险达34%(HR 0.66,P=0.0002)。而且PFS生存曲线在第9周时就能观察到明显的分离并持续超过24个月,试验组获益优势非常明显。此外,安全性分析表明,该方案的不良反应可控、可耐受。
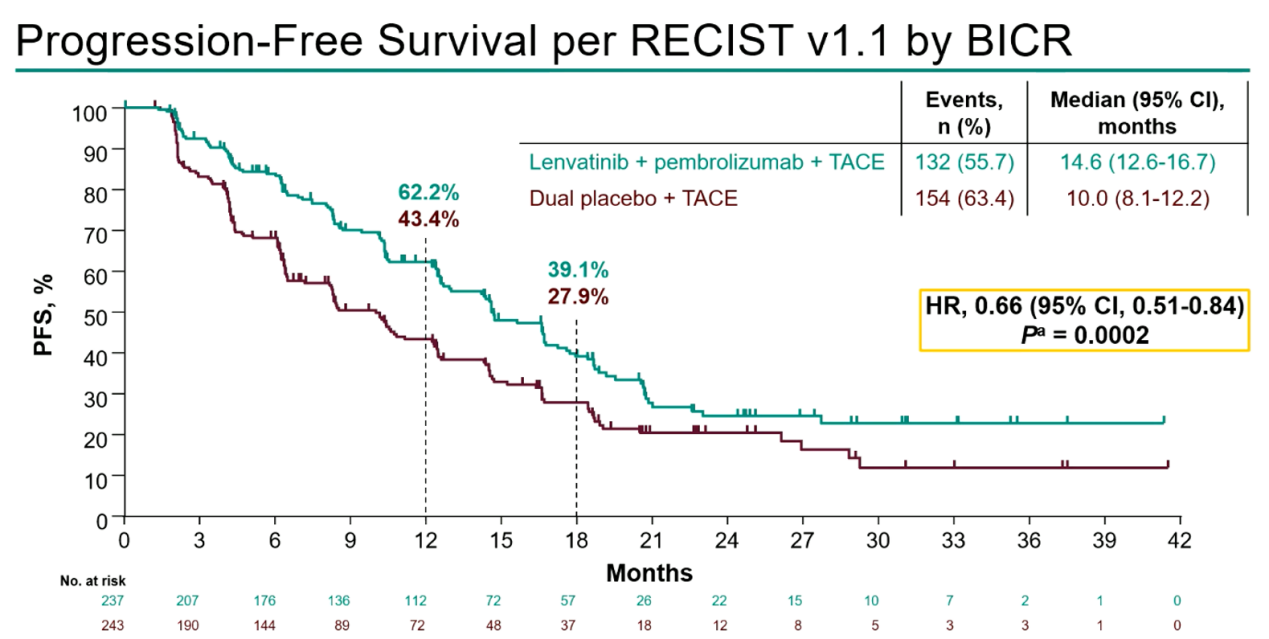 图 LEAP-012研究PFS结果
图 LEAP-012研究PFS结果
本次报道是PFS的最终分析。由于PFS结果阳性,按照研究设计,α值将从PFS完整传递到另一主要终点OS。由于事件数尚未成熟,OS暂未显示出统计学显著性差异(HR 0.8, 95%CI 0.57-1.11, P=0.0867),但显现出了获益趋势,期待未来的随访中能看到我们期待的结果。
记者:感谢韩教授以研究者身份对LEAP-012研究最新结果的分享和解读。同样,邵海波教授曾参与多项国际级HCC研究,如知名的CHANCE系列。现在我们特别连线国内的邵教授,对LEAP-012研究请您分享您的宝贵洞见:
TACE联合系统治疗循证级别升级,
在中国特色HCC中疗效凸显
邵海波教授:作为一名从事肝胆肿瘤介入领域多年的临床医生,我对LEAP-012研究结果的非常期待。其实在临床中我们也在尝试靶免联合TACE去寻找能够延长患者生存的治疗方案,所以LEAP-012研究为我们提供了高级别的循证医学证据。
正如韩教授刚刚提到的,LEAP-012研究PFS的最终分析显示出靶免联合TACE组较单纯TACE组的显著优势。在多数亚组中靶免联合TACE组有显著的生存获益,我个人比较关注HBV感染(PFS HR 0.59)和亚裔人群(PFS HR 0.57)这两组人群是否在研究中获益。
此外,研究采用mRECIST标准评估两研究组的客观缓解率(ORR),发现三联组ORR高达71.3%。虽然纳入的多为早中期人群,但是LEAP-012研究的短期疗效从侧面印证了这种联合模式在HCC转化治疗中的前景。
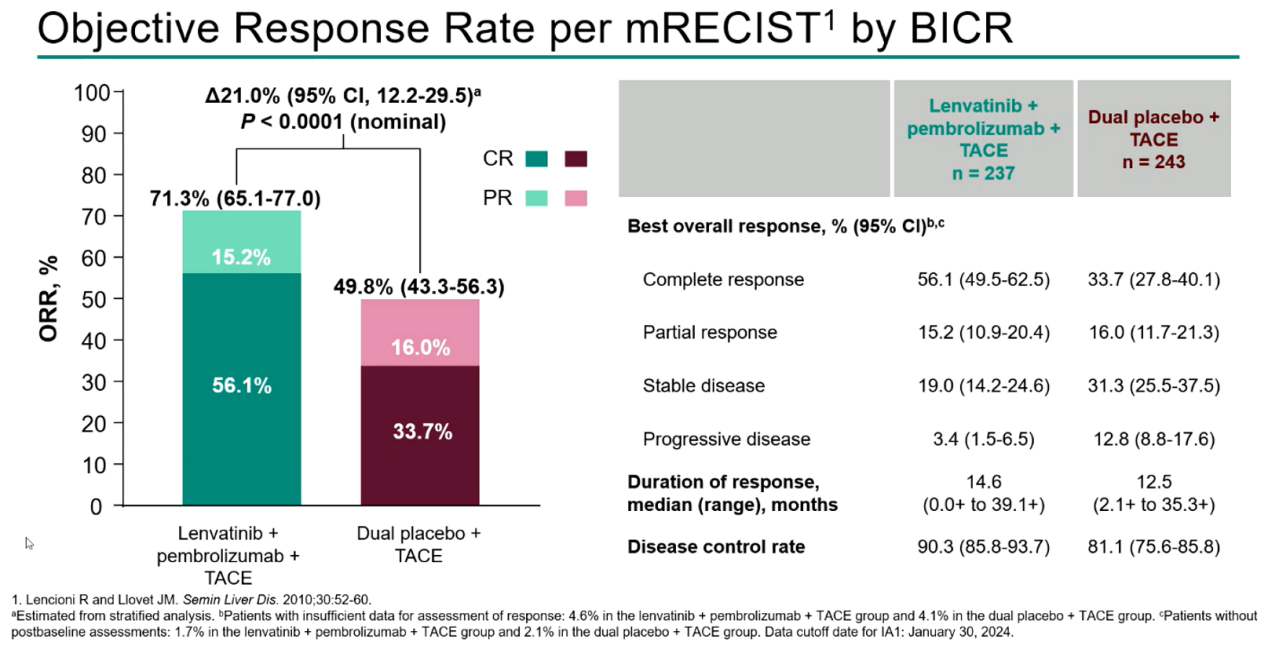 图 LEAP-012研究中基于mRECIST评估的ORR
图 LEAP-012研究中基于mRECIST评估的ORR
LEAP-012研究使我想到今年ASCO GI上公布的另一项研究,也就是EMERALD-1研究。这项研究的PFS也呈阳性[2],同样也是靶免联合TACE的III期临床研究。在这次的ESMO大会上也更新了EMERALD-1研究中根据 “up to 7 ” 标准,按肿瘤负荷基线分析了各治疗组的疗效[3]。结果显示,与仅TACE治疗相比,无论肿瘤负荷如何,“靶免+TACE”在PFS和至疾病进展时间(TTP)方面具有优势,且安全性可控,也验证了局部与系统三联疗法在不可切除HCC(uHCC)患者中的应用价值。
虽然EMERALD-1研究和LEAP-012研究均为靶免+TACE治疗,但是在药物选择上存在较大差异,EMERALD-1是用大分子抗体贝伐珠单抗联合PD-L1治疗,LEAP-012是小分子TKI联合PD-1治疗。我本人在临床实践中更倾向于选择小分子TKI联合PD-1治疗。这种治疗可选择的TKI更广泛,同时价格也更加亲民。此外,PD-1单抗的种类也较为丰富,能够根据患者的具体情况进行个性化选择。所以考虑到患者应用的因素,另外药物的效果、便利性、不良反应等等,我还是推荐这个 TKI 联合PD-1,对于这个大多数的患者是更合适。
记者:感谢两位教授的精彩分享。邵教授,您团队发起并参与了多项关键肝癌临床研究,更见证了中国学术界在全球舞台上影响力的日益壮大。今年ESMO大会上国内专家也展示了丰硕的研究成果,据此想请您分享对中国肝癌介入研究进展的看法:
中国学者在uHCC介入治疗领域探索不辍,
成果丰硕
邵海波教授:肝癌的术后辅助治疗一直是学术界探索的热点之一,而目前尚无公认有效预防肝癌复发转移的系统辅助治疗方案,存在着巨大的未被满足的临床需求。在本次ESMO会议上,有一项来自华西医院的研究探索了靶免+TACE在高危uHCC人群中辅助治疗的作用[4],在三联辅助治疗后,1年RFS超过90%。这种治疗方案对于高复发风险的患者具有显著效果。
伴有门静脉癌栓(PVTT)的HCC在临床中极大增加复发和转移风险,对于治疗方案的选择和疗效评估提出了挑战。在本次会议中另一项来自北京的研究给了我很深的印象,它利用HAIC+靶免对比单纯的靶免治疗,结果证实联合治疗可以大幅提高患者生存[5],并且三联方案的耐受较好。这项研究探索了HAIC+靶免在PVTT患者中的疗效和安全性,为门脉癌栓患者这种特殊人群提供了可借鉴的治疗方案。以上两项研究的对照组,一个研究对照组仅为介入治疗,另一研究对照组为靶免联合治疗,而治疗组均采用了局部联合靶免的治疗模式[4-5]。我们中国医生在局部联合系统治疗中积累了大量的临床经验和研究数据,这对于提高肝癌的综合治疗水平具有重要意义。
记者:感谢邵教授详细地解读本次ESMO大会上系统治疗联合局部治疗的多项报道,也让我们对肝癌在多种介入治疗基础上添加系统治疗的价值和空间有了更为深入的了解。第三个问题我想请问韩教授,如前所述,我们关注到了HCC的系统治疗已逐渐前移,此前公布了RFS的IMbrave050本次ESMO也以LBA的形式公布了它的最新结果。您可以简单和我们介绍一下吗?
IMbrave050最终结果公布,
肝癌辅助治疗任重道远
韩国宏教授:此次ESMO大会还公布了IMbrave050研究的最新结果[6]。尽管该研究的无复发生存期(RFS)阳性结果在去年的AACR大会上已经公布,但此次报告的更新数据是基于35.1个月的中位随访时间,与之前17.4个月的中位随访结果相比,RFS获益并未维持显著的统计学差异(阿替利珠单抗+贝伐珠单抗组和对照组的RFS分别为33.2个月vs 36个月,HR=0.9,95%CI 0.72-1.12)。可以看到,随着时间的推移,两条RFS生存曲线逐渐趋于重合,说明阿替利珠单抗+贝伐珠单抗的联合治疗并未使高危复发风险HCC患者在辅助治疗中获益。目前的更新结果并不支持阿替利珠单抗联合贝伐珠单抗作为所有高复发风险HCC人群的术后辅助治疗方案。
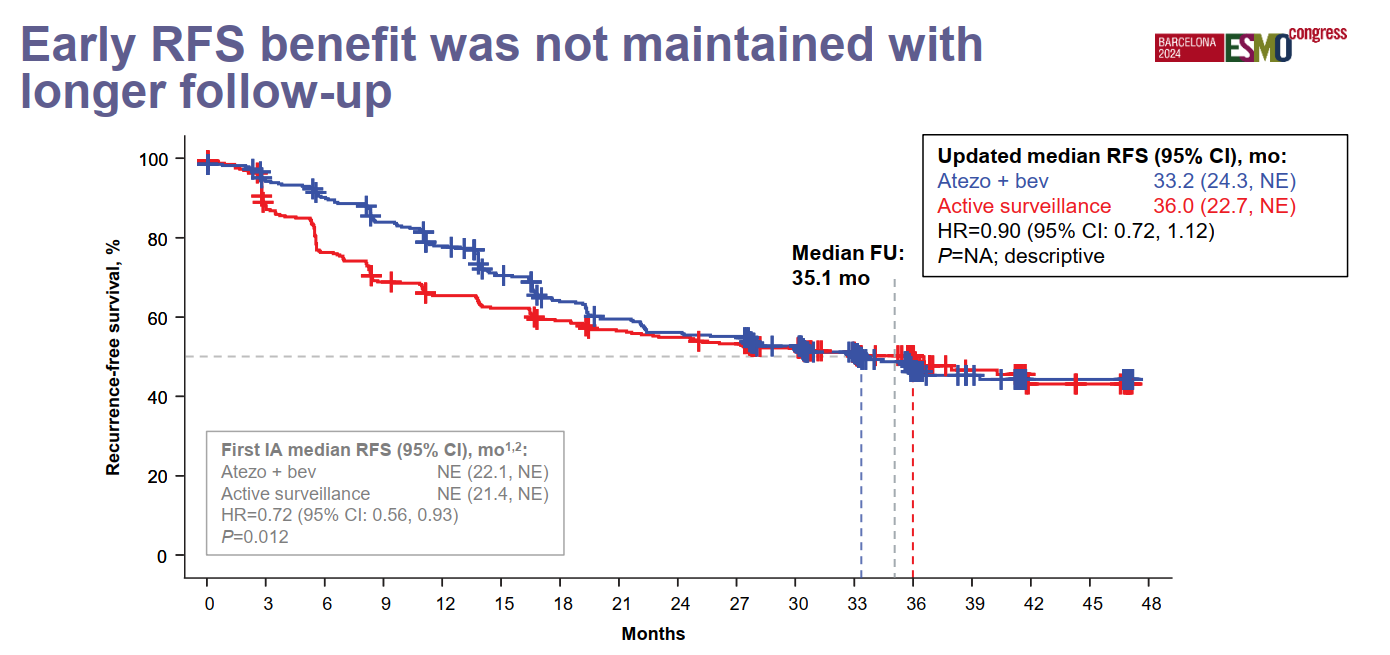 图 IMbrave050 RFS结果
图 IMbrave050 RFS结果
同样,早期的STORM研究也以失败告终[7]。这一现象再次强调了一个重要的事实,即无论是靶向治疗,还是靶向治疗联合免疫治疗,高危复发风险HCC的辅助治疗相关研究都尚未取得阳性结果。
这提醒我们,在对高复发风险的HCC患者进行手术切除前,特别是在评估其可切除性时,必须慎重决策是否实施根治性治疗。对于这类高危患者,如果在缺乏合理的系统性辅助治疗的情况下进行手术切除、消融甚至移植,可能会导致较高的复发风险,无法有效延长无复发生存期。因此,在选择这些治疗手段时,必须格外谨慎,避免患者术后陷入无药可治的境地。这也进一步强调了术前降期转化治疗的重要性,尤其针对术后容易复发的高危患者,通过降期转化治疗可以提升根治性切除的成功率,并有效降低术后复发的风险。
记者:感谢韩教授对辅助治疗的进一步深入点评,最后一个问题想请问两位教授。结合本次ESMO进展,您认为肝癌系统治疗联合局部治疗还存在哪些问题,以及您还有哪些展望和期待?
靶免联合TACE治疗在中期HCC的突破和挑战
韩国宏教授:LEAP-012研究结果的公布让我们欣喜地看到,在中期肝癌的治疗上,过去单纯依赖TACE的局面已经改变,局部治疗与靶向免疫治疗相结合的方式能显著提高疗效。然而,即便有了LEAP-012的结果,仍存在一些尚待解决的问题。
第一个问题在于,局部治疗与靶向免疫联合治疗的最佳顺序尚未明确。中国医生通常采取先行局部治疗(TACE),随后再进行靶向和免疫治疗的策略。而在LEAP-012研究中,采用了先行系统治疗的方案,即使用“可乐方案”(仑伐替尼+帕博利珠单抗)进行2-4周的治疗后,再进行TACE治疗。这种治疗顺序的差异仍需进一步研究,以明确最佳的临床应用路径。
另一个值得探讨的问题是,当局部治疗联合靶向免疫治疗后疾病进展时,下一步应如何选择治疗方案?我个人认为,在介入治疗联合靶向免疫治疗无效的情况下,应继续选择系统治疗,包括靶向治疗、或联合免疫治疗或单一的免疫治疗。而具体的药物选择可能会根据医生的个人经验和医院的条件有所不同。
最后,靶免联合TACE的疗效仍有提升空间。早期的TACE联合靶向治疗研究如SPACE和TACTICS[8-9],虽然显示出PFS的延长,但OS并未得到显著改善,因此这类方案最终未取得成功。但LEAP-012和EMERALD-1研究[1-2]提示,进一步将免疫治疗加入TACE联合靶向治疗可能带来更大程度的患者获益。
但实际上现有的TACE联合靶免治疗的疗效仍有提升空间,例如LEAP-012的中位PFS延长了4.6个月,疾病进展或死亡的风险减少了34%, 但仍然不能满足临床和患者需求,期待对这类患者的治疗效果还能进一步提高。
除了TACE,目前欧美国家对钇90治疗在肝癌局部治疗中的关注度逐渐增加。钇-90是一种局部内照射治疗,可以通过微球载钇90在肝肿瘤内进行内照射,发射β射线以最大程度地使肿瘤坏死。同时相较于TACE,钇90对周围肝实质和全身的副作用较少,患者的耐受性和体验也更好。
钇90在中国的问世给我们的中期和晚期HCC患者带来了一种新的局部治疗选择。TACE作为局部治疗有其自身优势,而钇90也具有其独特的优点。未来,钇90与靶向治疗和免疫治疗的联合是否能够进一步提升疗效,值得深入探索。
记者:感谢韩教授的真知灼见,钇90-SIRT治疗在欧美、日本等国家广泛应用于大肠癌肝转移及原发性肝癌的治疗。2022年这项技术在我国获批上市,您在临床实践中是否使用过这项新技术?请谈谈您的临床实践经验或探索方向。
钇90微球治疗在肝癌中的应用与临床探索
邵海波教授:钇90微球是一种具有放射性杀伤作用的树脂微球,其直径在30um左右。通过介入手段,在DSA设备的引导下可以精准地将钇90微球注射至肿瘤部位。由于其照射距离只有2.5mm左右,对患者身体的正常部位伤害极小,而且可以最大限度地沉积到肿瘤部位。通过术前评估的患者最大限度地保证了治疗的安全性。我们医院在2022年6月开始实行这项手术,也是东北地区首次开展这种肿瘤先进治疗技术,在结直肠癌肝转移、合并PVTT的晚期肝癌等患者中积累了较为丰富的临床经验。
结合我个人的临床体会,不同阶段的肝癌患者都可以进行钇90树脂微球治疗。早期患者能够进行根治治疗,避免手术,实现治愈目的;而中晚期患者可用钇90进行降期,缩小肿瘤增大残肝的体积,消退门静脉癌栓,为手术或肝移植争取机会;针对有高复发风险因素的肝癌患者,也可应用钇90进行辅助治疗,然后再行手术切除,降低复发风险。
曾有文献显示,钇90可激活免疫诱导[10]。去年ASCO GI大会的一项研究证实钇90联合PD-1抑制剂在预后不佳的HCC患者中取得了较好的疗效[11]。目前我们也参与了一项全国范围的多中心临床研究,这项研究是关于钇90联合靶免治疗的,期待后续有更多的数据,不断更新优化治疗策略,提高肝癌患者的生存质量。
小结
在2024年ESMO年中我们看到了肝癌领域的最新研究进展,尤其是在靶向治疗与免疫治疗联合局部治疗策略方面的突破。LEAP-012等研究成果为中期肝癌治疗提供了新的视角,进一步凸显了TACE联合靶免治疗成为标准临床方案的潜力。同时,中国专家在这一领域是在全球超前,且持续地做着探索。通过局部与系统治疗的联合,不断积累了大量临床证据,进一步强化了这一治疗模式的应用价值。尽管目前取得了显著成果,肝癌治疗仍然面临诸多挑战,如患者分层异质性以及有效的生物标志物的缺乏等。未来的研究将继续致力于优化治疗方案,并推动多学科协作,进一步提高肝癌患者的预后与生活质量。
[1] Transarterial chemoembolization (TACE) with or without lenvatinib (len) + pembrolizumab (pembro) for intermediate-stage hepatocellular carcinoma (HCC): Phase III LEAP-012 study. 2024 ESMO LBA3.
[2] Riccardo Lencioni,et al. EMERALD-1: A phase 3, randomized, placebo-controlled study of transarterial chemoembolization combined with durvalumab with or without bevacizumab in participants with unresectable hepatocellular carcinoma eligible for embolization.. 2024 ASCO GI, Abs LBA432.
[3] Outcomes by baseline tumour burden in EMERALD-1: A phase III, randomised, placebo (PBO)-controlled study of durvalumab (D) ± bevacizumab (B) with transarterialchemoembolisation (TACE) in participants (pts) with embolisation-eligible unresectable hepatocellular carcinoma (uHCC). 2024 ESMO 950P.
[4] Tislelizumab plus donafenib combined with transarterial chemoembolization in patients with resected high-risk hepatocellular carcinoma (TIDE): A prospective, single-arm, phase II trial. 2024 ESMO 976P.
[5] HAIC combined with lenvatinib and PD-1 inhibitors versus lenvatinib plus PD-1 inhibitors for advanced HCC with portal vein tumor thrombosis: A prospective controlled trial. 2024 ESMO 968P.
[6] Updated efficacy and safety data from IMbrave050: Phase III study of adjuvant atezolizumab (atezo) + bevacizumab (bev) vs active surveillance in patients (pts) with resected or ablated high-risk hepatocellular carcinoma (HCC).2024 ESMO LBA39.
[7] Bruix J, Takayama T, Mazzaferro V, et al. Adjuvant sorafenib for hepatocellular carcinoma after resection or ablation (STORM): a phase 3, randomised, double-blind, placebo-controlled trial[J].Lancet Oncol, 2015, 16(13): 1344-1354.
[8] Chen, X., Xu, H., Chen, X. et al. First-line camrelizumab (a PD-1 inhibitor) plus apatinib (an VEGFR-2 inhibitor) and chemotherapy for advanced gastric cancer (SPACE): a phase 1 study. Sig Transduct Target Ther 9, 73 (2024).
[9] Kudo M, Ueshima K, Ikeda M, et al. Randomised, multicentre prospective trial of transarterialchemoembolisation (TACE) plus sorafenib as compared with TACE alone in patients with hepatocellular carcinoma:TACTICS trial[J]. Gut, 2020, 69(8):1492-1501.
[10] Licia R, et al. Gut, 2022 May 4;gutjnl-2021-326869.
审批编号:MI-PD1-6524-CN
过期日期:31 Jul 2025
本资讯由默沙东医学团队提供,旨在用于医学专业人士间的学术交流,请勿随意转发或转载。文中相关内容不能以任何方式取代专业的医疗指导,也不应被视为治疗建议。医学专业人士对文中提到的任何药品进行处方时,请严格遵循该药品在中国批准使用的说明书。默沙东不承担相应的有关责任。
排版编辑:肿瘤资讯-niko











 苏公网安备32059002004080号
苏公网安备32059002004080号


