盐酸吉卡昔替尼片(简称吉卡昔替尼,曾用名"盐酸杰克替尼片")是一种新型的JAK和ACVR1抑制剂,其不仅能通过抑制JAK1、JAK2、JAK3和TYK2活性阻断JAK-STAT信号转导通路,从而缓解炎症和脾大症状,还能通过抑制ACVR1活性降低铁调素转录,从而改善铁代谢失衡和贫血。Ⅱ、Ⅲ期临床试验数据提示,吉卡昔替尼既能改善JAK抑制剂初治或芦可替尼经治的骨髓纤维化(MF)患者脾大、体质性症状,也能改善MF患者的贫血。文章就吉卡昔替尼治疗MF的作用机制、药代动力学特点、临床疗效及治疗相关不良反应等方面进行阐述,为该药在MF中的合理应用提供参考。
骨髓纤维化(MF)是一种BCR::ABL1阴性的骨髓增殖性肿瘤(MPN),患者主要临床特征为骨髓纤维组织增生、进行性脾大、伴有疾病相关的体质性症状以及出现不同程度的外周血细胞计数异常,并存在发生白血病转化的可能。MF的治疗决策主要依据患者的预后分组和临床症状。相较于西方人群,我国MF患者合并贫血的情况更常见(66.5%比35.2%)。针对这一问题,目前国内的治疗方案仍停留在传统的输血、雄激素、糖皮质激素、促红细胞生成素和免疫调节剂等,但上述方案均存在不良反应多、疗效有限和缓解持续时间短等问题。随着靶向药物的不断研发,有越来越多的酪氨酸激酶JAK抑制剂(JAKi)被应用到MF的治疗中。较早上市的两种JAKi药物(芦可替尼和fedratinib)对治疗脾大和改善体质性症状有较好效果,但是都存在贫血、血小板减少等血液学不良反应,长期使用可导致患者不耐受。芦可替尼是目前唯一在我国获批用于治疗MF的JAKi,但上市前的临床研究数据显示,其用于治疗我国MF患者的3~4级贫血发生率达47.6%,其药物不耐受情况逐渐受到关注。芦可替尼治疗失败后患者的中位生存期较短,范围为6个月至2年不等,这部分患者的预后有待进一步提升。然而芦可替尼停药后常规挽救性治疗的缓解率只有26%,国外获批的fedratinib、pacritinib和momelotinib均可作为二线治疗药物,但目前国内可供二线治疗选择的JAKi仍为空白。
盐酸吉卡昔替尼片(简称吉卡昔替尼,曾用名"盐酸杰克替尼片")是一种新型JAK和ACVR1抑制剂,目前已完成了关于该药治疗MF有效性和安全性的3项Ⅱ期临床试验(ZGJAK002、ZGJAK006和ZGJAK017)和1项Ⅲ期临床试验(ZGJAK016)( 表1 )。已报道的临床试验结果表明,该药可改善MF患者的脾大、体质性症状和贫血,且耐受性良好。本文介绍了吉卡昔替尼治疗MF的作用机制、药代动力学特点、临床疗效及治疗相关不良反应等,旨在为吉卡昔替尼的临床应用提供依据。

1 吉卡昔替尼的药理学特征
1.1 吉卡昔替尼治疗MF的作用机制
吉卡昔替尼通过抑制JAK1、JAK2、JAK3和TYK2活性,阻断STAT蛋白的磷酸化、二聚化和核转位,进而抑制STAT蛋白的转录调控活性,缓解炎症和脾大症状,抑制相关疾病的发生和发展。吉卡昔替尼通过抑制ACVR1活性下调铁调素表达,改善铁代谢失衡,增加血红蛋白,从而减少MF患者贫血发生和输血依赖。有研究表明,原发性骨髓纤维化(PMF)患者比健康对照者循环铁调素和促炎细胞因子水平均升高。促炎细胞因子白细胞介素6(IL-6)水平的升高会导致铁调素水平升高,引起功能性铁缺乏。IL-6与肝细胞膜上的受体结合,诱导JAK1/2磷酸化STAT3激活铁调素转录,并且需要BMP6-ACVR1-SMAD信号通路的参与。同样为JAKi的芦可替尼和momelotinib都表现出对于IL-6-JAK-STAT3通路的抑制,但芦可替尼并不作用于BMP6-ACVR1-SMAD,故不具备调节铁调素的作用。吉卡昔替尼也可通过影响BMP6-AVCR1-SMAD和IL-6-JAK-STAT3信号通路,阻断铁调素的生成,增加循环系统中的铁和血红蛋白,刺激红细胞生成,改善贫血。在Ⅱ、Ⅲ期临床试验中,吉卡昔替尼均有改善患者输血依赖、减少患者输血需求和提高患者血红蛋白水平的作用 。
1.2 吉卡昔替尼的药代动力学特点
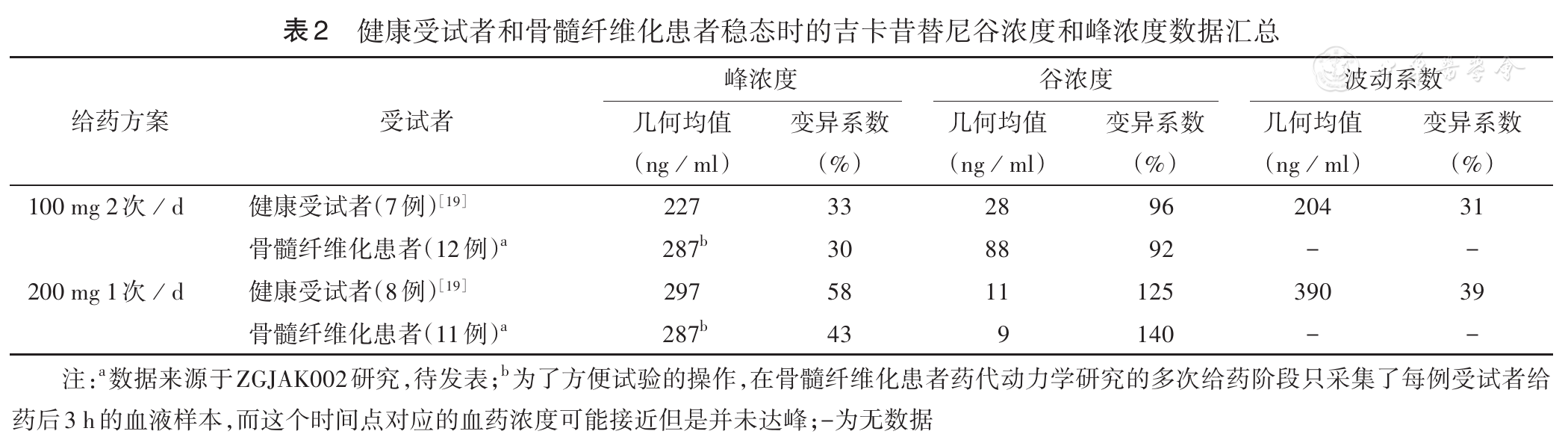
健康受试者和MF患者(数据来源于ZGJAK002研究,待发表)单次口服100 mg吉卡昔替尼后,在2~3 h时达到最大血药浓度。2次/d给药的峰浓度和谷浓度之间的波动较1次/d给药减小。食物对吉卡昔替尼的药代动力学影响较大,高脂标准餐可明显增加吉卡昔替尼的吸收,血浆暴露量(血浆药物浓度-时间曲线下面积)增加了160%,峰浓度增加了128%,所以,为了获得稳定的药物暴露,建议患者空腹状态下服药。吉卡昔替尼主要通过细胞色素P450 3A4酶(CYP3A4)代谢消除,少量由CYP1A2代谢,因此,在与强效CYP3A4抑制剂合用时,需适当减少吉卡昔替尼的给药剂量。在MF患者中吉卡昔替尼的平均清除半衰期约为3 h。吉卡昔替尼主要(73.9%)通过粪便排出体外,少量(25.2%)从尿液排出。如果患者存在轻、中度肝功能损伤,建议适当减少给药剂量;对于重度肝功能损伤患者,不建议使用吉卡昔替尼。
2 吉卡昔替尼治疗MF的临床数据
2.1 临床治疗推荐剂量
在健康受试者 和MF患者(数据来源于ZGJAK002研究,待发表)中的药代动力学研究均显示,吉卡昔替尼100 mg 2次/d给药方式相比200 mg 1次/d具有更高的药物谷浓度和较低的药物峰浓度,峰浓度和谷浓度之间波动的减小有利于药物更长时间发挥作用( 表2 )。在吉卡昔替尼Ⅱ期临床试验(ZGJAK002)中100 mg 2次/d组治疗24周时达到脾脏响应[脾脏体积较基线缩小≥35%(SVR35)]的患者比例达到54.8%,高于200 mg 1次/d组的31.3%,且组间差异具有统计学意义( P=0.019 9)。因此,推荐吉卡昔替尼100 mg 2次/d作为后续临床试验给药方案。
2.2 脾脏体积缩小和体质性症状改善情况
2.2.1 JAKi初治的MF患者
Ⅲ期临床试验ZGJAK016是一项随机、双盲、双模拟平行对照、多中心研究,比较吉卡昔替尼与羟基脲治疗中高危MF患者的有效性和安全性。期中分析显示,吉卡昔替尼组(47例)治疗24周时SVR35患者比例高于羟基脲组(23例),分别为72.3%、17.4%( P≤0.000 1)( 表1 )。对两组合计至少21例的亚组进行分析显示,在各亚组中吉卡昔替尼的脾脏有效率均高于羟基脲,各亚组分析结果趋势一致,且与主要分析结果趋势一致;无论是否存在JAK2 V617F突变,吉卡昔替尼的缩脾疗效均好于羟基脲。研究期间,吉卡昔替尼组80.9%的患者至少出现1次SVR35,羟基脲组为26.1%( P≤0.000 1)。两组分别有30例(63.8%)和10例(43.5%)达到MF相关症状总评分下降≥50%(TSS50)。
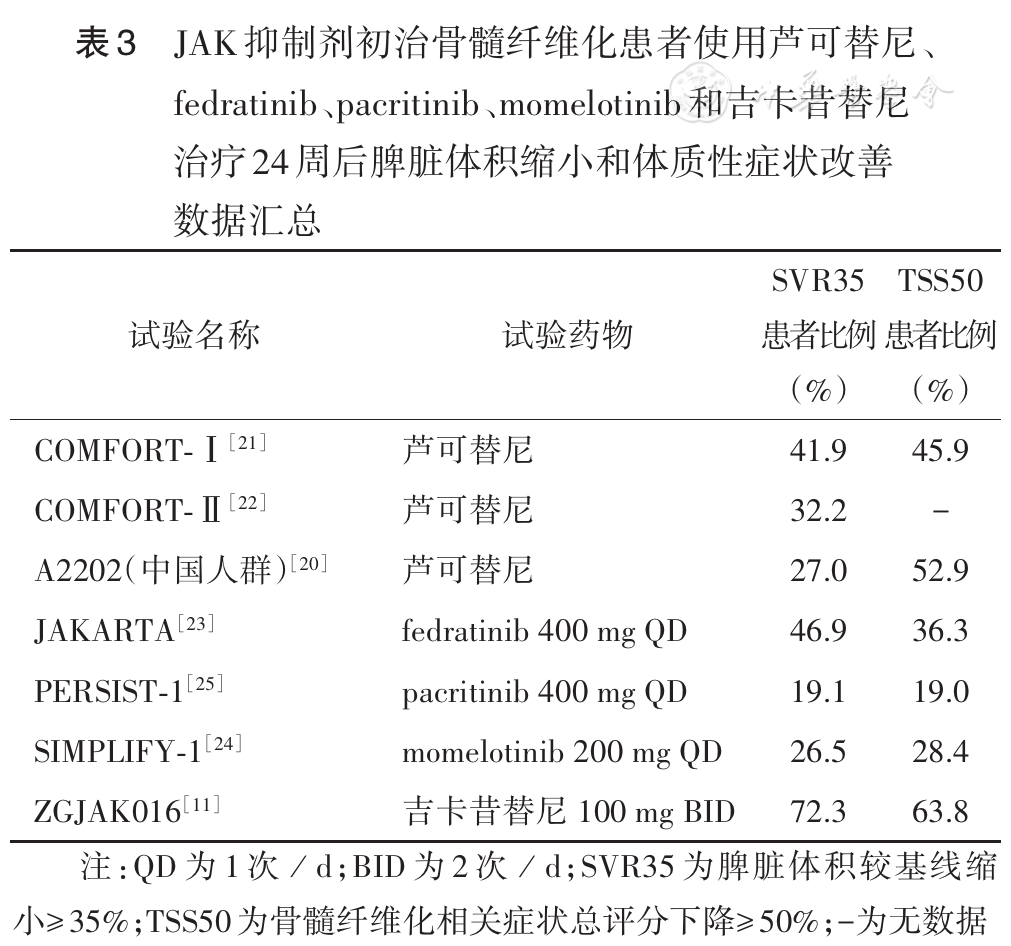
芦可替尼治疗欧美和我国MF患者的24周SVR35患者比例分别为41.9%(COMFORT-Ⅰ研究)、32%(COMFORT-Ⅱ研究)和27.0%[A2202研究(中国人群)],24周TSS50患者比例分别为45.9%(COMFORT-Ⅰ研究)和52.9%[A2202研究(中国人群)]。芦可替尼、fedratinib、pacritinib、momelotinib和吉卡昔替尼治疗24周的SVR35和TSS50结果汇总见 表3 。总体上,吉卡昔替尼在改善脾脏大小和体质性症状方面的结果与其他JAKi相当或更佳。
Ⅱ期临床试验ZGJAK002的长期随访数据(中位随访时间30.7个月)显示,吉卡昔替尼在JAKi初治MF患者中,100 mg 2次/d组74.2%的患者治疗持续超过48周,48周SVR35患者比例为60.9%,中位最佳脾脏体积缩小百分比为49.7%,50.4%的患者脾脏响应持续时间(DoMSR)超过120周;108周时有74.2%的患者达到TSS50。芦可替尼在我国MF患者中的48周SVR35患者比例为39.7%,中位最佳脾脏体积缩小百分比为34.7%。COMFORT-Ⅰ研究3年随访数据显示,芦可替尼治疗组DoMSR达到132周的概率为53.0%。可见,在我国MF患者中,吉卡昔替尼疗效持久,且治疗48周的脾脏响应结果可能较芦可替尼更佳。
2.2.2 JAKi治疗失败的MF患者
ZGJAK006是一项单臂、开放、多中心Ⅱ B期临床研究,共纳入44例芦可替尼治疗不耐受(接受芦可替尼治疗≥28 d,在芦可替尼治疗期间仍需红细胞输注或输注频率增加,或发生≥3级血小板计数降低、贫血或血肿/出血)的MF患者接受吉卡昔替尼100 mg 2次/d治疗,24周SVR35和TSS50患者比例分别为43.2%和61.8% ( 表1 )。ZGJAK017是一项单臂、开放、多中心Ⅱ期临床研究,共纳入34例芦可替尼难治、复发(难治定义:接受芦可替尼治疗累计≥3个月,磁共振成像(MRI)/CT检查显示与服用芦可替尼前比较,脾脏体积缩小<10%,或触诊较服用芦可替尼前脾脏体积缩小<30%;复发定义:接受芦可替尼治疗累计≥3个月,同服用芦可替尼前比较,脾脏响应后,再次增大,即较服用芦可替尼前,脾脏体积缩小<10%,或触诊脾脏体积缩小<30%)的MF患者接受吉卡昔替尼100 mg 2次/d治疗,24周SVR35和TSS50患者比例分别为32.4%和46.4%( 表1 )。fedratinib、pacritinib、momelotinib和吉卡昔替尼用于治疗芦可替尼耐药或不耐受患者的24周SVR35和TSS50数据汇总见 表4。对于二线治疗而言,吉卡昔替尼的缩脾和症状改善情况与fedratinib相当或略好。一项回顾性研究显示,重新服用芦可替尼能带来一定临床获益,但服用剂量需>10 mg 2次/d,这对于首次治疗不耐受患者而言较难实现。综上,对于芦可替尼治疗失败的患者来说,吉卡昔替尼可能是优先级较高的候选药物。
 2.3 贫血改善情况
2.3 贫血改善情况
Ⅲ期临床试验ZGJAK016中,吉卡昔替尼治疗2周后,MF患者血红蛋白水平相对基线出现升高,并稳定持续至24周;治疗24周内吉卡昔替尼组基线输血依赖的4例患者中有1例转化为非输血依赖,而羟基脲组基线输血依赖的3例患者均未转化为非输血依赖;治疗24周内吉卡昔替尼组基线非输血依赖且血红蛋白≤100 g/L治疗后血红蛋白升高≥20 g/L的患者比例较高(39.3%比15.4%),红细胞输注量较基线下降≥50%患者的比例也相对较高(71.4%比40.0%)。
Ⅱ期研究(ZGJAK002、ZGJAK006和ZGJAK017)中的89例接受100 mg 2次/d治疗且基线血红蛋白<正常范围低值的贫血改善目标人群(24周内基线输血依赖转化为非输血依赖,或基线非输血依赖且血红蛋白≤100 g/L治疗后血红蛋白升高≥20 g/L)的治疗数据表明,共34例(38%)在24周内达到贫血改善。其中33例(43%)基线非输血依赖且血红蛋白≤100 g/L的患者用药后24周内血红蛋白升高≥20 g/L,1例(8%)基线输血依赖患者治疗24周内转化为非输血依赖 。Ⅱ期ZGJAK002研究JAKi初治患者长期随访结果显示,长期药物暴露情况下接受100 mg 2次/d治疗患者的血红蛋白水平稳定,治疗后48、72、96、108、120周较基线升高的均值分别为4.8、9.1、6.9、6.1、8.7 g/L 。
在欧美MF人群中,芦可替尼治疗患者的血红蛋白水平在8~12周时较基线下降最多,下降达10 g/L左右,随后虽略有回升,但仍较基线下降5 g/L左右。近期,PERSIST-2研究更新数据显示,与最佳可用治疗组相比,pacritinib治疗组在24周时输血需求量较基线下降≥50%患者的比例大幅降低(9%比49%)。在MOMENTUM研究中,与达那唑组相比,momelotinib组基线非输血依赖治疗后血红蛋白升高≥20 g/L患者比例高(41.2%比30.0%)。由于国内外输血情况和各研究所采用的贫血改善评估标准存在差异,不同试验结果之间的比较需谨慎,仅从提高血红蛋白水平和改善输注负荷的情况看,吉卡昔替尼与pacritinib和momelotinib的表现相似。对我国642例PMF患者的流行病学调查结果显示,我国PMF患者较西方患者血红蛋白水平<100 g/L的比例更高(66.5%比35.2%, P<0.001),并且国内对同种异体输血指征的管理相对严格,输血率低,因此针对MF患者的贫血改善治疗迫切性高。目前,国内暂无既能改善脾脏大小和体质性症状又能改善贫血的药物,吉卡昔替尼可能会给国内MF患者带来更多的获益。
2.4 生存获益
Ⅱ期临床试验ZGJAK002的长期随访数据显示,中位总生存(OS)和无白血病生存(LFS)时间均未达到,12、24、36个月的LFS率分别为94.8%、90.6%和84.1%,12、24、36个月的OS率依次为92.3%、85.8%和78.2%。COMFORT-Ⅱ研究3年随访数据显示,芦可替尼组144周的OS率为81%。可见,吉卡昔替尼在我国人群中的生存获益结果与芦可替尼在欧美人群中的结果相当。
2.5 安全性评价
Ⅲ期临床试验的安全性数据显示,吉卡昔替尼组和羟基脲组的常见血液学不良事件为贫血(25.5%比43.5%)、血小板计数降低(17.0%比39.1%)、白细胞计数降低(2.1%比21.7%)、中性粒细胞计数降低(2.1%比21.7%)和淋巴细胞计数降低(2.1%比13.0%)。常见的非血液学不良事件为上呼吸道感染(21.3%比21.7%)、血胆红素升高(12.8%比26.1%)、发热(12.8%比21.7%)和腹泻(10.6%比21.7%),其中绝大部分是1~2级。从感染数据来看,Ⅲ期吉卡昔替尼临床试验目前公布的数据中最常见的感染是上呼吸道感染(发生率21.3%,≥3级发生率0),其中仅2.1%考虑与研究药物相关,上呼吸道感染发生率与芦可替尼中国人群相关研究中的发生率相当(20.6%,≥3级发生率4.8%)。考虑到Ⅲ期吉卡昔替尼研究处于全球新冠病毒大流行期间,吉卡昔替尼上呼吸道感染不良事件可能受新冠病毒影响有所增加。其他JAKi相关不良事件目前暂无中国人群数据。基于各自的美国食品药品监督管理局(FDA)说明书,fedratinib最常见的感染是尿路感染(6%,≥3级发生率0),parcitinib最常见的感染是上呼吸道感染(10%,≥3级发生率0),momelotinib最常见的感染是细菌感染(15%,≥3级发生率8%)。吉卡昔替尼组导致永久停药的不良事件发生率为8.5%,羟基脲组为17.4% 。Ⅱ期ZGJAK002研究吉卡昔替尼100 mg 2次/d组随访30.7个月的数据表明,随着治疗时间的延长,常见的不良反应谱未超过研究前期分析的结果,导致治疗终止的不良事件发生率为11.9%,常见的≥3级与研究药物相关的不良事件(发生率≥10%)包括贫血(15.2%)、血小板计数降低(15.2%)和感染性肺炎(10.6%)。芦可替尼在我国MF患者中导致治疗终止的不良事件发生率为9.5%,≥3级贫血的发生率为33.3%;随访1年的更新数据显示,导致治疗终止的不良事件发生率为14.3%,≥3级贫血的发生率为47.6%。可见,吉卡昔替尼治疗中≥3级贫血的发生率低于芦可替尼,导致治疗终止的不良事件发生率也较低。此外,momelotinib治疗中频发的周围神经病(发生率10.3%)、fedratinib和pacritinib治疗中频发的腹泻(发生率>50%)在吉卡昔替尼治疗过程中的发生频率均相对较低(4.5%、16.7%)。有研究显示,在使用JAK1/2抑制剂治疗MF期间发生了B细胞非霍奇金淋巴瘤(发生率5.8%)。目前30.7个月的随访数据暂未显示吉卡昔替尼用药暴露与该继发性肿瘤发生率相关,仍需更长时间随访观察其与继发肿瘤的相关性 。
3 总结与展望
Ⅱ、Ⅲ期临床试验结果表明,吉卡昔替尼应用于JAKi初治和芦可替尼经治MF患者均具有显著的有效性和良好的安全性,并在改善贫血方面有一定的优势。长期随访数据显示,吉卡昔替尼长期治疗可持续缩小脾脏和改善体质性症状并且不良反应可控。现有的临床数据提示吉卡昔替尼有望成为对我国MF患者有效性和耐受性佳、可及性好的本土创新药,同时临床长期使用时应注意感染的发生。此外,吉卡昔替尼在MF中的应用也存在如下尚待研究的问题。首先,尚无吉卡昔替尼与芦可替尼头对头比较的随机对照研究数据,未来临床实践中如何选择JAKi一线治疗方案仍有待进一步探讨。目前,国际上新一代的JAKi,即fedratinib、pacritinib和momelotinib都在探索各自适用的人群,为MF的治疗增加更多选择。其次,芦可替尼治疗失败的定义主要见于新药临床研究,尚未达成共识,且JAKi二线治疗的时机也有待明确。最后,吉卡昔替尼与其他治疗手段的联合应用,以及能否应用于其他MPN和其他血液肿瘤均有待更多探索。
张仪,周虎,肖志坚,等. 盐酸吉卡昔替尼片在骨髓纤维化治疗中的应用[J]. 白血病·淋巴瘤,2024,33:(07):392-398.DOI:10.3760/cma.j.cn115356-20240421-00054.











 苏公网安备32059002004080号
苏公网安备32059002004080号


