本期精选7篇在2024年1~3月发表的头颈部肿瘤治疗领域文章。邀请厦门大学附属第一医院吴三纲教授进行深入解读。
厦门大学附属第一医院 肿瘤放疗科 行政副主任
福建省医学会肿瘤放射治疗分会头颈组副组长
福建省医学会肿瘤放射治疗分会青年委员会副主任委员
福建省抗癌协会鼻咽癌专业委员会青年委员会副主任委员
《Frontiers in Oncology》Associate editor
厦门市第三批青年创新人才
福建省高层次人才(C类)
第一完成人获多个省市科技奖
累计发表超过100篇SCI论文
1.KEYNOTE-412研究:一项比较帕博利珠单抗与安慰剂联合同步放化疗治疗LA SCCHN的疗效及安全性的随机、双盲III期临床试验显示,帕博利珠单抗联合放化疗(CRT)未改善主要终点无事件生存期(EFS)
2.一项多中心回顾性研究数据显示R/M SCCHN患者一线西妥昔单抗治疗进展后二线西妥昔单抗再挑战可获得良好生存数据,提示西妥昔单抗治疗再挑战可能是一线西妥昔单抗治疗进展后患者的有效治疗方案
3.一项真实世界回顾性研究提示西妥昔单抗联合PD-1抑制剂可作为免疫检查点抑制剂(ICI)难治性R/M-SCCHN患者的挽救治疗方案
4.一项回顾性分析评估每周一次PCC(紫杉醇、卡铂和西妥昔单抗)方案治疗ICI进展后R/M SCCHN的疗效,结果显示PCC方案是ICI治疗进展后较为有效的二线治疗方案
5.全球多中心III期临床研究(XRay Vision)正在探索Xevinapant+RT辅助治疗术后高危铂不耐受LA-SCCHN患者的疗效及安全性,期待其进一步改善患者生存
KEYNOTE-412:
帕博利珠单抗联合同步放化疗相对于安慰剂联合同步放化疗未改善LA SCCHN患者EFS 1
KEYNOTE-412是一项在新诊断、病理学证实、未手术的局部晚期头颈鳞癌患者中比较帕博利珠单抗或安慰剂与CRT联合疗效差异的随机、III期临床研究。共纳入了全球130个医疗中心的804例新确诊高危不可切除LA-SCCHN。按1:1的比例将患者随机分至帕博利珠单抗200mg联合同步放化疗(CRT)组或安慰剂联合CRT组(图1)。分层因素包括研究者选择的放疗方案、肿瘤部位、p16状态与疾病分期。研究中,帕博利珠单抗与安慰剂均为IV Q3W最多17次(CRT前1次,CRT期间2次,维持治疗14次);CRT包括顺铂100mg/m2 IV Q3W 2-3次,并进行加速分割或标准分割放疗(均为35次,每次70Gy)。主要终点为EFS,次要终点为总生存期(OS)和安全性。
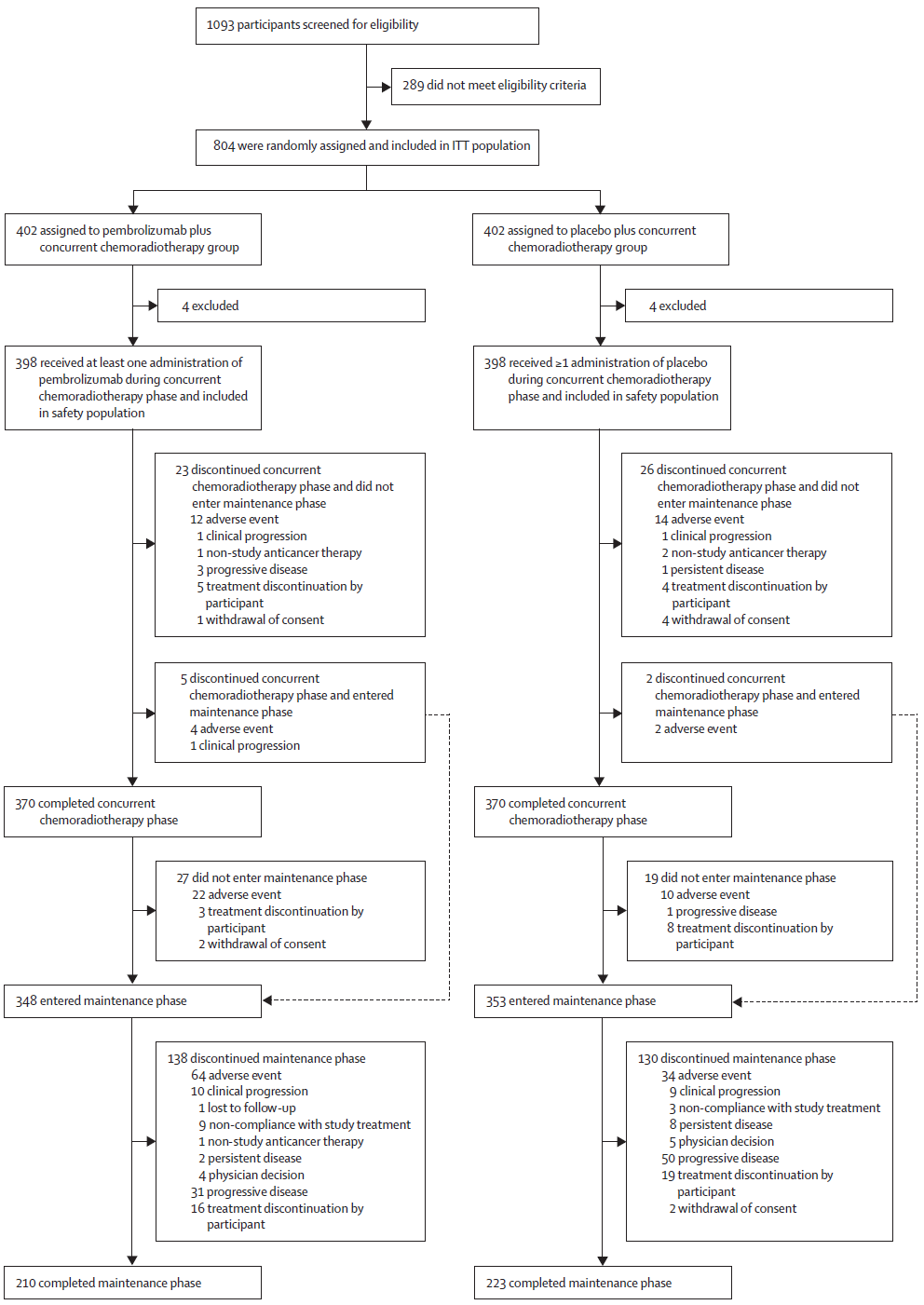
图1. 患者入组流程图
在2017年4月19日至2019年5月2日期间,804例参与者被随机分配到帕博利珠单抗组(n=402)或安慰剂组(n=402)。804例参与者中,男性660例(82%),女性144例(18%),白人622例(77%)。中位随访时间为47.7个月(IQR 42.1 ~ 52.3)。研究结果显示两组中位EFS无显著差异:帕博利珠单抗组vs安慰剂组的中位EFS:未达到 vs 46.6个月(HR=0.83; 95%CI:0.68-1.03; log-rank P=0.043, 显著性阈值P≤0.024)(图2);意向性分析人群中,两组3年OS率分别为72% 与 70%(HR=0.90, 95%CI:0.71-1.15)(图3A);在PD-L1 CPS ≥1的亚组中,两组3年OS率分别为71% 与 70%(HR=0.87, 95%CI:0.67-1.13)(图3B)。截至最终分析时,帕博利珠单抗组和安慰剂组分别有37%和41%的患者发生远处转移或死亡。
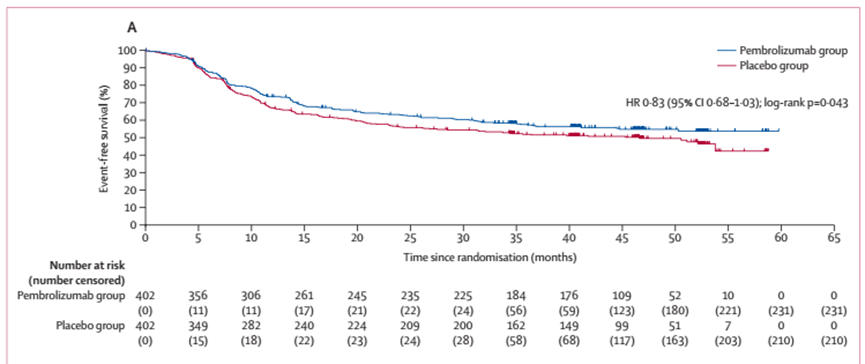
图2. KEYNOTE-412研究EFS结果
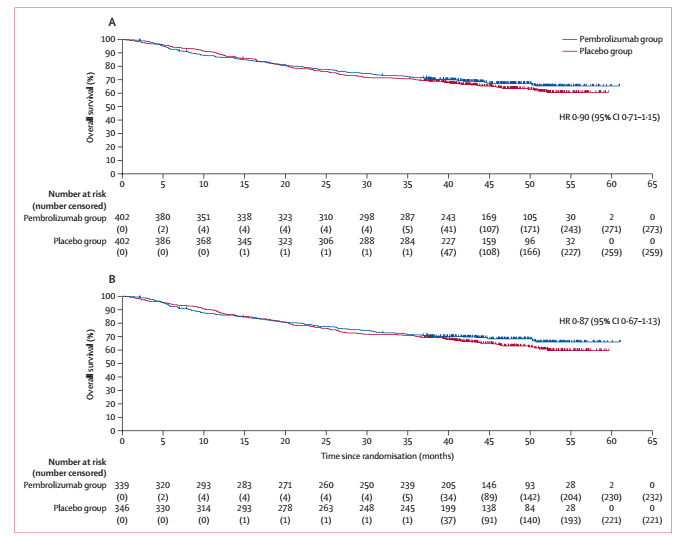
图3. KEYNOTE-412研究OS结果,A.ITT人群OS,B. PD-L1 CPS ≥1亚组OS
安全性方面,帕博利珠单抗组与安慰剂组的≥3级不良反应(AE)发生率分别为92%与88%,最常见的≥3级AE为中性粒细胞计数减少(27%/25%)、口腔炎(20%/17%)、贫血(20%/15%)、吞咽困难(19%/16%)和淋巴细胞计数减少(19%/20%)。两组严重不良事件(SAE)发生率分别为62%与49%,最常见的为肺炎(11%/6%)、急性肾损伤(8%/8%)、发热性中性粒细胞减少(6%/2%)。导致死亡的治疗相关AE分别为4例(1%)与6例(2%)。
在新诊断的未进行分子选择的LA-SCCHN患者中,帕博利珠单抗加CRT相对于单独CRT并没有显著提高无事件生存率,同时没有观察到新的安全性事件。LA-SCCHN仍然是一种具有挑战性的疾病,需要更好的治疗方法。
吴三纲教授:
高剂量顺铂联合放疗是LA-SCCHN的标准治疗方案,但疗效仍有待于进一步提升,需进一步更优的治疗方案。近年来,多种ICI在R/M-SCCHN中的疗效已经获得肯定,而在CRT或根治性放疗中加用ICI能否为LA-SCCHN患者带来获益成为近年来的研究热点之一。
既往多项研究在LA-SCCHN患者中探索了ICI联合放疗(RT)或CRT的疗效,均未改变目前的临床实践。GORTEC 2015-01 PembroRad研究比较了LA-SCCHN患者采用帕博利珠单抗联合RT与西妥昔单抗联合RT的疗效和安全性,结果显示,两组患者在15个月内的局部控制率(LRC)无统计学差异。NRG-HN004研究则比较了在不适宜顺铂治疗的LA-SCCHN患者中RT联合度伐利尤单抗 vs. RT联合西妥昔单抗的疗效,结果显示,两组患者无进展生存期(PFS)无统计学差异。JAVELIN Head and Neck 100研究评估了阿维鲁单抗(avelumab)联合CRT与单独使用CRT治疗LA-SCCHN患者的抗肿瘤活性,免疫联合治疗未改善PFS及OS结果。GORTEC 2017-01/REACH研究探讨了在不耐受顺铂类治疗的LA-SCCHN患者中,西妥昔单抗+ RT的基础上增加免疫治疗虽然延长了PFS,但未能达到统计学差异,可以降低远处转移发生率但未能转化为OS获益,由于含阿维鲁单抗组未获得阳性结果,JAVELIN Head and Neck 100研究和GORTEC 2017-01 REACH研究适合顺铂治疗队列被终止。另外,UPCI-15-132研究比较了帕博利珠单抗+CRT同步治疗与序贯治疗的疗效及安全性,结果发现,两组4年LRC率分别为64% vs 95%,4年PFS率分别为49% vs 67%,4年OS率分别为71% vs 83%,帕博利珠单抗+CRT序贯治疗的获益趋势更为明显。
本项KEYNOTE-412结果显示,CRT联合帕博利珠单抗与CRT联合安慰剂组相比,EFS无显著差异(HR=0.83; 95%CI:0.68-1.03; log-rank P=0.043, 显著性阈值P≤0.024)。安全性方面,在帕博利珠单抗组中,更多的患者因为AE而中断治疗,这可能是影响EFS的原因之一。另外,KEYNOTE-412研究事后分析显示CPS≥20人群可能是免疫联合放疗的优势人群。这提示着,改变治疗策略进一步提升免疫治疗的效果以及更好地筛选出免疫治疗获益人群具有十分重要的意义。
总体而言,LA SCCHN的治疗仍然非常具有挑战性。目前的标准治疗方案未改变,依然是高剂量顺铂联合放疗,对于铂不耐受的患者SoC为西妥昔单抗联合放疗。在头颈鳞癌探索日益活跃的今天,希望通过联合各种有效的治疗手段,进一步提升头颈部鳞癌患者的生存获益,改善预后,例如免疫联合不同靶向药物(包括联合EGFR单抗、EGFR-TKI、VEGFR抑制剂、LAG-3抑制剂、IDO抑制剂等)。PD-L1表达与临床预后的关系、不同治疗方案的评估,以及用于预测治疗反应和判断预后的生物标记物等均值得未来更多探索。另外,IAP抑制剂可增强RT及CRT疗效,既往II期xevinapant研究数据提示IAP联合CRT可显著改善患者的5年生存率,可能改变LA-SCCHN患者的SoC,期待其III期Trilynx研究数据披露。
R/M SCCHN患者一线西妥昔单抗治疗进展后二线西妥昔单抗再挑战获得良好生存2
目前R/M SCCHN患者预后较差,西妥昔单抗是一种作用于表皮生长因子受体(EFGR)的IgG1单克隆抗体。既往研究表明,西妥昔单抗可以显著延长患者生存期并改善治疗反应。近年来,进展后继续治疗(treatment beyond progression,TBP)已被普遍用于抗癌治疗,研究表明在疾病进展后继续使用分子靶向药物对预后有利。然而,目前尚不了解R/M SCCHN患者经过一线治疗(包含西妥昔单抗)进展后继续使用西妥昔单抗的疗效。本研究是一项多中心回顾性研究,旨在评估西妥昔单抗进展后TBP在R/M SCCHN患者中的作用。研究结局包括西妥昔单抗治疗至停药时间(TTD)、无进展生存期2(PFS2:从西妥昔单抗使用的第一天至二线治疗进展后或最后随访日),OS,客观缓解率(ORR),疾病控制率(DCR)。
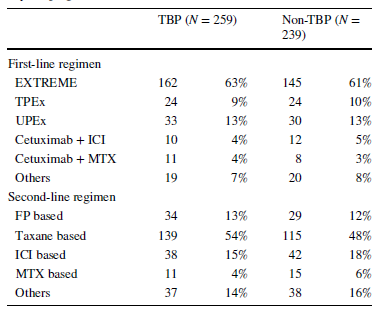
本研究共纳入498例患者,其中TBP组259例,非TBP组239例。两组患者最常用的一线化疗方案均为EXTREME方案(西妥昔单抗联合铂类和5-氟尿嘧啶)。对于二线治疗,TBP组最常用的方案是TPExtreme(西妥昔单抗联合铂类和紫杉类),非TBP组最常用的方案是紫杉类为基础的治疗。(表1)
表1:两组患者一线及二线治疗方案
TBP组和非TBP组的中位TTD分别为7.7个月和4.6个月(P<0.001),中位PFS2分别为11.7个月和7.7个月(P<0.001)。在生存方面,与非TBP组相比,TBP组中位OS1(西妥昔单抗治疗的第一天至死亡或最后随访日)显著延长:14.1个月 vs 10.9个月(P=0.016),TBP组中位OS2(从二线治疗第一天至死亡或最后随访日)显著延长:9.8个月 vs 6.5个月(P=0.002)(图4)。
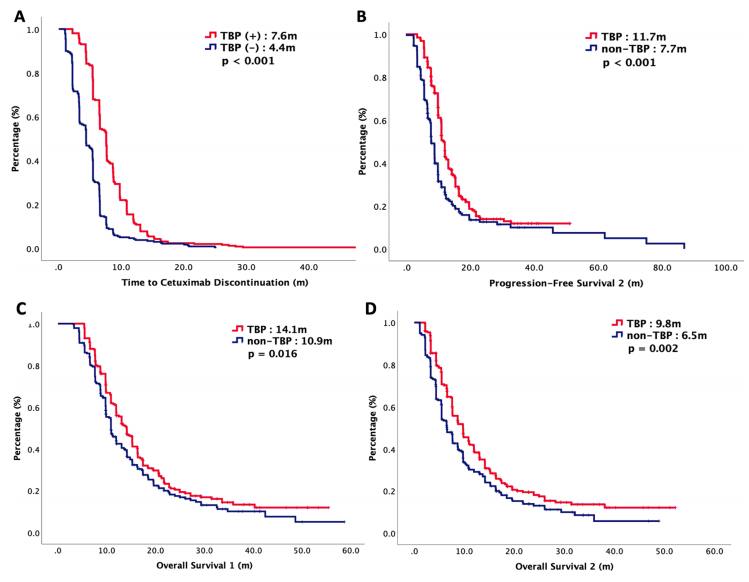
图4 根据TBP分层,接受西妥昔单抗一线治疗的498例R/M SCCHN患者的:A TTD;B PFS2;C OS1;D OS2
此外,多因素分析显示西妥昔单抗TBP是与OS独立相关的因素。在PD-L1阳性患者中,TBP组和非TBP组的中位OS1分别为22.8个月和9.2个月(P=0.013);另外,进一步亚组分析结果显示,无论程序性细胞死亡蛋白配体(PD-L1)表达和p16状态如何,这种生存获益仍然显著, 在PD-L1阴性患者中,TBP组和非TBP组的中位OS1分别为13.0个月和9.9个月(P=0.010)(图5)。
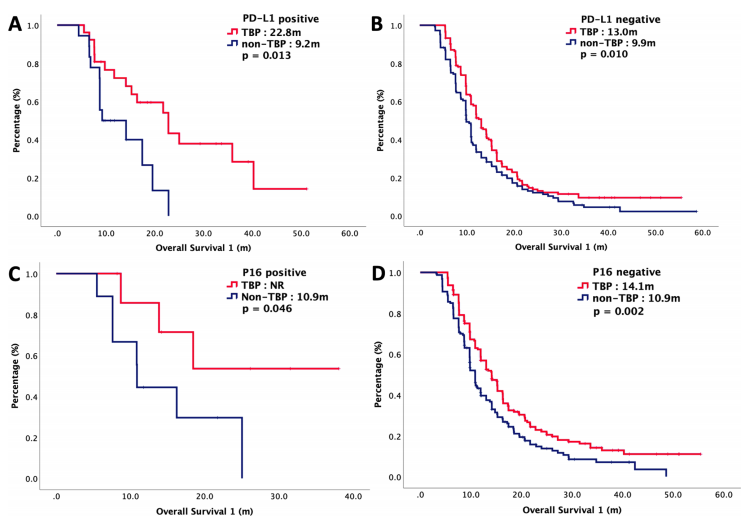
图5 根据TBP分层,接受以西妥昔单抗为基础的一线治疗R/M SCCHN患者的OS1。
A 患者PD-L1阳性;B 患者PD-L1阴性;C 患者p16阳性;D 患者p16阴性
本回顾性研究表明含西妥昔单抗的一线治疗进展后,西妥昔单抗再挑战是有效的,可延长患者西妥昔单抗治疗的TTD、PFS和OS。有必要开展进一步的前瞻性研究验证西妥昔单抗进展后继续治疗在R/M型SCCHN中的作用。
吴三纲教授:
这项研究是第一项关于西妥昔单抗进展后TBP对R/M SCCHN患者预后影响的研究。
本研究对于台湾头颈部癌症登记数据库(THNSCRD)中接受含西妥昔单抗一线治疗后进展并二线治疗的患者进行回顾性评估,其中部分患者继续以西妥昔单抗联合其他化疗方法作为二线治疗方案,而部分患者则接受西妥昔单抗以外的系统治疗作为二线治疗方案。结果显示西妥昔单抗进展后TBP可以延长一线含西妥昔单抗治疗失败后的R/M SCCHN患者生存期。亚组分析结果显示,无论程序性细胞死亡蛋白配体(PD-L1)表达和p16状态如何,这种生存获益仍然显著。同时多因素分析显示,ECOG PS和西妥昔单抗TBP是与生存相关的独立预测因子。因此本研究结果支持西妥昔单抗作为R/M SCCHN患者经一线含西妥昔单抗方案进展后的二线治疗方案。
既往研究表明,在含西妥昔单抗方案进展后,使用ICI在后线治疗中发挥重要作用。Keynote-040研究比较了帕博利珠单抗与研究者选择的标准方案后线治疗R/M SCCHN的有效性和安全性,结果显示,帕博利珠单抗可以延长患者中位OS(8.4月 vs 6.9月,P= 0.0161),且安全性良好,同时亚组分析发现,CPS≥1的患者预后优于CPS<1的患者。Checkmate-141是一项随机III期试验探索了纳武利尤单抗在铂类化疗进展后R/M-SCCHN患者中的作用,结果表明纳武利尤单抗获得比标准疗法更长的生存期,更新的一份2年随访的亚组分析报告证实,PD-L1≥1%的患者生存期比PD-L1 < 1%更长。尽管以上证据支持西妥昔单抗为基础的一线治疗进展后使用ICI作为二线治疗,但同时PD-L1阳性患者一线治疗方案改变。本项研究结果表明,对于CPS<1或存在ICI禁忌证的亚组患者,西妥昔单抗TBP可以作为R/M SCCHN患者的一种治疗选择,而ICIs可作为R/M SCCHN患者继西妥昔单抗TBP后的下一线治疗方案。本项研究是一项回顾性研究,需要进一步的前瞻性随机对照研究来验证结论。
西妥昔单抗联合PD-1抑制剂可作为PD-1难治的R/M-SCCHN患者挽救治疗方案3
程序性细胞死亡蛋白(PD-1)免疫治疗无效的R/M SCCHN患者预后相对较差,而目前挽救性治疗研究较少,亟待开展。西妥昔单抗可能与ICI治疗存在协同作用,本研究旨在探索西妥昔单抗联合PD-1抑制剂作为挽救治疗方案在抗PD-1免疫治疗进展后的R/M SCCHN患者中应用的有效性和可行性。
本研究是一项单中心回顾性真实世界研究。研究在上海交通大学医学院附属第九人民医院口腔颌面-头颈肿瘤科进行,回顾了2020年10月至2023年5月期间确诊为R/M SCCHN患者的临床资料。纳入接受过含有抗PD-1单抗一线治疗后,通过影像学确认肿瘤进展、二线治疗中至少接受过一次西妥昔单抗联合PD-1抑制剂治疗的患者,患者在一线治疗中无西妥昔单抗应用史,无持续性免疫相关不良反应。研究主要终点是ORR(定义为肿瘤从基线缩小30%并维持4周以上的患者比例)。次要终点是PFS、OS和治疗相关不良事件。
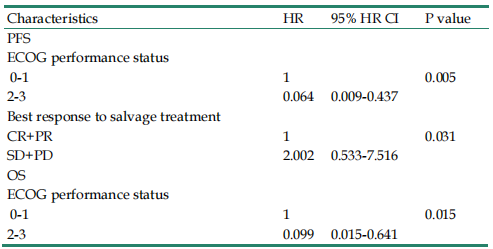
本研究共纳入28例R/M SCCHN患者。2023年9月24日最后一次随访时,西妥昔单抗联合PD-1抑制剂挽救治疗的ORR为46.4%,DCR为82.1%。Kaplan-Meier生存分析结果显示,患者中位PFS为6.87个月,中位OS为9.76个月(图6)。多变量回归分析结果显示,美国东部肿瘤协作组评分(ECOG)体能状态是挽救治疗PFS和OS的预后因素,挽救治疗的最佳反应是PFS的预后因素(表2)。在安全性方面,挽救治疗期间最常见的治疗相关不良反应是皮疹(72.1%)、贫血(64.3%)和疲劳(46.5%),最常见的潜在不良反应是甲状腺功能减退(25%)和肺炎(14.3%),没有发生与治疗相关的死亡病例。本项研究表明西妥昔单抗联合PD-1抑制剂存在潜在疗效和安全性,可能是PD-1难治性R/M SCCHN是一种有效挽救治疗方法,有待进一步前瞻性研究确认。
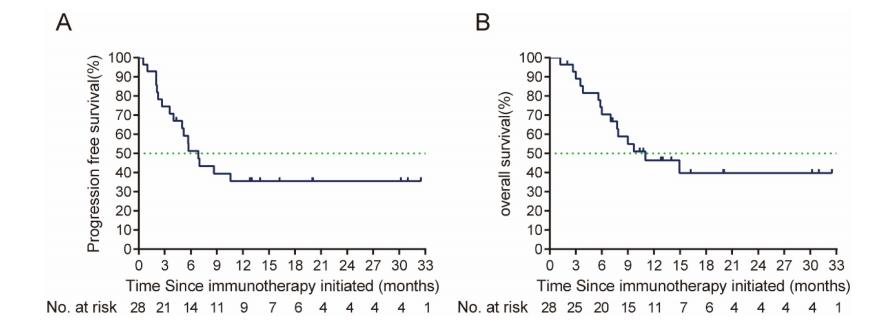
图6 西妥昔单抗联合PD-1抑制剂挽救治疗中的:A 无进展生存期;B 总生存期
表2 挽救疗法PFS和OS多变量分析
吴三纲教授:
这项研究首次报道了西妥昔单抗联合PD-1抑制剂作为一线免疫治疗进展后的挽救治疗方案,显示了在抗PD-1单抗难治的R/M SCCHN患者的疗效和安全性,ORR达46.4%,疾病控制率82.1%,中位PFS为6.87个月,中位OS为9.76个月。
既往文献报道,抗PD-1免疫治疗和西妥昔单抗具有协同作用。西妥昔单抗可以阻断EGFR,通过抑制MAPK和PI3K信号的活性,抑制肿瘤细胞增殖、生存、血管生成和迁移;并可通过增加细胞毒性淋巴细胞的活性,减少Treg细胞的数量和活性,增加MHC I和MHC II的表达等逆转免疫抑制作用。Sacco AG 等人的研究提示帕博利珠单抗联合西妥昔单抗治疗既往无PD-1、PD-L1或EGFR治疗史的R/M-SCCHN患者6个月的总有效率达45% (15/33)并获得显著的生存获益。提示PD-1抑制剂联合抗EGFR单抗治疗R/M SCCHN具有协同作用并获得较好临床疗效。
对于一线免疫治疗进展的患者,既往多项研究曾报道挽救治疗方案可选含西妥昔单抗相关方案。另外,一线治疗进展的患者对于治疗的耐受性往往较差,且在既往研究中发现,含化疗的挽救性治疗毒性相对较高。Cabezas-Camarero S等的回顾性分析探索了23例患者在ICI治疗进展后接受西妥昔单抗为基础的联合治疗的毒性反应,结果显示,100%的患者发生了1级或2级不良事件,65%的患者发生了≥3级的不良事件,Suzuki S等的研究也显示,在ICI治疗进展后接受西妥昔单抗联合紫杉醇治疗的患者中,22.3%的患者发生≥3级的血液学毒性反应,16.8%发生≥3级的非血液学毒性反应。在这项研究中,西妥昔单抗联合PD-1抑制剂的≥3级的不良事件发生率显著低于既往报道,表明西妥昔单抗联合PD-1抑制剂作为挽救治疗具有良好的耐受性,未来可以进行更大规模的随机对照试验,进一步确认并优化R/M SCCHN的治疗。
PCC(紫杉醇、卡铂和西妥昔单抗)周疗方案是ICI治疗进展后有效的二线治疗方案4
既往缺乏有关ICI进展后SCCHN患者的最佳治疗方案的数据。与三周一次PCC(西妥昔单抗+紫杉醇+卡铂)相比,每周一次PCC的毒性降低,该研究探索了免疫治疗进展后,每周接受PCC治疗的患者结局。
2016年7月至2022年11月,研究入组的复发或转移性头颈鳞癌(R/M SCCHN)患者,在ICI治疗进展后,每周接受紫杉醇45mg/m2,卡铂(AUC为1.5),西妥昔单抗首次给药400 mg/m2,后续每周给药250 mg/m2。研究收集了肿瘤部位、P-16、联合阳性评分(CPS)、ORR、PFS和OS的数据。
在评估的44例患者中,84%为男性,中位年龄为60岁。最常见的肿瘤部位是口咽部(48%),其次是口腔(27%),其他部位占25%。19例患者(43%)最初接受ICI+化疗,25例(57%)仅接受ICI治疗。ICI治疗的中位持续时间为5.1个月。33例患者可评估CPS数据,其中8例患者CPS评分为0%,10例CPS评分为1%-20%,15例CPS评分为21%-100%。数据显示,PFS和OS的中位随访时间分别为4个月和8个月。PR 16例(36%),SD 12例(27%),PD 16例(37%)。中位PFS和中位OS分别为3.8个月(95%Cl:2.5-5.6)和9.2个月(95%Cl:7.8-14.4)。既往接受化疗联合免疫治疗的患者生存率较低。CPS阳性、ICI治疗持续时间较长和更长的OS之间存在相关性。
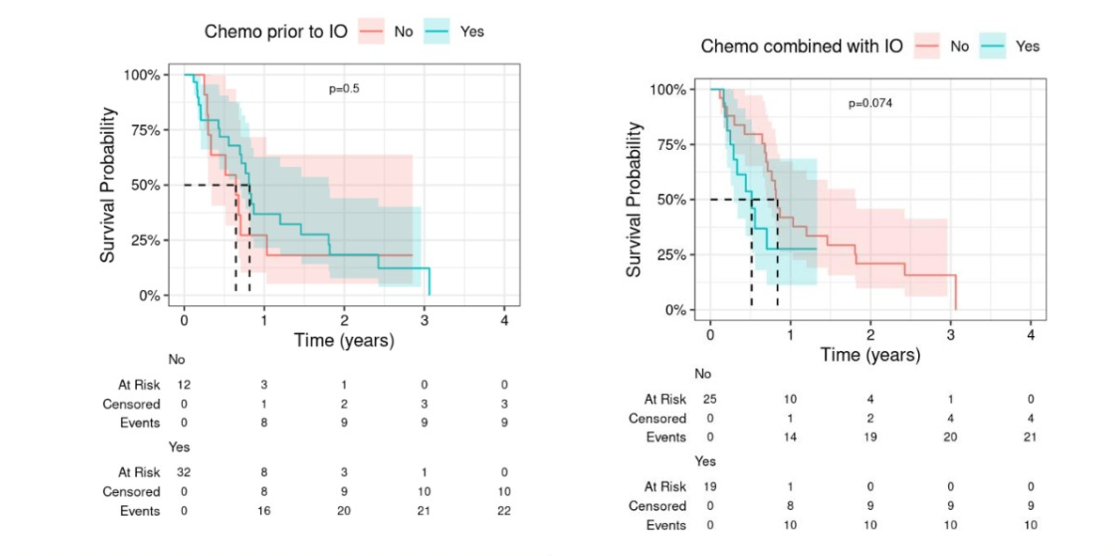
图7 研究结果
吴三纲教授:
目前RM SCCHN的二线标准治疗预后相对较差,平均ORR为14%,中位PFS为2个月。对于一线免疫治疗进展后的患者,二线治疗目前尚无标准治疗方案推荐,既往多项研究提示予西妥昔单抗相关治疗方案可获得较好的治疗效果,2021ASCO一项研究(poster 6038) 显示西妥昔单抗联合每周化疗治疗ICI进展的R/M SCCHN患者,ORR达 32%,mPFS为 5.6个月(单独化疗3.2个月,P=0.042);另外2022 ASCO上一项研究(poster 6036)提示 ICI治疗进展后,紫杉烷类+西妥昔单抗+/-铂类化疗的ORR高达63%;中位PFS为5.1个月,中位为OS 9.7个月;另一项II期研究(2023ASCO poster 6032)提示:紫杉醇联合西妥昔单抗双周治疗在既往接受含铂化疗和PD-1抑制剂治疗的R/M SCCHN的ORR为68.7%, DCR为93.9%;mPFS为 5.6个月, mOS为13.4个月。
本项回顾性分析,进一步补充了一线免疫治疗进展后挽救性治疗方案的选择。结果提示,每周一次的西妥昔单抗治疗是ICI进展后较为有效的二线治疗方案,缓解率方面,PR 16例(36%),SD 12例(27%),PD 16例(37%)。患者的中位PFS和中位OS分别为3.8个月和9.2个月,并且CPS阳性、ICI治疗持续时间较长的患者OS获益更为明显。
一线免疫治疗进展后患者的挽救治疗,多项研究提示西妥昔单抗相关联合治疗方案获得了较好的疗效,期待更多的研究数据支持。
Xevinapant联合放疗治疗术后高危、铂不耐受的LA SCCHN:III期XRay Vision研究5
头颈部癌是全球第八大最常见的恶性肿瘤,绝大多数病例(约90%)为鳞状细胞癌,约60%的患者被诊断为LA SCCHN。真实世界研究数据显示,40%的LA SCCHN患者接受了手术切除。对于术后复发风险高的患者,目前的标准治疗是辅助放化疗,但由于顺铂的毒性,许多患者无法接受以顺铂为基础的治疗,而这部分患者的治疗尚缺乏标准治疗推荐,亟需新的治疗方案以满足迫切的临床需求。
逃避细胞凋亡是癌症的关键标志,肿瘤细胞可通过多种机制抑制凋亡,包括改变调控凋亡的细胞内蛋白的表达。IAPs,如cIAP1/2和XIAP,是一类阻断内在和外在凋亡信号通路的蛋白质,可促进细胞存活。IAPs在包括SCCHN在内的多种恶性肿瘤中过表达,被认为会增加肿瘤细胞对凋亡的抵抗力。此外,IAPs的过表达与LA SCCHN的不良预后有关,而且在SCCHN的临床前模型中,IAPs已被证明会降低化疗和放疗的效果。
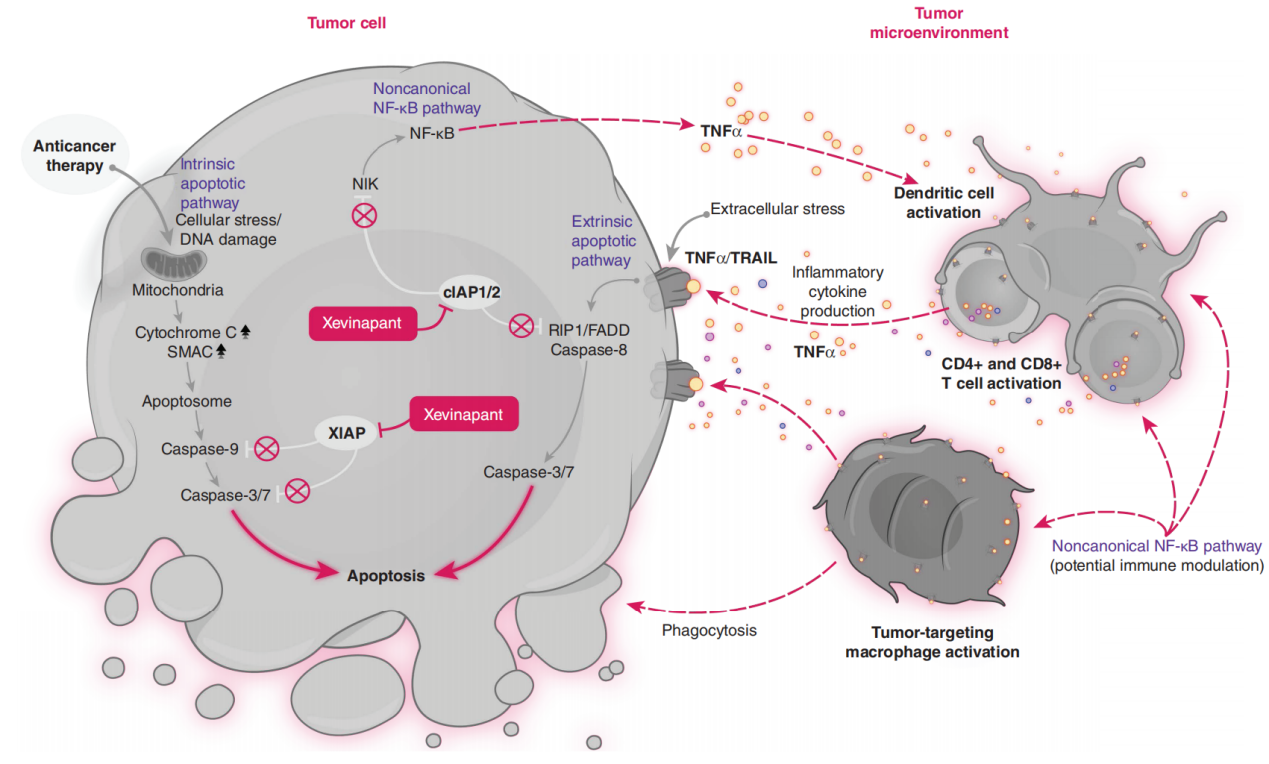
图8 Xevinapant作用机制
Xevinapant是首创强效口服小分子IAP抑制剂,被认为可恢复肿瘤细胞对凋亡的敏感性。临床前研究已证实xevinapant可抑制cIAP1/2和XIAP,因此,xevinapant被认为可释放对下游caspase活性的阻断,并重新激活内源性和外源性凋亡途径,从而增强化疗和放疗的抗肿瘤疗效,并通过激活非经典NF-κB信号通路增强免疫系统的抗肿瘤作用(图8)。
XRay Vision是一项全球、随机、双盲、III期研究,需入组700例术后高危、铂不耐受的LA SCCHN患者,将以1:1的比例随机接受6个周期的xevinapant或安慰剂治疗,并在前3个周期联合放疗。主要终点是无病生存期,次要终点包括OS、健康相关生活质量和安全性。目前中国有25个研究中心正在招募患者中。
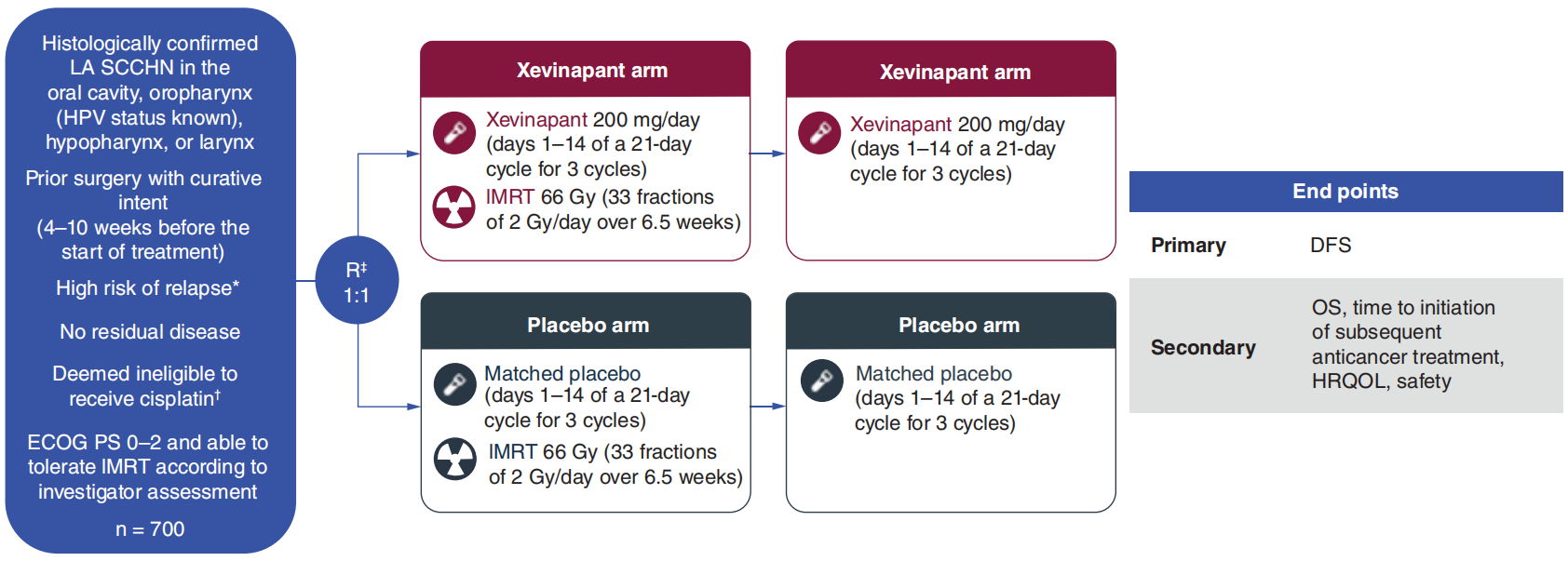
图9 III期XRay Vision研究设计
吴三纲教授:
回顾文献,在SCCHN的临床前模型中,xevinapant也显示出与RT的协同活性。Xevinapant联合CRT的抗肿瘤活性颇有前景,加上其与单独RT联合的临床前抗肿瘤活性,为评价xevinapant联合RT方案提供了依据。 Xevinapant I期研究提示RD2P 为200mg/天。Xevinapant II期研究在LA SCCHN患者中显示,与安慰剂+放化疗(标准治疗)相比,xevinapant+放化疗显著改善了患者的生存获益,并非常显著的降低了患者5年死亡风险(HR=0.47),且不增加毒性,基于II期研究的良好数据,进一步开展了III期Trilynx研究,目前该III期研究全球入组已结束,即将进行中期分析,期待该III期研究能进一步论证II期研究的疗效。
本项XRay Vision研究主要探索术后高危铂不耐受的LA SCCHN患者的辅助治疗方案,评估xevinapant+调强放疗(IMRT) vs 安慰剂+IMRT的疗效和安全性,约700例患者将按1:1的比例随机分配,并根据原发肿瘤部位(口咽/口腔 vs 喉 vs 下咽)、肿瘤分期(III vs IV)和人乳头瘤病毒(HPV)p16状态(口咽 p16阳性 vs 口咽 p16阴性或喉/下咽/口腔)进行分层。符合条件的患者将随机接受6个周期的治疗,口服xevinapant 200 mg/天或匹配的安慰剂(21天周期中的第1-14天),前3个周期联合IMRT。Xevinapant无需同时服用任何特定药物。主要终点是无病生存期,次要终点包括OS、健康相关生活质量和安全性。该研究于2022年10月开始,预计主要完成日期为2027年10月。
另外,Xevinapant 目前还有多项研究在进行中,如HyperlynX (I期,LA-SCCHN, Xevinapant + 顺铂40mg/m2 QW + IMRT)等, 期待这些研究为患者带来更有效的治疗方案。
目前RM SCCHN一线治疗可选择西妥昔单抗联合化疗或帕博利珠单抗相关方案。本期文献进展提示对于一线西妥昔单抗相关方案治疗进展的患者二线可以继续选择西妥昔单抗行再挑战;对于一线免疫相关方案治疗进展的患者,二线选择西妥昔单抗联合免疫或者联合化疗的方案都可获得良好疗效。对于LA SCCHN,多项免疫联合RT/CRT方案均未提高患者疗效,未改变目前高剂量顺铂联合放疗或西妥昔单抗联合放疗的SoC。针对LA SCCHN的探索,目前II期临床研究提示IAP抑制剂xevinapant联合CRT相对于标准治疗CRT可显著改善患者生存,期待III期Trilynx研究的疗效进一步论证此结论。同时目前xevinapant另一项全球多中心III期研究XRAY-VISION研究正在入组中,期待xevinapant及更多新药能进一步改善LA SCCHN患者的疗效。
1. Machiels JP, et al. Pembrolizumab plus concurrent chemoradiotherapy versus placebo plus concurrent chemoradiotherapy in patients with locally advanced squamous cell carcinoma of the head and neck (KEYNOTE-412): a randomised, double-blind, phase 3 trial. Lancet Oncol. 2024 Mar 29:S1470-2045(24)00100-1.
2. Wang HM, et al. Cetuximab Treatment beyond Progression in Patients with Recurrent or Metastatic Head and Neck Squamous Cell Carcinoma: A Nationwide Population-Based Study (THNS-2021-08). Target Oncol. 2024 Jan;19(1):51-58.
3. Hui R,et al.. The efficacy of cetuximab plus PD-1 inhibitors as salvage therapy in PD-1 refractory patients with recurrent or metastatic head and neck squamous cell carcinoma. J Cancer. 2024;15(6):1668-1674. Published 2024 Jan 27. doi:10.7150/jca.92689
4. Bhateia P, et al. Weekly paclitaxel, carboplatin, and cetuximab as treatment for recurrent or metastatic head and neck squamous-cellcarcinoma (RM-SCCHN) that progressed on immune checkpoint inhibitors (ICI): a retrospective analysis.2024.
5. Ferris RL, et al. Xevinapant plus radiotherapy in resected, high-risk, cisplatin-ineligible LASCCHN: the phase III XRay Vision study design. Future Oncol. 2024 Apr;20(12):739-748.
排版编辑:肿瘤资讯-











 苏公网安备32059002004080号
苏公网安备32059002004080号


