值此三八国际妇女节之际,我们不仅颂扬女性的力量与成就,也关注国家对女性健康的重视,特别是对“两癌”筛查的投入和支持。在这个特别的日子,2024年欧洲妇科肿瘤协会(ESGO)年会(3.7-3.10)正在西班牙举行。由中国医学科学院肿瘤医院吴令英教授牵头的研究“国创ADC维迪西妥单抗(RC48)治疗HER2表达的复发性宫颈癌”人选大会口头报告,彰显了中国在宫颈癌治疗领域的创新实力。为了深入探讨这项研究的深远意义以及宫颈癌HER2检测的现状与未来发展方向,【肿瘤资讯】特邀吴令英教授和应建明教授,共同解读研究数据,展望宫颈癌治疗的新篇章。
吴教授,您的团队关于MMAE类ADC维迪西妥单抗治疗HER2表达复发性宫颈癌的研究入选2024年ESGO大会的口头报告。能否请您分享研究背景和设计考量?
吴令英教授:宫颈癌的发病率在我国女性恶性肿瘤中位居前列。据2023年数据显示,宫颈癌新发病例数仍高达11.93万例[1]。尽管我们在早诊、早治、早预防方面取得一定进步,但仍需寻求更有效的治疗策略。特别是对于晚期或复发的宫颈癌患者,在经历一线治疗后,往往面临缺乏标准化后线治疗方案的挑战,导致五年生存率不理想,许多患者面临治疗困境。
为了突破这一瓶颈,我们迫切需要寻找新的治疗策略。目前,在宫颈癌的二线治疗中,靶向组织因子(TF)的MMAE类ADC药物Tisotumab Vedotin(TV)已获得FDA批准。在innovaTV 204研究中,TV治疗经治复发或转移性宫颈癌患者的客观缓解率(ORR)为23.8%,中位无进展生存期(PFS)为4.2个月,中位总生存期(OS)为12.1个月[2]。
HER2在多种实体瘤中表达,靶向HER2的ADC药物在其他实体瘤研究中已经显示出疗效。维迪西妥单抗是由荣昌生物研发的中国首创靶向HER2超级抗微管-ADC药物,由HER2抗体部分、连接子和细胞毒药物MMAE构成。RC48作为我国首个获得美国FDA和中国药监局突破性疗法双重认定的ADC药物,已在我国获批用于胃癌和尿路上皮癌治疗,并纳入国家医保目录,药物可及性佳[3]。基于“异病同治”的理念和过往研究经验,针对HER2表达的ADC药物在复发性宫颈癌二线及后线治疗中的潜在效果值得进一步研究,有望引领宫颈癌治疗进入一个全新的抗HER2类ADC时代。基于此,我们团队开展了RC48单药在HER2表达(HER2阳性和HER2低表达)妇科恶性肿瘤的临床研究C018,也是抗HER2-ADC药物治疗宫颈癌中为数不多的探索性临床研究。C018采用Ⅱ期、开放标签、多中心篮式设计,在宫颈癌队列评估RC48单药治疗HER2表达的复发性宫颈癌的有效性和安全性[4]。该研究计划招募至少接受过一线抗肿瘤治疗后疾病进展、HER2 IHC≥1+的复发或转移性宫颈癌患者。截至目前共入组了25例患者,接受了至少1个周期的药物治疗,其中22例患者的疗效可评估。RC48治疗剂量为2 mg/kg(Q2W)。研究的主要终点为ORR,同时关注缓解持续时间(DoR)、PFS、OS以及安全性等次要终点。这样的设计旨在全面评估RC48的临床应用潜力,并为后续研究提供科学依据。
本研究中宫颈癌队列RC48的疗效和安全性如何?该成果对我国复发性宫颈癌患者有怎样的意义?
吴令英教授:总体而言,我们的研究取得了良好的疗效和安全性结果。在疗效可评价的22例患者中,mPFS为4.37个月,mDoR为5.52个月,中位OS未达到,12个月的OS率为66%,特别是主要研究终点ORR高达36.4%(95%CI:17.2~59.3 )[4]。亚组分析的结果显示,HER2 IHC 1+的患者明显获益(ORR率50%),而且RC48的疗效也惠及了既往经过抗PD1、紫杉醇联合铂类治疗的人群,在复发性宫颈癌的二线及后续治疗中展现出了非常出色的治疗效果。

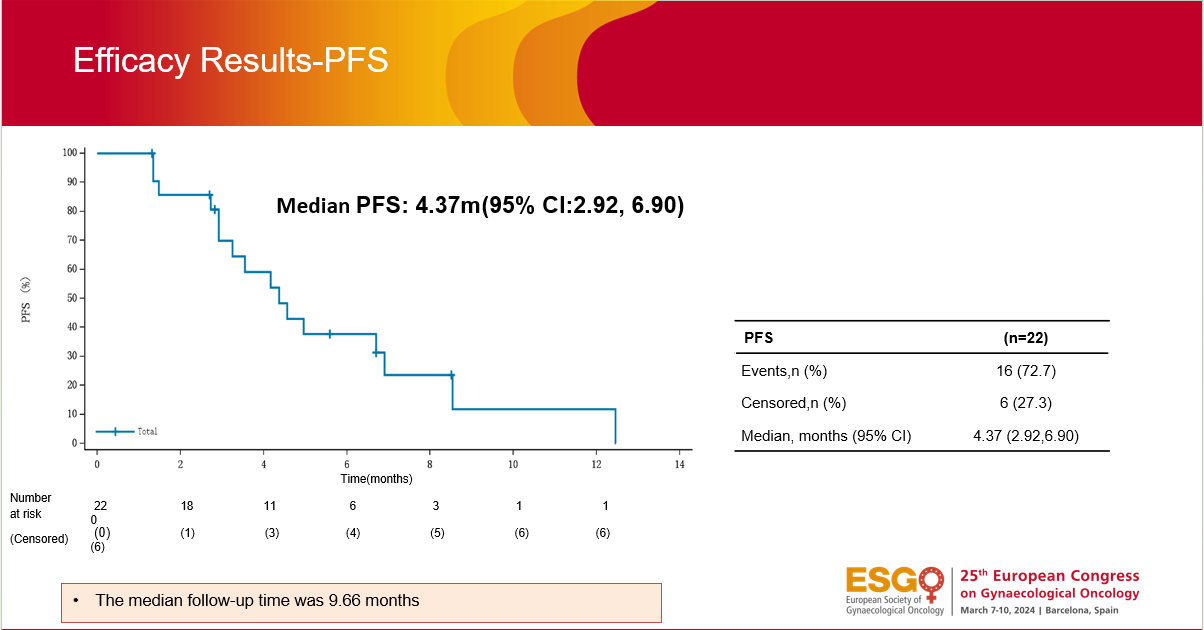
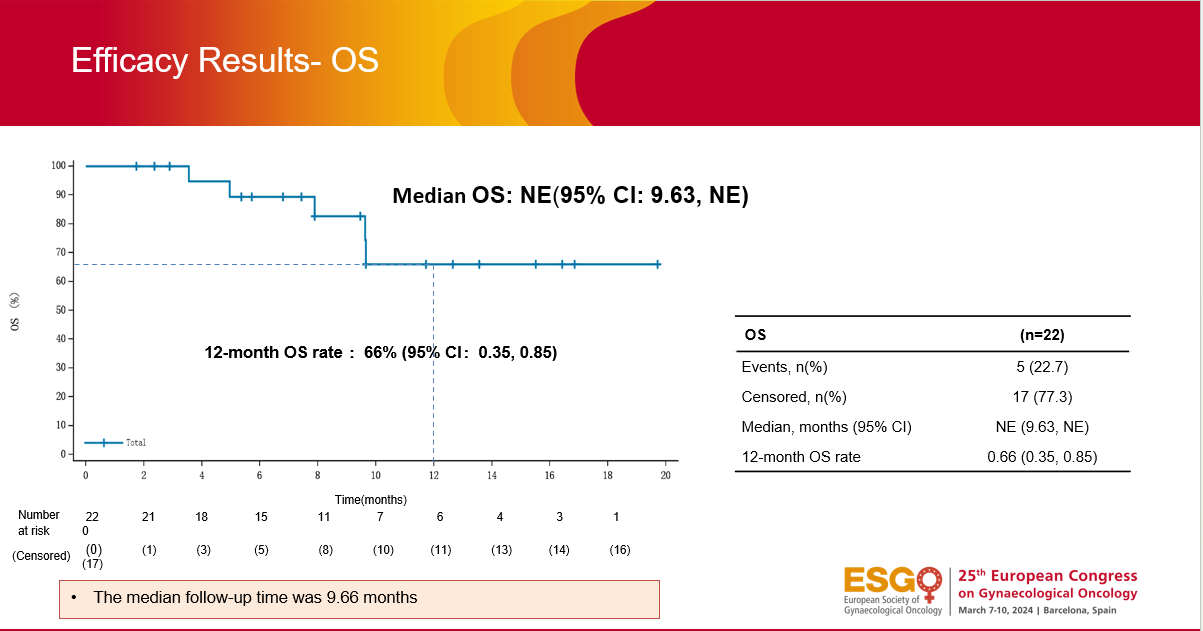 图1 C018宫颈癌队列患者的疗效结局
图1 C018宫颈癌队列患者的疗效结局
RC48治疗相关不良事件(TRAEs)主要为血液学相关。≥3级TRAEs的发生率较低,包括中性粒细胞计数降低(12%)、γ-谷氨酰转移酶升高(8%)和谷丙转氨酶增高(8%),整体安全性可耐受且可控,没有出现眼毒性、肺部毒性或致死性TRAEs。
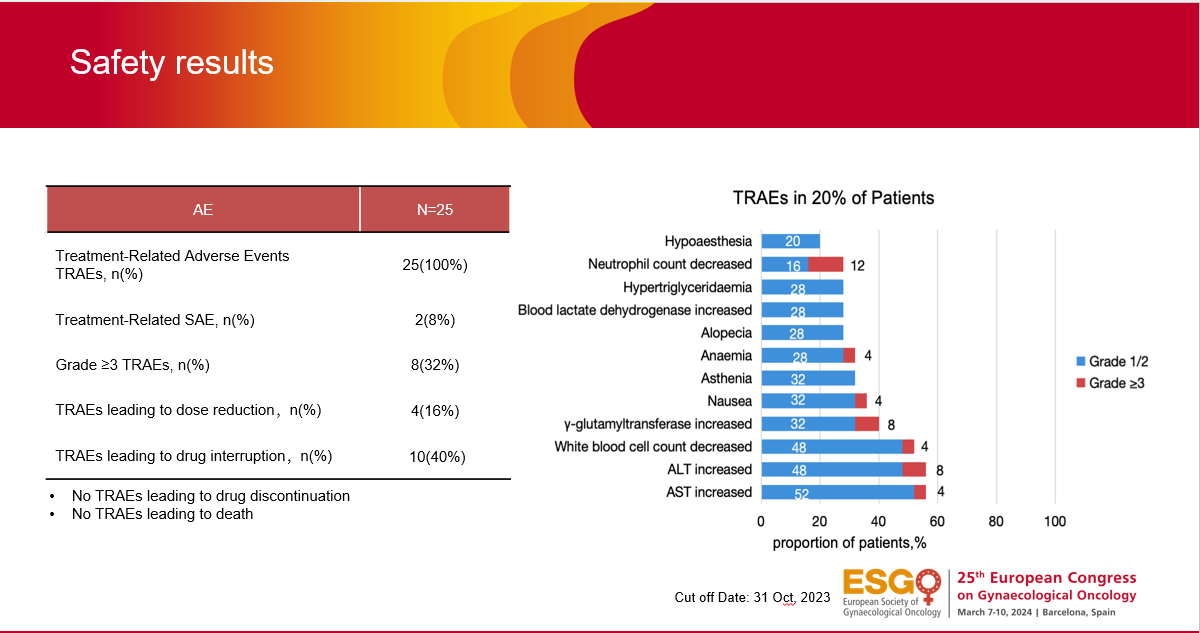 图2 C018研究安全性分析结果
图2 C018研究安全性分析结果
鉴于国创RC48在单药治疗宫颈癌中已显示出显著疗效,您如何看待其与化疗、免疫疗法等方案联合使用的前景?
吴令英教授:在本研究中,RC48作为单药治疗宫颈癌在疗效方面有相当不错的表现,其与化疗、免疫疗法联合使用的前景非常值得期待。
首先,联合治疗策略的潜在优势在于能够发挥不同治疗手段的协同效应,从而增强疗效。例如,化疗或可提升肿瘤细胞对RC48的敏感性,免疫检查点抑制剂可能与RC48共同激活患者自身的免疫系统,以更有效地攻击肿瘤细胞。此外,联合治疗有助于降低肿瘤细胞对单一治疗手段产生耐药性的风险。
其次,已有研究数据支持MMAE ADC药物与免疫疗法或铂类治疗联合使用的疗效。TV205研究中,一线TV+帕博利珠单抗/卡铂、二/三线TV+帕博利珠单抗的组合均获得较好的ORR结局[5]。基于此,我们有理由期待同为MMAE类ADC药物的RC48在与化疗、免疫疗法等联合使用时,能取得优异的疗效。
最后,作为具有中国特色的HER2-ADC药物,RC48在可及性和性价比方面具有明显优势。它不仅为宫颈癌患者提供了新的治疗选择,还在国际市场上展现出竞争力。随着未来研究的深入,RC48联合治疗策略的前景十分广阔,有望为宫颈癌的治疗带来新的突破。
 图3 TV205研究设计和主要结果
图3 TV205研究设计和主要结果
C018研究疗效获益人群扩展到HER2 IHC 1+、2+以及3+的患者群体,似乎打破了仅HER2阳性患者才能从抗HER2治疗中获益的固有观念。请问妇科肿瘤HER2表达情况如何,与妇瘤治疗预后之间有怎样的关系?
应建明教授:妇科肿瘤中HER2有表达(IHC 1+~3+)人群远高于传统HER2阳性(IHC 3+,IHC 2+/FISH+)人群。据国际研究数据显示,子宫内膜癌HER2表达率为59.1%,卵巢癌HER2表达率37.6%,宫颈癌HER2表达率35.7%[6]。福建省肿瘤医院在2020年至2022年间对246例宫颈癌患者进行了非标准化的HER2检测,结果显示HER2 IHC表达率达50%,而在腺癌患者中这一比例更是高达72%。
HER2表达是妇科肿瘤预后不良的重要因素。关于卵巢癌和子宫内膜癌的数据显示,HER2表达水平高的患者PFS和OS更差[7]。在宫颈癌研究中,一项研究采用IHC分析229例宫颈癌组织(包括194例腺癌和35例腺鳞癌)的HER2表达与临床结果的相关性,单变量分析和多变量分析均显示HER2阳性与不良预后之间有相关性的趋势(P=0.071;P=0.059),按HER2表达阴性、中度、过表达的分层KM分析显示,HER2过表达与更差的预后相关(P=0.014),HER2过表达为宫颈腺癌和腺鳞癌患者的独立预后标志物[8]。在C018宫颈癌队列研究中,RC48抗HER2治疗的获益人群已经显著扩展至IHC 1+ 2+ 3+人群,IHC 1+的患者ORR甚至高达50%[4]。这一发现强调了对HER2表达水平进行更细致分类的重要性,对于指导宫颈癌的个性化治疗至关重要。
能否请您为我们介绍宫颈癌中HER2检测的现状?在临床实践中,HER2检测的标准和普及情况如何?
应建明教授:首先,标本的取材和规范化前处理对HER2检测结果的准确性具有决定性影响。由于肿瘤组织中HER2表达存在时间和空间的异质性,不同来源的样本(如活检与手术样本)、同一样本不同的取样点都可能呈现不同的HER2表达水平。此外,样本处理的各个环节,包括固定时间的适宜性、固定液的选择、骨转移样本的特殊处理,以及白片的适当保存时间,都对最终的检测结果起着至关重要的作用。这些细节的精确控制对于确保HER2检测的准确性和可靠性至关重要。
根据最新NCCN指南(2024.V1),对于晚期复发或转移性宫颈癌患者,推荐进行HER2 IHC检测[9]。然而,目前临床上在宫颈癌HER2检测的流程和判读标准方面,尚缺乏统一的规范。
在妇科肿瘤HER2的检测标准方面,我们通常借鉴胃癌和乳腺癌的HER2检测标准,但这可能导致检测结果的不一致性。例如,一项Meta分析显示,采用ASCO/CAP标准与未采用此标准的宫颈癌HER2 IHC过表达发生率分别为5.7%和27.0%[10]。RC48-C018研究采用乳腺癌的HER2检测标准,发现HER2表达率为29%[4]。此外,不同类型的宫颈癌,如腺癌和鳞状细胞癌,其HER2表达水平也存在较大差异。这强调了妇科肿瘤制定统一HER2检测标准的必要性,以确保检测结果的一致性和治疗决策的准确性。
HER2表达的判读标准,尤其是阳性阈值的界定,对检测结果的判定有显著影响。在胃癌和乳腺癌的手术切除标本中,HER2阳性的阈值均设定为10%。然而,在胃癌的判读标准中,除了要求细胞膜呈现完整的环周染色外,也允许侧面或基底面的膜染色,这使得判读标准相对宽松。在乳腺癌领域,HER2阳性的判定标准经历过由IHC细胞核着色>30%调整为>10%的变迁。妇科肿瘤的HER2检测标准同样需要经历一个探索和完善的过程。近年来除了乳腺癌和胃癌之外,其他泛瘤种(包括妇科肿瘤)的HER2 IHC检测的阈值标准似乎正在逐渐趋于统一,也为宫颈癌HER2 检测标准的制定带来了启示。
总而言之,妇科肿瘤领域,我们需要建立一套完善的检测流程,包括HER2检测的样本类型、标本处理、检测方法、检测质量控制和检测结果判读,以提高检测的可靠性,最终为临床治疗决策提供依据。
专家介绍
国家癌症中心/中国医学科学院北京协和医学院肿瘤医院妇瘤科主任
中国临床肿瘤学会(CSCO)副理事长
中国临床肿瘤学会(CSCO)妇科肿瘤专家委员会主任委员
中国妇幼保健协会妇幼微创专业委员会主任委员
国家抗肿瘤药物临床应用监测委员会副主任委员
中国临床肿瘤学会临床研究专家委员会副主任委员
中华医学会北京分会妇科肿瘤专委会副主任委员
中国妇幼保健协会常务理事等
《中华妇产科杂志》《中华放射肿瘤杂志》《Cancer Biology & Medicine》《Oncology and Translational Medicine》等杂志编委
擅长卵巢癌|宫颈癌及子宫内膜癌等妇科肿瘤的手术、化疗、靶向治疗等综合治疗;主持国家级及多项国内外多中心妇科肿瘤药物临床研究。
专家介绍
国家癌症中心/中国医学科学院肿瘤医院病理科主任
分子肿瘤学全国重点实验室PI
享受国务院政府特殊津贴专家
中国抗癌协会肿瘤病理专业委员会主任委员
中国抗癌协会个案管理专委会副主任委员
中国研究型医院学会超微及分子病理专委会副主任委员
中国医师协会病理科医师分会委员
国家肿瘤质控中心单病种质控专家委员会委员
国家抗肿瘤药物临床应用监测专家委员会委员
国家药品监督管理局医疗器械技术评审专家咨询委员会委员
中国合格评定国家认可委员会CNAS认可评审专家、评定专家
[1] 郑荣寿, 张思维, 孙可欣, 等. 2016年中国恶性肿瘤流行情况分析 [J] . 中华肿瘤杂志, 2023, 45(3) : 212-220. DOI: 10.3760/cma.j.cn112152-20220922-00647.
[2] Ignace Vergote et al., Trial in progress update on ENGOT-cx8/GOG-3024/innovaTV 205: Addition of a new cohort with first-line (1L) tisotumab vedotin (TV) + pembrolizumab (pembro) + carboplatin (carbo) ± bevacizumab (bev) in recurrent/metastatic cervical cancer (r/mCC).. JCO 40, TPS5603-TPS5603(2022).DOI:10.1200/JCO.2022.40.16_suppl.TPS5603.
[3] 荣昌生物.荣昌生物泰它西普、维迪西妥单抗成功续约新版医保目录. https://mp.weixin.qq.com/s/VNZEoKpSyXB4DDYJEUfGgA.
[4] Lingying Wu, Guiling Li, Youzhong Zhang, et al. Evaluation Of The Effectiveness And Safety Of Disitamab Vedotin For HER2-Expressing Recurrent Cervical Cancer After Progression On Platinum-Based Treatment-A Single-Arm, Multicenter, Open-Label, Phase II Clinical Study. 2024 ESGO abstract #342 Oral.
[5] Ignace Vergote et al.T rial in progress update on ENGOT-cx8/GOG-3024/innovaTV 205: Addition of a new cohort with first-line (1L) tisotumab vedotin (TV) + pembrolizumab (pembro) + carboplatin (carbo) ± bevacizumab (bev) in recurrent/metastatic cervical cancer (r/mCC).. JCO 40, TPS5603-TPS5603(2022).DOI:10.1200/JCO.2022.40.16_suppl.TPS5603.
[6] Uzunparmak B, Haymaker C, Raso G, et al. HER2-low expression in patients with advanced or metastatic solid tumors. Ann Oncol. 2023 Nov;34(11):1035-1046. doi: 10.1016/j.annonc.2023.08.005.
[7] 全慧霞,林仲秋.妇科肿瘤人表皮生长因子受体2相关研究进展及检测方法[J].中国实用妇科与产科杂志2024,40(1):74-84.
[8] Martinho O,Silva-Oliveira R,Cury FP,et al. HER family receptors are important theranostic biomarkers for cervical cancer:blocking glucose metabolism enhances the therapeutic effect of HER inhibitors[J]. Theranostics,2017,7(3):717-732.
[9] NCCN Guidelines Version 1.2024: Cervical Cancer.
[10] Xiang L,Jiang W,Ye S,et al.ERBB2 mutation:a promising target in non-squamous cervical cancer[J]. Gynecol Oncol, 2018,148(2):311-316.
排版编辑:盐盐











 苏公网安备32059002004080号
苏公网安备32059002004080号


