浙江大学医学院附属第一医院血液科金洁教授团队应用CAR-T细胞疗法泽沃基奥仑赛(CT053)治疗1例抗CD38单抗治疗后早期复发的高危MM患者。该患者经泽沃基奥仑赛治疗后疗效达到了严格意义上的完全缓解,后续随访显示无进展生存期超过60个月。本文特整理该病例的诊治经过及用药体会,以供参考。
病例简介
多发性骨髓瘤(MM)是一种克隆浆细胞异常增殖的恶性疾病,在很多国家是血液系统第2位常见恶性肿瘤,多发于老年人,目前仍无法治愈。随着新药不断问世及检测手段的提高,MM的诊断和治疗水平得以不断改善1。但由于MM疾病呈现高度异质性,导致高危患者从新一代免疫调节剂、新一代蛋白酶体抑制剂、抗CD38单抗、双抗、ADC等新型药物和自体造血干细胞移植(ASCT)中获益非常有限。尤其是功能性高危患者(FHR,对诱导治疗反应不佳或早期复发)和超高危细胞遗传学异常患者(存在≥2种高危细胞遗传学异常)预后会更差2-3。改善这些高危患者的预后是目前MM临床实践过程中的重大挑战之一,而CAR-T细胞疗法有望为这些高危MM患者的治疗带来新的突破和发展。
我院2018年3月收治1例抗CD38单抗治疗早期复发的高危MM患者,经过泽沃基奥仑赛(CT053)CAR-T细胞治疗后达到严格意义上的完全缓解,后续随访显示无进展生存期(PFS)超过60个月。
病例资料
一般情况:患者,女,40岁,汉族,已婚,诊断MM 3年余,因患者3线抗CD38单抗靶向治疗后疗效欠佳,仅仅半年病情再次进展,因此考虑行BCMA CAR-T细胞治疗。现患者为求CAR-T细胞治疗来我院门诊,门诊拟“多发性骨髓瘤”于2018年3月19日收住入院。
现病史:患者3年余前(2014年12月)无明显诱因下出现腰背痛,初不剧可忍,无胸闷胸痛,无腹痛腹泻,无头晕头痛等明显不适,后疼痛加重,不能下地,就诊于外院。①查血常规-CRP:WBC 4.1×109/L,HGB 96g/L,PLT 144×109/L,CRP 1.32 mg/L;②血生化:总蛋白163.2 g/L,白蛋白32.1 g/L,球蛋白131.1 g/L;③免疫球蛋白:IgG 92.55 g/L,IgM 0.19 g/L,IgA 0.006 g/L;④腰椎MR扫描示:弥漫性骨病;⑤血免疫固定电泳示:IgG-λ阳性,血轻链λ/κ明显升高;⑥骨髓涂片:浆细胞比例增高,可见双核、三核浆细胞;⑦流式细胞术免疫分型示:骨髓中可见单克隆增生的浆细胞,约占有核细胞的10.74%,考虑为浆细胞骨髓瘤。免疫表型特征描述:主要强表达CD38,CD138,CD56,CD38强阳性的细胞λ阳性,κ阴性。染色体核型46 XX[20]。多发性骨髓瘤首先考虑。
后续治疗如下:
2014.12-2015.1(1线诱导治疗):先后予2疗程PAD(硼替佐米+表阿霉素+地塞米松)方案化疗,自诉化疗后四肢麻木刺痛明显。
2015.2-2015.6(1线诱导治疗):后予VAD(长春地辛+表阿霉素+地塞米松)方案化疗1疗程,TCD(沙利度胺+环磷酰胺+地塞米松)方案化疗2疗程,RD(来那度胺+地塞米松)方案化疗2疗程。2015.3复查IgG 8.71g/L,血免疫固定电泳示:IgG-λ阳性。
2015.11-2015.12(1线自体移植):2015年11月于当地医院巩固治疗。①查血常规:WBC 5.19×109/L,HGB 122 g/L,PLT 190×109/L;②血生化:前白蛋白 412.1 mg/L;③免疫球蛋白:IgG 11.34 g/L,IgA 0.06 g/L;④CT示:多发胸椎溶骨性骨质破坏。进一步行自体造血干细胞移植(移植前评估为PR),2015年11月10日起采用马法兰进行预处理,2015年11月12日回输外周血干细胞,并输成分血支持治疗,G-CSF、TPO刺激造血。移植后出现肝功能不全,消化道不良反应。移植第30天发生胆囊炎,后经治疗恢复。
2015.12-2016.9(1线维持治疗):移植后一直维持治疗,方案先后为TD(沙利度胺+地塞米松)、TCD(沙利度胺+环磷酰胺+地塞米松);2016年3月复查①免疫球蛋白:IgG 15.35 g/L;②血免疫固定电泳示:IgG-λ阳性;③骨髓涂片:个别部位原、幼细胞稍增多。
2016.9-2017.5(2线治疗):2016年9月予IFN+RD(干扰素+来那度胺+地塞米松)方案治疗;2016年10月复查①免疫球蛋白:IgG 10.30 g/L;②血免疫固定电泳示:IgG-λ阳性。2017年5月于当地医院复查①免疫球蛋白:IgG 15.9 g/L,IgA 0.08 g/L,IgM 0.54 g/L;②血沉 41.00 mm/h。
2017.5-2018.1(3线抗CD38单抗治疗):后患者疾病进展,为进一步治疗入组抗CD38单抗临床试验,但患者对于抗CD38单抗的疗效欠佳,仅仅半年就病情再次进展,临床试验出组。
2018.3-2018.4(4线CAR-T治疗):患者经抗CD38单抗治疗后病情再次进展。现患者为求CAR-T治疗来我院门诊,门诊拟“多发性骨髓瘤”收住入院。具体前期诊疗经过见表2-1。自病来,神志清,精神可,胃纳佳,睡眠安,小便量较少,大便无殊,体重增加15kg。
表2-1.前期诊疗经过
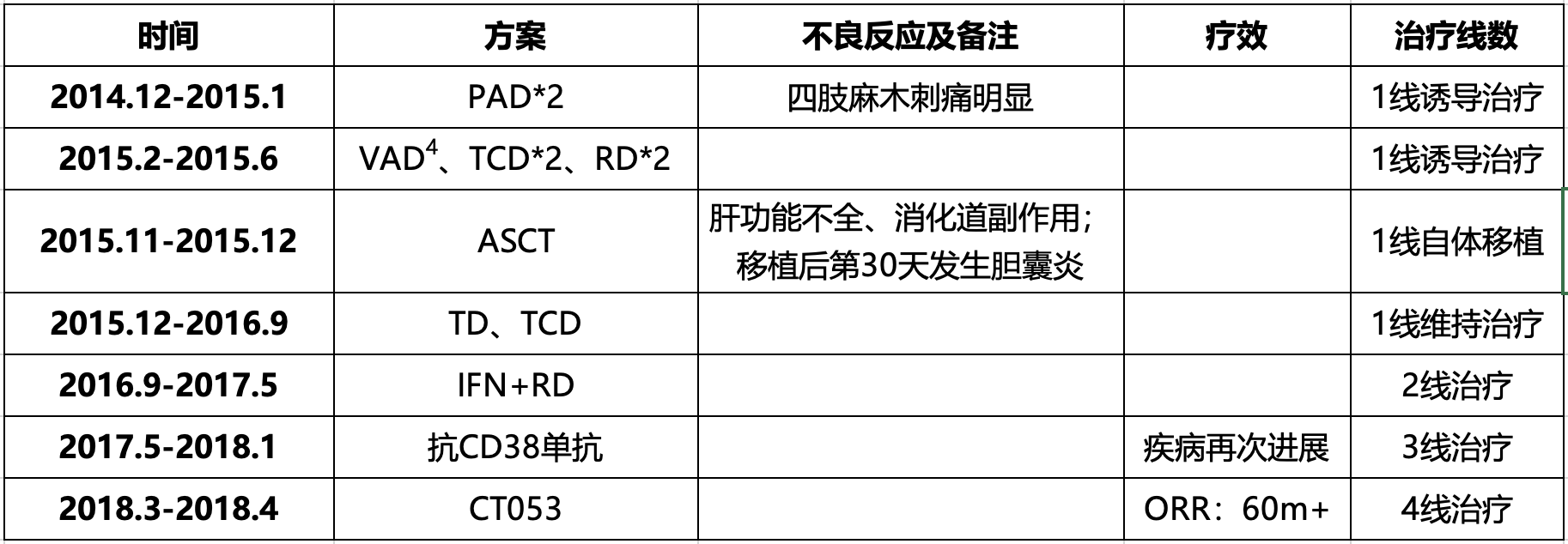
P:硼替佐米;A:表阿霉素;D:地塞米松;T:沙利度胺;C:环磷酰胺;R:来那度胺;V:长春地辛;ASCT:自体干细胞移植;IFN:干扰素;CT053:泽沃基奥仑赛。
辅助检查:①免疫球蛋白IgG:92.55 g/L(2014.12),8.71 g/L(2015.3.3),11.34 g/L(2015.11.5),15.35 g/L(2016.3.2),10.30 g/L(2016.10.25),15.90 g/L(2017.5.11)。②血免疫固定电泳:IgG-λ阳性(2014.12),IgG-λ阳性(2015.3.3),IgG-λ阳性(2016.3.2),IgG-λ阳性(2016.10.25)。
临床诊断:多发性骨髓瘤(IgG-λ型,DS ⅢA期,ISS ⅡA期)。
治疗过程
因患者抗CD38单抗靶向治疗后疗效欠佳,仅仅半年就病情再次进展,因此考虑行BCMA CAR-T治疗。
2018年3月,患者顺利单采到了足够量的T淋巴细胞。2018年4月,患者预处理清淋后成功回输1.5*108个CAR BCMA阳性T细胞(泽沃基奥仑赛),期间淋巴细胞监测情况如图3-1所示,淋巴细胞在回输后第9天恢复到正常水平。体温监测情况:回输当天最高体温37.4℃,但回输后第1天开始发热,最高体温38.5℃,持续发热9天(具体见图3-2),炎症指标如CRP等略高,呈缓慢上升趋势(2.96~48.58 mg/L),回输第1天结合患者鼻塞、咽痛等症状考虑急性上呼吸道感染,采用哌拉西林他唑巴坦和莫西沙星抗感染治疗;回输第10天,体温恢复正常,无再发热出现,回输后第13天CRP为4.78mg/L。
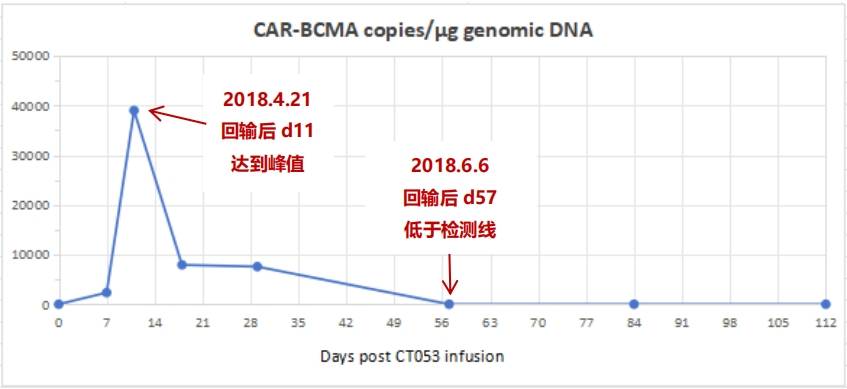
此外CAR-T细胞监测显示回输后在体内也呈迅速扩增趋势,11天达峰,峰值为38988 CAR-BCMA copies/μg genomic DNA(具体见图3-3);存续时间为8周(2个月),8周后CAR-BCMA copies低于检测下线,无法检测到,但是缓解一直存在,后续随访显示疾病长期控制,无病缓解时间超过60个月。该例患者回输后未发生ICANS(免疫效应细胞相关神经毒性综合征)和≥3级的CRS(细胞因子释放综合征),只出现一过性的IL-6升高,未做处理,第二天降低至正常值水平。
患者经评估后顺利出院,后续随访显示达到严格意义上的完全缓解,2016 IMWG MRD疗效标准评估结果显示达到二代流式MRD阴性。
图3-1.淋巴细胞监测情况
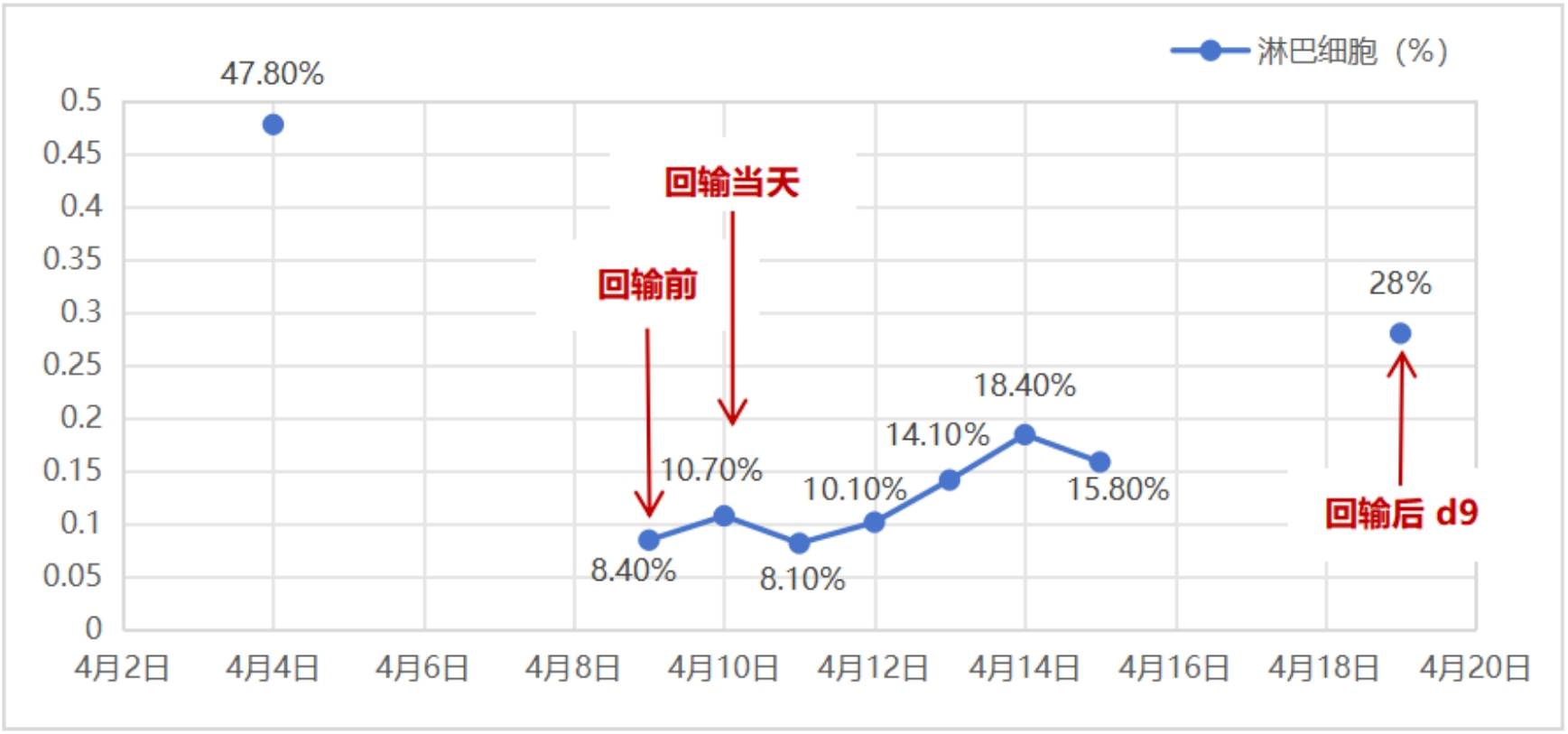
图 3-2.体温监测情况(2018 年 4 月 3 日-4 月 23 日)
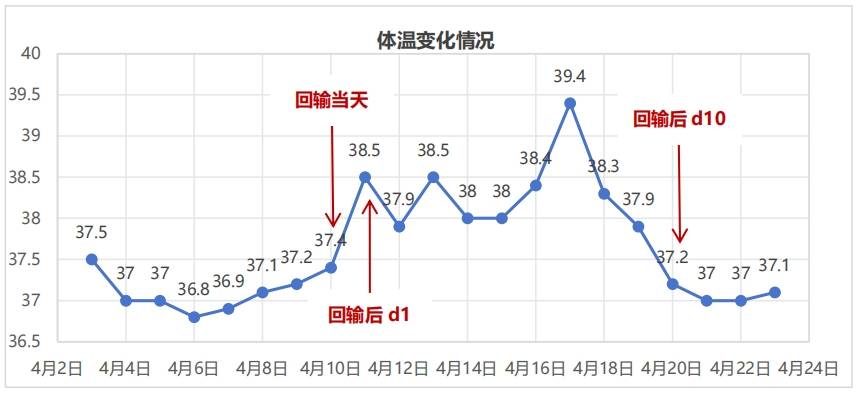
图 3-3.CAR-T 细胞扩增监测(回输当天至回输后第 112 天)
分析讨论
2016年Ali等人5全球首次报道了抗BCMA CAR-T细胞疗法治疗复发/难治性MM,证实其有效性和安全性。随后,国内外陆续开展了大量的抗BCMA CAR-T细胞治疗MM的相关临床研究,目前总体有效率在73%~100%,部分研究中严格意义上的完全缓解/完全缓解率超过50%。本病例采用的是泽沃基奥仑赛(CT053)CAR-T细胞疗法,2022版中国CAR-T共识显示其sCR/CR率在79%,同类中表现卓越,同时泽沃基奥仑赛的mPFS为22.7个月6,2023年ASH最新3年随访数据显示mPFS已达到25个月7。在mPFS方面,从数据上来看,泽沃基奥仑赛表现更好。除外BCMA CAR-T细胞疗法与治疗淋巴瘤的CAR-T具有相似的CRS发生率,同时超过80%的患者会发生3级及以上的血液学毒性;但重度CRS和ICANS的发生率较其他B细胞肿瘤低。本病例使用泽沃基奥仑赛治疗后未发生ICANS和重度CRS,安全性良好。
表4-1.国内外部分BCMA CAR-T细胞治疗多发性骨髓瘤的临床研究
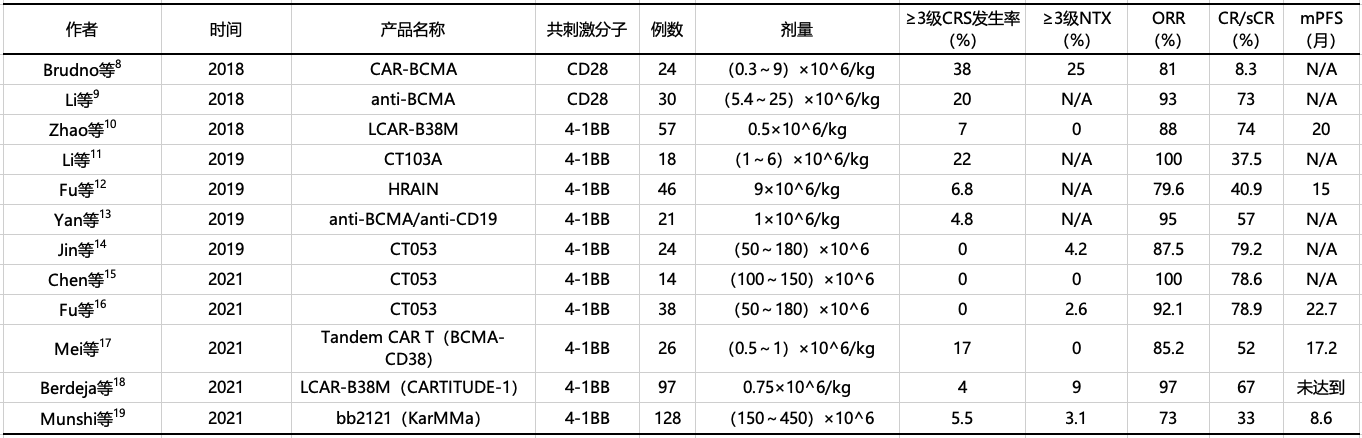
注:BCMA:B细胞成熟抗原;CAR-T细胞:嵌合抗原受体T细胞;CRS:细胞因子释放综合征;NTX:神经毒性;ORR:总缓解率;sCR/CR:严格意义的完全缓解/完全缓解;PFS:无进展生存;N/A:未报告。
目前常用的预处理方案包括环磷酰胺联合氟达拉滨或环磷酰胺单药等,但推荐的常用方案为氟达拉滨(25 mg/m2,-5~-3 d)联合环磷酰胺(300 mg/m2,-5~-3 d)预处理方案,预处理的方案跟能否获得更好的治疗反应及持续缓解密切相关20。从各款BCMA CAR-T临床研究中的预处理方案来看,目前只有CT053和HRAIN采用了标准的氟达拉滨(25 mg/m2,-5~-3 d)联合环磷酰胺(300 mg/m2,-5~-3 d)预处理方案;尽管FDA已获批的LCAR-B38M、bb2121两款CAR-T采用了同样的环磷酰胺剂量,但氟达拉滨的剂量相对更高(30 mg/m2,-5~-3 d),具体见表4-2所示。本病例采用了标准的环磷酰胺联合氟达拉滨预处理方案,清淋效果良好。
表4-2.国内外部分BCMA CAR-T细胞治疗多发性骨髓瘤临床研究的预处理方案
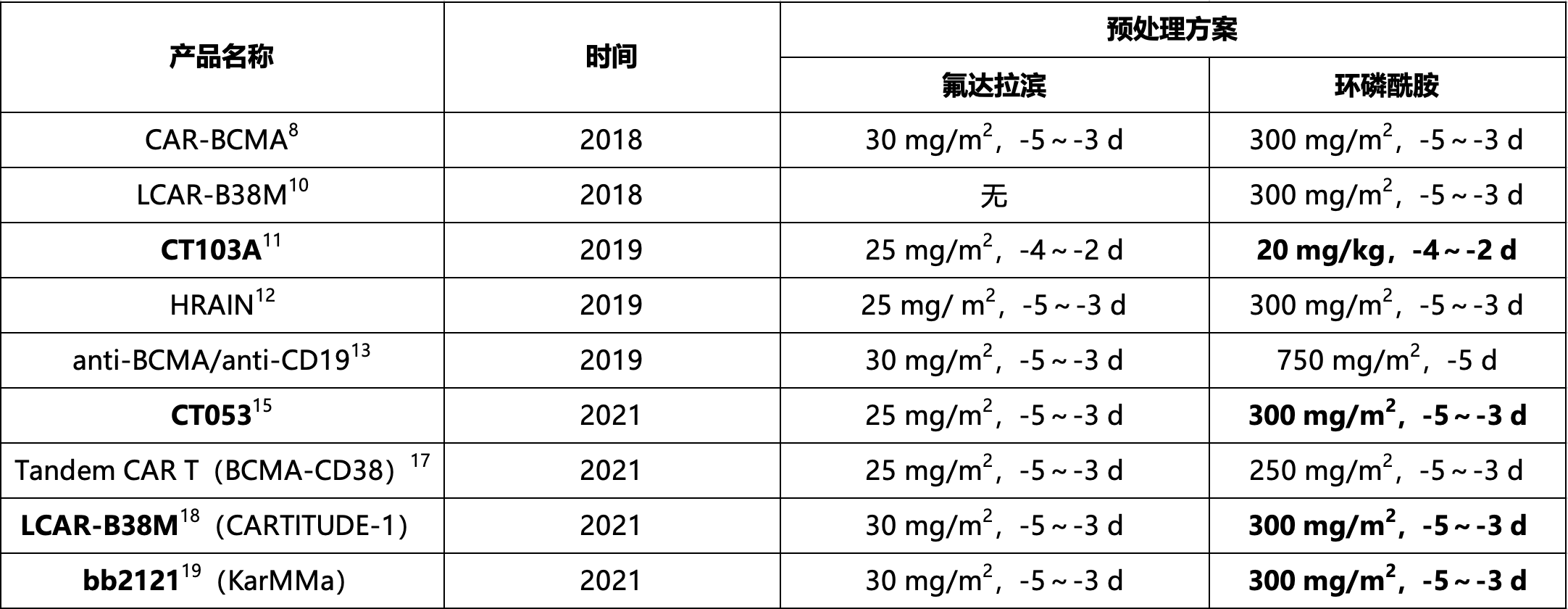
注:BCMA:B细胞成熟抗原;CAR-T细胞:嵌合抗原受体T细胞。
在CAR-T细胞治疗后持续缓解的影响因素方面,据Cappell KM等人2023年发表在Nat Rev Clin Oncol(IF=78.8)的综述20显示,CAR-T细胞治疗的疗效(包括初始治疗反应及持续缓解)与CAR-T 细胞动力学中的CAR-T细胞峰值水平有一定相关性,而与CAR-T细胞在体内的存续时间似乎并没有相关性。本例患者虽然8周后CAR-BCMA copies无法检测到,但是患者一直处在缓解状态,总的缓解时间达到60个月以上(260周+)。除细胞动力学中的CAR-T细胞峰值水平以外,持续缓解还与治疗反应深度、恶性血液肿瘤类型、肿瘤大小和位置、预处理方案等密切相关。
泽沃基奥仑赛是国内原研的一款全人源靶向BCMA CAR-T产品。目前,基于相关IIT、Ⅰ、Ⅱ期临床数据显示泽沃基奥仑赛在有效性和安全性方面表现优异,同类中优势显著。
①泽沃基奥仑赛长缓解,12个月PFS率85.7%,mPFS长达25个月,同类中表现卓越
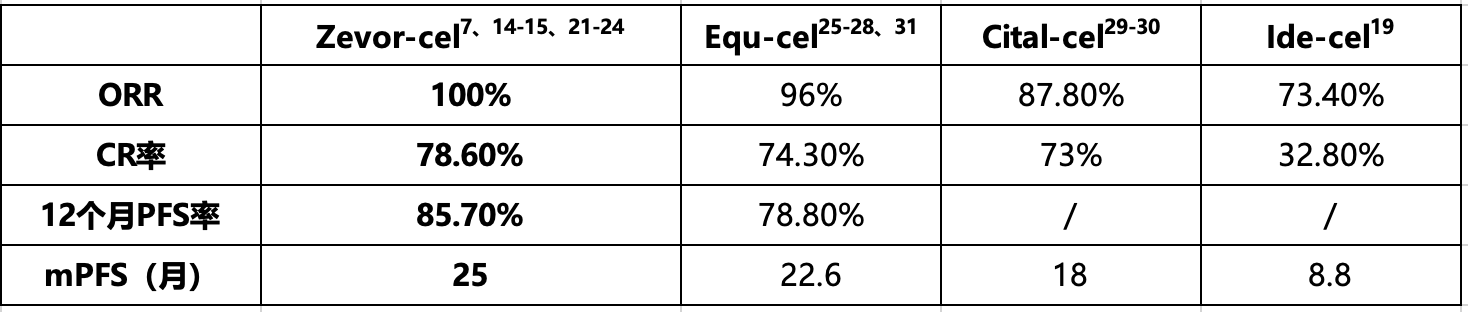
注:ORR:客观缓解率;CR:完全缓解;mPFS:中位无进展生存期。Zevor-cel, 泽沃基奥仑赛,CT053;Equ-cel, 伊基奥仑赛, CT103A;Cital-cel, 西达基奥仑赛, LCAR-B38M;Ide-cel, 艾基维仑赛, bb2121。
②泽沃基奥仑赛唯一固定剂量,3级以上CRS发生率低,治疗相关死亡率低,安全耐受
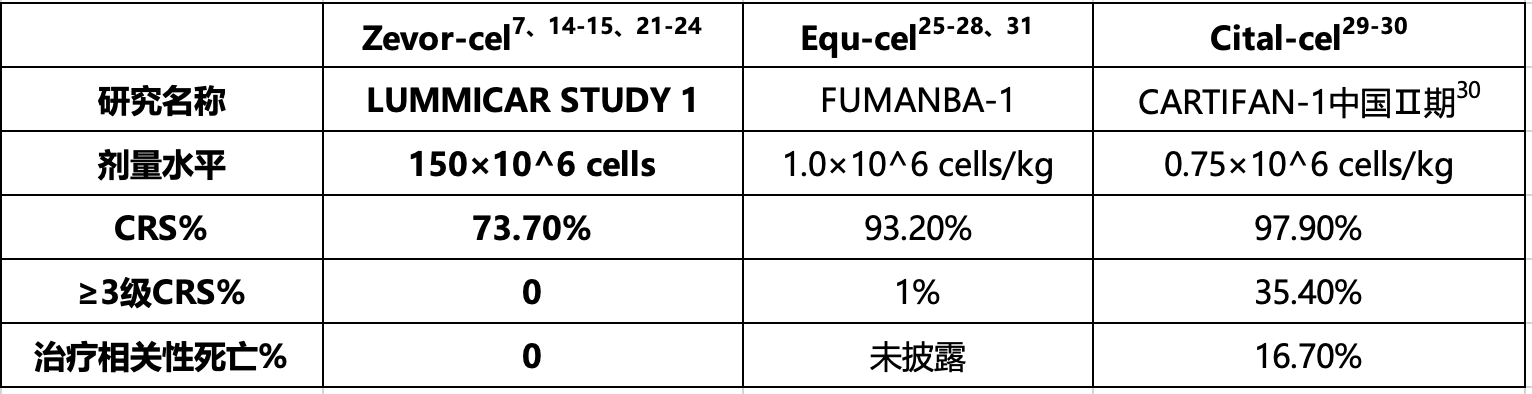
注:CRS:细胞因子释放综合征。Zevor-cel, 泽沃基奥仑赛,CT053;Equ-cel, 伊基奥仑赛, CT103A;Cital-cel, 西达基奥仑赛, LCAR-B38M;Ide-cel, 艾基维仑赛, bb2121。
泽沃基奥仑赛及同类CAR-T的临床试验数据汇总显示:①泽沃基奥仑赛CAR-T治疗后能够实现长期疾病控制,12个月PFS率85.7%高于CT103A的78.8%,mPFS长达25个月,高于LCAR-B38M的18个月和bb2121的8.8个月,泽沃基奥仑赛在有效性方面表现优异,3年OS率为92.9%7,从数据上来说,同类中最高。②泽沃基奥仑赛是唯一一个采用固定剂量给药的CAR-T产品,固定剂量为150*106个CAR BCMA阳性细胞,使用更加方便;同时3级以上CRS发生率低,治疗相关死亡率低,可安全耐受。
本例病例为经单抗治疗早期复发的高危MM患者,预后较差,后经泽沃基奥仑赛CAR-T细胞疗法治疗后达到严格意义上的完全缓解,长期随访显示PFS超过60个月。以上结果表明泽沃基奥仑赛治疗高危MM患者疗效显著,安全性良好,能够真正助力临床及患者实现MM疾病的长期控制,甚至是治愈。
专家点评
浙江大学医学院附属第一医院血液科名誉主任、学科带头人
浙江大学血液肿瘤(诊治)重点实验室主任
浙江省血液病临床研究中心主任
浙江大学癌症研究院恶性血液病团队负责人
国家卫建委临床重点学科-浙一医院血液学科带头人
浙江省重点创新团队-白血病基础与临床研究创新团队带头人
中国女医师协会血液学专委会主任委员
中国抗癌协会血液病转化专委会前任主任委员
CSCO抗白血病联盟副主任委员
CSCO抗淋巴瘤联盟常务委员
中国医师协会血液学会常委委员
中国医师协会整合血液学会副主任委员
海峡两岸血液学会、中国健促会常务委员
浙江医学会血液学分会前任主任委员
浙江省医师学会血液学分会会长
享受国务院特殊政府津贴,全国卫生系统先进工作者
在Lancet Oncology、Cell、Blood、Leukemia等SCI收录杂志上发表学术论文270余篇
以第一获奖人获得国家科技进步二等奖1项、浙江省科技进步1-3等奖9项
金洁教授点评
该患者为年轻女性,前期采用充分治疗后(包括3线采用抗CD38单抗治疗)病情再次进展的高危IgG-λ型多发性骨髓瘤患者,DS分期ⅢA期,ISS分期ⅡA期,预后相对较差。后线采用泽沃基奥仑赛CAR-T细胞疗法治疗,达到严格意义上的完全缓解,且IMWG MRD疗效标准评估为二代流式MRD阴性。长期随访结果显示PFS超过60个月。尽管该病例是泽沃基奥仑赛IIT试验中的个案报道,但以上结果初步表明了泽沃基奥仑赛的疗效显著,安全性良好,能够真正助力临床及患者实现疾病的长期控制,期待其早日上市后能够惠及更多MM患者。
浙江大学医学院附属第一医院
中国抗癌协会血液病转化委员会常委兼秘书长
浙江省抗癌协会血液肿瘤委员会委员
中国女医师协会血液专委会秘书兼青年委员会副主任委员
国家食品药品审评中心国家级核查员
获浙江首届“优秀青年副主任医师”称号,及2018年度浙江省医师协会优秀青年医师称号
负责国家自然基金、浙江省自然基金、省科技厅级课题一项。从事多发性骨髓瘤,B细胞淋巴瘤亚专科方向。先后参加多项国家项目等重大课题的研究工作。在Front Oncol、Hematologica、British Journal of Hematology、Leukemia Lymphoma等杂志发表多篇论文。作为主要参与人获得浙江省科技进步奖三等奖、浙江省医药卫生科技进步奖二等奖。
杨敏教授用药体会
该患者为40岁年轻女性,前期经过一线标准治疗及自体移植,复发后经过挽救治疗再次疾病进展,后入组新药CD38单抗临床试验仍早期复发,当时2018年已无其它新药可用于该病患。作为较早开展复发/难治性多发性骨髓瘤CAR-T临床试验的中心,患者恰巧符合泽沃基奥仑赛(CT053)IIT临床试验的入排标准,后续患者单采及回输过程顺利,回输后观察到患者出现发热,CRS 1级,ICANS 0级,对症治疗后经评估顺利出院。后续随访超 60个月,患者持续缓解。
综上可见泽沃基奥仑赛疗法表现出优异的安全性以及持续深度的缓解特性,同时泽沃基奥仑赛能够明显改善高危MM患者的生存预后,进而帮助更多患者获益。
排版编辑:Jessica
1.中华血液学杂志, 2022, 43(10) : 810-817.
2.Soekojo CY,et al.Blood (2020) 136 (Supplement 1): 51–52.
3.Pasvolsky O, et al. Transplant Cell Ther. 2023 Dec;29(12):757-762.
4.郭智,等. CVAD方案序贯治疗多发性骨髓瘤的临床研究[J].肿瘤研究与临床,2015,27 (4): 246-249.
5.Ali SA, et al. Blood. 2016 Sep 29;128(13):1688-700.
6.中华血液学杂志, 2022, 43(4) : 265-271.
7.Fu CC, et al. Blood. 2023;142(Suppl. 1):4845.
8.Brudno JN,et al.J Clin Oncol. 2018 Aug 1;36(22):2267-2280.
9.Li CR,et al.Blood (2018) 132 (Supplement 1): 1013.
10.Zhao WH, et al. J Hematol Oncol. 2018 Dec 20;11(1):141.
11.Li CR,et al. Blood (2019) 134 (Supplement_1): 929.
12.Fu WJ,et al. Blood (2019) 134 (Supplement_1): 3154.
13.Yan ZL,et al. Lancet Haematol. 2019 Oct;6(10):e521-e529.
14.Jin J, et al.Blood (2019) 134 (Supplement_1): 4435.
15.Chen WM, et al.Blood (2021) 138 (Supplement 1): 2821.
16.Fu CC,et al.Blood (2021) 138 (Supplement 1): 1751.
17.Mei H,et al. J Hematol Oncol. 2021 Oct 9;14(1):161.
18.Berdeja JG, et al. Lancet. 2021 Jul 24;398(10297):314-324.
19.Munshi NC, et al.N Engl J Med. 2021 Feb 25;384(8):705-716.
20.Nat Rev Clin Oncol. 2023 Jun;20(6):359-371.
21.Yang M, et al. Haematologica. 2022 Aug 1;107(8):1960-1965.
22.Chen WM, et al.Blood (2020) 136 (Supplement 1): 49–50.
23.Chen WM, et al.Blood (2022) 140 (Supplement 1): 4564–4565.
24.Chen WM, et al.2022 ASH Poster #1994.
25.Wang D, et al. Blood. 2021 May 27;137(21):2890-2901.
26.Li CR, et al. Journal of Clinical Oncology. 2023 ASCO #8025.
27.Li CR, et al.Blood (2022) 140 (Supplement 1): 7435–7436.
28. Li CR, et al. Blood(2023) 142 (Supplement 1): 761.
29.Zhao WH, et al. J Hematol Oncol. 2022 Jul 6;15(1):86.
30.Mi JQ, et al. J Clin Oncol. 2023 Feb 20;41(6):1275-1284.
31.Li CR, et al. Blood (2023) 142 (Supplement 1): 4854.











 苏公网安备32059002004080号
苏公网安备32059002004080号


