2023 ESMO年会日前已圆满落幕,肺癌领域数项临床研究披露重磅结果,Dato-DXd在肺癌领域的首个III期TROPION-Lung01研究亮相ESMO主席大会。TROPION-Lung05也在口头报告专场公布阳性结果。Dato-DXd单药及联合疗法在近两年学术会议上频繁更新研究数据,在肺癌领域显示出极大应用潜力。本期【肿瘤资讯】特邀上海交通大学附属胸科医院陆舜教授点评Dato-DXd相关研究进展。
免疫、靶向和化疗是当前晚期NSCLC治疗重要的 “三驾马车”,很大程度上改善了晚期NSCLC患者的生存获益。但耐药是不可避免的临床难题,在免疫治疗和靶向治疗进展后的治疗选择及疗效均有限,仍存在大量未被满足的临床需求,研究者和临床医生高度关注和亟需更有效、更安全的新型疗法。令人鼓舞的是,使用Dato-DXd单药方案的研究TROPION-Lung01[1]是ADC在肺癌领域首个取得阳性结果的III期国际多中心随机对照研究,将为有或无可靶向基因组改变(AGA)晚期经治NSCLC患者带来全新的后线治疗选择。
III期TROPION-Lung01力证:Dato-DXd对比化疗明显延长经治晚期NSCLC患者PFS
TROPION-Lung01是一项开放标签、全球化、III期随机对照研究,旨在评估Dato-DXd对比多西他赛用于伴有或无可靶向基因组改变(AGA)经治晚期NSCLC患者的疗效和安全性。其研究结果首次在今年ESMO主席大会专场重磅公布。分别有299例和305例患者被随机分配接受Dato-DXd(6.0mg/kg,IV,Q3W)或多西他赛(75mg/m2,IV,Q3W)治疗。主要终点是按RECIST v1.1标准由BICR评估的无进展生存期(PFS)和总生存期(OS),次要终点包括BICR评估的客观缓解率(ORR)、缓解持续时间(DoR)和安全性。
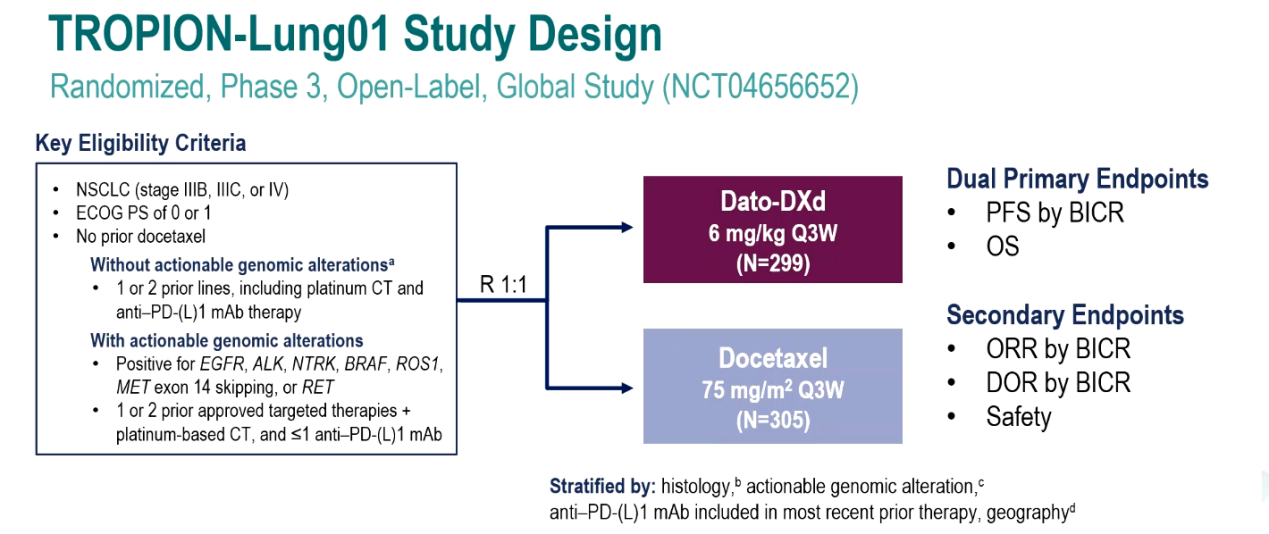 图1 研究设计
图1 研究设计
截至2023年3月29日数据分析时,Dato-DXd组和多西他赛组的中位随访时间分别为13.1个月和13.0个月。结果显示,两组患者基线特征均衡,Dato-DXd组和多西他赛组携带AGA患者占比均为17%,两组中分别有17%和15%的患者基线时有脑转移,Dato-DXd组和多西他赛组分别有43%/42%的患者既往接受过2线及以上的治疗。
表1 基线特性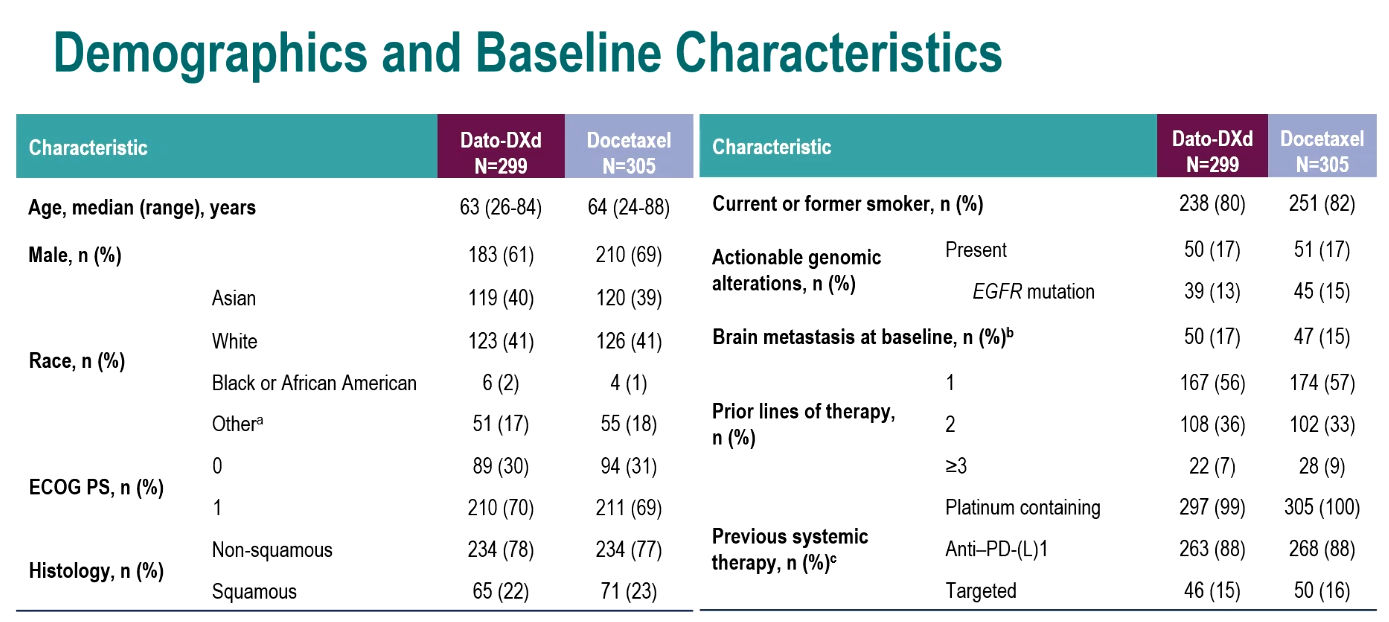
Dato-DXd对比多西他赛显著提升PFS,使全人群患者疾病进展或死亡风险显著降低25%(HR=0.75),确认的ORR分别为26.4%和12.8%,Dato-DXd对比多西他赛提升ORR超2倍,中位DoR分别为7.1个月和5.6个月。
亚组分析中,非鳞状NSCLC患者(包括有和无AGA)中观察到Dato-DXd对比多西他赛显著提升PFS(5.6 vs 3.7个月),Dato-DXd延长PFS近2个月,降低疾病进展或死亡风险达37%(HR=0.63)。Dato-DXd组和多西他赛组的ORR分别为31.2%和12.8%,对比多西他赛,Dato-DXd提升ORR近3倍。总体而言,无论是否存在AGA,Dato-DXd能为患者带来超2倍或近3倍的客观缓解,单药可降低患者疾病进展或死亡风险最高达37%。
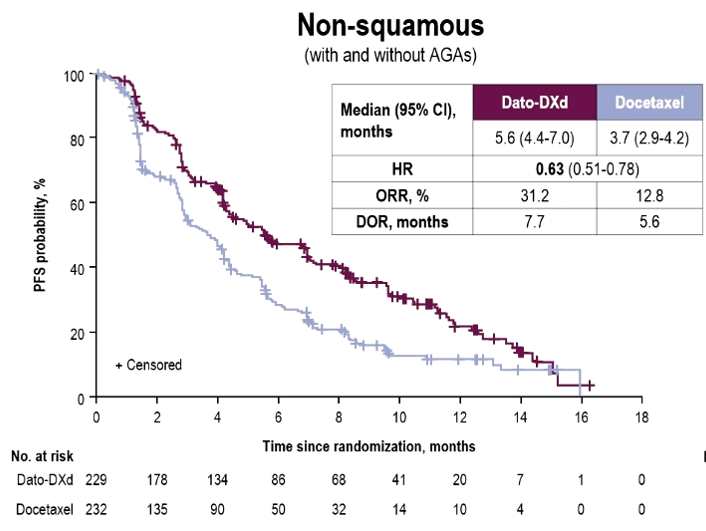 图2 非鳞状NSCLC患者PFS结果
图2 非鳞状NSCLC患者PFS结果
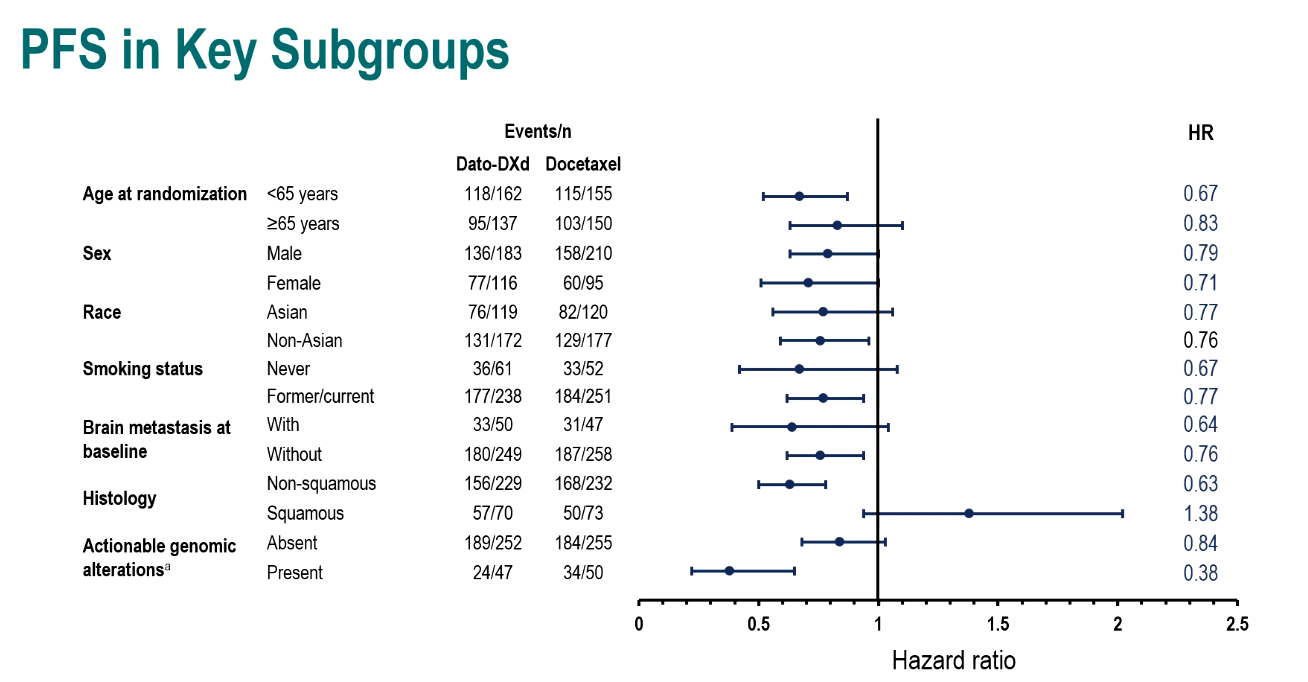 图3 关键亚组PFS分析
图3 关键亚组PFS分析
Dato-DXd组和多西他赛组的中位治疗持续时间分别为4.2个月和2.8个月。总体上,与多西他赛组(41%)相比,Dato-DXd组3级及以上治疗相关不良事件(TRAE)发生率(25%)更低,Dato-DXd组导致剂量减少、停药的TRAEs发生率更低。Dato-DXd组最常见的TRAEs是口腔炎(47%)和恶心(34%),且主要为1/2级。血液学毒性在多西他赛组中更常见,包括中性粒细胞减少(Dato-DXd组vs多西他赛组:4%/1% vs 26%/23%[任意级别/≥3])和发热性中性粒细胞减少(Dato-DXd组vs多西他赛组:7% vs 0.3%),未观察到新的安全性事件。
表2 总体安全性分析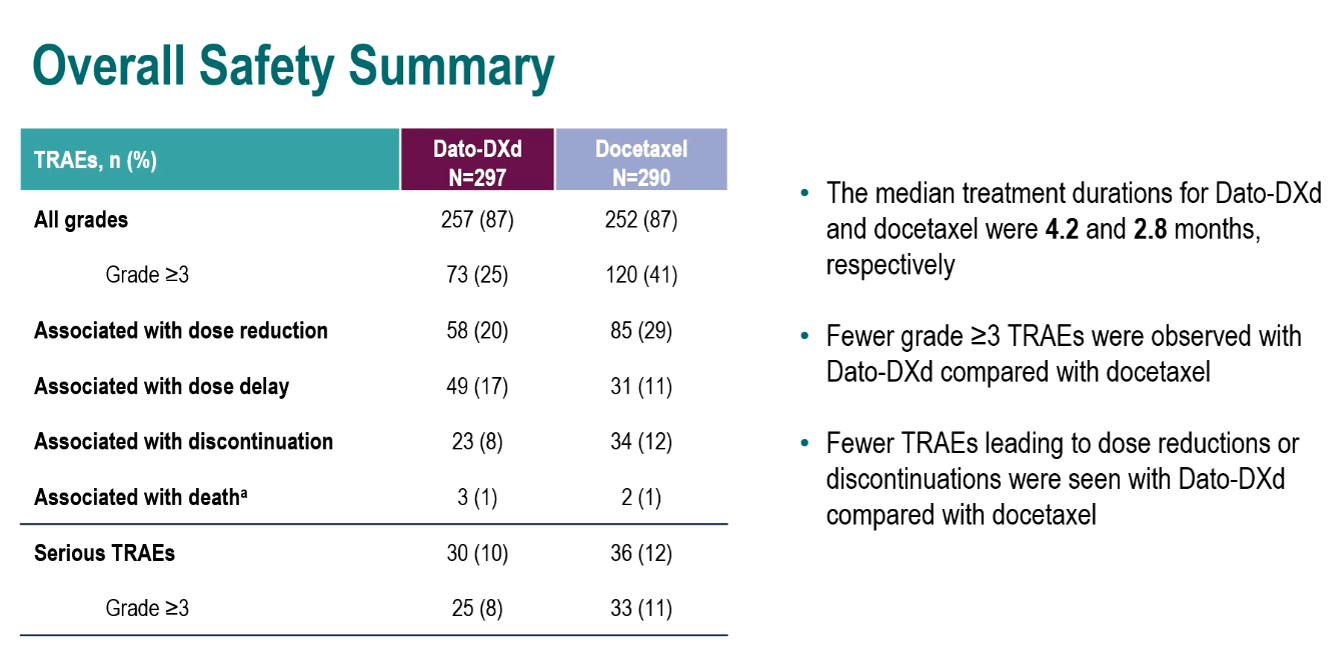
表3 常见不良事件分析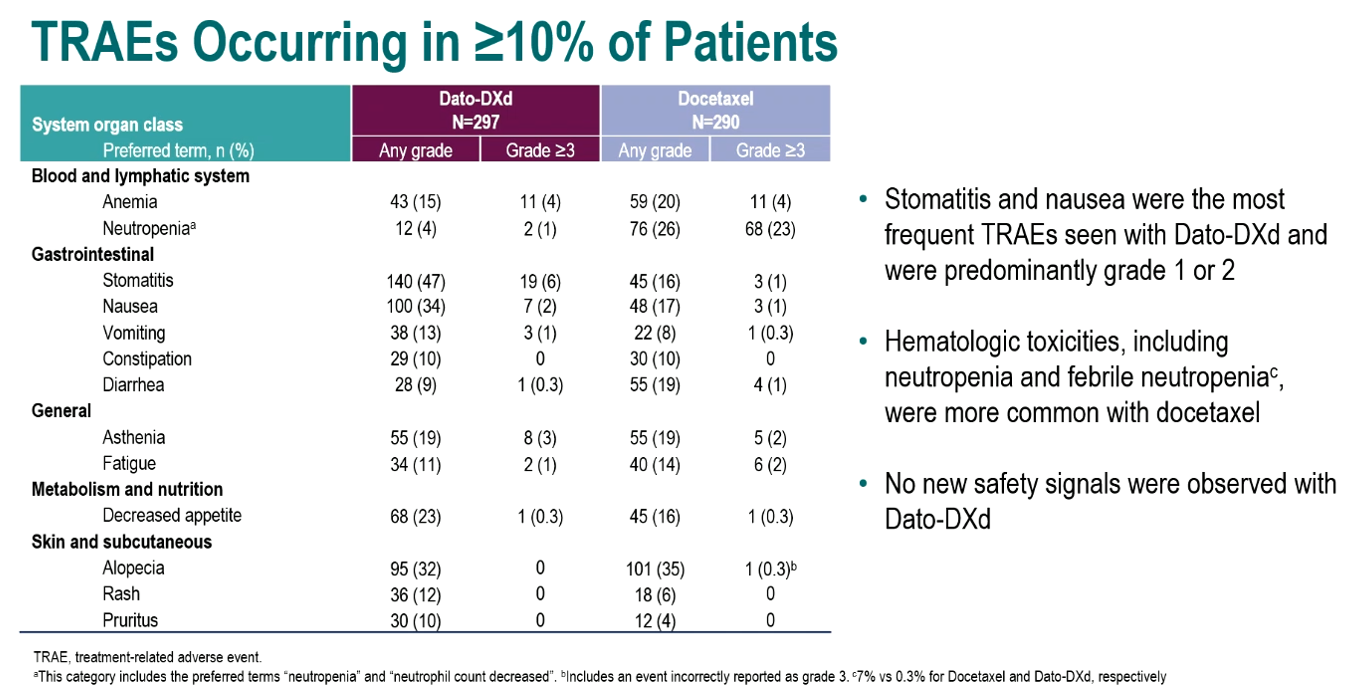
总体而言,此前TROPION-PanTumor01初步显示Dato-DXd单药极有潜力,有望改善目前晚期NSCLC二线治疗现状,有希望成为此类患者的新选择。此次公布的III期研究是目前为止ADC药物在肺癌领域的最高级别证据,同时也是最大样本量、最大规模的临床研究,结果进一步证实Dato-DXd在经免疫、靶向和化疗进展后的晚期患者中取得了PFS显著获益,是晚期NSCLC全人群二线治疗的突破,也是ADC药物在后线治疗的大突破。
Dato-DXd单药也因此成为首个在经治晚期NSCLC患者的后线治疗领域有明显PFS获益的ADC药物。此次详细研究结果的公布提示,Dato-DXd是经治非鳞状NSCLC患者极有潜力用于临床的新型疗法。
结构属性决定疗效和安全性,Dato-DXd因此率先取得成功
针对多种靶点开发而来的ADC药物不断有新进展,包括HER2、TROP2、HER3、MET、CEACAM-5以及近年来新兴的双特异抗体等,目前ADC药物已发展至第三代。近年来发展最为火热的ADC当属TROP2 ADC,研究者利用DXd-ADC技术开发出了针对TROP2的新型ADC——Dato-DXd。此外,TROP2 ADC还包括戈沙妥珠单抗(SG)、SKB264等新型ADC药物。Dato-DXd能从此类ADC药物中率先突围,并得到III期研究的证实,离不开其明显的结构优势[2,10]:
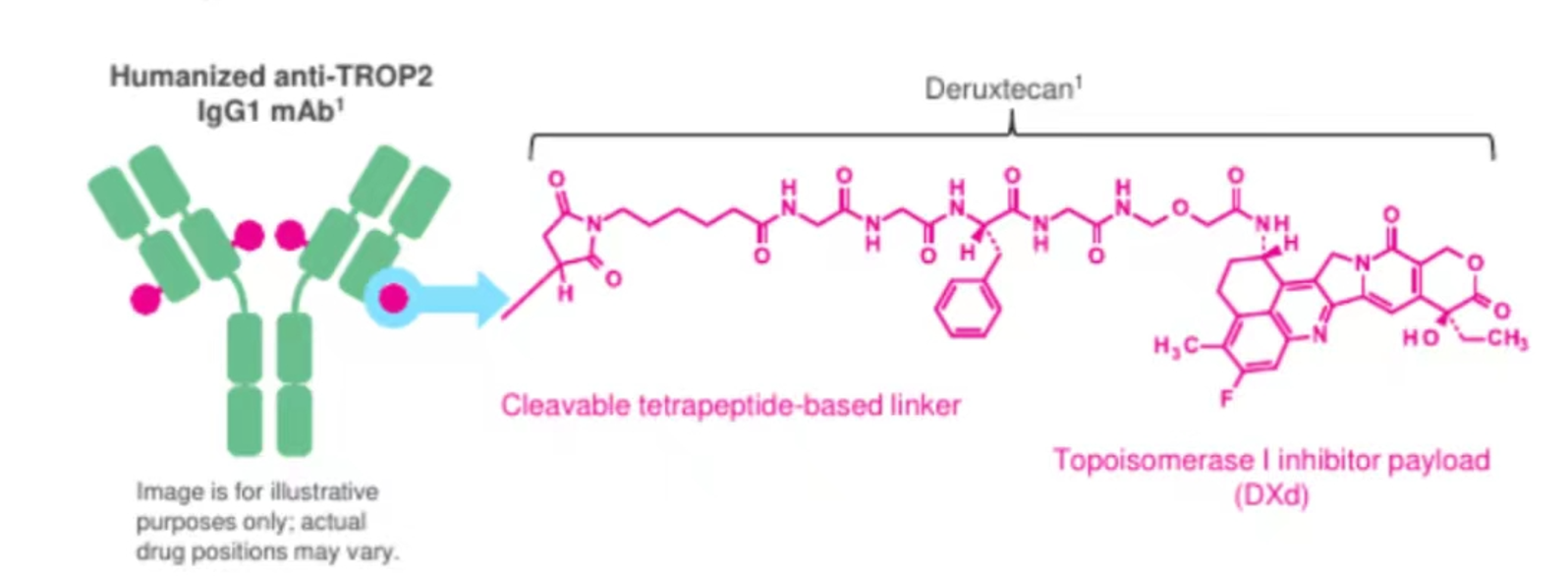 图4 Dato-DXd结构示意图
图4 Dato-DXd结构示意图
高效且半衰期短的游离DXd:①DXd衍生物可阻断DNA复制,强效杀伤肿瘤细胞而被ADC选用为有效载荷,其活性约是SN-38(SG载荷)的10倍。②游离DXd的半衰期非常短,有利于控制全身毒性。TROP2 ADC半衰期长则不利于全身毒性的控制。
稳定且肿瘤选择性的可裂解四肽连接子:在血液循环中稳定的连接子使完整ADC在血浆中保持高稳定性,因此全身毒性小。Dato-DXd仅在肿瘤特异性上调的溶酶体作用下而释放DXd,可避免载荷提前释放,从而使DXd特异性杀伤肿瘤并有利于控制毒性。而采用酸敏感连接子的其他TROP2 ADC,可在肿瘤溶酶体低PH环境以及酸性肿瘤微环境中被释放,导致更高的脱靶效应而使系统毒性增加。
优化药物抗体比率(DAR)的抗体:Dato-DXd在设计之初即最优化了DAR。研究显示,DAR为7(vs 4)时显示更窄的治疗窗、更差的耐受性。因此,Dato-DXd采用的DAR优化为4,兼顾了安全性与疗效,以最大化治疗窗。
后线到一线全线布局:Dato-DXd研究进展盘点
二线及以上治疗领域
Ib期TROPION-PanTumor01研究
TROPION-PanTumor01最初在2021年WCLC大会上首次亮相,今年6月,JCO杂志公布最新结果,这是一项关于Dato-DXd的首次人体剂量递增和剂量扩展研究[2]。研究纳入复发/难治性晚期NSCLC患者,入组患者在每周期的第1天接受Dato-DXd(Q3W)。剂量递增部分旨在确定Dato-DXd 0.27-10mg/kg的最大耐受剂量(MTD),剂量扩增队列旨在确定4、6 或8 mg/kg Dato-DXd的疗效和安全性。主要终点包括确认MTD、安全性和耐受性。结果显示,6mg/kg Dato-DXd显示出可耐受的安全性,且显示较好的疗效。
Dato-DXd在经多线治疗的晚期NSCLC患者中显示出令人鼓舞的抗肿瘤活性和可控的安全性。入组患者中50%以上患者接受了3线及以上的治疗。21.7%患者接受了5线及以上治疗,Dato-DXd仍展现出优异的疗效和可接受的安全性。6mg/kg Dato-DXd的ORR、DCR分别达到26%和70%,中位DoR为10.5个月,中位PFS和中位OS分别达6.9个月和11.4个月。
II期TROPION-Lung05研究[3]
今年ESMO大会上,TROPION-Lung05研究在口头报告专场公布结果,这是一项全球化、开放标签、II期研究,旨在评估Dato-DXd用于经靶向疗法和含铂化疗进展后AGA晚期NSCLC患者的疗效。主要终点是由BICR评估的确认的ORR,次要终点包括DoR、DCR和安全性。结果显示,共137例患者接受1剂治疗,中位年龄为60岁,72%患者既往接受过针对晚期或转移性疾病的3线及以上的治疗,所有患者均接受过化疗,36%患者既往接受过PD-L1/PD-1单抗,60%患者既往接受过针对AGA的靶向疗法。
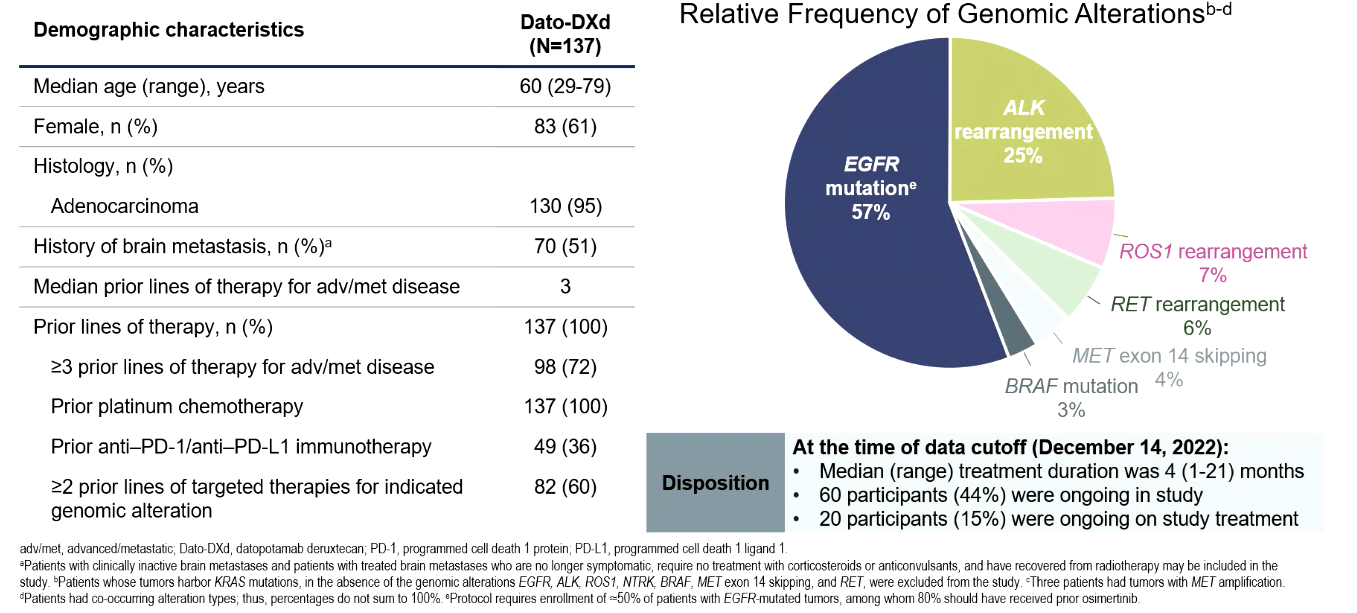 图5 患者基线特征
图5 患者基线特征
截至2022年12月14日,中位随访时间为15.2个月,总人群的ORR为35.8%,DCR为78.8%,中位DoR为7个月;EGFR突变患者确认的ORR超过40%,达到43.6%,DCR达到82.1%,中位DoR为7个月。在EGFR敏感突变或T790M突变患者中,既往接受奥希替尼治疗患者的ORR接近50%,达49.1%。
总体上,早期研究显示,Dato-DXd单药在经初始治疗进展的全人群患者中、以及经靶向和化疗进展的AGA患者中均显示出优异的疗效和良好的耐受性。
表4 疗效分析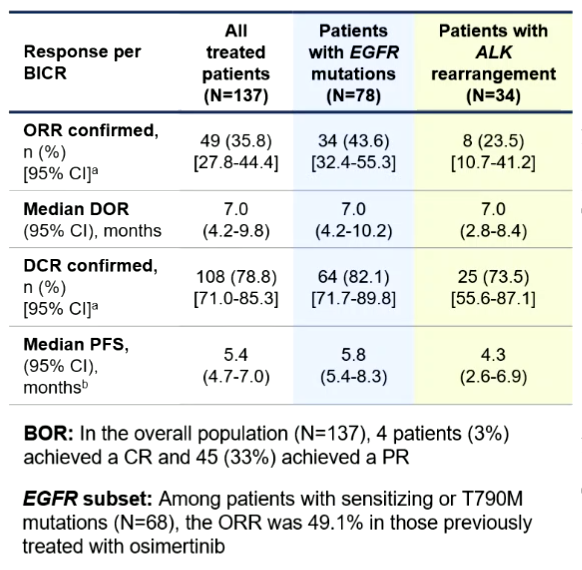
一线治疗领域
Ib/II期TROPION-Lung02研究
TROPION-Lung02 是一项全球性、剂量递增、Ib 期扩展研究,旨在评估Dato-DXd +帕博利珠单抗±含铂化疗用于无驱动基因突变晚期NSCLC患者的疗效和安全性。2022 WCLC大会上该研究首次公布结果[4],在75例可评估疗效患者中,两药和三药用于一线治疗时的ORR分别为62%和50%。二线治疗的ORR分别为24%和29%。今年ASCO大会上,该研究公布更新结果[5]。数据截止时,共136例患者接受治疗。两药组和三药组分别有36%和46%患者仍在接受治疗。一线治疗时Dato-DXd+帕博利珠单抗(两药)的ORR为50%,Dato-DXd+帕博利珠单抗+含铂化疗(三药)的ORR高达57%,DCR均为91%;用于任意治疗线数时,两药和三药的ORR达到38%和49%,DCR高达84%和87%,中位DoR均未达到,双药和三药组的中位PFS分别为8.3个月和7.8个月。
表5 疗效分析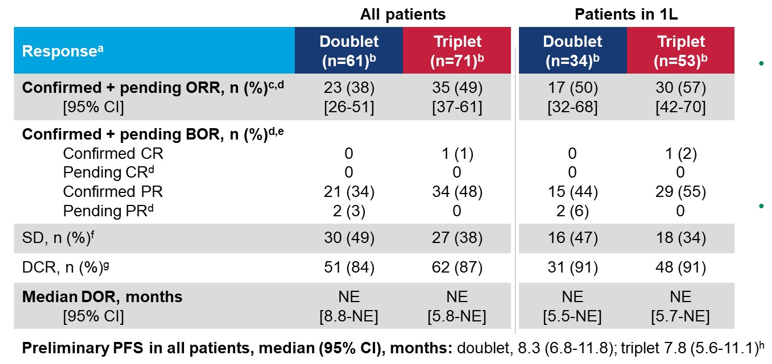
Ib/II期TROPION-Lung04研究
今年WCLC大会上,TROPION-Lung04首次公布中期分析结果[6],这是一项Ib期、多中心、开放标签、剂量递增/确认和扩展研究,旨在探索Dato-DXd+度伐利尤单抗±卡铂治疗晚期/转移性NSCLC患者的疗效。此次分析来自队列1~4数据。患者接受Dato-DXd(队列1/3:4mg/kg,队列2/4:6mg/kg)+度伐利尤单抗(1120mg)+至多4周期卡铂(队列3/4 AUC=5)治疗,Q3W,直至疾病进展或出现不可耐受的毒性。截至2023年3月6日,队列1(n=5)、队列2(n=19)和队列4(n=14)共38例患者可评估疗效。队列2(两药)和队列4(三药)剂量扩展未观察到DLT。在队列2(两药)一线治疗患者中,ORR和DCR分别可达到50.0%和92.9%;在队列4中,三药的疗效更高,ORR高达76.9%,DCR高达92.3%。
总体上,早期研究初步结果显示,一线Dato-DXd+PD-1/PD-L1单抗均显示良好的疗效和耐受性。基于此,研究者正在III期研究中进一步验证一线Dato-DXd+PD-1/PD-L1单抗的结果。
表6 疗效分析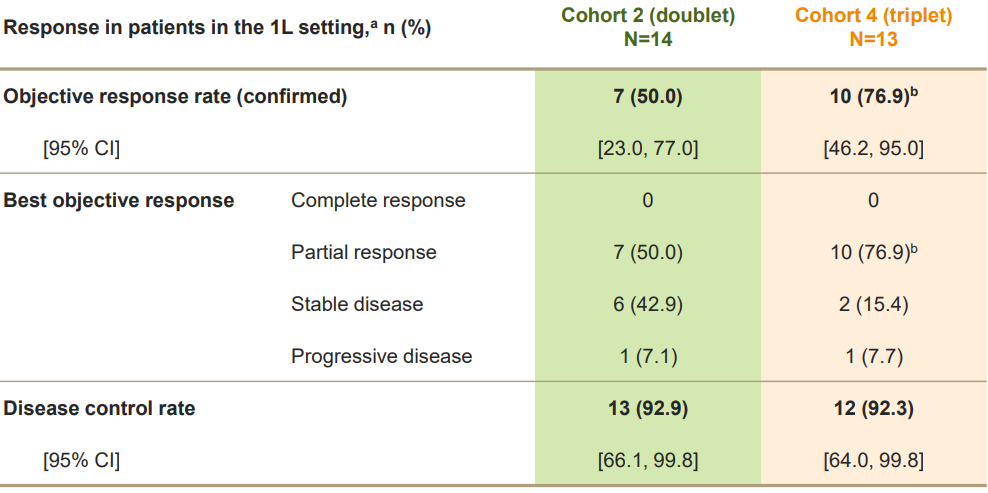
III期TROPION-Lung08研究[7]
该研究在今年WCLC大会上公布设计方案,这是一项全球、随机化、开放标签、III期随机对照研究,旨在探索Dato-DXd+帕博利珠单抗对比帕博利珠单抗一线治疗无驱动基因突变且PD-L1≥50%晚期NSCLC的疗效。主要终点为BICR评估的PFS和OS。
III期AVANZAR研究[8]
AVANZAR同样在今年WCLC大会上公布设计方案,这是一项开放标签、III期随机对照研究,旨在评估Dato-DXd+度伐利尤单抗+化疗用于晚期NSCLC患者的疗效和安全性。入组患者将按1:1比例随机分配接受Dato-DXd(6.0mg/kg)+度伐利尤单抗(1120 mg)+卡铂(AUC 5)序贯Dato-DXd+度伐利尤单抗维持治疗,或按组织学类型接受帕博利珠单抗联合化疗。双重主要终点为BICR评估的TROP2阳性患者的PFS和OS。AVANZAR计划纳入来自230个地区约1000例NSCLC患者,目前该研究正在入组中。该研究同样头对头比较了Dato-DXd联合免疫对比目前免疫联合化疗标准方案的疗效。
III期TROPION-Lung07研究[9]
令人关注的是,今年ESMO大会上该研究公布了设计方案,这是一项全球化、开放标签、III期随机对照研究,计划招募约975例患者,PD-L1 TPS<50%、无AGA、不适合手术的IIIB/IIIC以及IV期非鳞状NSCLC患者入组研究,并按1:1:1随机分配接受Dato-DXd+帕博利珠单抗+化疗、Dato-DXd+帕博利珠单抗、帕博利珠单抗+化疗,直至疾病进展或出现不可耐受的毒性。主要终点是BICR评估的PFS和OS,关键次要终点为BICR评估的ORR,其他次要终点包括研究者评估的PFS、ORR、BICR和研究者评估的DOR、TTR、DCR等。该研究直接头对头比较Dato-DXd联合免疫治疗vs 标准治疗用于PD-L1 TPS<50%晚期NSCLC患者的疗效,目前该研究正在患者入组中。
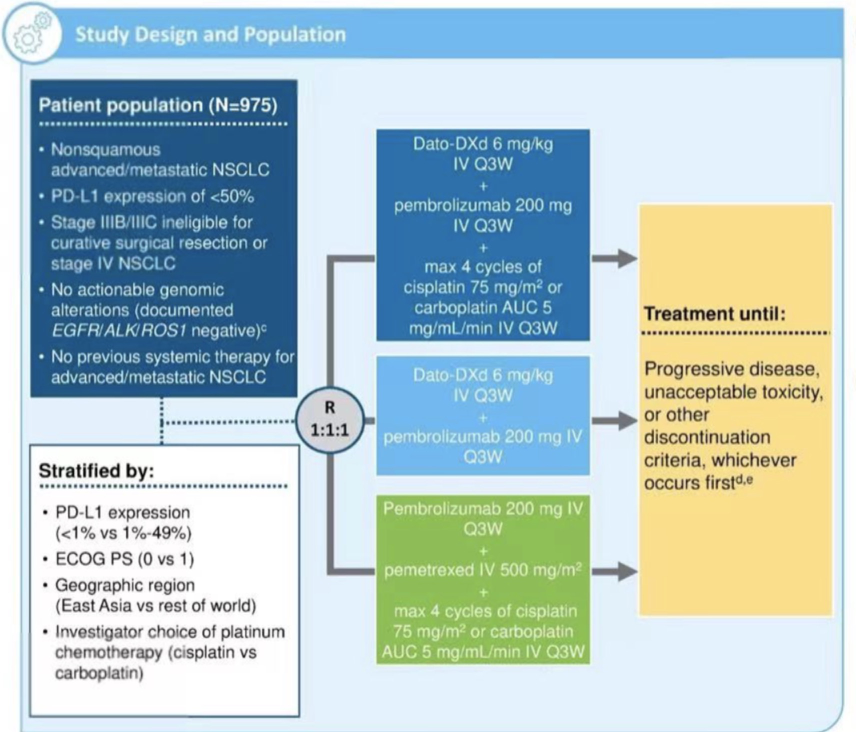
图6 研究设计
Dato-DXd联合免疫治疗在一线治疗领域崭露头角,目前开展的一系列研究令Dato-DXd联合疗法一线应用充满期待。
陆舜教授:靶向和免疫治疗为晚期NSCLC带来了前所未有的变局,目前二者分别是驱动基因阳性和阴性患者的基石方案,但不得不提的是,靶向或免疫和化疗治疗后进展的晚期患者的后线治疗目前面临着较大困境,而且多项免疫联合策略的探索包括SAPPHIRE、CANOPY-02、CONTACT-01、LEAP-008等研究折戟沉沙。因此,从临床研究的探索到临床实践的治疗策略,此类患者均面临着较大的挑战。继HER2 ADC之后,TROP2 ADC再度迎来突破,开发者利用DXd-ADC 技术开发出具有更高活性和更低毒性的Dato-DXd,临床前研究显示出良好的疗效和安全性,其首次人体试验TROPION-PanTumor01显示,Dato-DXd在经多线治疗NSCLC患者中显示出优越的疗效和可控的安全性。
今年ESMO大会上,该领域首个III期TROPION-Lung01研究的公布为Dato-DXd单药用于靶向或免疫和化疗进展后晚期患者提供了高级别循证医学证据,结果提示Dato-DXd为非鳞状NSCLC带来新的力量和希望,具有极大潜力能成为新疗法,同时期待后续更多的研究结果。同期公布的TROPION-Lung05结果提示,Dato-DXd单药在伴有AGA尤其是经靶向治疗后进展的EGFR突变患者中更具有疗效优势,同样期待后续更多研究结果的公布。此外,从今年学术会议上公布的多项早期研究结果来看,Dato-DXd联合免疫治疗已展现出更令人鼓舞的疗效,研究者也正在III期研究中验证这一疗效,期待这种模式能在一线治疗领域大展拳脚,同样期待更多的研究数据能为晚期NSCLC患者带来新的曙光。
主任医师,博士生导师,二级教授 ,国家卫生健康突出贡献中青年专家,上海市领军人才,上海市优秀学术带头人,国家重点专项首席专家,享受国务院特殊津贴
上海交通大学附属胸科医院,上海市肺部肿瘤临床医学中心主任
上海交通大学医学院学术委员会委员
中国抗癌协会理事,肺癌专业委员会前任主任委员
中国临床肿瘤学会(CSCO)常务理事 ,希斯科基金会副理事长
DIA中国区顾问委员会副主席
上海市医学会肿瘤学会前任主任委员
中华医学会肿瘤学会常委,肺癌专家委员会主任委员
上海市医师协会肿瘤科分会副会长,专科规培组长
国际肺癌研究会(IASLC)出版委员会委员
美国临床肿瘤协会(ASCO)中国区代表
国际肺癌研究会官方杂志Journal of Thoracic Oncology,Lung Cancer副主编,The Oncologist杂志编委
上海市抗癌协会常务理事
中国医药生物技术协会精准医疗分会副主任委员
作为负责人主持科技部国家慢病重点专项,国际合作课题;国家新药创新重大专项,863重大课题子课题2项;国家自然基金重点项目和面上项目
中国抗癌协会科技奖一等奖;上海市医学科技奖一等奖;华夏医学科技奖二等奖;上海市科技进步一等奖;上海交通大学校长奖; 2018年获得仁心医者·上海市杰出专科医师提名奖,2021获“药明康德生命化学研究奖”
[1]LBA12-Datopotamab deruxtecan (Dato-DXd) vs docetaxel in previously treated advanced/metastatic (adv/met) non-small cell lung cancer (NSCLC): Results of the randomized phase III study TROPION-Lung01.2023ESMO.
[2] Shimizu T, Sands J, Yoh K, et al. First-in-Human, Phase I Dose-Escalation and Dose-Expansion Study of Trophoblast Cell-Surface Antigen 2-Directed Antibody-Drug Conjugate Datopotamab Deruxtecan in Non-Small-Cell Lung Cancer: TROPION-PanTumor01. J Clin Oncol. 2023 Jun 16:JCO2300059. doi: 10.1200/JCO.23.00059. Epub ahead of print. PMID: 37327461.
[3] 1314MO-TROPION-Lung05: Datopotamab deruxtecan (Dato-DXd) in previously treated non-small cell lung cancer (NSCLC) with actionable genomic alterations (AGAs) .2023ESMO.
[4]MA13.07 - TROPION-Lung02: Initial Results for Datopotamab Deruxtecan Plus Pembrolizumab and Platinum Chemotherapy in Advanced NSCLC.2022 WCLC.
[5]TROPION-Lung02: Datopotamab deruxtecan (Dato-DXd) plus pembrolizumab(pembro) with or without platinum chemotherapy (Pt-CT) in advanced non-small cell lung cancer.9004 Oral Abstract Session,2023 ASCO
[6] Abstract OA05.06-Datopotamab Deruxtecan (Dato-DXd) + Durvalumab ± Carboplatin in Advanced/mNSCLC: Initial Results from Phase 1b TROPION-Lung04.2023 WCLC.
[7]P2.08-01TROPION-Lung08: Datopotamab Deruxtecan Plus Pembrolizumab in Untreated Advanced/Metastatic Non-small Cell Lung Cancer (NSCLC).2023WCLC
[8]P2.04-02AVANZAR: Phase III Study of Datopotamab Deruxtecan (Dato-DXd) + Durvalumab + Carboplatin as 1L Treatment of Advanced/mNSCLC.2023WCLC.
[9]1505TiP-TROPION-Lung07: A phase III trial of datopotamab deruxtecan (Dato-DXd) plus pembrolizumab (pembro) with or without platinum chemotherapy (Pt-CT) as first-line (1L) therapy in advanced/metastatic (adv/met) non-small cell lung cancer (NSCLC) with PD-L1 expression.2023ESMO.
[10]Okajima D, Yasuda S, Maejima T, et al. Datopotamab Deruxtecan, a Novel TROP2-directed Antibody-drug Conjugate, Demonstrates Potent Antitumor Activity by Efficient Drug Delivery to Tumor Cells. Mol Cancer Ther. 2021 Dec;20(12):2329-2340. doi: 10.1158/1535-7163.MCT-21-0206. Epub 2021 Aug 19. PMID: 34413126; PMCID: PMC9398094
排版编辑:Maggie











 苏公网安备32059002004080号
苏公网安备32059002004080号


