本次2023 ESMO大会上,Adagrasib联合帕博利珠单抗一线治疗携带KRASG12C晚期NSCLC的KRYSTAL-7研究的更新数据[1]在Proffered Paper session专场重磅公布。在PD-L1 TPS≥50%的患者中,Adagrasib联合帕博利珠单抗ORR达到63%,肝脏相关TRAE发生率<10%。我们有幸邀请到浙江大学医学院附属第一医院的周建娅教授为我们解读。
浙江大学医学院附属第一医院呼吸内科副主任(主持工作)
浙江省呼吸系统疾病临床医学研究中心主任
中国临床肿瘤学会(CSCO)理事,非小细胞肺癌专委会委员
中国临床肿瘤学会(CSCO)肿瘤生物标志物专家委员会常委
中华医学会呼吸分会烟草病学组委员
浙江省抗癌协会肺癌专委会青委,肿瘤标记物专委会委员
国家药监总局新药核查专员
美国约翰霍普金斯医院Sidney Kimmel癌症中心访问学者
主持国家自然基金3项,发表第一作者SCI论文10余篇,主参多项国际多中心临床试验。
研究设计
KRYSTAL-7研究(NCT04613596)II期研究队列部分纳入携带KRASG12C突变、未经治疗的局晚期/转移性NSCLC(允许稳定脑转移),一线接受Adagrasib联合帕博利珠单抗治疗(Cohort1a/2)或帕博利珠单抗单药治疗(Cohort1b)。主要终点是研究者评估的ORR,次要终点包括研究者评估的DOR、PFS、OS、安全性和PK。本次报道了Cohort1a/2中所有治疗患者的安全性和PD-L1 TPS≥50%患者的疗效。
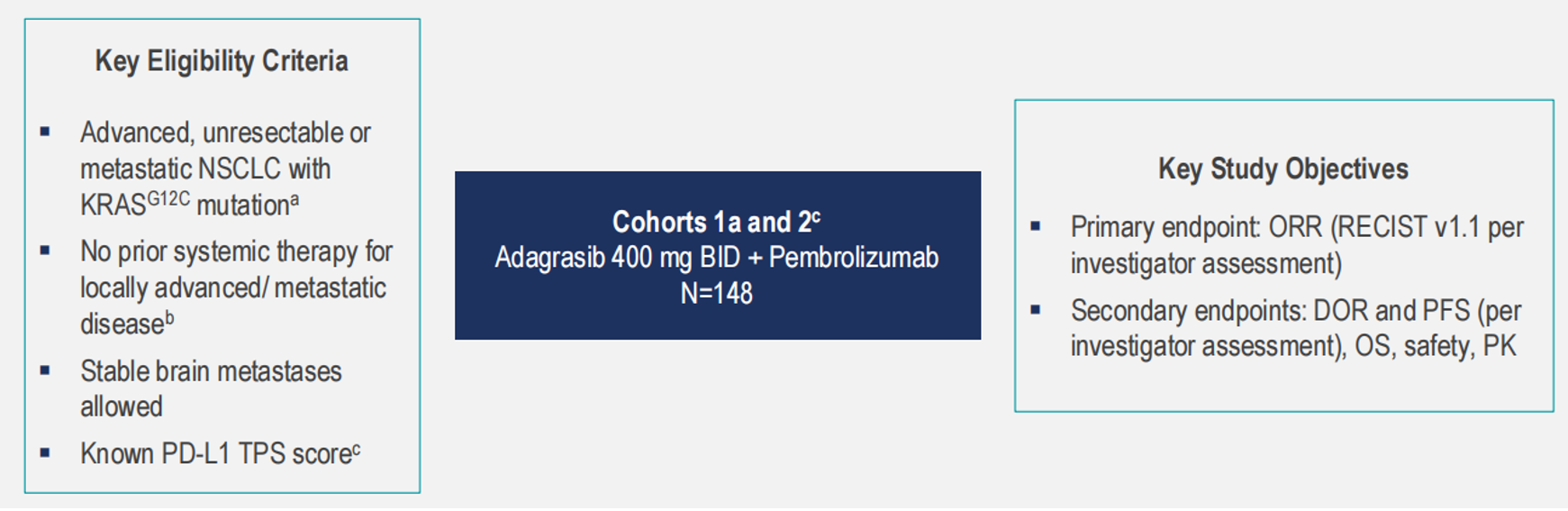
研究结果
截至2023年6月19日,共148例患者接受了Adagrasib+帕博利珠单抗治疗,中位随访时间为8.7个月,PD-L1 TPS≥50%的患者中位随访时间为10.1个月。
总人群的中位年龄为67岁,亚洲或其他种族人群占比18%,几乎所有患者有吸烟史或目前仍在吸烟,基线伴CNS转移的比例为14%。PD-L1 TPS≥50%的人群基线和总人群相近。
PD-L1 TPS≥50%的患者接受Adagrasib+帕博利珠单抗一线治疗的ORR为63% (32/51; 95% CI, 48–76),DCR为84% (43/51; 95% CI, 71–93)。曾出现过任何级别肝毒性的患者ORR为70% (14/20; 95% CI, 46–88)。中位应答时间为1.4个月,中位DOR未达到(95% CI, 12.6–NE),中位PFS未达到(95% CI, 8.2–NE)。
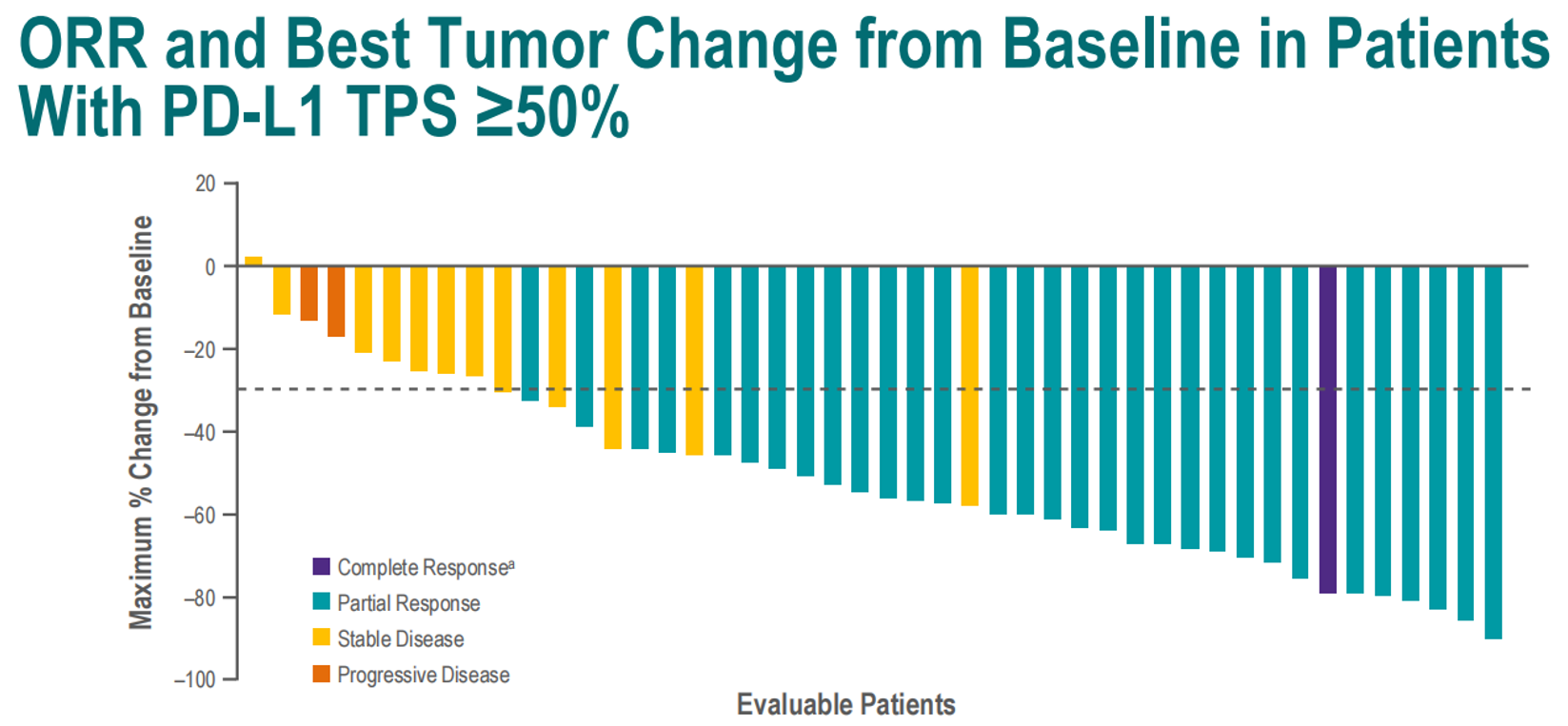
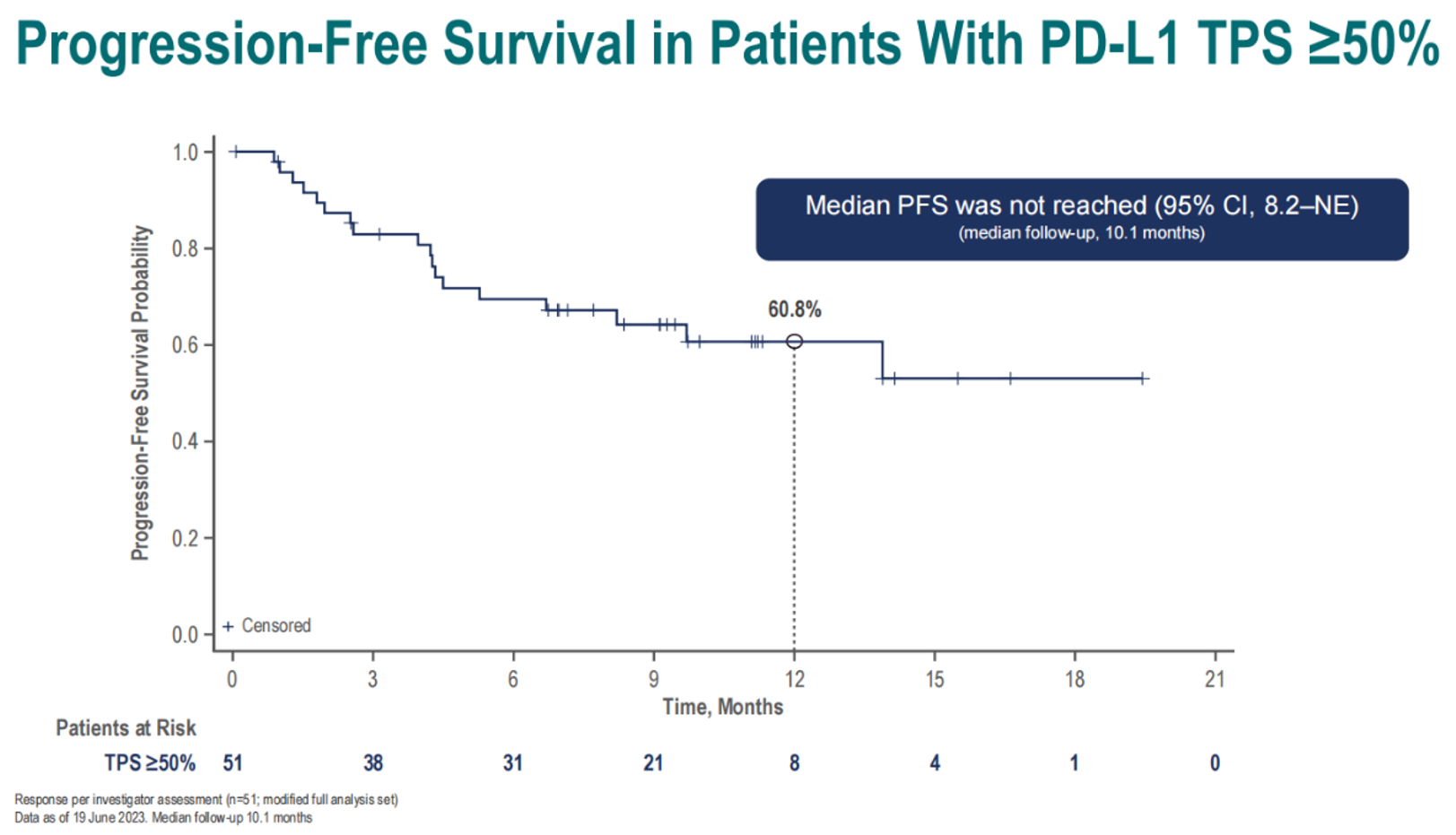
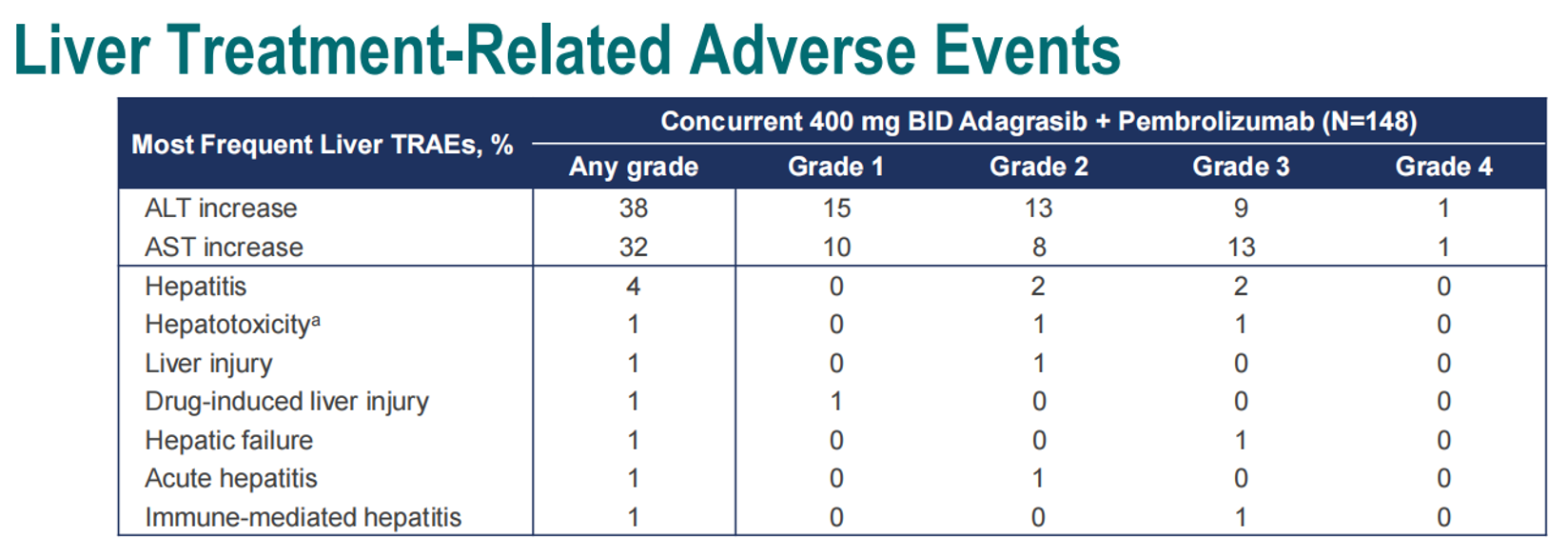
在所有患者中,出现任何级别TRAE的比例为94%(139/148),3级、4级、5级TRAE发生率分别为55%、 9%、 1%。任何级别和3级免疫相关TRAE的发生率分别是18%(26/148)和5%(8/148)。TRAE导致的Adagrasib剂量下调或中断治疗的比例分别是46%(68/148)和59%(88/148)。仅4%(6/148)的患者因TRAE永久停用了两种药物(TRAE导致Adagrasib或帕博利珠单抗永久停药的比例分别为6%(9/148)和11%(16/148))。
虽然有ALT/AST升高,但治疗相关肝脏事件的发生率<10%,没有患者因ALT/AST升高或肝脏TRAE而停药。大部分(约80%)的ALT/AST升高可以缓解,至首次缓解的中位时间为22天。
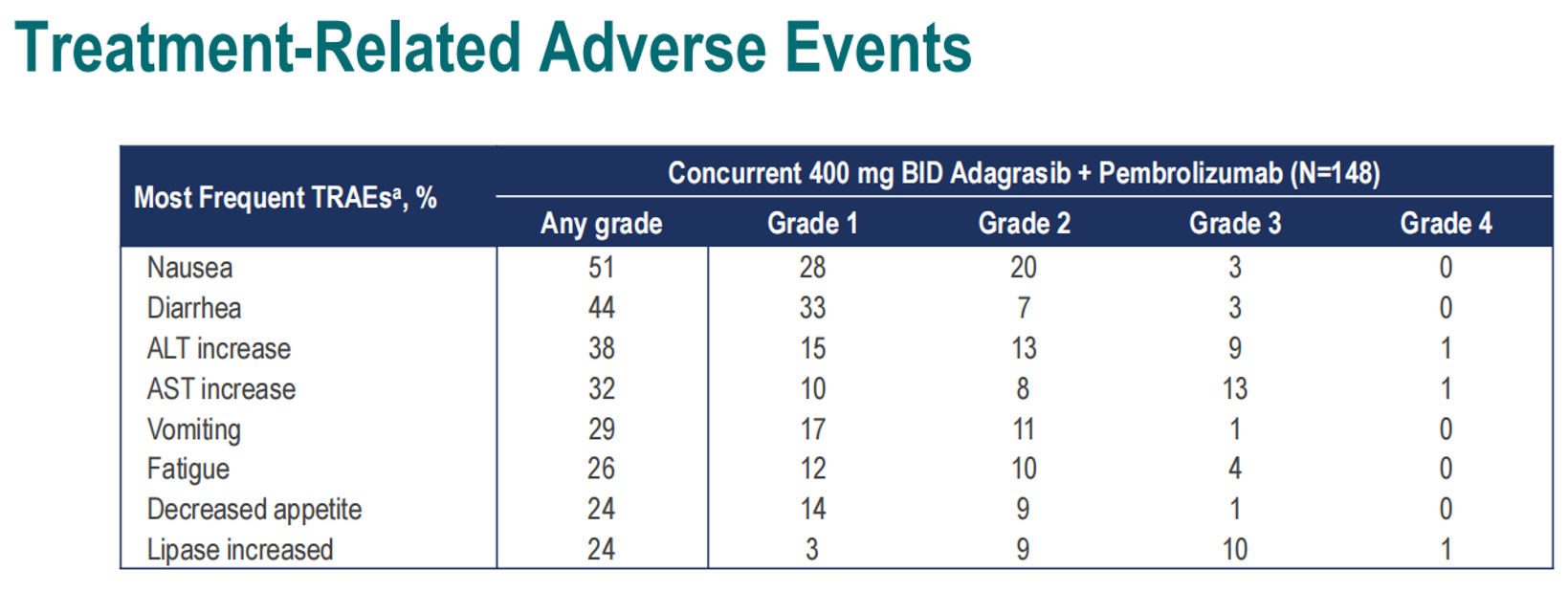
研究结论
在PD-L1 TPS≥50%的NSCLC患者中,Adagrasib联合帕博利珠单抗一线治疗展现出令人鼓舞的疗效和可控的安全性。
Adagrasib联合帕博利珠单抗的安全性与单药使用相似。肝脏相关的TRAE绝大部分为低级别且可控,大部分可管理,不会导致两药的停用。
在PD-L1 TPS≥50%的患者中,与帕博利珠单抗单药相比,联合Adagrasib展现出更高的ORR(63% vs 39%-45%)。
周建娅教授点评
Adagrasib打破“不可成药”困境,KRASG12C阳性NSCLC进入靶向治疗时代
KRAS是NSCLC最早确定的驱动基因之一,其中KRASG12C在中国NSCLC发生率~3%[2],是NSCLC不容忽视的亚群。但由于KRAS蛋白表面光滑、近乎球形的结构,且无明显结合位点,要合成一种能靶向结合并抑制其活性的化合物非常困难,长期以来无法攻克。KRASG12C突变开关II结合口袋的发现,让共价抑制KRAS成为可能, Adagrasib是KRASG12C抑制剂的先行军,率先打破"不可成药"困境,开启KRASG12C阳性NSCLC靶向治疗时代。
2年随访数据显示Adagrasib二线治疗疗效持久,安全性可控
既往KRASG12C阳性NSCLC患者遵循驱动基因阴性治疗原则,二线接受免疫或单药化疗。然而,KRASG12C阳性NSCLC二线/三线接受培美曲塞或多西他赛的OS相比于KRASG12C阴性患者更短[3],是二三线化疗的不良预后因素,此类人群亟需新的治疗手段去满足临床需求。目前Adagrasib已获得FDA批准用于KRASG12C突变局部晚期或转移性NSCLC ≥2L治疗,并得到NCCN和CSCO指南的推荐,成为新的二线治疗选择。
在前不久结束的2023 WCLC大会上,Adagrasib二线治疗携带KRASG12C的不可切除或转移性NSCLC的KRYSTAL-1试验2年随访数据更新,仍显示出持久疗效,mDOR 12.4m,2年OS率31.3%。且在基线伴CNS转移的患者中,mOS长达14.7个月,与总人群OS获益一致,再次显示Adagrasib优秀的颅内活性[4]。目前Adagrasib全球3期验证性研究已经启动,将进一步验证其靶向治疗地位。中国也于2022年7月同步加入全球KRYSTAL-12研究,期待Adagrasib早日惠及中国患者!
一线Adagrasib联合帕博利珠单抗疗效喜人,安全可控
目前KRASG12C阳性NSCLC患者一线标准治疗以含铂化疗、免疫联合化疗或免疫单药(PD-L1 TPS≥50%)为主。一项来自FDA的汇总分析显示,CPI单药一线治疗ORR~35%,mOS~12个月;CPI+化疗ORR~50%,mOS~21个月。与其他驱动基因(EGFR、ALK等)不同的是,KRASG12C突变患者亦能从CPI治疗中获益,ORR、mOS和KRAS野生型相似[5]。这不禁让人思考KRASG12C抑制剂联合CPI是否能够进一步提高人群获益(尤其是对于化疗不耐受的患者,仍存在巨大未被满足的临床需求)。
本次KRYSTAL-7报道的数据显示,PD-L1 TPS≥50%的患者接受Adagrasib+帕博利珠单抗一线治疗的ORR达到63% (32/51; 95% CI, 48–76),DCR为84% (43/51; 95% CI, 71–93),12个月PFS率60.8%。相比于帕博利珠单抗单药一线治疗NSCLC的KEYNOTE-024/ KEYNOTE-042研究中的疗效数据(ORR 39%-46%,mPFS 6.5m-7.7m)[6],ORR数值上有较大的提升,从PFS率来看也提示Adagrasib+帕博利珠单抗可能带来更持久的获益。
联合治疗不可避免会带来安全性上顾虑,在既往报道的其他KRASG12C抑制剂联合CPI的研究中,出现较大的肝毒性[7]。而让我们感到欣慰的是,Adagrasib联合帕博利珠单抗一线治疗肝毒性较小,肝脏相关TRAE发生率<10%,且大多数是低级别可管理的,没有患者因ALT/AST升高或肝脏TRAE而停药。
Adagrasib是差异化的KRASG12C抑制剂,具有长半衰期(23h)、剂量依赖性PK、CNS穿透能力、优化的非共价结合能力和最小化半胱氨酸反应性的特点。具有较低峰谷比、稳定的PK特性以及最小化的半胱氨酸反应性使Adagrasib在肝脏和其他器官脱靶效应极小。本次KRYSTAL-7的数据也确实让我们看到了Adagrasibs联合CPI的可行性,让我们对KRASG12C抑制剂联合CPI的治疗模式有了更多信心。基于以上数据,Mirati 已计划开展KRYSTAL-7研究III期部分,在携带KRASG12C突变、PD-L1 TPS≥50%的NSCLC患者中,比较Adagrasib联合帕博利珠单抗vs 帕博利珠单抗单药一线治疗的疗效和安全性(NCT04613596),期待II期试验的结果能在III期试验中得到验证和夯实,带来临床治疗格局的改变。
总之,KRYSTAL-7研究初步数据展现了Adagrasib联合帕博利珠单抗一线治疗KRASG12C阳性NSCLC不错的疗效信号(PD-L1 TPS≥50%)和可控的安全性,为三期临床研究的开展提供了支持和信心。Adagrasib的研发并没有止步,我们也希望尽快看到总体人群队列(包括PD-L1 TPS<50%)、以及中国人群的疗效数据和安全性。
KRASG12C阳性NSCLC已正式进入靶向时代。新的药物需要不断的研究探索真正的获益人群。道阻且长,行则将至!期待以Adagrasib为代表的KRASG12C抑制剂能为患者带来更多治疗希望!
[1] Marina C. Garassino, et al. 2023 ESMO LBA65.
[2] Liu SY, et al. Biomarker Research.2020;8(1):22.
[3] Martin Svaton, et al. ANTICANCER RESEARCH 36: 1077-1082 (2016).
[4] Shirish M. Gadgeel, et al. 2023 WCLC, MA06.
[5] Erica C.Nakajima, et al. 2022ASCO. Abstract 9001.
[6] Reck M, et al, J Clin Oncol. 2022 Feb 20;40(6):586-597.
[7] Bob T. Li, et al. 2022 WCLC, OA03.06.
*仅供医疗卫生专业人士学术参考之用
ZMCNNP20231028001 Expire Date 2024/10/28
排版编辑:肿瘤资讯-CYX











 苏公网安备32059002004080号
苏公网安备32059002004080号


