随着特异性靶向治疗药物和免疫治疗药物的发展迭代,非小细胞肺癌(NSCLC)的治疗版图壮丽变革,为NSCLC患者带来了长生存曙光。表皮生长因子受体(EGFR)作为NSCLC的重要致癌驱动基因之一,始终是NSCLC领域研究的焦点。2023年10月20-24日,欧洲肿瘤内科学会(ESMO)年会在西班牙马德里隆重召开,EGFR突变晚期NSCLC的诸多创新疗法华彩呈现,引来了医疗界同仁的广泛瞩目。大会期间,特邀同济大学附属上海市肺科医院周彩存教授,分享晚期NSCLC的前沿进展和热议话题,解读最新研究成果及其对临床实践的影响。
同济大学附属上海市肺科医院 肿瘤科主任
同济大学医学院肿瘤研究所 所长
享有国务院特殊津贴
国际肺癌研究联合会(IASLC)董事会董事
CSCO 非小细胞肺癌专委会 主委
中国医促会胸部肿瘤分会 主委
上海抗癌协会肺癌分子靶向与免疫治疗专委会 主委
中国抗癌协会肿瘤药物临床研究专委会 候任主委
CSCO肿瘤转化医学专业委员会 候任主委
上海市领军人才、重中之重学科带头人
中国抗癌协会肺癌专业委员会 常务委员
中国医师学会肿瘤分会 常务委员
2023 ESMO 大会在20 日盛大开幕!大会前两日,晚期NSCLC的诸多重磅进展数据发布,这些研究结果的独特性、重要性将可能改变未来临床实践。在这其中,有哪些令您印象深刻的研究?可否简要介绍一下?
周彩存教授:今年ESMO大会上,有很多肺癌重磅研究发表。在EGFR 外显子20 插入突变(EGFR ex20ins)靶点研究中,PAPILLON研究[1]脱颖而出,展示了广阔的治疗前景。该研究是首个在晚期或转移性NSCLC 初治患者中,评估Amivantamab 联合化疗与单独化疗相比的疗效和安全性的Ⅲ期研究,成果令人振奋。在其它罕见靶点研究中,LIBRETTO-431研究[2]的成功报阳让原癌基因酪氨酸蛋白激酶受体RET基因融合阳性晚期NSCLC治疗再遇生机;KRYSTAL-7研究[3]中Adagrasib打破不可成药魔咒,满足初治原癌基因Kirsten大鼠肉瘤病毒癌基因同源物(KRAS) G12C突变NSCLC未尽之需。此外,晚期NSCLC领域也有针对新靶点的新药物在本次ESMO大会上公布最新研发进展。国产首创的EGFR×HER3双特异性抗体药物偶联物(ADC)药物BL-B01D1公布首次人体试验Ⅰ期研究结果,彰显EGFR抑制剂耐药后的治疗潜力[4];TROPION-Lung05 研究[5]的滋养细胞表面抗原2 (TROP2) ADC药物Dato-DXd 在既往经治的伴可靶向基因突变的晚期NSCLC中不断突破,进一步夯实了其在NSCLC领域的循证医学证据。晚期NSCLC领域研究硕果累累。总而言之,今年无疑是肺癌领域的重大突破之年,众多重磅研究隆重发布,预示着可能会对临床实践产生革命性影响,为患者带来更多治疗希望。
随着研发的深入,EGFR ex20ins 逐渐被攻克,针对EGFR ex20ins 靶点的新型治疗药物正在加速崛起,请问您如何评价本次会议上最新发布的EGFR ex20ins 领域重磅研究的疗效和安全性数据?这些研究对未来治疗格局有何影响?
周彩存教授:EGFR ex20ins 突变是EGFR 突变的一种亚型,在腺癌、女性、从不吸烟患者中常见,其恶性程度高,患者预后差[6]。不同于EGFR 常见突变 NSCLC患者,酪氨酸激酶抑制剂(TKI)治疗EGFR ex20ins NSCLC患者疗效不佳。近期,莫博赛替尼由于III期EXCLAIM-2研究确证性研究未达到主要研究终点,不符合FDA授予的附条件批准上市,因而申请主动退市[7]。而PAPILLON研究勇立潮头,成为EGFR ex20ins 领域一次划时代的里程碑。本次ESMO 大会公布的PAPILLON研究结果显示[1]:
Amivantamab联合化疗组相较于单独化疗组,在多个主要和次要研究终点中均观察到明显的治疗获益。无进展生存期(PFS)显著改善,从6.7个月提高到11.4个月[HR=0.395;P<0.0001];客观缓解率(ORR) 显著提高(73% vs. 47%),且缓解程度更深;缓解持续时间(DoR)也观察到显著延长(9.7 vs. 4.4个月)。
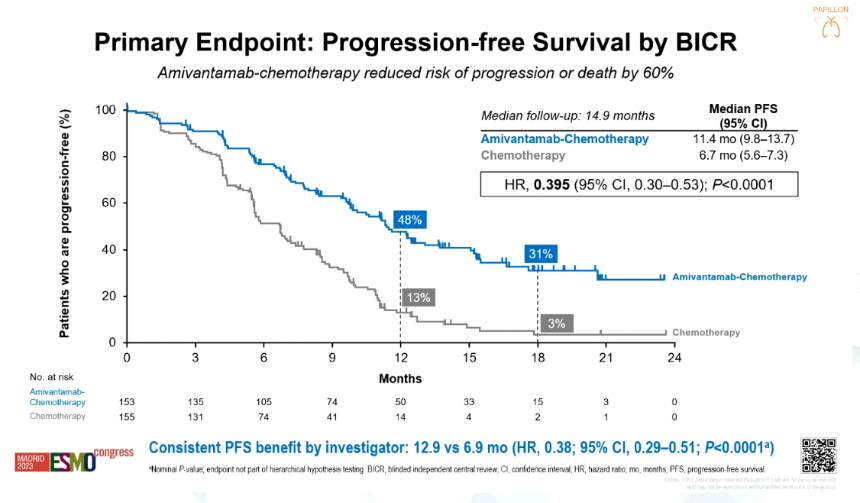 图1:PAPILLON研究的主要研究终点PFS
图1:PAPILLON研究的主要研究终点PFS
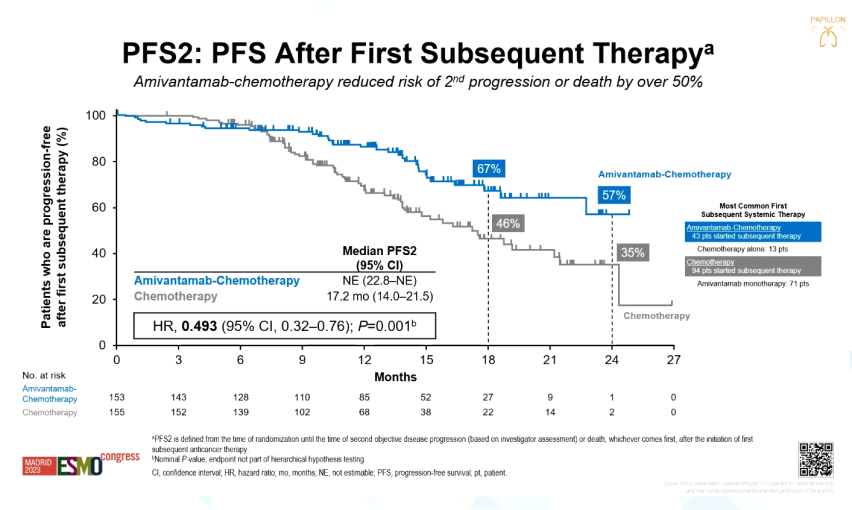 图2:PAPILLON研究中患者的PFS2
图2:PAPILLON研究中患者的PFS2
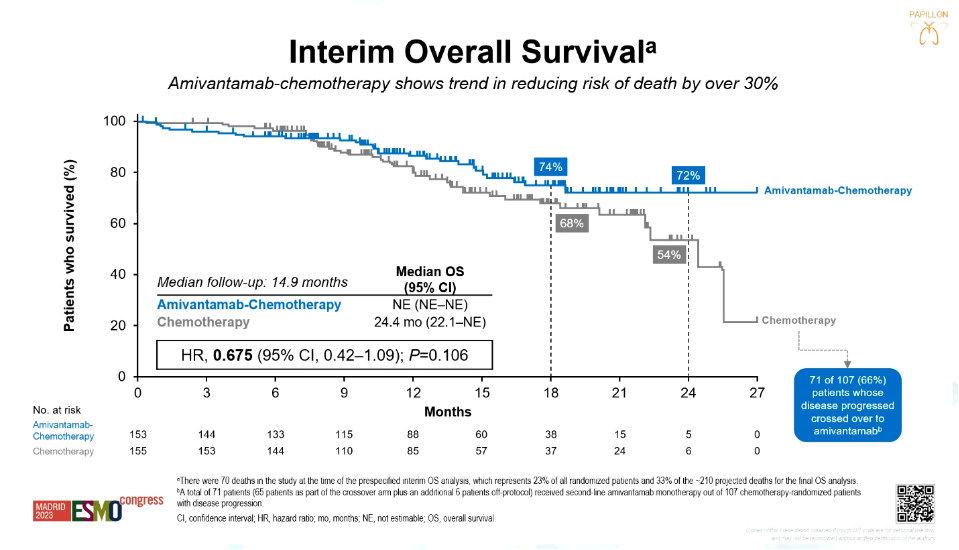 图3:PAPILLON研究中患者的OS
图3:PAPILLON研究中患者的OS
此外, Amivantamab联合化疗组安全性可控。虽然Amivantamab联合化疗产生的不良反应相较于单独化疗发生率高,但主要与EGFR和间质表皮转化因子(MET)抑制相关,如皮疹、腹泻等,临床医生针对此类不良反应有着丰富的管理经验。
PAPILLON研究在EGFR ex20ins晚期NSCLC领域掀起了巨大涟漪,其不仅在ESMO大会上傲然亮相,还在同一时间段,荣誉刊登新英格兰医学杂志。基于强大的疗效和可控的安全性,Amivantamab联合化疗未来有望改变EGFR ex20ins NSCLC一线治疗的临床实践,成为新的一线治疗标准方案。
EGFR 经典突变的靶向治疗家族日益壮大,为携带EGFR 经典突变NSCLC 患者提供了多样化的治疗选择,目前新型药物及药物联合治疗方案已经带来令人期待的成果。请您就本次ESMO 大会公布的EGFR 经典突变NSCLC 重磅研究的疗效和安全性最新数据谈谈您的看法与期待?
周彩存教授:随着EGFR酪氨酸激酶抑制剂(EGFR TKI)的发展,三代EGFR TKI单药的临床应用,显著延长EGFR经典突变晚期NSCLC患者的PFS和OS,但远远未达到“治愈”的目标。为此学界近年来不断尝试联合治疗策略以期望打破三代EGFR TKI单药治疗获益的“瓶颈“,进一步改善患者长期生存。在FLAURA2研究中,研究者探讨了奥希替尼联合化疗一线治疗EGFR经典突变晚期NSCLC的疗效和安全性。结果显示,奥希替尼联合化疗组较奥希替尼单药组有显著的PFS获益,经独立审查委员会(BICR)评估的中位PFS分别为29.4个月 vs 19.9个月(HR=0.62;P=0.0002),尤其在CNS转移患者中,联合组获益显著[8]。然而生存获益的提升伴随着不良反应的增加,奥希替尼联合化疗组≥3级的不良事件发生率上升了37%。临床上迫切需要新的治疗方案以打破目前治疗瓶颈,并且更期待“chemo-free“治疗策略。MARIPOSA 研究中[9],研究者将Amivantamab联合Lazertinib 作为“chemo-free”的联合方案与奥希替尼单药方案进行了头对头比较,联合组降低患者疾病进展或死亡风险达30%,中位PFS为23.7个月,值得注意的是,MARIPOSA 研究强调了对脑转移患者的密集影像学监测,检测频率高会带来PFS的缩短,期待MARIPOSA 研究的重磅成果能开启EGFR 经典突变晚期NSCLC一线治疗新纪元。
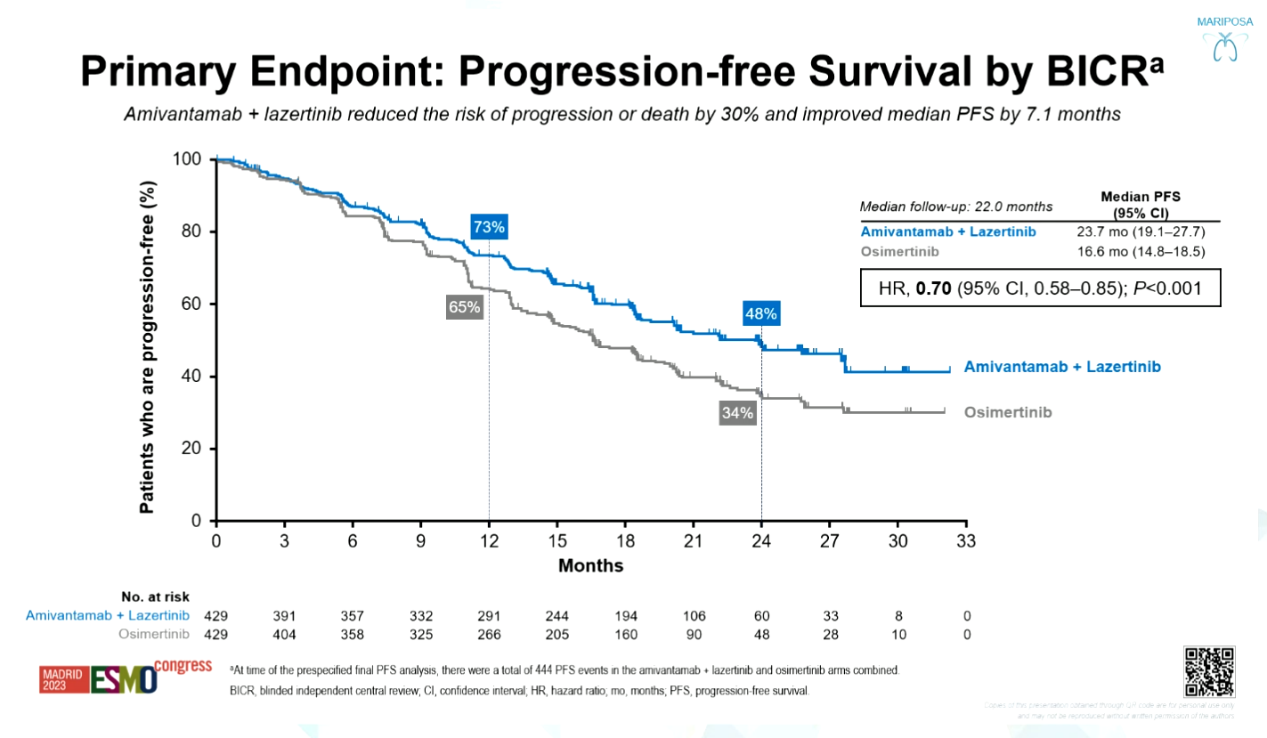 图4:FLAURA2研究的PFS
图4:FLAURA2研究的PFS
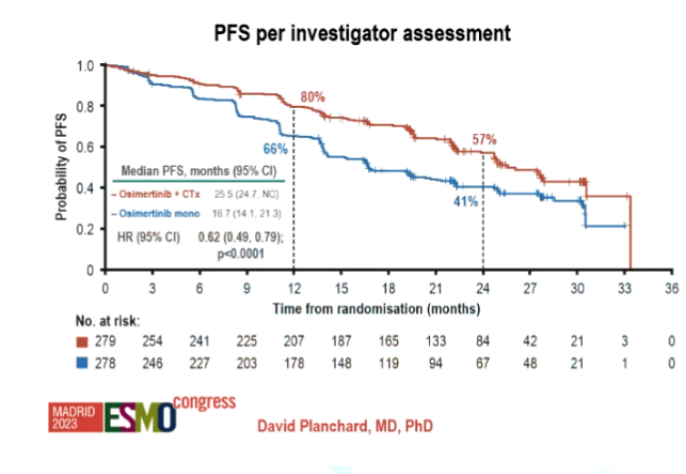 图5:MARIPOSA研究的PFS
图5:MARIPOSA研究的PFS
而在EGFR经典突变的后线治疗中,ATTLAS, KCSG-LU19-04 研究[10]展示了与IMpower151相似的生存获益,证明了靶向治疗耐药的EGFR/ALK 突变的NSCLC 患者可从阿替利珠单抗联合贝伐珠单抗和化疗的四药方案中获益;TROPION-Lung01研究[11]中TROP2 ADC药物Dato-DXd用于晚期NSCLC二线/后线治疗的PFS为4.4个月,较化疗组有了明显的提升。基于ADC药物的不良反应表现,今后Amivantamab联合第三代EGFR靶向药和ADC药物的治疗方案或许值得探索。总的来说,今年ESMO大会涌现了EGFR经典突变晚期NSCLC的大量精彩研究,未来仍需肺癌领域的同道们笃定前行,赓续奋斗,共同创铸肺癌领域崭新篇章,延续患者更长生存奇迹。
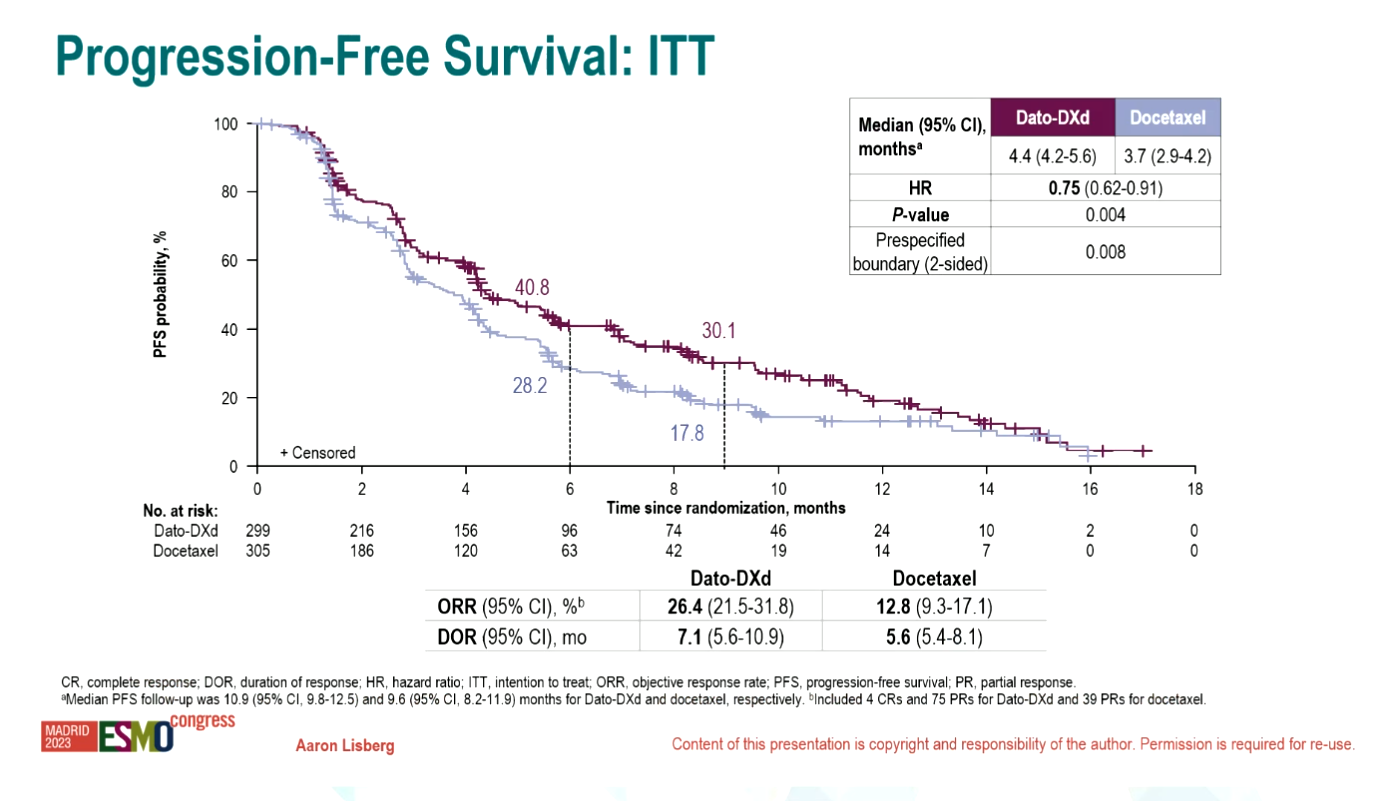 图6:ATTLAS研究的PFS
图6:ATTLAS研究的PFS
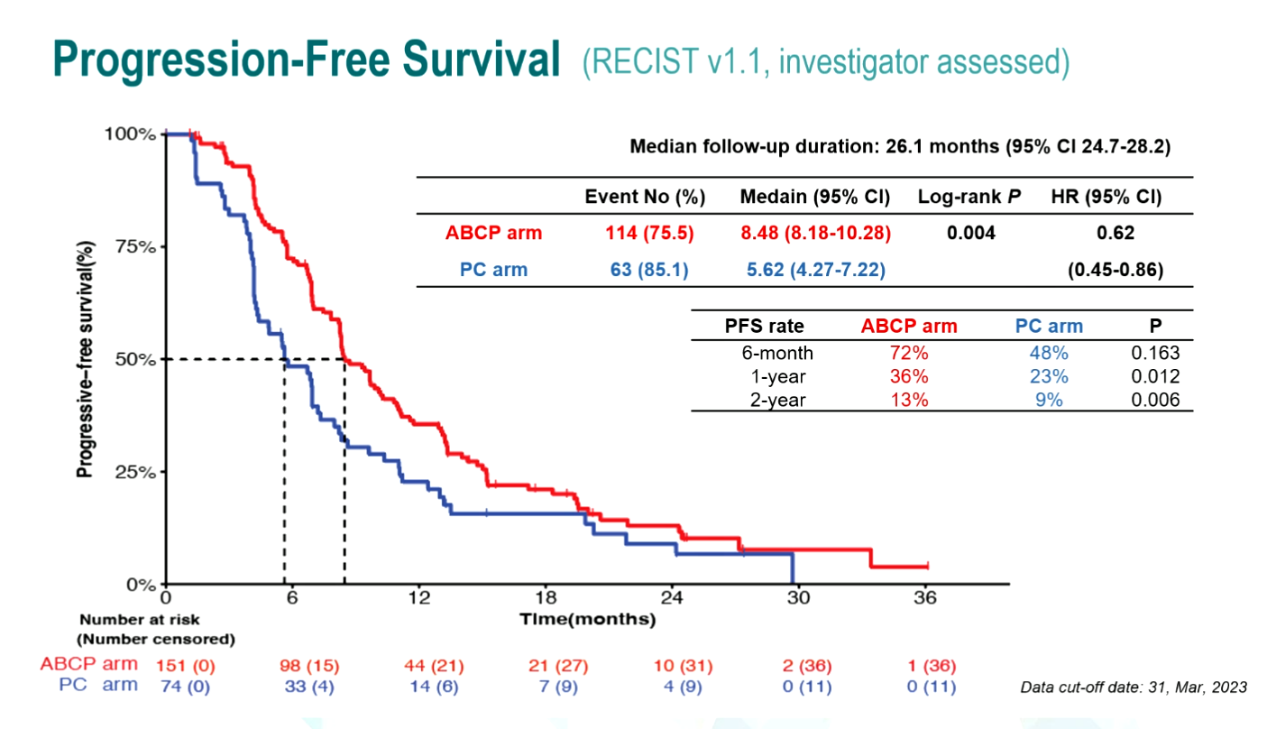 图7:TROPION-Lung01研究的PFS
图7:TROPION-Lung01研究的PFS
CRC code: EM-176504
Approve date:2025-02-19
[1] N. Girard, K. Park, K. Tang, et al. Amivantamab plus chemotherapy vs chemotherapy as first-line treatment in EGFR Exon 20 insertion-mutated advanced non-small cell lung cancer (NSCLC): Primary results from PAPILLON, a randomized phase III global study. 2023 ESMO, LBA 5.
[2] H.H.F. Loong, K. Goto, B.J. Solomon, et al. Randomized phase III study of first-line selpercatinib versus chemotherapy and pembrolizumab in RET fusion-positive NSCLC. 2023 ESMO, LBA 4.
[3] M.C. Garassino, W.S.M.E. Theelen, R. Jotte, et al. KRYSTAL-7: Efficacy and safety of adagrasib with pembrolizumab in patients with treatment-naïve, advanced non-small cell lung cancer (NSCLC) harboring a KRASG12C mutation. 2023 ESMO, LBA 65.
[4] L. Zhan, Y. M, Y. Zha, et al. BL-B01D1, a first-in-class EGFRxHER3 bispecific antibody drug conjugate, in patients with non-small cell lung cancer: Updated results from first-in-human phase I study. 2023 ESMO, 1316MO.
[5] L. Paz-Are, M-J. Ah, A.E. Lisberg, et al. TROPION-Lung05: Datopotamab deruxtecan (Dato-DXd) inpreviously treated non-small cell lung cancer (NSCLC) with actionable genomic alterations (AGAs). 2023 ESMO, 1314MO.
[6] 中国临床肿瘤学会非小细胞肺癌专家委员. EGFR 20外显子插入突变非小细胞肺癌规范化诊疗中国专家共识(2023版)
[7] 武田官网:https://www.takeda.com.cn/newsroom/statements/2023/takeda-latest-announcement-on-mobocertinib
[8] D. Planchard, P.A. Jänne, Y. Cheng, et al. FLAURA2: Safety and CNS outcomes of first-line (1L) osimertinib (osi) ± chemotherapy (CTx) in EGFRm advanced NSCLC. 2023 ESMO, LBA 68.
[9] B.C. Cho, E. Felip, A.I. Spira, et al. Amivantamab plus lazertinib vs osimertinib as first-line treatment in patients with EGFR-mutated, advanced nonsmall cell lung cancer (NSCLC): Primary results from MARIPOSA, a phase III, global, randomized, controlled trial. 2023 ESMO, LBA 14.
[10] M-J. Ahn, S. Park, T.M. Kim, et al. A phase III, randomized study of atezolizumab plus bevacizumab and chemotherapy in patients with EGFR or ALK mutated in non-small cell lung cancer (ATTLAS, KCSGLU19-04). 2023 ESMO, LBA 67.
[11] M-J. Ahn, E. Lisber, L. Paz-Ares, et al. Datopotamab deruxtecan (Dato-DXd) vs docetaxel in previously treated advanced/metastatic (adv/met) non-small cell lung cancer (NSCLC): Results of the randomized phase III study TROPION-Lung01. 2023 ESMO, LBA 12.











 苏公网安备32059002004080号
苏公网安备32059002004080号


