近年来,EGFR突变肺癌一直是临床研究热点,本次世界肺癌大会(WCLC2023)发布多项EGFR突变NSCLC诊疗现状及新药研究最新结果。EGFR ex20ins NSCLC患者中,真实世界的疗效不尽人意,研究者将CHRYSALIS研究与中国真实世界外部队列(EC)的系统性抗癌治疗(SACT)进行比较, Amivantamab是否可以成为这一特定人群的标准治疗方案,改善此类患者的生存获益,结果值得我们期待。FLAURA2研究此次数据发布证实,与单药相比,奥希替尼+铂类化疗在1L EGFR突变晚期NSCLC患者的PFS方面有统计学显著且具有临床意义的改善,对一线治疗格局有何影响?此次大会给我们探索EGFR突变肺癌治疗格局提供了哪些新启发和新思路?就以上热点话题,我们有幸邀请到北京大学肿瘤医院赵军教授进行分享。
北京大学肿瘤医院胸部肿瘤中心副主任、胸部肿瘤内一科副主任、肿瘤内科教研室主任
北京医学奖励基金会肺癌青年专委会主任委员
北京科创医学发展基金会肺癌专委会主任委员
中国医师协会肿瘤多学科诊疗专委会委员
中国临床肿瘤学会非小细胞肺癌专委会委员
中国抗癌协会肿瘤科普防治专委会委员
中国临床肿瘤学会智慧医疗专委会常务委员
中国医药教育协会疑难肿瘤专委会常务委员
EGFR 经典突变NSCLC一线治疗新进展
三代EGFR-TKI奥希替尼一线治疗相较一代药物有明显的生存获益,但是奥希替尼在NSCLC的治疗过程中会出现耐药,那么如何在三代EGFR-TKI的基础上进一步追求卓越疗效,是目前待解决的临床热点话题。本次WCLC会上发布多项一线治疗方案相关的研究,或将为NSCLC患者带来更多临床获益。
【PL03.13】FLAURA2研究[1]:奥希替尼联合/不联合铂类化疗作为EGFR突变晚期NSCLC患者一线治疗
众所周知,FLAURA研究[2]和FLOURISH研究[3]已证实三代EGFR-TKI奥希替尼相较于一代EGFR-TKI(吉非替尼或厄洛替尼)显著延长无进展生存期(PFS),并在中国人群观察到了同样的获益。FLAURA2研究旨在探索三代EGFR-TKI联合治疗模式,重点关注奥希替尼联合铂类化疗作为一线治疗方案是否能够获益。
研究方法:纳入557例既往未经治疗且携带EGFR敏感突变的局部晚期或转移性NSCLC患者,按照1:1随机分配,试验组接受4个周期奥希替尼+含铂双药化疗,随后接受奥希替尼+培美曲塞维持治疗;对照组接受奥希替尼单药治疗,直至疾病进展或出现不可耐受的毒性。主要终点是PFS,次要终点包括总生存期(OS)、客观缓解率(ORR)、缓解持续时间(DoR)和疾病控制率(DCR)等。
研究结果:截至2023年4月3日,研究整体成熟度达到51%,其中联合组和单药组中位随访时间分别为19.5个月和16.5个月,研究者评估的中位PFS为25.5个月和16.7个月,HR为0.62 (95% CI: 0.49-0.79,P<0.0001)达到了主要研究终点。在敏感性分析中(BICR评估的PFS) 观察到一致的结果,整体成熟度为43%,其中联合组和单药组的中位随访时间分别为19.4个月和14.6个月,中位PFS为29.4个月和19.9个月。在此中期分析中,PFS2和OS数据尚不成熟。治疗安全性与预期相符并可管理。
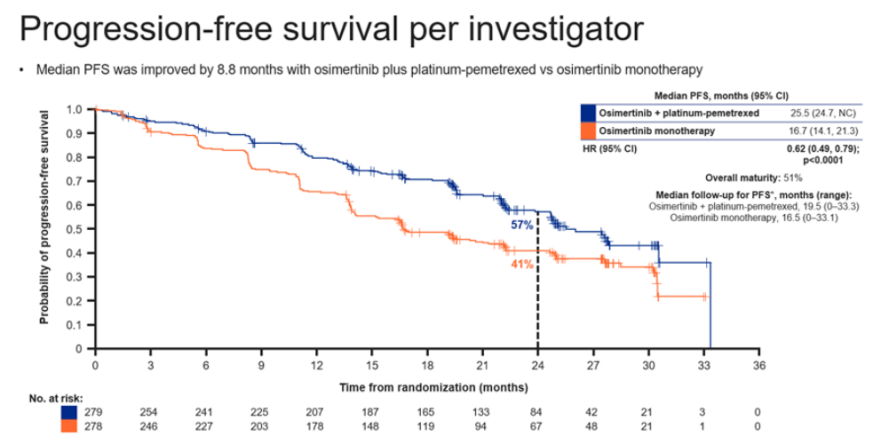
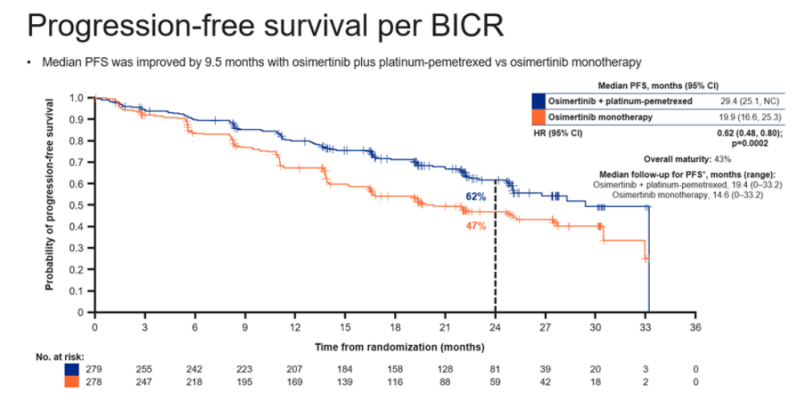
研究者和BICR评估的中位PFS
研究结论:在FLAURA2研究中,与奥希替尼单药治疗相比,奥希替尼+铂类化疗一线治疗EGFR突变晚期NSCLC患者的PFS方面有显著的临床意义改善。遗憾的是,目前我们尚未看到FLAURA2研究OS结果,因此还不能说奥希替尼联合化疗的优劣性。
除此以外,三代EGFR-TKI中尚有一些潜在新药, Lazertinib是口服、高选择性作用于EGFR敏感突变和T790M突变,且可穿透血脑屏障的三代EGFR-TKI。同样是三代EGFR-TKI,其一线疗效如何?本次大会结果也让我们眼前一亮。
【P2.09-03】第三代TKI Lazertinib疗效优于吉非替尼,且安全性可控[4]
研究方法:LASER301研究评估Lazertinib在未经治EGFR突变(ex19del/L858R)局部晚期或转移性NSCLC患者的疗效和安全性。
研究结果:在LASER301的393例入组患者中,258例患者为亚裔(129例接受Lazertinib治疗,129例接受吉非替尼治疗)。各治疗组的人口统计学和基线疾病特征均衡。在数据截止日(2022年7月29日),Lazertinib组中位PFS显著超过吉非替尼(20.6个月 vs. 9.7个月; HR, 0.46; 95% Cl:0.34-0.63; P<0.001)。在亚洲患者中,Lazertinib和吉非替尼PFS获益在各预设亚组中一致(ex19del突变: 20.8个月 vs. 12.3个月; HR,0.47; 95%CI:0.31-0.71; P<0.001; L858R突变: 16.7个月 vs. 9.6个月; HR, 0.44; 95% CI:0.28-0.71; P=0.002;入组时存在CNS转移:20.7个月 vs. 9.5个月; HR, 0.33; 95% Cl:0.18-0.58; P<0.001)。两组的ORR和疾病控制率相似。Lazertinib和吉非替尼的中位DoR分别为19.4个月(95% CI:16.6-24.9)和9.6个月(95% CI:6.9-12.4)。亚洲患者的不良事件发生率与总体LASER301人群相当。Lazertinib组的皮疹和腹泻发生率(分别为42%和30%)低于吉非替尼组(分别为47%和44%)。
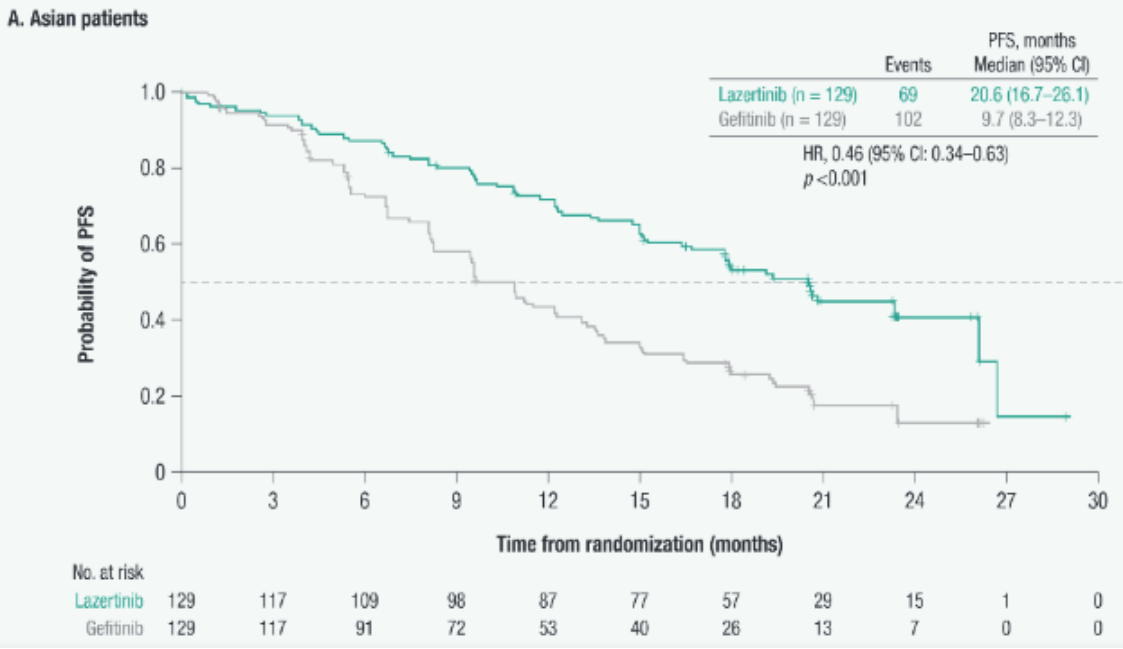
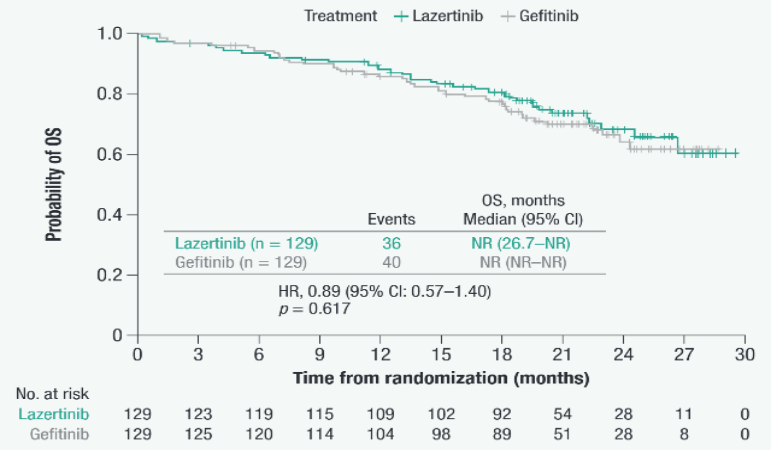
PFS和OS
研究结论:在LASER301中, EGFR突变晚期NSCLC亚裔患者的疗效和安全性结果与总体人群一致,在亚洲患者中,Lazertinib的疗效优于吉非替尼,疾病控制率也更高,安全性可控。
三代EGFR-TKI单药是EGFR经典突变晚期NSCLC患者的一线优选吗?现在还不能下这样的结论,尽管三代EGFR-TKI为EGFR突变NSCLC患者带来了更多的生存获益,耐药问题仍然无法避免。面对耐药,全新的联合方案,其结果值得临床期待。
【P2.09-17】奥希替尼联合Amivantamab一线治疗EGFR突变晚期NSCLC患者疗效令人期待[5]
MET扩增是奥希替尼一线治疗最常见的获得性耐药机制之一,而Amivantamab是一种靶向EGFR和MET的双特异性单克隆抗体,两者联合有可能阻断MET驱动的奥希替尼耐药机制,从而改善结局。OSTARA (NCT05801029) 研究旨在评估一线奥希替尼联合Amivantamab治疗 EGFR突变晚期NSCLC患者的疗效和安全性。本次大会公布了该研究的方案设计。OSTARA研究是一项2期、单臂、多中心研究。80例患者将接受奥希替尼和Amivantamab治疗,研究者采用RECIST v1.1标准进行疗效评价,主要终点是评估奥希替尼联合Amivantamab的安全性(包括AE、严重AE、导致剂量调整或停药的AE)和PFS。关键次要终点包括安全性、客观缓解率、缓解持续时间和总生存期。探索性终点包括CNS疗效、早期ctDNA水平和其他生物标志物分析。目前,2023年7月第一个患者已经登记入组,预计2024年1月进行性安全性分析及中期疗效分析,研究预计将于2028 年2月完成。让我们共同期待,这样的组合会为我们带来怎样的获益!
 OSTARA研究设计
OSTARA研究设计
靶向药物治疗后会产生耐药,既往治疗方案选择时关注如何延缓耐药的出现,随着医药研发的不断进步,当下研究方向更加侧重于如何对抗耐药问题,持续探索疾病进展后的新型解决方案。
【OA09.06】IMpower151研究:阿替利珠单抗 +贝伐珠单抗+化疗一线治疗转移性NSCLC[6]
本次会议中公布在中国进行的III期IMpower151研究 (NCT04194203)评估阿替利珠单抗、贝伐珠单抗、卡铂+紫杉醇或培美曲塞(ABCP四药方案)与贝伐单抗联合卡铂+紫杉醇(BCP三药方案)作为转移性NSCLC的一线治疗的有效性和安全性。
研究设计:既往未接受过化疗的转移性nsqNSCLC患者按1:1随机分组,接受阿替利珠单抗/安慰剂(1200mg) +贝伐珠单抗(15mg/kg)、卡铂(AUC 6)和紫杉醇(175mg/m2)或培美曲塞(500mg/m2) IV Q3W,持续4个周期,随后阿替利珠单抗/安慰剂维持治疗,直至不可接受的毒性或疾病进展,贝伐珠单抗和培美曲塞(如果在诱导期间给予)直到进展(RECIST 1.1)。两组患者均有超过50%的患者接受过TKI治疗。分层因素为EGFR/ALK基因型(上限为50%野生型)和PD-L1表达。
 IMpower151研究设计
IMpower151研究设计
研究结果:截至数据截止(2023年2月2日),中位随访时间为14个月,疗效结果如下图所示。安全性方面,全因AE发生率分别为99.3%(ABCP:3/4级,66.4%)和100%(BCP:3/4级,61.4%)。全因5级AE发生率为7.9%(ABCP:治疗相关,5.9%)和7.8%(BCP:治疗相关,6.5%)。特殊不良事件(AESIs)发生率分别为67.8%(ABCP:3/4级,11.2%)和71.2%(BCP:3/4级,7.2%),没有发现新的安全性信号。
 IMpower151在ITT人群中没有达到INV-PFS的主要终点
IMpower151在ITT人群中没有达到INV-PFS的主要终点
研究结论:IMpower151研究在转移性NSCLC中未达到其主要终点,ABCP与BCP的中位PFS差异并未显示出统计学意义,因此ABCP四药方案并未体现出作为一线选择的临床优势,同时观察到ABCP严重不良反应[不良事件99.3%(3/4级,66.4%;5级,7.9%)],临床处方此类方案时需谨慎。
免疫治疗联合方案似乎并未给到临床足够的信心,抗体偶联药物(ADC)是目前药物研发的又一热点,随着ADC技术的成熟,ADC联合免疫治疗方案正在显示出其治疗潜力。2023WCLC大会公布了Dato-DXd一线联合用药方案在mNSCLC患者中的安全性,有望为患者带来新的治疗方向。
【OA05.06】1b期TROPION-Lung04研究:Dato-DXd+度伐利尤单抗±卡铂治疗晚期/m NSCLC[7]
TROPION-Lung04 (NCT04612751)是一项针对晚期/转移性NSCLC的1b期、多中心、开放标签、剂量递增/确认和扩展研究,在本次大会首次分析报告了队列1-4的数据。
研究设计:患者接受Dato-DXd(4mg/kg,队列1和3;6mg/kg,队列2和4)+度伐利尤单抗(120mg,所有队列)+最多4个周期的卡铂(AUC 5,队列3和4),Q3W,直至疾病进展(RECIST v1.1)或毒性不可接受。第一部分(剂量递增)采用改良毒性概率间隔-2(mTPI-2)设计,由3~6例患者依次进行。根据观察到的剂量限制性毒性(DLTs),启动第二部分(剂量扩展,队列3为按需降级队列)。
 研究设计
研究设计
研究结果:数据截止时(2023年3月6日),38例患者接受评估,分别在队列1(n=5)、队列2(n=19)和队列 4(n=14)。由于队列1患者(n=5)第一部分完成后未出现DLT,因此对队列2患者(n=3)第一部分开始进行评估。由于队列2没有出现DLT,因此跳过队列3,开始对队列4患者(n=6)第一部分进行评估。队列4中有两例患者报告了 DLT(3级发热性中性粒细胞减少症;3级斑丘疹和口腔炎,导致第2周期治疗延迟2周以上)。随后在队列2和队列4中扩大剂量,但未再观察到 DLT。在队列2/4中,患者肿瘤细胞PD-L1表达<1%、1-49%和≥50%比例分别为31.6%/42.9%、31.6%/21.4%和36.8%/35.7%。
 安全性结果
安全性结果
研究结论:Dato-DXd +度伐利尤单抗±卡铂在晚期/转移性NSCLC中显示出可控的安全性和令人鼓舞的抗肿瘤活性。
FLAURA2研究结果受业内关注,与奥希替尼单药治疗相比,奥希替尼+铂类化疗在一线EGFRm晚期NSCLC患者的PFS方面有显著的临床意义。
FLAURA2研究OS数据尚不成熟,奥希替尼+化疗在EGFRm晚期NSCLC患者中的研究获益目前尚不能下定论。考虑到EGFR突变肺癌的整体情况,奥希替尼单药治疗仍将是一线标准治疗。
近年来,三代EGFR-TKI药物涌现,显示出较好的疗效。LASER301研究结果显示Lazertinib疗效优于吉非替尼,且安全性较吉非替尼更佳。目前正在进行的MARIPOSA研究是一项令人关注的头对头研究,直接对比Amivantamab联合Lazertinib对比三代EGFR-TKI奥希替尼单药一线治疗EGFR敏感突变晚期NSCLC患者的疗效与安全性,其疗效及安全性结果令人期待。此次大会上还公布了Amivantamab联合奥希替尼一线治疗EGFR晚期NSCLC患者的研究设计,以Amivantamab为基础的一线治疗联合用药方案能否为患者带来更多生存获益,让我们拭目以待。
免疫治疗和ADC作为备受关注的抗肿瘤新药,并未为晚期NSCLC患者的治疗带来足够的“信心”,今年WCLC大会更新的有关免疫治疗阿替利珠单抗+贝伐珠单抗+化疗的方案疗效不足,且全因AE发生率为99.3%,这可能与样本量、人种差异、分子学特征等诸多因素有关,该方案目前看并不能够堪当一线治疗大任。Dato-DXd与抗PD-1±铂类化疗联合治疗(TROPION-Lung02)显示出了令人鼓舞的早期疗效和安全性,但这仅是早期疗效数据,距离解决临床实际问题,依然距离尚远。
EGFR经典突变二线及以上治疗
EGFR突变患者二线及以上治疗在临床上仍存在未被满足的需求,尤其耐药方面,其机制复杂多样,耐药后的治疗策略更为繁杂,为临床治疗带来困境。为了探索TKI耐药后的治疗策略,研究人员探索了以EGFR-TKI为基础的联合治疗以及新型ADC在TKI耐药患者中的疗效作用。
【MA13.06】:Amivantamab、Lazertinib联合化疗在EGFR经典突变晚期NSCLC患者中显示出有意义和持久的缓解率,客观缓解率达50%[8]
研究设计:CHRYSALIS-2研究队列入组20例中位年龄为61岁(38-76),其中55%为女性,55%为亚洲人,40%为白人,中位既往治疗为2线(70%既往接受过奥希替尼,45%既往接受过1/2代EGFR TKIs药物)的EGFR经典突变晚期NSCLC患者。
研究结果:截至2022年11月15日,客观缓解率为50%,中位缓解持续时间未达到(中位随访时间为13.1月)。10个应答者中有8个应答持续时间≥6个月。11例(55%)患者正在接受治疗,PFS为14.0个月(95% Cl, 4.3个月-不可估计)。共有5例患者在疾病进展后接受治疗,中位治疗时间为4.2个月(范围3.1-7.1)个月。在12例有脑转移病史患者中,中位PFS为6.7个月(95% Cl, 1.4-不可估计)。最常见的不良事件是皮疹(100%)、中性粒细胞减少(90%)和输液相关反应(65%)。

 肿瘤治疗的疗效评估
肿瘤治疗的疗效评估
研究结论:在接受EGFR TKI治疗后出现疾病进展的EGFR突变晚期NSCLC患者中,Amivantamab、Lazertinib联合化疗显示出有意义且持久的缓解率。
【OA05.03】:HER3-DXd用于既往接受过EGFR-TKI和铂类为基础化疗后进展,治疗需求未得到满足且方案有限的EGFR突变NSCLC患者[9]
研究设计:HERTHENA-Lung01这项II期试验随机纳入曾接受过EGFR-TKI和铂类为基础化疗治疗的晚期EGFR突变NSCLC患者。在 5.6mg/kg治疗组中,225例患者接受HER3-DXd治疗。主要终点为BICR确认的ORR。
研究结果:截至2023年5月18日,中位随访时间为18.9 个月(14.9-27.5个月)。在接受EGFR TKI和铂类化疗的晚期EGFR突变NSCLC患者中cORR为29.8%。,HER3-DXd显示出有显著的疗效和可控的安全性。此外,本研究还首次报道了HER3-DXd在中枢神经系统中的疗效,BICR所确认的CNS ORR为33.3%(95% CI,17.3%-52.8%;9/30完全缓解,1/30部分缓解)。
 BICR确认的疗效终点
BICR确认的疗效终点
研究结论:在既往接受过EGFR-TKI和铂类为基础化疗后进展的这类治疗需求未得到满足且方案有限的EGFR突变NSCLC患者群体中,HER3-DXd显示出了有临床意义的疗效;此外,本研究还首次报道了HER3-DXd在中枢神经系统中的疗效。
EGFR经典突变二线及以上治疗相关临床研究推陈出新,靶点探索和药物研发持续推进。CHRYSALIS-2研究展示了在接受EGFR-TKI治疗后出现疾病进展的EGFR突变晚期NSCLC患者中,在这项亚洲人群占比高达55%的研究中,Amivantamab、Lazertinib联合化疗显示高达50%的客观缓解率,同时缓解时间仍未达到。Amivantamab、Lazertinib联合化疗显示出了持续的疗效和安全性,极大改善了EGFR-TKI复发/难治性NSCLC患者的治疗结局,是一种非常有前途的治疗策略。与此同时,ADC药物的研发方兴未艾,HERTHENA-Lung01这项II期试验展示了HER3-DXd在接受EGFR-TKI和铂类化疗的晚期EGFR突变NSCLC患者中具有不错的疗效和安全性。可以预见的是,NSCLC诊疗逐渐步入精准化、规范化时代。EGFR经典突变二线及以上治疗的探索不断,发展迅速。
EGFR ex20ins和MET ex14治疗
2004年在NSCLC中EGFR ex20ins突变首次提出,随后针对EGFR ex20ins NSCLC进行了一系列的药物研发,多款新药正在探索中,然而,EGFR ex20ins NSCLC患者的临床可及治疗选择仍然有限。获批适应症或正在全球开展III期临床研究的药物包括莫博赛替尼、舒沃替尼及Amivantamab等。对于EGFR ex20ins突变,此次大会公布的CHRYSALIS研究对比真实世界疗法显示出Amivantamab更有意义和更持久的缓解率,并且CHRYSALIS研究纳入的METex14患者疗效数据也将在本次会议公布,让我们一起看一下最新研究进展。
【P2.09-35】:在中国Amivantamab VS.真实世界疗法治疗EGFR ex20ins晚期NSCLC[10]
接受Amivantamab治疗具有显著改善的TTNT和更高的ORR,且PFS和OS在数值上更优,具有临床获益,推荐Amivantamab成为铂类化疗后这一特定人群的标准治疗方案。
研究设计:CHRYSALIS cohort D旨在评估Amivantamab在ex20ins患者中的临床获益,并与中国真实世界外部队列(EC)的系统性抗癌治疗(SACT)进行比较。纳入2015年3月至2020年7月既往接受过铂类化疗,符合资格标准的晚期NSCLC EGFR ex20ins患者。采用加权cox比例风险回归模型对EC和CHRYSALIS患者的PFS、下一次治疗时间(TTNT)和OS进行比较,并使用重复测量总缓解率(ORR)的广义估计方程。
研究结果:共纳入115例CHRYSALIS患者和41例EC患者(87例经铂类化疗后)。中位PFS分别为6.93(5.59 ~ 8.84)和5.62(3.88 ~ 8.97)个月(HR=0.647, P=0.013)。中位TTNT分别为12.16 (9.10~18.50)和6.01 (4.27~9.46)个月(HR=0.545,P=0.02)。中位OS分别为23.13和11.63个月(HR=0.668, P=0.191)。然而,与EC相比,CHRYSALIS的ORR更高(36.8% vs 1.0%),优势比为56.37 (P<0.001)。


CHRYSALIS 整体人群与External队列人群 (a) PFS 和 (b) TTNT 的 Kaplan-Meier 图
研究结论:与接受当前真实世界治疗的患者相比,接受Amivantamab治疗的ex20ins的aNSCLC患者具有显著改善的TTNT和更高的ORR,而PFS和OS在数值上更好。由于来自EC数据源的疾病进展记录的完整性有限,TTNT被认为是这项现实世界研究中更好的有效性评估。该研究结果还显示,对于aNSCLC ex20ins患者,Amivantamab在铂类化疗后具有临床获益,并表明Amivantamab应该成为这一特定人群的标准治疗方案。
【OA.21.04】:Amivantamab在原发性METex14的NSCLC患者中同样展示了抗肿瘤活性,包括MET抑制剂治疗失败的患者,安全性与先前报道一致[11]
研究设计: CHRYSALIS纳入当前标准治疗方案后进展或拒绝治疗的原发性METex14的97例患者。中位年龄70岁(范围43-88岁),54%为女性,49%为亚裔,39%为白人,14%基线脑转移。
研究结果:截至2023年6月19日,中位随访时间10个月。Amivantamab在METex14晚期NSCLC患者中显示出有意义的抗肿瘤活性,初始治疗患者ORR为50%,未使用过MET抑制剂的患者ORR为46%,曾使用过MET抑制剂的患者ORR为21%。在32例应答者中,中位缓解持续时间(DOR)为11.2个月(95%CI,5.3-19.0个月);其中15例患者DOR ≥6个月,12例正在接受治疗。在会议上公布了Amivantamab单药治疗的最新疗效数据,中位PFS 5.4个月(95%Cl,4.3-7.0),中位OS 15.8个月(95%Cl,13.1-21.8)。最常见的治疗期间不良反应(TEAEs)是皮疹(76%),输注相关反应(72%)和甲沟炎(45%),安全概况与先前的报告一致,没有观察到新的安全信号。

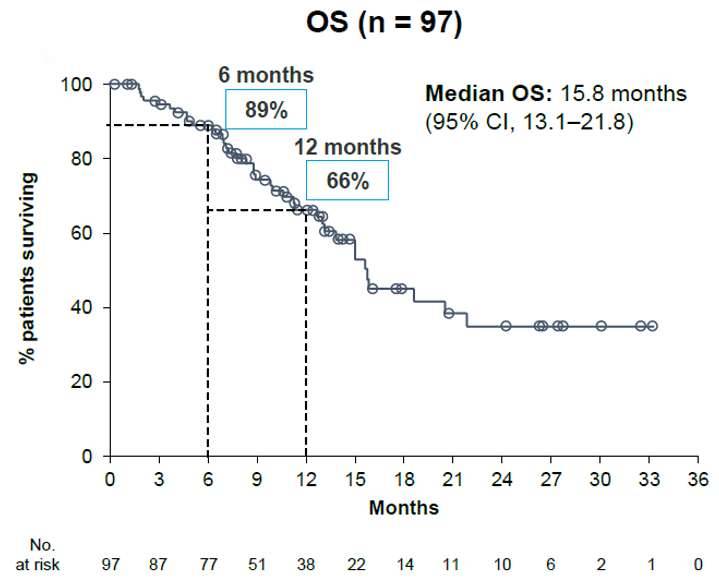
Amivantamab单药治疗的PFS和OS
研究结论:在扩大患者人群中,Amivantamab在原发性METex14的NSCLC患者中展示了抗肿瘤活性,包括MET抑制剂治疗失败的患者。安全性与先前报道的Amivantamab在EGFR阳性NSCLC中一致。
EGFR ex20ins突变的非小细胞肺癌异质性和恶性程度高,患者普遍预后不佳,临床上EGFR ex20ins突变的NSCLC亟需新的治疗药物。目前我国已经上市的治疗EGFR ex20ins突变NSCLC有莫博赛替尼和舒沃替尼。莫博赛替尼的一项全球单臂研究纳入了114例既往接受含铂化疗的EGFR ex20ins突变患者,这项研究取得了惊人的疗效,最长随访时间25.8个月,中位PFS 7.3个月,中位OS 20.2个月,也因此获得FDA的加速批准上市。但随后的3期确证性试验Exclaim-2研究结果未达到FDA授予加速批准的验证性数据要求和其他国家授予有条件上市的要求,试验终止。武田于2023年10月2日宣布在FDA撤市[12],后续可能考虑全球撤市。舒沃替尼数据来自WU-KONG1及WU-KONG15,口服舒沃替尼200mg或300mg,经IRC评估的ORR分别为68.4%和77.8%,尚无PFS数据结果。Amivantamab与肿瘤细胞表面的EGFR、MET受体结合,抑制EGFR、MET信号通路,还能通过抗体的Fc段介导的ADCC/ADCP作用激活免疫系统,同时可触发EGFR和cMET这两种受体“内化”和溶酶体“降解”,药物三重机制让Amivantamab对EGFR ex20ins患者有了亮眼的疗效数据,在多项临床研究中显示出其卓越疗效,中位TTNT显著改善(12.16个月 vs 6.08个月)、更高的ORR (41.7% vs 1.5%)、PFS和OS在数值上也更优。EGFR ex20ins的治疗这一难治性突变已有多个治疗药物可及,让更多患者获益。同样地,在此次大会上研究者更新了CHRYSALIS研究中扩大METex14患者人群的结果,Amivantamab在原发性METex14的NSCLC患者中也展示了抗肿瘤活性。随着药物研发不断蓄力,创新的难治突变药物或可为患者带来长期生存希望,相信不久的将来,更多有价值的新药也将加速走入临床,为患者带来更多治疗选择,提高肺癌生存率,实现高质量的长生存。
[1]. P. Janne, et al. Osimertinib With/Without Platinum-Based Chemotherapy as First-line Treatment in Patients with EGFRm Advanced NSCLC (FLAURA2).2023WCLC: PL03.13.
https://meetingsapp.iaslc.org/event/wclc2023/planning/UGxhbm5pbmdfMTUyNjAxNg==
[2]. Ramalingam SS, et al. N Engl J Med. 2020 Jan 2;382(1):41-50.
[3]. Jianying Zhou, et al. Real-World Outcomes of First-Line Osimertinib for EGFR Mutated Advanced NSCLC Patients in China: Interim Analysis of FLOURISH Study. 2022ESMO: 1123P.
[4]. T. Reungwetwattana, et al. Lazertinib vs Gefitinib in Treatment-Naïve Patients with EGFR-mutated NSCLC: LASER301 Asian Subpopulation Analysis. 2023WCLC: P2.09-03.
https://meetingsapp.iaslc.org/event/wclc2023/webview/RXZlbnRWaWV3XzQ4OTc3Nw==
[5]. D.S.W. Tan, et al. OSTARA: A Phase II Study of First-line Osimertinib Combined with Amivantamab in EGFRm Advanced Non-Small Cell Lung Cancer 2023WCLC: P2.09-17.
https://meetingsapp.iaslc.org/event/wclc2023/webview/RXZlbnRWaWV3XzQ4OTc3Nw==
[6]. C. Zhou, et al. IMpower151: Phase III Study of Atezolizumab + Bevacizumab + Chemotherapy in 1L Metastatic Nonsquamous NSCLC. 2023WCLC: OA09.06.
https://meetingsapp.iaslc.org/event/wclc2023/planning/UGxhbm5pbmdfMTUyNzU2MA==
[7]. K.P. Papadopoulos, et al. Datopotamab Deruxtecan (Dato-DXd) + Durvalumab ± Carboplatin in Advanced/mNSCLC: Initial Results from Phase 1b TROPION-Lung04. 2023WCLC: OA05.06.
https://meetingsapp.iaslc.org/event/wclc2023/planning/UGxhbm5pbmdfMTUyNDQwMw==
[8]. S-H. Lee, et al. Amivantamab, Lazertinib Plus Platinum-based Chemotherapy in EGFR-mutated Advanced NSCLC: Updated Results from CHRYSALIS-2. 2023WCLC: MA13.06.
https://meetingsapp.iaslc.org/event/wclc2023/planning/UGxhbm5pbmdfMTUyNTg1OA==
[9]. H.A. Yu, et al.Patritumab Deruxtecan (HER3-DXd) in EGFR-Mutated NSCLC Following EGFRTKI and Platinum-Based Chemotherapy: HERTHENA-Lung01. 2023WCLC: OA05.03.
https://meetingsapp.iaslc.org/event/wclc2023/planning/UGxhbm5pbmdfMTUyNDQwMw==
[10]. L. Shen, et al. Amivantamab vs Real World Therapies for Advanced NSCLC with EG
[11]. N. Leighl, et al. Amivantamab in Patients with Advanced NSCLC and MET Exon 14 Skipping Mutation: Results from the CHRYSALIS Study.2023WCLC: OA21.04.
https://meetingsapp.iaslc.org/event/wclc2023/planning/UGxhbm5pbmdfMTUyNjk3NA==
[12].https://www.takeda.com/newsroom/newsreleases/2023/Takeda-Provides-Update-on-EXKIVITY-mobocertinib/
Document Number: EM-176879
Approval Date: 2025-02-21
往期回顾
1、【2023 ASCO】破茧成蝶 向森而生 | 范云教授:EGFR突变NSCLC 2023 ASCO速递
2、【2023 ELCC】破茧成蝶 向森而生 | 周清教授:EGFR突变阳性晚期NSCLC 2023 ELCC速递
3、【2023 ELCC】破茧成蝶 向森而生 | 赵军教授:EGFR阳性晚期非小细胞肺癌2023 ELCC速递
4、破茧成蝶 向森而生 | 吴一龙教授:EGFR常见及少见突变非小细胞肺癌2023研究进展展望
5、破茧成蝶 向森而生|周彩存教授:双特异性抗体引领肿瘤药物研发新风向 双靶点带来更多新希望
6、破茧成蝶 向森而生 | 程颖教授点评:2022肺癌年终盘点之EGFR外显子20插入突变
7、破茧成蝶 向森而生 | 2022肺癌年终盘点之EGFR经典突变
8、【2022 ESMO ASIA】破茧成蝶 向森而生 | 王洁教授解读2022 ESMO ASIA:EGFR突变非小细胞肺癌治疗新进展
9、【2022 ASCO速递】破茧成蝶 向新而生 | 吴一龙教授解读非小细胞肺癌EGFR和MET通路靶向治疗新进展
10、【2022ELCC&AACR】破茧成蝶 向新而生| 赵军教授:EGFR exon 20ins NSCLC靶向治疗新突破
11、【2022 ELCC】破茧成蝶 向新而生| EGFR 20ins非小细胞肺癌治疗前沿进展盘点
12、ESMO2021|囊括EGFR/MET途径,克服奥希替尼耐药,Amivantamab联合Lazertinib研究数据闪耀ESMO
13、【2021 ASCO】陆舜教授分享肺癌靶向治疗最新进展,创新组合疗法有望克服EGFR TKI耐药
14、吴一龙教授谈EGFR 20外显子插入突变NSCLC诊疗现状与进展,Amivantamab(JNJ-61186372)机制独特或可带来突破
15、周彩存教授:WCLC重磅来袭!NSCLC EGFR Exon 20ins难治突变靶向治疗迎来重大突破!EGFR经典突变靶向治疗新组合惊艳全场!
排版编辑:DND











 苏公网安备32059002004080号
苏公网安备32059002004080号


