近年来,我国乳腺癌患者的5年生存率已提升至83.2%[1],在患者长生存的情况下,保障治疗安全性成为临床管理的重点内容。我国国内外多部指南、专家共识均推荐,含曲妥珠单抗辅助治疗后序贯奈拉替尼强化治疗,以进一步降低人类表皮生长因子受体2(HER-2)阳性早期乳腺癌患者的复发风险,提高患者治愈的可能性。腹泻是包括奈拉替尼在内的分子靶向药物常见的不良反应,及时发现并对应处理可有效改善患者生活质量,提高患者治疗依从性,减少因药物相关不良反应导致减量、停药等情况,进而提高治疗疗效,使患者取得最佳获益。
本文特别分享一例新辅助治疗后手术治疗的右乳浸润性导管癌患者的长期治疗经历,并探讨腹泻这一常见不良反应的管理。该患者术后经化疗+曲妥珠单抗联合帕妥珠单抗(HP)辅助治疗6周期后补充化疗4周期,后给予局部放疗+内分泌治疗、HP靶向辅助治疗1年,继续给予奈拉替尼强化辅助治疗1年,至今病情稳定。在开始奈拉替尼治疗1周内即提前给予腹泻管理。患者在治疗1个周内出现腹泻情况,经参苓白术散治疗后好转,至今未发现其他不良反应,患者一般情况良好。
病例分享专家简介
中国医科大学附属盛京医院肿瘤治疗中心肿瘤内科
2009年毕业于中国医科大学七年制,2019年肿瘤学博士毕业。
承任中国医科大学塔城医院肿瘤内科主任
辽宁省细胞生物协会委员
辽宁省细胞生物学会粒子治疗委员会理事
辽宁省中西医结合学会慢病委员会委员
北京乳腺病防治学会委员
以第一作者发表SCI论文,影响因子7.068
从事恶性肿瘤诊治工作十余年,重点从事乳腺恶性肿瘤的诊断及治疗。
擅长鼻咽恶性肿瘤、胸部肿瘤、消化道肿瘤、泌尿系肿瘤等恶性肿瘤的化疗,内分泌治疗,靶向治疗及免疫治疗等。
病例介绍
患者:女,年龄45岁,未绝经。
主诉:发现右乳肿块5天。
家族史:否认家族性肿瘤病史及其他遗传病史。
既往史:既往健康,无基础疾病。阿莫西林过敏。
现病史:患者5天前发现右乳肿物,能触及鸡蛋黄大小肿物,经期胀痛,无乳头溢血、溢液。为求进一步诊治而入我院。患者自患病以来,无发热,饮食睡眠正常,大小便正常,体重无明显变化。
辅助检查:
■ 乳腺彩超(2020-9-17)示:双乳腺体回声粗糙,右乳腺相当于10-11点钟可见2.6×1.9×1.8cm肿物,边界模糊,形态不规整,内呈低回声伴少许强回声点,较大者直径约0.11cm, CDFI可检出血流信号,其旁另可见1.4×1.5×1.4cm肿物,边界模糊,形态不规整,内呈低回声伴少许强回声点,较大者直径约0.09cm,CDFI可检出血流信号,两者分界不清;左乳腺未见明显占位性病变;双腋下未见明显副乳影像;右侧腋下可见少许肿大淋巴结,较大者约1.5×2.1×0.8cm,边界较清,形态不规整,内呈低回声, CDFI可检出血流信号。左侧腋下淋巴结可见,较大者约1.3×1.2×0.6cm,边界清,周边呈低回声,中心呈高回声。提示:1.双乳腺增生;2.右乳腺肿物(BI-RADS 4c);3.右侧腋窝淋巴结肿大。(图1)
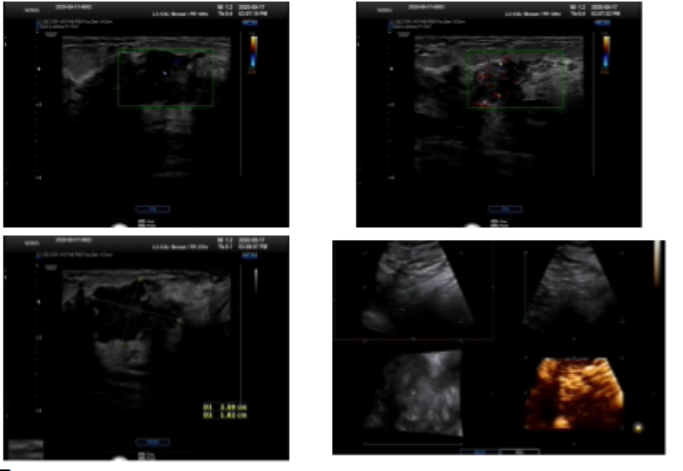
图1 乳腺彩超结果
■ 乳腺钼靶(DR)(2020-9-17):右乳不均匀致密腺体型,右乳外上象限结构稍扭曲,见等密度结节影,范围约1.4cm×1.2cm,边缘遮蔽状,余乳内未见确切肿块及异常钙化征象;右腋窝见小圆形致密淋巴结,直径约11mm;皮肤未见增厚;乳头未见异常。(图2)
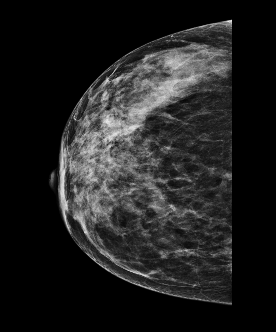
图2 乳腺DR结果
■ 乳腺核磁共振(MRI)(2020-9-28):双侧乳腺不对称,双乳腺体呈不均匀致密腺体型;双侧乳腺背景强化少量、对称;右乳多发不规则肿块,较大者位于外上象限,范围约37 mm× 21mm,边缘不规则,T1WI呈等信号,T2WI呈稍高信号,弥散加权呈高信号,病灶ADC值约为0.96×10-3mm2/s;肿块注药后早期强化快速,延迟期平稳强化,曲线呈平台型;余双乳未见异常强化灶;右腋窝见增大并强化淋巴结,大小约13mm×10mm,双侧皮肤、乳头、乳晕及乳后间隙未见异常信号。(图3)
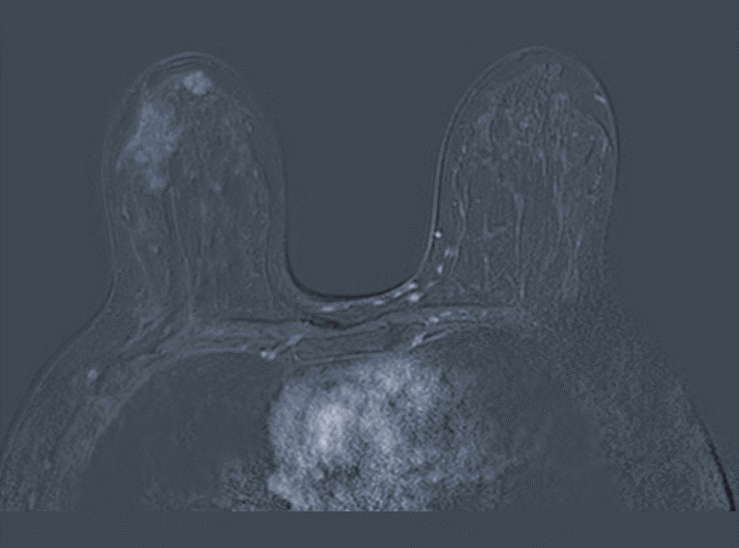
图3 乳腺MRI结果
■ CT(2020-9-17)提示:双肺多发模糊结节,性质待定,建议密切复查;右乳病变,右侧腋下多发肿大淋巴结,请结合专科检查。
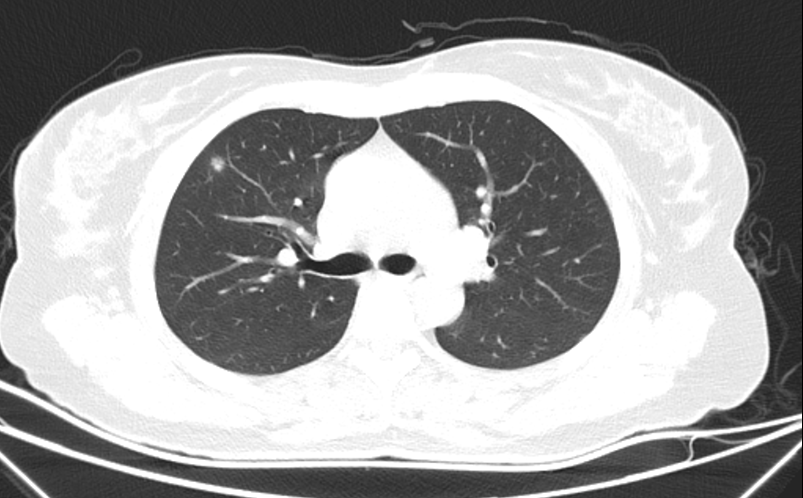
图4 CT结果
■ 右乳腺及腋窝淋巴结穿刺活检病理(2020-9-22):右侧乳腺浸润性导管癌。免疫组化结果:ER(90%强+);PR(40%强+);HER-2(2-3+);FISH检测基因扩增;Ki67(20%+);P53(30%+);AR(40%+);P63(-);D2-40(-)。右腋窝淋巴结细胞学:(右腋窝淋巴结)转移癌(图5)。
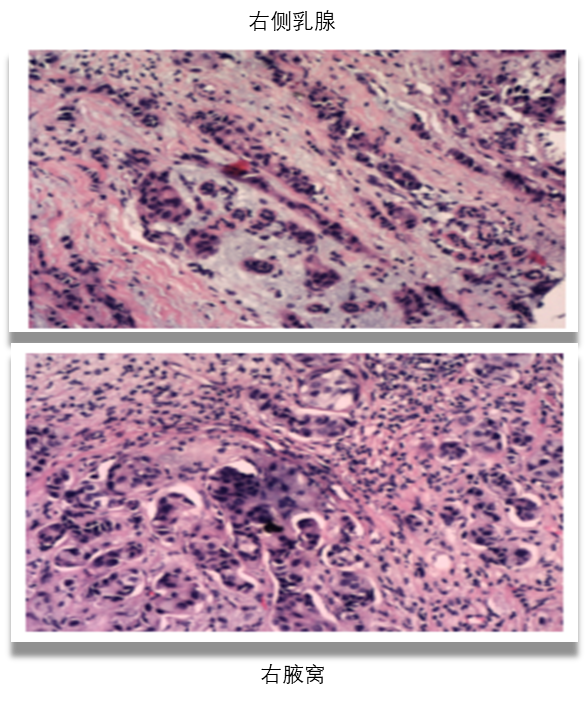
图5 穿刺活检结果
■ 实验室检查:血常规(白细胞、中性粒细胞计数、血红蛋白、血小板)、生化(肝肾功能ALT等)均正常,心肺功能正常,肿瘤指标(CEA、CA125、CyFRA21-1、NSE、SCC、TPA)均未见异常。
临床诊断:右乳浸润性导管癌,cT2NxM0。
治疗经过
一、新辅助治疗
与患者及家属沟通后,入组临床试验,予吡咯替尼+CDK4/6抑制剂+醋酸戈舍瑞林+来曲唑片治疗5个月。
2021年3月2日,复查乳腺彩超示:右乳腺1.4×0.7×0.8cm肿物,右腋下淋巴结0.7×0.6×0.4cm;乳腺DR示:右乳腺外上象限结构扭曲,右腋下密度增高淋巴结。2021年3月2日,复查乳腺MRI示:右乳腺肿块范围为16mm×8mm,右腋下未见肿大淋巴结,较前(2020年9月28日)缩小。
二、手术治疗
2021年3月5日,行右侧乳腺癌保乳术。术后病理诊断为:(右)乳腺浸润性导管癌(Ⅱ级);Miller-Payne分级:3级。免疫组化:ER(约90%中-强+);PR(约10%+弱+);Her-2(3+);AR(约10%+);CD31,D2-40染色未见明确脉管内癌栓(乳腺上、下、内、外、底切缘、腋窝组织及肌内组织)均未见癌;1站淋巴结中3个为淋巴结宏转移,2个为微小转移癌,1个为孤立肿瘤细胞,余下13个为反应性增生;2站淋巴结中2个为淋巴结宏转移,1个为微小转移癌,余下1个为反应性增生。诊断为:右乳浸润性导管癌,pT2N3M0 Ⅲc期。
三、术后辅助治疗
2021年7月29日,开始给予白蛋白紫杉醇化疗+曲帕双靶(HP)治疗6周期(乳腺外科),2021年8月至2021年10月,给予补充化疗(EC方案:表柔比星/环磷酰胺)4周期(外院),化疗期间给予亮丙瑞林内分泌治疗以保护卵巢功能、右乳腺及右锁骨上区放疗(50GY/25次)加强局部控制、OFS+来曲唑片进行内分泌治疗(乳腺外科)。2021年10月25日-2022年5月30日,给予HP靶向治疗。
四、强化辅助治疗
2022年6月-2023年5月,给予奈拉替尼强化抗HER-2治疗1年。
患者服用奈拉替尼一周内出现腹泻(每天6次),2级腹泻。经参苓白术散治疗之后有所好转(每天1-2次),经过治疗之后半个月腹泻明显改善,恢复正常。
专家点评
中国医科大学附属盛京医院乳腺肿瘤内科主任
CSCO抗肿瘤药物安全管理专家委员会委员
中国抗癌协会肿瘤营养专业委员会放疗营养学组委员
北京癌症防治协会精准靶向专委会委员
辽宁省抗癌协会乳腺癌专业委员会委员
辽宁省老年肿瘤专业委员会常委
住院医师规范化培训放射肿瘤科评审委员会委员
辽宁省中西医结合学会慢病委员会副主任委员
积极管理腹泻,提高治疗依从性
乳腺癌是我国女性发病率最高的恶性肿瘤,其中20%~30%的乳腺癌患者为HER-2阳性乳腺癌[2],抗HER-2治疗可有效改善患者预后。随着HER-2相关酪氨酸激酶抑制(TKI)的广泛应用,TKI药物相关不良反应越来越受到临床重视。腹泻作为TKI临床治疗过程中最为常见的不良反应之一,不仅可能降低患者的生活质量,还可能成为临床安全用药的制约因素。
随着分子靶向药物的不断更新,临床对其相关腹泻机制研究也逐步开展。本世纪初,曾有学者认为分子靶向药物相关性腹泻的发病机制与化疗相关性腹泻(CID)相同,但一项组织病理学研究显示,分子靶向药物相关性腹泻的病变部位通常是小肠,与CID发生部位不同。目前,国内外多位学者认为分子靶向药物相关性腹泻是由多因素共同导致的,涉及药物刺激小肠黏膜、离子转运失调、胃肠道感染、肠道菌群紊乱和胰腺外分泌功能障碍等多种可能机制[3]。
腹泻的临床表现主要为大便的性状改变和次数增多,TKI相关性腹泻往往发生于用药早期,并随着治疗时间延长,腹泻发生率逐渐降低[2]。因此,尽早进行抗腹泻管理尤为重要。临床治疗前应充分告知患者及其家属治疗中可能出现的腹泻风险,且多为2级,避免患者的过度忧虑;收集患者在治疗开始前6周的大便信息,以便更好评估腹泻的状况;在治疗过程中及时监测,收集患者同时服用的其他药物情况,以便评估药物对消化系统的潜在影响,以早日诊断。对于在分子靶向治疗前无腹泻而治疗后出现腹泻症状者,或治疗前已有腹泻而治疗后腹泻症状显著加重者,均应考虑分子靶向药物导致腹泻的可能性。在进行诊断时,应尽可能排除高渗性药物、消化不良、肠道细菌或病毒感染等导致的腹泻。
确诊后,需先合理评估腹泻的严重程度,并对应治疗[2,3]。出现1~2级腹泻不伴并发症时,应密切观察,避免脱水;补液支持,每天饮用1~1.5L等渗液体;改变饮食,避免摄取乳制品及高渗食物,清淡饮食,少量多餐;止泻处理,使用洛哌丁胺从4mg开始,此后每次腹泻服用2mg,最高剂量为16mg/d,并根据病情变化调整止泻治疗方案[2]。出现任何等级腹泻伴并发症或3~4级腹泻,需住院治疗,应暂停TKI及化疗,4级腹泻应永久停用TKI;静脉补液,维持水电解质平衡;合并中性粒细胞减少者可酌情使用抗生素治疗;改变饮食,避免食用乳制品及高渗食物,清淡饮食,少量多餐;止泻治疗,洛哌丁胺治疗,也可与阿托品、可待因片联用[2]。
中医止泻有良方,辨证论治疗效佳
中医称腹泻为“泄泻”,首载于《内经》,古将大便溏薄而势缓者称为泄,大便清稀如水而势急者称为泻,今统称为泄泻[4]。泄泻可见于多种疾病,分子靶向药物相关性腹泻亦属于“泄泻”范畴[3]。其病位在脾胃,脾病湿盛是泄泻发生的关键病机,明·李中梓在《医宗必读·泄泻》中提出了著名的治泻九法:淡渗、升提、清凉、疏利、甘缓、酸收、燥脾、温肾、固涩。而恶性肿瘤患者体质虚弱,脏腑亏虚,《EGFR-TKI不良反应管理专家共识》亦指出泄泻的发生与“药毒”和“体虚”有关,或因久病而脾胃虚弱,或因情志抑郁而肝郁乘脾,或因日久而伤肾,最终脾胃运化失常,内生湿滞,易感寒湿,而致泄泻,此为体虚之因;表皮生长因子受体(EGFR)-TKI是攻伐之品,属中医“药毒”的范畴,易伤脾胃而致泄泻,此为药毒之因[3]。
既往研究提示,参苓白术散可有效减轻靶向药物引起的腹泻,且对免疫有正向调节作用[3]。参苓白术散出自《太平惠民和剂局方》,其功效为健脾益气、渗湿止泻,主要用于脾气虚弱挟湿证,是治疗泄泻的重要方剂之一。方中人参、白术、甘草健脾益气,山药、莲子肉、茯苓、炒白扁豆、薏苡仁健脾益气、渗湿止泻,砂仁芳香醒脾,开胃助运,并可止泻,为桔梗,载药上行,达上焦以益肺气,肺气充足,通调水道之功能方可正常运转、利于祛湿以健脾,并可清肺化痰。此方从脾虚角度出发立法组方,可用于各种原因引起的泄泻,临床可根据患者实际情况辨证加减使用,治疗泄泻效果显著[5]。
本例患者经辨证,在奈拉替尼治疗一周内即给予参苓白术散治疗后腹泻明显好转。当然,本病例中参苓白术散的用法属于“既病防变”,用于发病之初。而“治未病”才是中医养生保健治病的最高境界以及特色优势。因此,在开始奈拉替尼治疗前,应使用中医特有的体质辨识(阴阳气血虚实等),对患者辨证性给予参苓白术散以提前干预可能发生的腹泻,后续若仍出现腹泻,再根据患者腹泻情况调整处方。做到未病先防,治在未病之先。
同时,中医以“正气内存,邪不可干”的论述强调重视体质的内在因素。因此在治疗期间,应嘱咐患者优化饮食结构,保持低脂高蛋白饮食,少食多餐,忌食用咖啡因、酒精、奶制品、脂肪、纤维、橘子汁、葡萄汁以及辛辣食物[3]。
[1] 我国乳腺癌患者5年生存率已提升至83.2%.[J]健康时报, 2023.06.30. http://paper.people.com.cn/jksb/html/2023-06/30/content_26002748.htm
[2] 王碧芸,葛睿,江泽飞,等.乳腺癌靶向人表皮生长因子受体2酪氨酸激酶抑制剂不良反应管理共识[J].中华肿瘤杂志,2020,42(10):798-806.
[3] 王施元,王致红,李春雨,等.抗肿瘤分子靶向药物相关性腹泻研究进展[J].药学学报, 2021, 56(12):8.
[4] 周仲瑛,中医内科学[M].中国中医药出版社,2003,4.
[5] 刘全喜,王微,张义军,等.参苓白术散治疗泄泻体会[J].中国中医药现代远程教育, 2022, 20(4):3.DOI:10.3969/j.issn.1672-2779.2022.04.057.
排版编辑:肿瘤资讯-Phoebe











 苏公网安备32059002004080号
苏公网安备32059002004080号


