对于HER-2阳性晚期胃癌,经典抗HER-2靶向药物曲妥珠单抗联合化疗已成为一线标准治疗方案,但对于有心脏基础病的患者,曲妥珠单抗可能诱发的心脏毒性让医患在用药时存在顾虑。因此,抗HER-2治疗仍存在未满足的临床需求。近年来靶向HER-2的新型抗体偶联药物(ADC)对HER-2阳性肿瘤取得较好疗效,不良反应可耐受。上海交通大学医学院附属仁济医院林晓琳、韩婷、江卫华和肖秀英医师分享1例HER-2阳性晚期胃癌病例:患者女性,71岁,残胃癌伴多发肝、骨、淋巴结转移,HER-2阳性,pMMR型。标准一线SOX方案治疗达到部分缓解(PR),因奥沙利铂神经毒性暂停用药,开始抗HER-2 ADC药物+替吉奥治疗,后出现消化道出血停用替吉奥口服,抗HER-2 ADC药物单药维持治疗至今,疗效持续PR,目前无进展生存期(PFS)已经超过2年。
病例介绍
基本情况
患者,女性,71岁,体重55kg,身高176cm,体表面积1.71kg/m2,ECOG评分1分。
主诉:“体检发现肝占位”于2021-4月就诊。
体格检查:神清,精神可,贫血貌,生命体征平稳,腹部软,无压痛、反跳痛。
既往史:1983年因胃溃疡出血行胃大部分切除术;2020年确诊为冠心病、心律失常、房早。
家族史:否认家族遗传病史及肿瘤相关病史。
辅助检查
2021年4月上腹部增强CT:胃肠道充盈欠佳,胃及小肠局部结构异常,胃壁粘膜可疑增厚伴强化,肝脏多发占位,后腹膜多发淋巴结肿大(图1)。
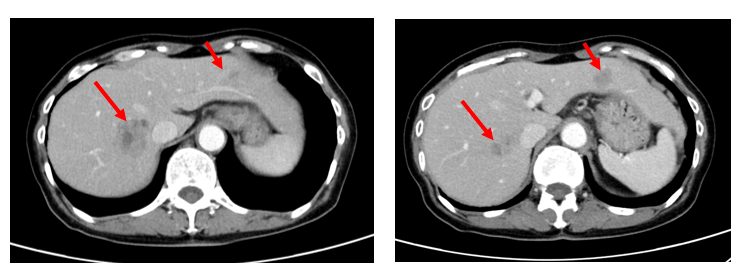
图1 2021年4月上腹部增强CT
2021年4月PET-CT:胃部术后,残胃壁明显增厚,FDG代谢异常增高(SUVmax=11.1),考虑恶性病变可能性大,伴腹主动脉旁、双侧髂血管旁、左侧锁骨上多发淋巴结转移(SUVmax=3.6-8.8),肝脏多发转移(3.6*2.6cm,SUVmax=11.6-12.8),右侧第6前肋、右侧髋臼骨转移可能(SUVmax=3.4-9.1)(图2)。
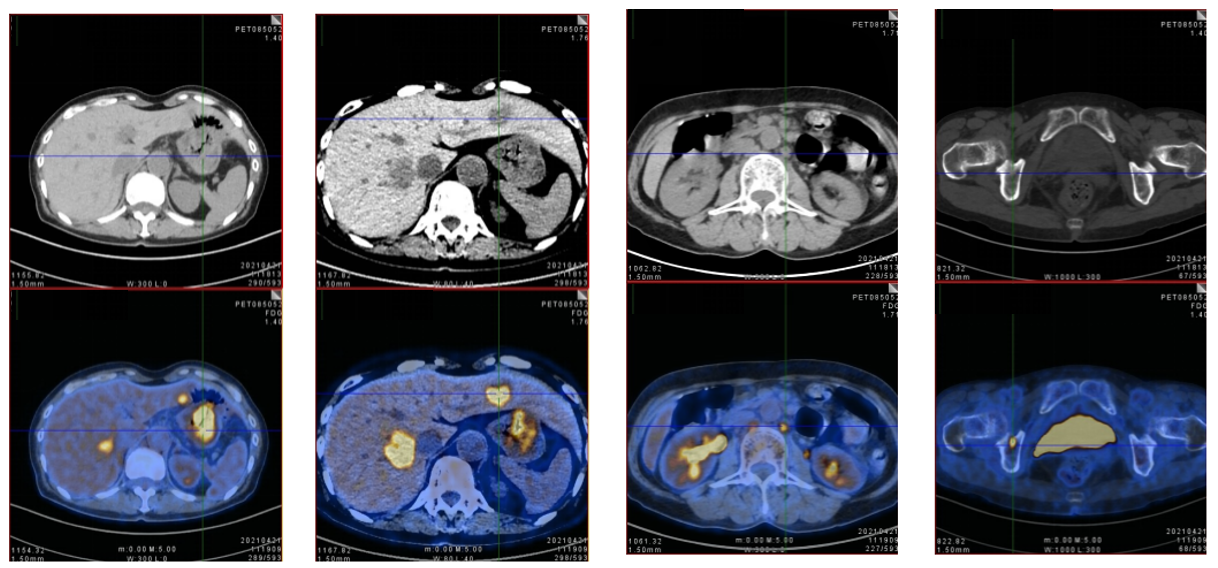
图2 2021年4月PET-CT
2021年4月胃镜:胃大部切除术后,吻合口浸润性改变(恶性可能),活检病理:管状腺癌。免疫组化:肿瘤细胞Ki67(70%),HER-2(3+),PD-1(-),PD-L1(-),MLH1(+),MSH2(+),MSH6(+),PMS2(+)。
2021年5月血常规:血红蛋白75g/L。心超:房间隔膨胀瘤形成;三尖瓣轻度反流;左室心肌顺应性下降;心律不齐,LVEF 58%。
诊断
残胃管状腺癌,cTxN+M1,IV期,肝、骨、多发淋巴结转移,HER-2阳性,pMMR型;胃大部切除术后,贫血;冠心病,心律失常,房早。
一线治疗
考虑患者贫血,无呕血黑便,2021年5月行替吉奥 50mg bid 口服 d1-14 联合唑来膦酸骨修复治疗,口服2周后复测血常规:血红蛋白98g/L。
2021年6月行SOX方案治疗,具体:奥沙利铂 200mg 静滴 d1+替吉奥 50mg bid 口服 d1-14,q21d。2周期后疗效评估疾病稳定(SD,肝脏病灶较2021-5略缩小)。
2021年6月底至2021年9月行一线第3-6程SOX化疗,剂量同前。4周期后疗效评估:部分缓解(PR)。
2021年9月上腹部增强CT显示肝脏多发转移灶,较前变小、部分显示不清,肝右叶较大者约2.4cm*1.6cm,见图3)。不良反应:II度神经毒性,II度血小板,III度粒细胞下降。

图3 上腹部增强CT
一线维持治疗
2021年10月初至2022年7月中旬行一线维持治疗,具体:维迪西妥单抗120mg d1+替吉奥50mg bid d1-14,q21d,联合唑来膦酸4mg骨修复治疗。
不良反应:II度骨髓抑制(白细胞及粒细胞下降),口腔黏膜炎I级,消化道出血。
期间多次疗效评估:持续PR。
2022年7月底因黑便于我院急诊就诊,血红蛋白55g/L。复查胸腹部CT:“胃癌术后、化疗后”改变;肝脏多发转移灶较前(2022-5)基本相仿。胃镜:胃大部切除术后;吻合口复发伴出血;残胃息肉。胃动脉造影+栓塞,术中见肿瘤染色明显,予输血等对症支持治疗后缓解,血红蛋白上升至80g/L。
考虑患者既往维迪西妥单抗治疗有效,替吉奥口服不耐受,2022年8月中旬至2023年4月继续予维迪西妥单抗治疗:120mg d1,q21d,同时唑来磷酸4mg继续骨修复治疗。
期间于2022年10月和2023年1月分别行胸腹部增强CT:胃壁局部可疑增厚;肝脏多发转移灶较前略缩小;余较前相仿。疗效评估:持续PR。
病例总结
该患者老年女性,初诊即胃癌晚期伴多发肝、骨、淋巴结转移,HER-2阳性。患者因中度贫血(血红蛋白75g/L),一线治疗首先采用替吉奥单药化疗联合唑来膦酸骨修复治疗,待血红蛋白恢复至98g/L后,行SOX方案(奥沙利铂联合替吉奥)治疗,2周期后达到SD。因患者顾虑曲妥珠单抗心脏毒副作用,继续行一线SOX化疗,4周期后评估PR。患者出现奥沙利铂神经毒性,考虑到抗HER-2 ADC药物安全性良好,一线维持治疗选择抗HER-2 ADC药物+替吉奥方案,同时联合唑来膦酸骨修复治疗。治疗期间患者出现消化道出血,经胃动脉栓塞术及输血等对症支持治疗后缓解,贫血纠正(血红蛋白恢复至80g/L)。考虑到患者既往抗HER-2 ADC药物治疗有效,替吉奥口服不耐受,采用抗HER-2 ADC药物单药维持治疗至今,疗效评价持续PR,目前PFS已经超过2年。
病例点评
上海交通大学医学院附属仁济医院肿瘤科副主任
毕业于复旦大学
中国抗癌协会整合肿瘤肾脏病学专委会常委兼副秘书长
中国临床肿瘤学会(CSCO)胃癌专委会委员
中国研究型医院学会消化道肿瘤专委会委员
中国医药教育协会胸部肿瘤专委会委员
上海健康生活促进会肿瘤科普与综合诊疗专委会主任委员
上海市医学会肿瘤专科分会委员兼秘书
上海市抗癌协会青年理事会副理事长
上海市抗癌协会胃癌分子靶向与免疫治疗专委会委员
上海市抗癌协会肿瘤免疫治疗专委会委员
国家卫健委人才交流服务中心人才评价专家
HER-2过表达是胃癌发生的重要驱动基因,10%~20%的胃癌患者存在HER-2过表达[1]。既往研究表明,HER-2阳性胃癌患者预后差,侵袭性更强[2]。ToGA研究[2]首次证实,对于HER-2阳性晚期胃癌患者,抗HER-2靶向药物曲妥珠单抗联合化疗可显著改善预后。但对于有心脏基础病的患者,临床用药会顾虑曲妥珠单抗心脏毒性。近年来,靶向HER-2的ADC药物在包括胃癌在内的多种HER-2阳性肿瘤治疗中崭露头角,我国自主研发的抗HER-2 ADC药物在HER-2 IHC2+/3+晚期胃癌患者中显示出明显的疗效和安全性优势[3],为临床医生带来了新的抗HER-2治疗手段。
在抗HER-2 ADC药物维迪西妥单抗的关键研究C008[3]中纳入了125例≥2线标准治疗失败的HER-2 IHC 2+/3+晚期胃癌患者,结果显示:抗HER-2 ADC药物治疗的客观缓解率(ORR)达到24.8%,中位PFS为4.1个月,中位总生存期(OS)达到7.9个月。进一步分析发现,对于既往接受过曲妥珠单抗治疗的患者(n=72),抗HER-2 ADC药物治疗的ORR达到27.8%,中位PFS为4.1个月,中位OS达到8.1个月;对于既往未接受过曲妥珠单抗治疗的患者(n=53),抗HER-2 ADC药物治疗的ORR为20.8%,中位PFS为4.0个月,中位OS达到7.5个月。安全性方面,主要不良反应为白细胞减少、虚弱、脱发、中性粒细胞减少等,对症支持治疗后可获得缓解;未发现间质性肺炎、心脏毒性等严重不良反应,无治疗相关死亡。基于C008研究结果,维迪西妥单抗在国内获批HER-2过表达(IHC 2+/3+)晚期胃癌治疗适应证,并获得权威指南推荐,2023版《CSCO胃癌诊疗指南》进一步提升了其推荐等级[4]。
目前CSCO和CACA胃癌诊疗指南等均推荐晚期胃癌按照HER-2状态进行分层治疗[4,5],HER-2 ADC药物已经成为HER-2 IHC 2+/3+且既往接受过≥2个系统化疗的局部晚期或转移性胃癌患者的标准治疗,由于其良好的疗效和可控的安全性,治疗前移是大势所趋。本例患者因有冠心病病史,采用抗HER-2 ADC药物维持,持续PR超过2年,可见ADC药物在HER-2阳性晚期胃癌前线治疗中有较好的应用前景,我们亦期待更多研究数据的发表,使ADC药物惠及更多患者,为HER-2阳性晚期胃癌患者带来更多治疗方案选择,以延长患者的生存时间和提高患者生活质量。
[1] Van Cutsem E, Bang YJ, Feng-Yi F, et al.HER2 screening data from ToGA: targeting HER2 in gastric and gastroesophageal junction cancer. Gastric Cancer. 2015;18(3):476-84.
[2] Bang YJ, Van Cutsem E, Feyereislova A, et al. Trastuzumab in combination with chemotherapy versus chemotherapy alone for treatment of HER2-positive advanced gastric or gastro-oesophageal junction cancer (ToGA): a phase 3, open-label, randomised controlled trial. Lancet. 2010;376(9742):687-97.
[3] Peng Z, Liu T, Wei J, et al. Efficacy and safety of a novel anti-HER2 therapeutic antibody RC48 in patients with HER2-overexpressing, locally advanced or metastatic gastric or gastroesophageal junction cancer: a single-arm phase II study. Cancer Commun (Lond). 2021;41(11):1173-1182.
[4] 2023版《CSCO胃癌诊疗指南》.
[5] 2022版CACA胃癌诊疗指南.
排版编辑:肿瘤资讯-Ivy











 苏公网安备32059002004080号
苏公网安备32059002004080号


