在2021成功举办“广东大会诊”的基础上,为了汇聚更大范围内的专家智慧,更广泛地推广肺癌多学科专家诊疗模式,广东省医学会肺部肿瘤学分会及广东省临床试验协会/中国胸部肿瘤研究协助组(GACT/CTONG)牵头,于2022年2月起组织开展“中国胸部肿瘤大会诊”活动。我们邀请全国各地胸部肿瘤治疗领域各专业专家组成会诊决策团队,每个月定期针对有代表性的肺癌疑难病例进行多学科会诊,集众人智慧之利剑,拾循证医学之护盾,为中国肺癌诊治攻坚任务贡献力量。

本场大会病例

01
病例介绍
▶病史概要
男性,41岁,PS =1分,硬皮病病史20余年,长期口服羟氯喹治疗。
2022-5-30检查发现CEA=26.09ng/ml。
2022-6-10广东省中医院行胸部CT平扫示:左侧下叶背段结节,考虑周围型肺癌;左侧胸腔少量积液。
2022-6-17行PEC-CT示(图1):左肺下叶背段高代谢结节灶,约2.7*2.5*2.1cm,考虑为周围型肺癌,伴灶周阻塞性炎症;左侧肺门及纵隔多发淋巴结转移;左侧胸膜多发转移,伴双侧少量胸腔积液;骶骨右侧单发骨转移;双肺下叶间质性肺炎,双肺上叶间隔旁型肺气肿;盆腔少量积液。

诊断:左下肺腺癌:cT1cN2M1b(胸膜、骶骨)IVA期。
表1. 2022-06-24穿刺标本NGS检测结果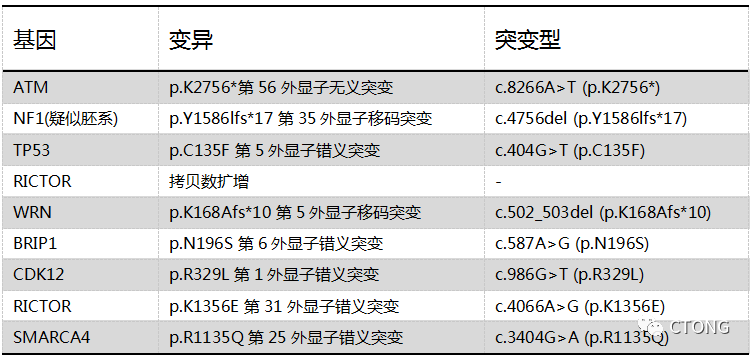
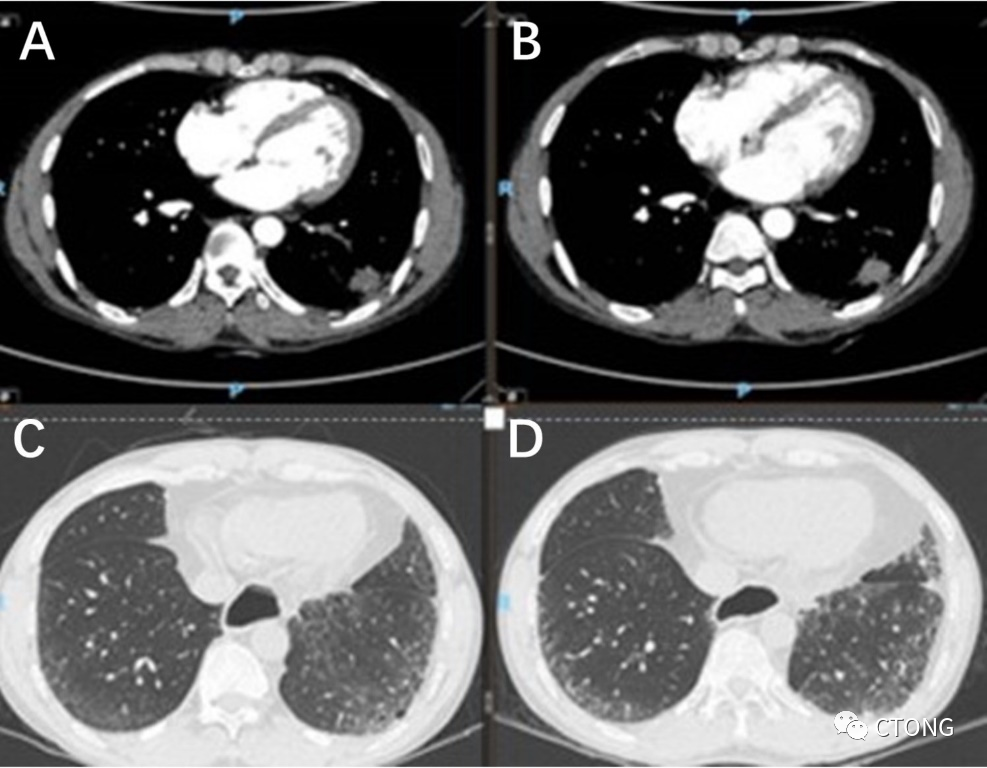
图2. 治疗前(A,C)和治疗后(B,D)肺部病灶对比
2022-7月开始行卡瑞利珠单抗+培美曲塞+卡铂治疗4周期

02
病史补充
颜黎栩医生:
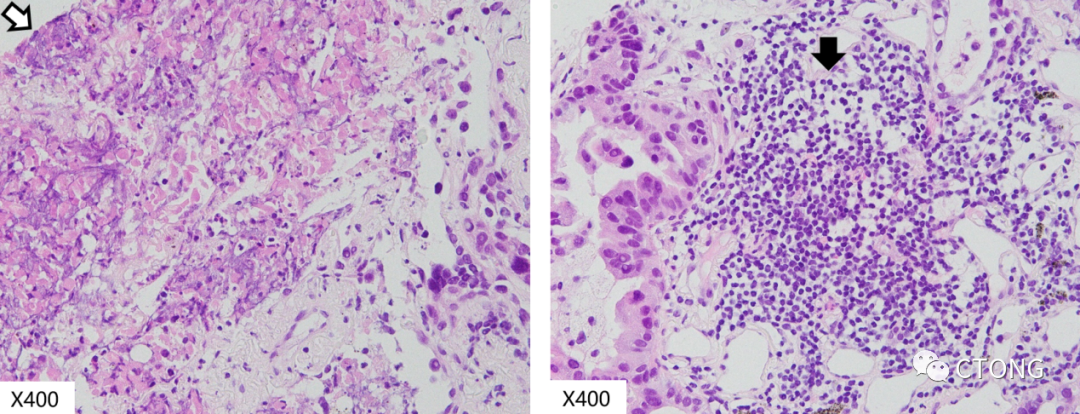
2022-06-27送检的肺穿刺标本一共有3条,分两个蜡块。白色箭头指示的是小灶肿瘤坏死,黑色箭头指示的是间质小灶淋巴细胞浸润,蓝色箭头指示的是间质纤维化(图3)。

图3. 2022-06-27送检肺穿刺标本;小灶肿瘤坏死(白色箭头),间质小灶淋巴细胞浸润(黑色箭头),间质纤维化(蓝色箭头)
在高倍镜下可以观察到灶性肿瘤坏死(白色箭头),间质灶性淋巴细胞浸润(黑色箭头)(图4)。在非小细胞肺癌中,坏死是肿瘤分化不良的影响因素,但该患者只有小灶的坏死,说明该肿瘤分化尚可。
大部分肿瘤组织呈现不规则的腺泡状排列,部分肿瘤细胞在肺泡腔内呈微乳头状生长。因为穿刺标本看不到瘤床外的肺组织,所以穿刺标本无法评估是否气道内播散(STAS),STAS一般只在手术的肿瘤组织中评估。微乳头的出现与肿瘤的肺内播散以及淋巴结转移相关(图5)。
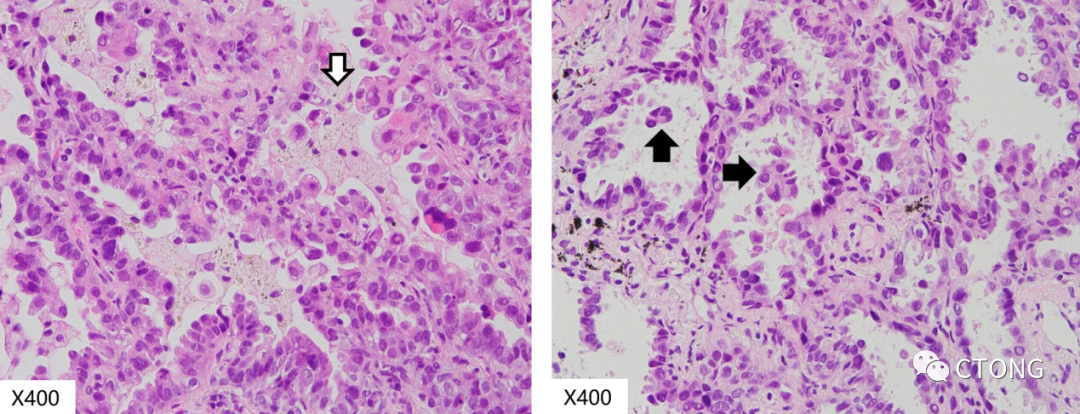 图5. 2022-6-27送检肺穿刺标本;肿瘤呈腺泡(白色箭头)及微乳头(黑色箭头)生长方式。
图5. 2022-6-27送检肺穿刺标本;肿瘤呈腺泡(白色箭头)及微乳头(黑色箭头)生长方式。03
病例讨论


涂海燕医生(主持人):总结一下病史:这是一个左肺IVA期的肺腺癌患者,有20多年硬皮病史,长期口服羟氯喹治疗。它的胸部CT上可以看到有间质样肺炎的改变,经过免疫治疗以后肺部间质样的改变仍然存在,甚至稍许增加。
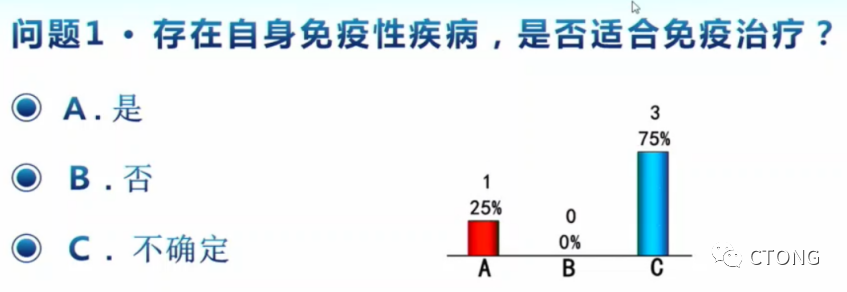

刘卓星医生:我在B和C之间纠结。我认为有自身免疫性疾病的病人,不适合做免疫治疗。

曹小龙医生:目前该患者硬皮病仍在治疗中,虽然此时加用免疫治疗可能会对硬皮病影响,但在多学科的监测的治疗下还是可以进行的。

张海波医生:如果是以前我会选B,因为患有自身免疫性疾病的患者,在进行免疫治疗时要非常谨慎,曾经有来自日本的研究,患有自身免疫性疾病的患者,即使只是存在自身免疫性异常,在接受免疫治疗时发生不良反应的风险也高于正常人群。现在我会选择C,是因为我们对这种疾病有了更多的认识,也在临床上积累了更多经验,我觉得对于存在自身免疫性疾病的患者需要更加细化的管理,比如说它是哪一种自身免疫性疾病,它的疾病处在什么样的阶段,它的活动程度怎么样,这都能决定我们是否使用免疫治疗,而且如果是患有自身免疫性疾病的患者,我们一般会选择化疗加免疫治疗。曾经我有一位患类风湿关节炎的患者,在经过风湿科的会诊之后,也进行了免疫治疗。因此对于患有自身炎性疾病的患者,我们需要更加细化的管理来进行免疫治疗。

吴一龙医生:你选择了C,那对于该患者你是否选择使用免疫治疗?

张海波医生:对于该患者,他的硬皮病控制良好,我会选择使用免疫治疗。虽然我们看到基因检测结果中包含有SMARCA4的错义突变,但这是一个杂合突变,所以应该也是一个二类的突变,影响不大。

江冠铭医生:在肺癌患者中有大概10%的人群同时患有自身免疫性疾病,既然免疫治疗已经成为肺癌的一线治疗,所以对于这种患有自身免疫性疾病的患者也不应该缺失。我们看到有一些回顾性的研究[1],患有自身免疫性疾病的患者使用免疫治疗与没有患自身免疫性疾病的患者在疗效上相当,毒性大一些,但大多数是1°和2°不良反应。3°的不良反应,大概在10~20%左右,所以这种不良反应的程度是可以接受的,即使是有活动性自身免疫性疾病的患者,在吃激素的同时也可以使用免疫治疗。在我的临床实践中,也经常遇到一些皮肤性的自身免疫性疾病的患者使用免疫治疗后,他们也可以从中获益。但对于严重的自身免疫性疾病,我觉得使用免疫治疗还是要慎重。

叶升医生:这是一个局限期、得到了良好控制的硬皮病患者,我会请皮肤科医生会诊,共同制定治疗方案,并且跟病人做好充分的病情告知,如果患者可以接受,我会考虑使用免疫治疗。对于该患者使用免疫治疗加上化疗可以提高疗效,不过还有一个保守的方案是化疗加上抗血管治疗。

聂强医生:我选择的是可以进行免疫治疗,目前对于患有自身免疫性疾病的肺癌患者是否能够使用免疫性治疗,其实没有更高级别的循证医学证据,几乎所有的免疫治疗的临床试验的研究都把患有自身免疫性疾病的患者排除在外,但在国外的真实世界研究中有报道相关的研究,在患有艾滋病的患者中使用免疫治疗的副作用与没有自身免疫性疾病的人群相比没有升高,长期使用激素也没有影响免疫治疗的疗效。

潘燚医生:我认为在临床实践中患有自身免疫性疾病的患者不应该完全排除免疫治疗。患有自身免疫性疾病的患者使用免疫治疗时只有47%的患者出现了原有疾病的加重,出现的80%以上的免疫不良反应基本都是1~2°的[2]。虽然有一些回顾性研究认为激素治疗可能与免疫治疗疗效和不良反应相关,但回顾性研究可能会存在偏倚,因为使用激素的患者会推迟免疫治疗,并且使用免疫治疗的疗程更短。基于上面的证据,我认为这个病例可以使用免疫治疗,该患者硬皮病的病情稳定,在严密监控下使用免疫治疗是可以耐受的。

刘志刚医生:我赞同前面专家的观点。硬皮病的病情稳定,NGS检测到ATM基因,说明DNA损伤修复基因存在缺陷,说明该患者可以从免疫治疗中获益。但是进行免疫治疗时需要谨慎,不是所有的自身免疫性疾病都适合进行免疫治疗,特别是那些重症的、活动性的自身免疫性疾病的患者。

涂海燕医生(主持人):该患者有20多年的硬皮病病史,疾病稳定,没有使用激素治疗,只是用羟氯喹治疗,但该患者双侧肺同时有轻微的间质样的肺炎改变。该肺炎可能是硬皮病引起的,也可能是肺癌引起的。在这种情况下,大家是否还要考虑使用免疫治疗加上化疗?

郑燕芳医生:我认为具有自身免疫性疾病的肺癌患者是否使用免疫治疗,应该根据她的病情来决定,如果是非常严重的自身免疫性疾病,使用了免疫治疗药物而复发可能会致死,因此对于这种情况我会非常的谨慎。但这位硬皮病的患者病情稳定,虽然双下肺有间质性改变,但并不严重,我觉得可以使用免疫治疗。

张海波医生:对于患有间质性炎症的患者,我还会考虑联合抗血管的药物,特别是这种轻微的间质性炎症。

吴一龙医生:刚刚的问题是说我们是否使用免疫治疗,那如果我们选择了免疫治疗,那我们会用免疫治疗维持多长时间?是否会一直使用免疫治疗直到进展?

张海波医生:我觉得刚开始进行免疫治疗时,我会密切关注他对免疫治疗的耐受程度,假如使用免疫治疗之后 ,耐受程度很好,不良反应轻微,那我会继续进行免疫维持治疗,就像该患者的情况我会继续免疫维持。

郑燕芳医生:我觉得有轻微的自身免疫性疾病的肺癌患者,使用免疫治疗联合化疗是比较合适的。但是免疫治疗之后,我不赞成免疫单药维持,因为免疫治疗维持可能会引起自身免疫性疾病发作。

王媛媛医生:对于自身免疫性疾病是否适合免疫治疗,我有去咨询过风湿免疫科的教授,他一直跟我们强调:自身免疫性疾病是一个免疫功能的紊乱,而不仅仅是免疫系统的过度激活。患有自身免疫性疾病的肺癌患者使用免疫治疗,并不一定会使自身免疫性疾病更严重。有研究者经过分析18,000例的患者免疫疾病的肿瘤患者使用免疫治疗后,发现患有自身免疫性疾病的肿瘤患者使用免疫治疗并不会增加明显不良反应风险和死亡风险[3]。因此,对于该患者, 我赞成使用免疫力治疗,同时我也支持使用免疫维持治疗。

张健医生:目前硬皮病的机制尚未明确,我觉得我们可以活检的时候检测肿瘤细胞周围T细胞的数量。如果周围T细胞浸润较少,说明免疫功能较弱,那我们可以使用免疫治疗。

张海波医生:我觉得需要跟风湿科的医生商量,对自身免疫性疾病进行再细分。对自身已经有攻击性的自身免疫性疾病应该谨慎使用免疫治疗,比如像系统性红斑狼疮。如果是比较弱的就可以使用。因此,我建议是根据自身免疫性疾病的分类进行更加个体化的治疗。

曹小龙医生:自身免疫性疾病可能都是以免疫亢进为主。
第二次投票:
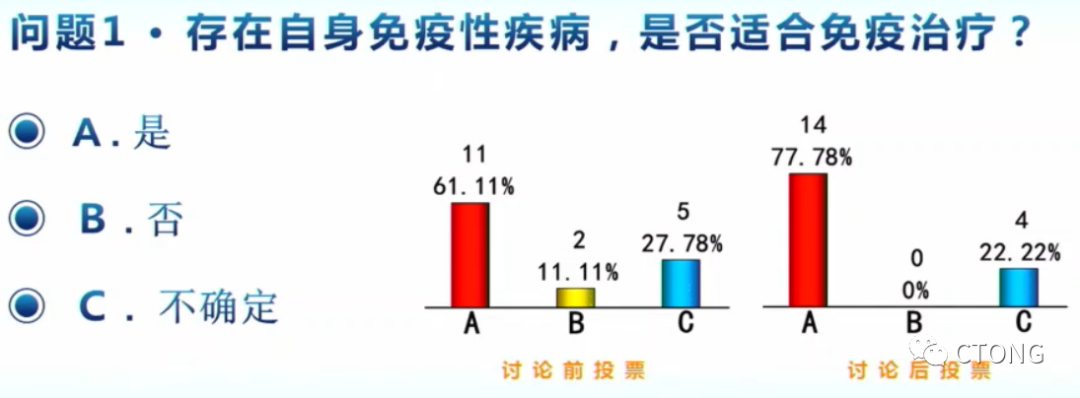
问题2. 针对此病例,4期肺癌免疫治疗后可能局部干预时机?
A. 2周期免疫治疗后
B. 4周期免疫治疗后


张健医生:这是硬皮病合并肺癌的患者,该患者的CT影像上有间质性肺炎表现,而且治疗之后有增加,因此该患者可能会因为免疫治疗相关性不良反应导致用药停止,因此我觉得局部干预会给他带来益处。该患者的肿瘤病灶处于外周,通过楔形手术切除,可以获得病理和基因的信息,能够指导下一步的治疗。

聂强医生:我同意张教授的观点,我认为经过4周期免疫治疗之后,能够给该患者带来获益。出现免疫相关性不良反应的概率与免疫治疗的时长相关。我遇到一些要准备进行新辅助治疗的患者,经过三周期的治疗之后出现了免疫相关性肺炎,导致手术就无法进行。

吴一龙医生:新辅助免疫治疗的患者经过免疫治疗之后,出现免疫相关性不良反应,导致手术不能进行,你认为这是好事还是坏事?

聂强医生:我认为可以从两方面看待这个事情。患者因为免疫相关性不良反应而无法接受手术,从我们外科医生的角度来讲,这是一个遗憾。但是也有一些证据表明,出现免疫相关性不良反应说明他们的疗效较好,因此对治疗疗效这是一个好事。

潘燚医生:我选择的是4周期免疫治疗后加入局部治疗。目前寡转移的临床研究一般都是经过4个周期或者三个月全身系统治疗,病灶达到稳定之后,加入局部的干预能够取得生存获益。针对该病例,我们可以看到2周期和4周期的免疫治疗后,病灶的缩小程度几乎一致,那么假如该患者继续行免疫治疗的获益也不大。因此,我觉得目前4个周期的免疫治疗是一个最佳的局部治疗切入点。当然该患者有胸膜的转移,不能完全按照寡转移的治疗模式,因此我建议该患者进行PET/CT检查,如果胸膜病灶可控,那么我会针对骨转移病灶进行放疗。如果有胸膜转移,那么我认为他暂时不适合进行局部治疗。

刘志刚医生:我赞同潘教授的观点。前面的研究表明,寡转移的病灶经过局部治疗之后可以提高三倍的PFS,OS可以从17个月延长到44个月。因此我赞同该患者在经过4周期免疫治疗之后进行局部干预[4]。

肖林医生:我选择C,疾病处于稳定阶段再进行局部干预。我认为需要在局部干预之前进行PET/CT评估,如果局部干预能够控制局部进展才需要加上局部治疗。局部治疗的目的防止病灶再次转移到相同的部位。

刘卓星医生:我也选择C,该患者2周期和4级周期的疾病状态都是SD,我觉得都可以进行局部干预。但是我不认为该患者马上需要进行局部干预,该患者髂骨的病灶控制稳定,我认为局部干预的意义不大,但如果骨转移部位进展较快,并且出现症状,那么可以考虑放疗干预。

王芬医生:我对该患者是否可以定义为寡转移存在疑问,我想请放射科的刘教授帮我们解读一下CT结果。

刘春玲医生:对比该患者治疗前和治疗后的CT影像,该患者肺内的原发灶和淋巴结经过治疗之后都有缩小。肿瘤病灶累及胸膜,但胸膜其他部位并没有看到转移,也没有胸水,因此认为该患者没有胸膜转移,而是局部的肺不张。双下肺的间质性纤维灶在经过治疗之后更明显,有新发的网格状改变。

王芬医生:如果没有胸膜转移,那我会考虑在进行4个周期免疫治疗之后进行局部干预。

叶升医生:目前确定该患者没有胸膜转移,那么可以称为寡转移。对于寡转移的患者我认为要等该患者真正的病情稳定之后再进行局部干预,目前并不着急进行局部干预。比如PET/CT复查后,病灶SUV值降低; CEA处于稳定的状态。

涂海燕(主持人):因为该患者在治疗前有多发纵隔淋巴结转移,如果此时外科医生考虑手术干预,那么需要病人治疗效果达到什么程度?

叶升医生:我补充一下,如果要进行局部干预,我认为需要把转移灶和原发灶一起处理,这样才能达到最佳的治疗效果。

张健医生:我认为外科干预的作用有两个:第一是可以更加精确的诊断。经过外科微创手术可以拿到肿瘤原发灶,纵隔淋巴结的组织进行活检得到病理类型和基因检测结果,另外可以观察胸膜是否有转移。要等到其他转移病灶稳定,只有一个病灶局部进展时才有局部治疗的意义。我认为患者只有得到了精确的病理诊断和分子诊断,并且使用相应的药物才能够提高获益。

曹小龙医生:我认为IV期的肺癌患者主要是以姑息治疗为主,如果该患者转移病灶稳定,可以不需要局部治疗,但如果转移病灶有进展,可以考虑手术或放疗干预。或者等患者稳定相当长一段时间之后再考虑局部干预治疗。

郑燕芳医生:局部治疗有两种,有手术干预和放疗干预。我认为局部干预治疗的时机与局部干预的种类有关。因为放疗的创伤较小,而且不影响全身的免疫治疗,而且该患者髂骨转移病灶较小,两周期的免疫治疗之后可以进行放疗。但因为肺部手术的创伤较大,而且对患者的纵隔淋巴结转移的范围有要求,对患者的心肺功能有要求,因此需要更加谨慎。

肖林医生:对于寡转移的肺癌患者,我一般进行6周期的免疫治疗之后再进行根治性的放疗。我不建议进行同步放化疗,只需要单纯的放疗。因此对于该患者,我认为应该再进行两周期的免疫治疗之后再进行根治性放疗。

刘志刚医生:我认为应该关注干预的时效性问题,我认为应该现在行局部治疗干预。如果该患者一年或一年半之后再进行局部治疗干预,那么它就属于治疗进展之后的治疗干预,而不属于寡转移局部治疗。

张健医生:我认为局部手术干预不一定要做肺叶切除或者系统性淋巴结清扫,达到R0切除状态,而可以仅仅去处理进展的病灶。通过微小的外科创伤治疗,同样也可以延长患者生存。

江冠铭医生:如果该患者没有胸膜转移,只有骨转移,我个人会积极的进行局部干预。经过免疫治疗病灶缩小到稳定之后,我会主动进行放疗干预;另外如果该病灶出现增大,我就会马上进行局部的放疗干预。
第二次投票:


吴一龙医生:目前有一些回顾性的结果表明[1-2]:肺癌患者中患有自身免疫性疾病的比例非常高,占比20%~40%。因此我们需要特别重视这部分人群的治疗。在有效性上,不管是否患有自身免疫性疾病,他们使用免疫治疗的疗效没有明显差异。在安全性上,患有自身免疫性疾病的肺癌患者使用免疫治疗比没有患有自身免疫性疾病的患者更加容易出现爆发性进展,占比23%,并且出现三度以上的不良反应的比例也是没有自身免疫性疾病人群的2~3倍,因为毒副反应而中断治疗的人群占比10%~15%。因此,对于自身免疫性疾病的肺癌患者,我们仍然可以使用免疫治疗,而且不需要缩短使用免疫治疗的疗程,但我们需要密切关注这部分患者的毒副作用。
对于使用免疫治疗的IV期的肺癌患者使用局部治疗可以提高患者的生存期 [5]。因此,对于这部分患者应该积极进行局部治疗干预。对晚期的患者进行局部干预,我觉得需要与早期的新辅助治疗区别开来,新辅助治疗是根治性的治疗,经过两周期或者4周期的治疗可以进行。但是晚期的不一样,应该在全身控制良好,只剩下寡残留或者寡进展的时候再加入局部治疗。像单发肺肿瘤、肾上腺或者是孤立的脑都可以加入局部治疗。局部治疗的手段应该根据病灶的部位选取相应的治疗方案。目前,该患者原发肿瘤病灶稳定,只有单发的骨转移,因此我们需要考虑加入局部干预。
04
MDT小结
05
吴一龙医生评述

2.寡病灶的概念,近年来也有了较为清晰的定义,包括了肺癌初诊时的寡转移,即肺部病变分期相对较早可做到R0切除,但伴有孤立性的脑转移或孤立性肾上腺转移;寡转移还包括术后出现的孤立性转移,这类患者已经有较多的队列研究证实了局部干预的价值;另外的寡病灶概念主要见于4期肺癌治疗后存在的的情况,一是寡残留,患者全身病变控制得非常好,只剩下某一个地方的残留病灶;二是寡进展,病变稳定一定时间后某一个病灶在缓慢进展。这两种情况在靶向治疗和免疫治疗中比较常见。
3.局部治疗的干预时机也是值得研究的。寡残留的干预,实际上是主动性更强的治疗,即在全身治疗疗效最佳时候的局部干预;寡进展的干预,实际上是选择在全身治疗可能失败的时机进行;两者孰优孰劣,没有强的循证医学证据可供参考。鉴于目前局部治疗的创伤性低,我更倾向于在寡残留时的积极干预。

06
追踪随访
2022-10-14 予以第5周期卡瑞利珠单抗联合化疗治疗。
参考文献:
1.Tison A, Garaud S, Chiche L, Cornec D, Kostine M. Immune-checkpoint inhibitor use in patients with cancer and pre-existing autoimmune diseases [published online ahead of print, 2022 Oct 5]. Nat Rev Rheumatol. 2022;10.1038/s41584-022-00841-0. doi:10.1038/s41584-022-00841-0
2.Tang K, Tiu BC, Wan G, et al. Pre-Existing Autoimmune Disease and Mortality in Patients Treated with Anti-PD-1 and Anti-PD-L1 Therapy. J Natl Cancer Inst. 2022;114(8):1200-1202. doi:10.1093/jnci/djac046
3.Leonardi GC, Gainor JF, Altan M, et al. Safety of Programmed Death-1 Pathway Inhibitors Among Patients With Non-Small-Cell Lung Cancer and Preexisting Autoimmune Disorders. J Clin Oncol. 2018;36(19):1905-1912. doi:10.1200/JCO.2017.77.0305
4.Olson R, Jiang W, Liu M, et al. Treatment With Stereotactic Ablative Radiotherapy for Up to 5 Oligometastases in Patients With Cancer: Primary Toxic Effect Results of the Nonrandomized Phase 2 SABR-5 Clinical Trial [published online ahead of print, 2022 Sep 29]. JAMA Oncol. 2022;10.1001/jamaoncol.2022.4394. doi:10.1001/jamaoncol.2022.4394
07
本期讨论专家

涂海燕 广东省人民医院 广东省肺癌研究所
吴一龙 广东省人民医院 广东省肺癌研究所
曹小龙 广州市番禺中心医院
陈荣辉 东莞东华医院
江冠铭 南方医科大学附属东莞医院
李建国 中山大学孙逸仙纪念医院
刘卓星 河源市人民医院
涂海燕 广东省人民医院 广东省肺癌研究所
王 芬 北京大学深圳医院
王媛媛 南方医科大学南方医院
阳 隽 广州医科大学附属第二医院
叶 升 中山大学附属第一医院
郑燕芳 广州医科大学附属肿瘤医院
张 健 中山大学附属第三医院
肖 林 江门市中心医院
颜黎栩 广东省人民医院
刘春玲 广东省人民医院
文稿整理 | 揭光灵(广东省肺癌研究所)
指导 | 董 嵩(广东省肺癌研究所)


以上信息转自CTONG官方微信平台
-End-











 苏公网安备32059002004080号
苏公网安备32059002004080号


