移植物抗宿主病(GvHD)是异基因造血干细胞移植后常见的严重并发症,其标准一线治疗为全身性糖皮质激素治疗,但约有50%的患者无法获得持续性缓解,而对于激素治疗效果不佳的患者,目前缺乏公认有效的挽救手段。芦可替尼(RUX)是一种高选择性JAK1/2抑制剂,3期临床研究结果表明,与现有最佳可用疗法(BAT)相比,RUX可提高患者总体反应率(ORR)和无失败生存率(FFS),已成为GvHD二线治疗的首选。一年一度的美国血液学会(ASH)年会是全球血液学领域规模最大、涵盖最全面的国际学术盛会之一。今年12月11日~14日,第63届ASH盛大召开。会议汇集世界各地的血液病学专家,公布众多的临床及科研成果。本次大会期间公布了多项芦可替尼治疗移植物抗宿主病的研究成果,为移植物抗宿主病的治疗提供了新的治疗选择。【肿瘤资讯】第一时间筛选其中的重要研究特作梳理,以供参考。
研究一:RUX对比BAT治疗糖皮质激素耐药或依赖的慢性移植物抗宿主病(SR/D cGvHD)的患者报告的结局(PROs)
标题:Patient-Reported Outcomes (PROs) Among Patients With Steroid-Refractory or -Dependent Chronic Graft-vs-Host Disease (cGvHD) Randomized to Ruxolitinib (RUX) vs Best Available Therapy (BAT)
摘要号:3909(Poster)
发布日期:2021年12月13日
目的:
该项研究对 REACH3中的PRO进行了分析,并对mLSS的分量表结果与客观的排异器官缓解进行了比较。
方法:
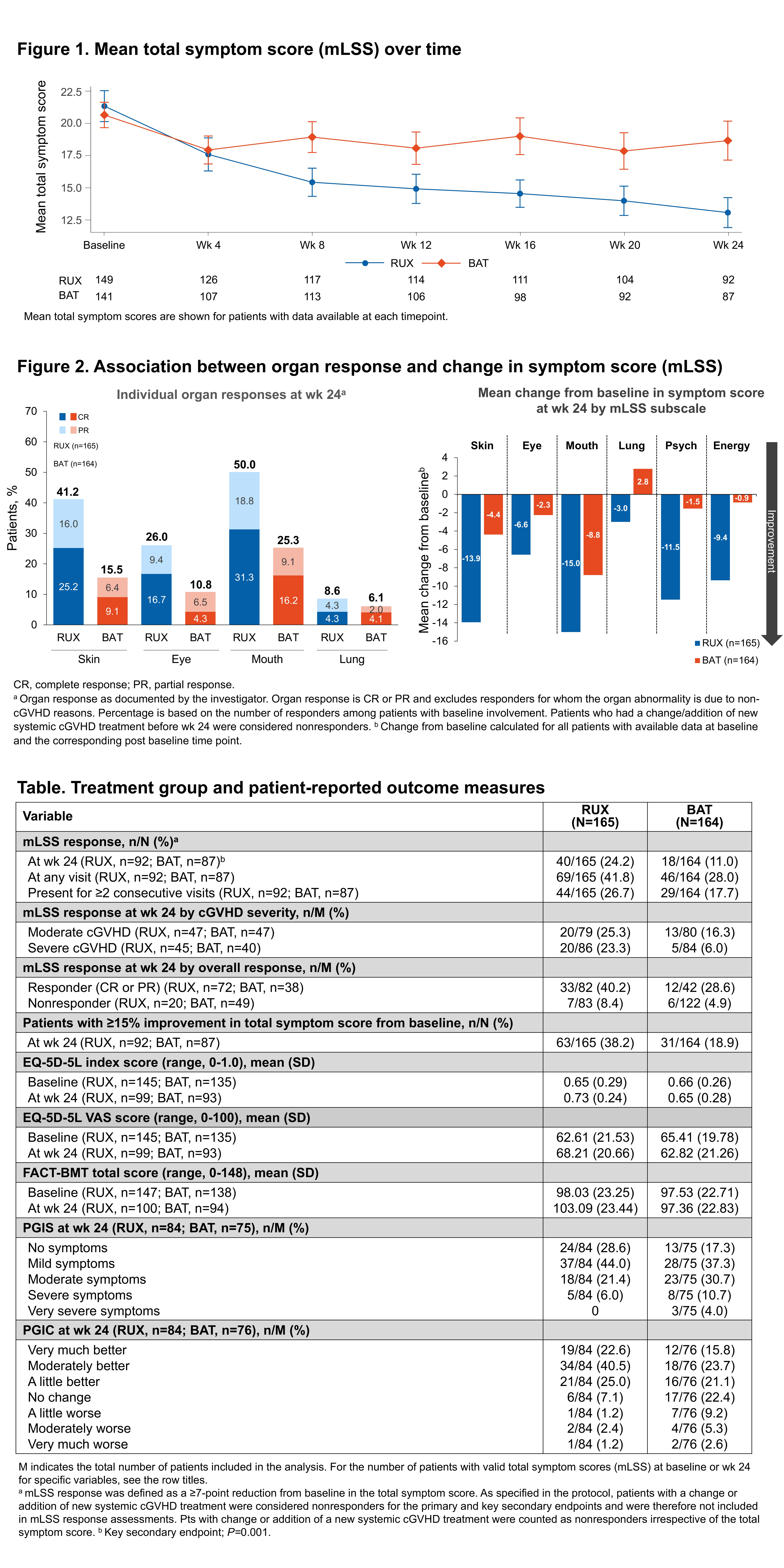
纳入年龄≥12 岁的中度或重度SR/D cGVHD患者,随机 (1:1) 接受RUX 10mg每天两次的治疗,或者接受研究者从10种常用BAT中选择的方案进行治疗。患者接受随机治疗药物+皮质类固醇±一种钙调神经磷酸酶抑制剂共同治疗≥6 个周期(28天/周期)。开始或增加新的系统性抗cGvHD药物治疗则被认为治疗失败。PRO在基线至第 24 周期间以4周间隔方式进行收集,或直到治疗失败或从主要研究期中止。在第24 周时,mLSS总分(0 [无症状] 至100 [最严重症状])相比基线改善≥7分的患者缓解率是一个关键的次要终点(α控制)。其他研究终点为个体器官缓解和其他PRO变化(癌症治疗的功能评估-骨髓移植 [FACT-BMT]、EQ-5D-5L、患者总体严重程度印象 [PGIS]、患者总体变化印象 [PGIC] )。55.8%的RUX患者 (92/165) 和53.0%的 BAT患者(87/164) 在第24 周获得了mLSS数据(其他PRO可评估的患者见表)。
结果:
共纳入329例患者,RUX组165例,BAT组164例。两组患者的基线特征包括症状负担无统计学差异,分别有48%和52%的患者有中度或重度cGvHD。两组的中位基线mLSS得分分别为18.7 (RUX) 与18.5 (BAT)。
RUX组患者在第24周、第24周之前的任何时间以及≥2 次连续随访的mLSS 缓解率均高于BAT组患者(表)。 RUX组患者的平均总体mLSS 症状评分呈快速持续降低趋势,而BAT组仅在第4周出现初始降低(图1)。在亚组分析中,中度和重度cGVHD患者RUX治疗的 mLSS 反应率相似。在达到完全或部分缓解的cGvHD患者中,接受RUX治疗患者的缓解率高于BAT(RUX,40.2%;BAT,28.6%)。
所有7个mLSS分量表中,RUX组的mLSS分量表缓解率较BAT组高(优势比,>1.7;P<0.05,肺除外)。第24周时RUX组较BAT组在7个mLSS分量表的平均分数降低幅度更大,器官特异性分量表的改善程度与两组在第24周时各自器官的更高客观缓解率相关(表2)。与BAT组相比,RUX组的与器官缓解不直接相关的整体症状负担也更好。
根据 PGIS,RUX组患者报告“没有症状”较BAT组多(28.6% vs 17.3%),根据 PGIC,RUX组患者报告“非常好”或“中等好”也较BAT组多(63.1% vs 39.5%)。RUX治疗对第24周时非cGvHD特异性PRO测量(EQ-5D-5L 和 FACT-BMT)也有积极影响。
结论:
与BAT治疗相比,RUX治疗对 PROs 产生了更实质性的改善,症状缓解更加快速和持久,且在改善各mLSS分量表方面也有优势,这些数据表明RUX治疗不仅在医生评估的疗效方面优于 BAT,而且在改善患者cGvHD症状方面也优于BAT。RUX治疗的EQ-5D-5L和 FACT-BMT量表分数在数值上高于BAT,但数值变化较小提示这些量表过于通用,无法完全反应cGvHD对患者QOL的影响. 重要的是,患者的器官特异性症状改善与医生评估的客观器官缓解均在RUX治疗组更好。
研究二:RUX治疗糖皮质激素难治性cGvHD患者的ORR和EFS的多中心回顾性评估更新
标题:Update of Multicenter, Retrospective Evaluation of Overall Response and Failure Free Survival Following Ruxolitinib Therapy for Heavily Pre-Treated Chronic Gvhd Patients with Steroid-Failure: A Proposal of Risk Score Model for Failure-Free Survival
摘要号:3905(Poster)
发布日期:2021年12月13日
目的:
评估RUX治疗糖皮质激素失败cGvHD的ORR、EFS和总体生存率(OS),并探讨与患者预后的关系。
方法:
该研究回顾性分析了2016年至2021年接受RUX治疗的115例cGvHD患者。患者疾病特征如下:中位年龄57.5岁,男性67例(60%),RUX治疗时器官受累比例:皮肤75.7%,口腔51.3%,眼42.6%,胃肠道19.1%,肝39.1%,肺 31.3%,骨骼肌肉38.3%。在HSCT前有可用HCT-CI数据的108例患者中,29例(26.9%) 患者的HCT-CI评分为3以上,而79例 (73.1%) 患者的HCT-CI评分为0-2。
在第3、6和12个月对ORR进行了回顾性分析。治疗失败定义为: 1) 耐药需要转换治疗;2) 非复发死亡率 (NRM);3) 复发;4) 不耐受。FFS和OS从RUX起始治疗cGvHD之日起计算。
用logistic回归评估6个月时ORR的风险因素,用Cox比例风险模型评估12个月时FFS和OS的风险因素。以下变量用于风险因素分析:GvHD相关因素(cGVHD 严重程度、器官受累数量、开始治疗时的泼尼松剂量或RUX 剂量、既往急性GvHD病史)、宿主因素(年龄或体能状态、性别、HSCT前的HCT-CI合并症评分)、移植因素(预处理强度、供者类型、HLA匹配情况、T细胞耗竭)。在多变量分析中有显著性的变量作为预后风险评分。
结果:
共115例患者纳入研究,69例(60%)为重度cGvHD,44例 (38.3%)为中度cGvHD,2例(1.7%) 为有高风险特征的轻度cGvHD。中位器官受累数为3(范围1~7)。 96例患者(84.2%)接受RUX 作为4线或后线的cGvHD治疗。既往治疗包括吗替麦考酚酯(n=46, 40.0%)、体外光分离置换(n=45, 39.1%)、伊马替尼(n=13, 11.3%)和伊布替尼(n=9, 7.8%)。RUX的初始剂量为每天10~20mg,后在第3、6和12个月每天分两次服用20mg。
中位随访时间为12个月,3、6和12个月的ORR分别为46.8%、61.8% 和 62.3%,与REACH3研究中的类似(6个月ORR率为49.7%)。6个月时,所有受累器官的ORR范围为48.1%~64.5%。糖皮质激素耐药、糖皮质激素依赖或前期有TKI治疗史患者之间的ORR无差异。重度cGvHD 6个月时的ORR低于轻中度cGvHD(46.8% vs 81.1%,P=0.001)。
在泼尼松减量方面,到12个月时,有63.8%患者的泼尼松剂量减至0.1mg/kg/d以下,在0、3、6和12个月时泼尼松剂量低于0.1mg/kg/d的患者比例分别为14.83%、33.6%、47.6%和63.8%。
共有39例患者 (33.4%) 治疗失败,包括需要转换治疗方案 (n=17)、NRM (n=14)、原发病复发 (n=3) 和不耐受 (n=5)。整体FFS率为 64.6% (54.1~73.2),12个月的OS率为83.3% (74.4%~89.4%) 。
确定了FFS的两个风险因素(图):1)RUX开始时的cGvHD严重程度(P=0.008,HR2.496 [1.229~5.072]);2) HCT-CI合并症评分为3以上(P=0.001,HR 2.802 [1.493~5.259])。当生成风险评分模型时,产生的预后风险模型对12个月时的风险进行分层评估(P=0.0001):评为0占85.8% (n=32),评分为1占58.7% (n=57),评分为2占36.8% (n=19)。
结论:
本研究更新结果证实RUX是cGvHD患者有效的治疗选择。RUX治疗对所有GvHD累及器官中均显示出良好反应。RUX治疗失败与cGvHD严重程度及HCT-CI评分有关。

研究三:倾向评分匹配(PSM)分析比较RUX与历史对照作为2线及后线cGvHD治疗的患者结局
标题:Propensity Score Matching Analysis Comparing Ruxolitinib Vs Historical Controls in 2nd Line or Beyond Treatment for Chronic Gvhd after Therapy Failure
摘要号:1805(Poster)
发布日期:2021年12月11日
目的:
PSM比较2005年至2013年间接受RUX和BAT(历史对照)作为2线及后线治疗的cGVHD患者临床结局。
方法:
BAT 包括霉酚酸酯 (43%)、泼尼松 (29%)、泼尼松/环孢素 (12%)、体外光分离置换 (6%)、利妥昔单抗 (3%) ,其他 (7%)。RUX组的重度GvHD患者比例高于BAT组(59.1% vs 20.3%,P<0.0001),RUX组中4线以上方案治疗比例高于BAT组(84.3% vs 17.0%,P<0.0001)。
从开始RUX或BAT治疗之日开始计算FFS和OS,根据患者体重计算0、3和6个月的每日泼尼松剂量。应用PSM 分析来调整两组间的不平衡因素,包括开始治疗时的 GvHD严重程度(轻度/中度vs重度)、HCT-CI 评分(0~2分 vs 3分以上)和治疗线数(2线vs 3线 vs 4线或后线)。最终通过PSM在0.2的差异内提取了共100例患者(50例接受RUX治疗,50例接受BAT治疗)。PSM 分析平衡了两组之间的危险因素差异:GvHD 严重程度 (P=1.0)、HCT-CI评分(P=1.0) 和治疗线数 (P=1.0)。应用Cox比例风险模型比较治疗12个月时的 FFS和OS率。
结果:
共纳入426例患者,中位随访时间为19 个月,244例患者治疗失败(57.3%)。两组由于NRM导致的治疗失败率相似,但RUX组需要治疗转换的失败率显著低于BAT组。 RUX组有40例治疗失败,其中有23例需要治疗转换(33.4%),14例NRM (12.2%) ,3例复发(2.6%) 。BAT组204例治疗失败,其中治疗转换142例(45.7%),NRM 36例(11.6%),复发26例(12.7%)。
RUX组与BAT组12个月的FFS 率分别为64.7%和40.1%(P<0.0001;图 1A),OS 率分别为83.4%和83.7%(P =0.913 ;图 1B)。在PSM队列 (n=100) 中,RUX的生存获益优于BAT组:RUX组与BAT组12个月的FFS 率分别为74.0%和29.7%(P<0.0001;图 2A),OS率分别为90.5%和80.2%(P =0.109;图 2B)。
PSM队列中的多变量分析证实:HCT-CL评分0-2的患者中,RUX在FFS获益方面优于BAT(P<0.001,HR 0.267 [0.139~0.516]),而HCT-CL评分≥3的患者中,RUX组显示出获得更高生存获益的趋势(P=0.110,HR 0.402 [0.131~1.228])。
泼尼松剂量随时间逐渐减少:RUX 组在第0、3 和6 个月的中位泼尼松剂量分别为0.34、0.16和0.02 mg/kg/d,BAT组的分别为0.95、0.24和0.15 mg/kg/d。
RUX治疗有助于停用泼尼松。 RUX组在第 0、3和6个月时停用泼尼松的患者比例分别为8.7%、15.9%和24.1%,BAT组的分别为0.7%、0% 和2.0%。在第0、3和6个月时,两组之间停用泼尼松的患者比例差异分别为8.0%、15.9%和22.1%(图 3)。
结论:
RUX作为2线以上治疗cGvHD优于BAT,且有助于减少糖皮质激素用量。

研究四:RUX治疗异基因造血干细胞移植后闭塞性细支气管炎综合征(BOS)
标题:Ruxolitinib for Bronchiolitis Obliterans Syndrome after Allogeneic Hematopoietic Stem Cell Transplantation
摘要号:3899(Poster )
发布日期:2021年12月13日
目的:
RUX治疗成人移植后BOS疗效。
方法:
2008年至2020年间,共有52例根据2014年NIH标准诊断为BOS的患者纳入研究,中位年龄为33岁(18~58),女性占48%。中位FEV1%为 41.6% (20.0-74.1)。严重BOS占44%。由于有既往肺外cGVHD病史,大多数患者 (81%)有前期治疗史,包括钙调神经磷酸酶抑制剂、全身性糖皮质激素、体外光分离置换、酪氨酸激酶抑制剂和RUX。 BOS诊断后给予以下治疗:FAM样方案(氟替卡松、阿奇霉素和孟鲁司特)(94%)、CNI(50%)、mTOR 抑制剂(35%)、全身性糖皮质激素(52%)、体外光分离置换(25%) 或低剂量 rIL-2 (19%) 作为一线和后续治疗。17例患者 (33%) 接受TKI治疗。共20例BOS患者接受了RUX(中位剂量为15 mg/d)治疗,其余32例患者被纳入对照组。
根据NIH评估量表(2014),通过FEV1动态变化评估疗效:部分缓解(PR,FEV1 增加≥10%)、稳定(<10% 变化)、进展(减少≥10%)(n=45 ),根据NIH基于症状的肺评分和mMRC量表评估呼吸困难程度,PR定义为呼吸困难减少至少1分 (n=52)。从BOS诊断起,应用Kaplan-Meier评估患者的OS。
结果:
中位随访27个月 (5~102) 时,5 (26%) 例患者达到PR,分别有7例患者(37%)稳定和进展。在对照组中,PR、稳定和进展分别有 3 (12%, P=0.253)例、17 (65%)例和6 (23%) 例(图 1)。呼吸困难改善的PR率无统计学差异:根据 NIH-CC为15%vs 19%,根据 mMRC量表为30%vs31%(P = 1.0)。RUX组中全身性糖皮质激素的使用率较低(35% vs 63%,P = 0.049)。截至2021年7月1日,有32例(62%)患者存活,20例患者死于cGvHD和感染并发症(n = 16, 80%)或疾病复发(n = 4, 20%)。5年OS率为54.4%(95% CI,36.7~69.1),RUX组和对照组之间无统计学显著差异:59.1%(95% CI,25.6~81.6)vs 50.2(95% CI,29.5~67.7) (P =0.387)。
结论:
与回顾性对照组相比,RUX对HSCT后BOS患者的FEV1和临床缓解率方面没有带来显著获益。因此,尽管RUX在一般性cGvHD中取得了良好的疗效,但BOS仍然是一个尚未解决的难题,亟需新的治疗方式。

图:末次随访时治疗反应情况(n = 45)
研究五:EBMT关于糖皮质激素难治性GvHD管理的调查
标题:Management of Steroid-Refractory Graft-Versus-Host Disease – a Survey By the Transplant Complications Working Party of the EBMT
摘要号:2884(Poster)
发布日期:2021年12月12日
目的:
由于指导糖皮质激素难治性GvHD (SR-GvHD) 患者管理的证据有限,临床实践方面也存在着较大的差异。为评估当前临床实践及新药对SR-GvHD 的影响,EBMT的移植并发症工作组 (TCWP)在EBMT中心进行了一项涵盖了aGvHD和cGvHD的一线和二线治疗的调查问卷。
方法:
该调查于2020年12月至2021年3月在EBMT中心进行。调查问卷由研究作者开发并用于数据收集。调查问卷包括40个问题,重点是一线治疗的一般治疗、SR-GvHD的首选二线治疗以及aGvHD和cGvHD的辅助护理。
结果:
来自 33个国家的145个中心同意参与并回复了问卷。
aGvHD的一线治疗方案相对一致:68%的中心在较低级别aGvHD(2a 级)中启用较低剂量糖皮质激素(<2mg/kg) 治疗,88%的中心在较高级别aGvHD(≥2b 级)中启用较高剂量糖皮质激素 (2mg/kg) 治疗。但糖皮质激素疗效评估的差异性较大:分别有33%、30%和15%的中心在第3天、第5天和第7天进行疗效评估,而其他大多数中心则根据aGvHD的严重程度进行评估。在SR-aGvHD 的管理中,50%的中心考虑将患者纳入临床试验。尽管有85%的中心报告有SR-aGvHD管理的标准操作程序 (SOP),但只有45% (n=66)的中心已建立一种或两种二线治疗方案:最常见的是RUX (n=46) 和/或体外光分离置换(n=29)。而其他所有中心则报告了不同的治疗方案,并列出了多种药物(范围,3~10)作为二线治疗选择。总的来说,常用于SR-aGVHD 药物有RUX(68%)、体外光分离置换(59%)、霉酚酸酯 (27%)、钙调神经磷酸酶抑制剂 (25% )、大剂量糖皮质激素 (>2mg/kg)(15%)、间充质干细胞 (MSC) (14%),依那西普(13%)、英夫利昔单抗占(11%)和抗胸腺细胞球蛋白 (ATG) (10%)(图1A)。
cGvHD的一线治疗也比较接近:58% 的中心仅用局部治疗(无法局部治疗的受累器官除外)。在中度/重度cGvHD 中,71%的中心以 0.5~1mg/kg 糖皮质激素开始治疗,45% 的中心加用钙调神经磷酸酶抑制剂治疗,而其他中心则使用更大剂量的糖皮质激素 +/- 其他药物治疗。41%的中心在4周内进行疗效评估,41%的中心在5~8周进行疗效评估,而少数中心则在8周以后或根据受累器官/严重程度进行疗效评估。在SR-cGvHD 的管理中,56% 的中心考虑纳入临床试验,而只有65%的中心有管理这类患者的SOP。有35%的中心拥有成熟的多学科cGvHD团队。SR-cGvHD的临床实践的差异很大,大多数中心应用2种以上药物(范围,3~13)作为二线药物(图 1B),68% 的中心使用RUX和体外光分离置换,40%使用钙调神经磷酸酶抑制剂,37%使用霉酚酸酯,27%使用利妥昔单抗,25%使用伊马替尼,23%使用 mTOR 抑制剂,19%使用伊布替尼和甲氨蝶呤 (MTX),17%使用糖皮质激素脉冲,12%中心使用间充质干细胞,10% 的中心使用PUVA治疗。
结论:
大多数中心基于糖皮质激素的aGvHD 和cGvHD的一线管理相对一致。但一线治疗失败后,对SR-GvHD的定义仍存在很大差异,对SR-GvHD仍用“反复试验”的方式治疗,各中心二线治疗方案差异显著。与最近的前瞻性临床试验结果一致,RUX与体外光分离置换为SR-aGvHD和SR-cGvHD的最常用治疗方式。 而伊布替尼尚不是GvHD的标准治疗。未来可通过前瞻性试验直接比较应用比较广泛的二线药物及以循证医学为基础的个性化治疗来寻找SR-GvHD 的标准化治疗。

本文内容仅供医疗卫生等专业人士参考。
部分产品或适应症尚未在中国获得批准,相关内容仅供学术交流。
[1].https://ash.confex.com/ash/2021/webprogram/Paper144576.html
[2].https://ash.confex.com/ash/2021/webprogram/Paper148859.html
[3].https://ash.confex.com/ash/2021/webprogram/Paper151683.html
[4].https://ash.confex.com/ash/2021/webprogram/Paper153548.html
[5].https://ash.confex.com/ash/2021/webprogram/Paper152305.html
排版编辑:Raffle











 苏公网安备32059002004080号
苏公网安备32059002004080号


