PAP方案助力K药成为起始PD-1的优选
2020年6月17日,PD-1免疫检查点抑制剂帕博利珠单抗(国内商品名“可瑞达”,俗称“K药”)在国内获批用于PD-L1表达阳性[综合阳性评分(CPS)≥10]的、既往一线全身治疗失败的、局部晚期或转移性食管鳞状细胞癌(ESCC)患者的治疗。自2018年7月26日帕博利珠单抗首次在国内获批治疗恶性黑色素瘤适应证后,该药在国内获批适应证数量已达到5个(纳武利尤单抗获批数量为3个),是目前获批适应证最多的PD-1单抗。 7月18日(本周六),主题为“食现K能,钥启新生”可瑞达治疗食管癌适应证上市会将在全国17个城市召开。上市会将云集来自全国食管癌跨学科治疗的顶级专家,共同见证当前站在全球免疫治疗前沿的PD-1单抗在国内食管癌治疗领域扬帆起航改变食管癌治疗格局,乘风破浪为中国患者带来长期生存。
7月18日(本周六),主题为“食现K能,钥启新生”可瑞达治疗食管癌适应证上市会将在全国17个城市召开。上市会将云集来自全国食管癌跨学科治疗的顶级专家,共同见证当前站在全球免疫治疗前沿的PD-1单抗在国内食管癌治疗领域扬帆起航改变食管癌治疗格局,乘风破浪为中国患者带来长期生存。
帕博利珠单抗是目前唯一被循证医学证据证明一线和/或二线治疗可以显著提升包括晚期肺癌和恶性黑色素瘤在内的实体瘤患者5年生存率的PD-1单抗。
帕博利珠单抗治疗亚洲和中国食管癌OS获益更明显
帕博利珠单抗获批食管癌适应证是基于一项包括中国患者在内的全球多中心、开放标签、随机对照的Ⅲ期临床研究KEYNOTE-181的结果,旨在评估帕博利珠单抗单药对比研究者选择的化疗药物二线治疗晚期/转移性食管癌的疗效和安全性。
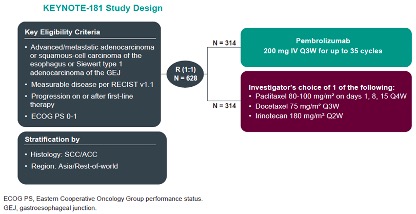
该研究结果首次于2019年美国临床肿瘤学会消化道肿瘤(ASCO-GI)年会上公布结果, 并由北京大学肿瘤医院副院长、消化内科主任沈琳教授分别在2019年中国临床肿瘤学(CSCO)年会和2019欧洲肿瘤内科学会(ESMO)年会上公布亚洲亚组人群和中国人群的研究结果。
KEYNOTE-181研究纳入了628名晚期或转移性腺癌或鳞状细胞癌食管癌,或胃食管连接部Siewert Ⅰ型腺癌患者,其中包括401例(64%)食管鳞癌(ESCC)、222例(35.3%)CPS≥10的食管癌; 研究入组了包括123例中国患者在内的243例(39%)亚洲患者(看下图) [1]。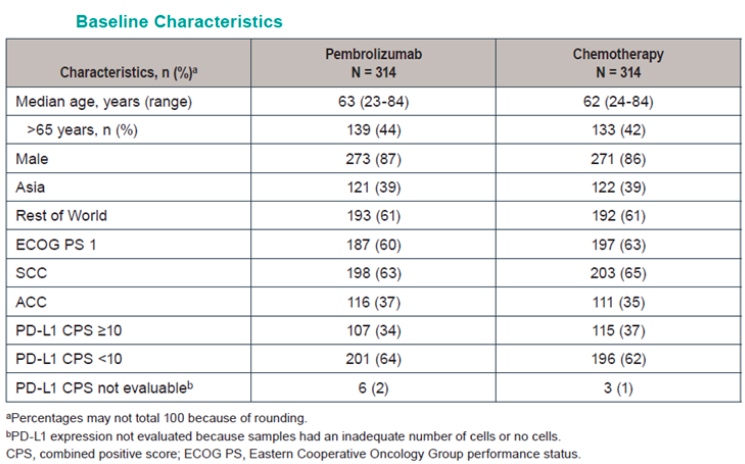 研究结果显示,无论是在ITT人群,还是ESCC人群,相比整体人群,帕博利珠单抗治疗为中国和亚洲食管癌患者带来的总生存(OS)获益趋势更明显[2,3]。
研究结果显示,无论是在ITT人群,还是ESCC人群,相比整体人群,帕博利珠单抗治疗为中国和亚洲食管癌患者带来的总生存(OS)获益趋势更明显[2,3]。
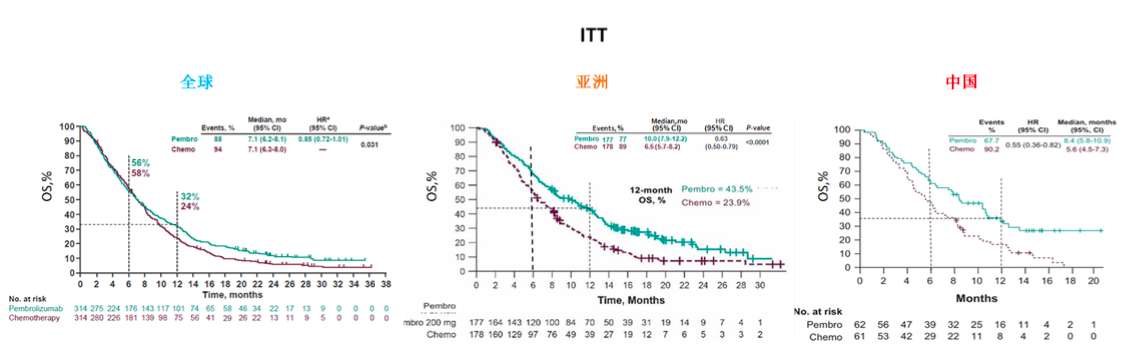
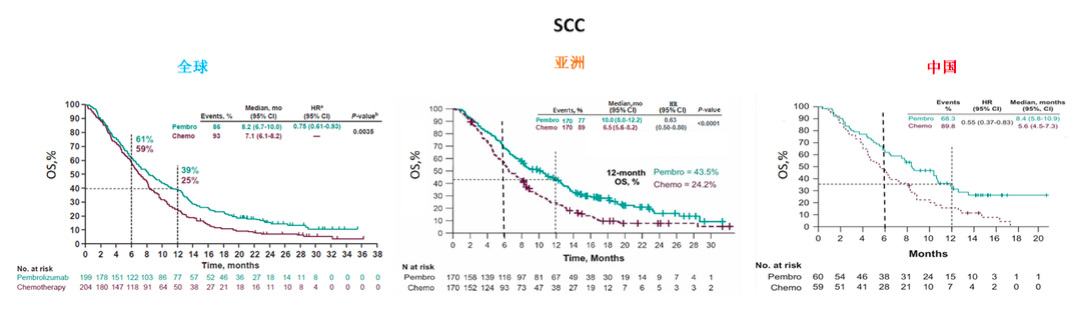
KEYNOTE-181研究中全球,以及亚洲和中国亚组ITT和ESCC人群的OS [1-3]
在中国95%的食管癌属于ESCC。帕博利珠单抗治疗中国和亚洲ESCC人群,可分别降低45%(HR=0.55,95%CI 0.37~0.83)和37% (HR=0.63,95% CI 0.50~0.80, P<0.0001)的死亡风险,优于治疗全球ESCC人群所带来的25%(HR=0.75,95% CI 0.69~0.93,P=0.0035)的死亡风险降低幅度。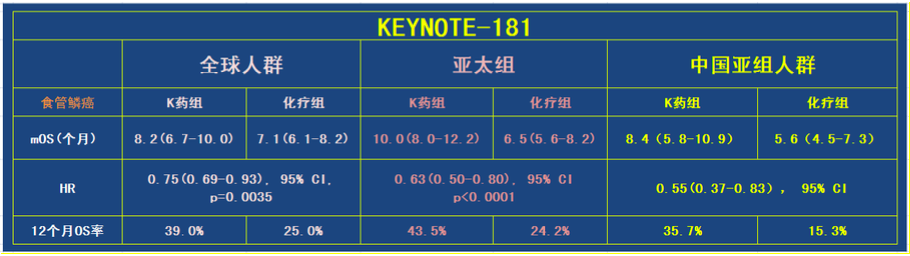
KEYNOTE-181的整体、亚洲和中国ESCC人群的OS数据对比[1-3]
帕博利珠单抗单药治疗PD-L1表达阳性(CPS ≥10)的食管癌,无论是在整体人群,还是亚洲或中国人群中,能带来显著的OS改善和死亡风险的降低,但在亚洲和中国人群中,随着时间的延长,两条OS曲线分离得更明显。

KEYNOTE-181研究中全球,以及亚洲和中国亚组PD-L1 CPS ≥10人群的OS [1-3]
帕博利珠单抗治疗PD-L1表达阳性(CPS≥10)的中国食管癌患者,中位OS达到12.0 (6.6 ~ NR)个月,比全球人群的9.3个月多了2.7个月;死亡风险降低幅度达66%,是全球人群(33%)的2倍;帕博利珠单抗组12个月的生存率达到了53%,意味着有超过一半的患者在12个月时仍然生存,这也优于全球人群42%的12个月生存率 [1-2]。
“生命之钥”——让更多食管癌患者活得久
今年7月1日,由中国初级卫生保健基金会发起的“生命之钥-肿瘤免疫治疗患者援助项目”开始正式接受符合援助条件的局部晚期或转移性食管鳞癌患者的援助申请。符合条件患者在使用2个疗程(共计6周)的帕博利珠单抗注射液后,经基金会审核通过后,可获得后续2个疗程(共计6周)的援助。这样12周疗程费用仅7.2万元人民币。
“2+2”的援助模式降低接受帕博利珠单抗治疗12周的费用至7.2万元,而更重要的是,这12周的疗程可以帮助医生预测哪些患者更有可能通过继续PD-1治疗获得长期生存。
针对帕博利珠单抗治疗恶性黑色素瘤、非小细胞肺癌等实体瘤的长期随访研究数据显示,帕博利珠单抗治疗可以让一部分晚期肿瘤患者获得5年或5年以上的生存,而在这部分“幸运者”中,有很大一部分显示了持久的肿瘤客观缓解。比如,2019年ASCO公布的帕博利珠单抗单药治疗晚期非小细胞肺癌的KEYNOTE-001的5年随访研究结果[4]。该随访结果显示:
客观缓解率(ORR)为26.4%(145例),多数应答在治疗开始后不久出现,72%在3个月内即出现应答;
在145例出现ORR的患者中,有78例(54%)在中位随访60.6(51.7~77.9)个月时仍然显示肿瘤客观缓解,占据所有幸存人群的78%。
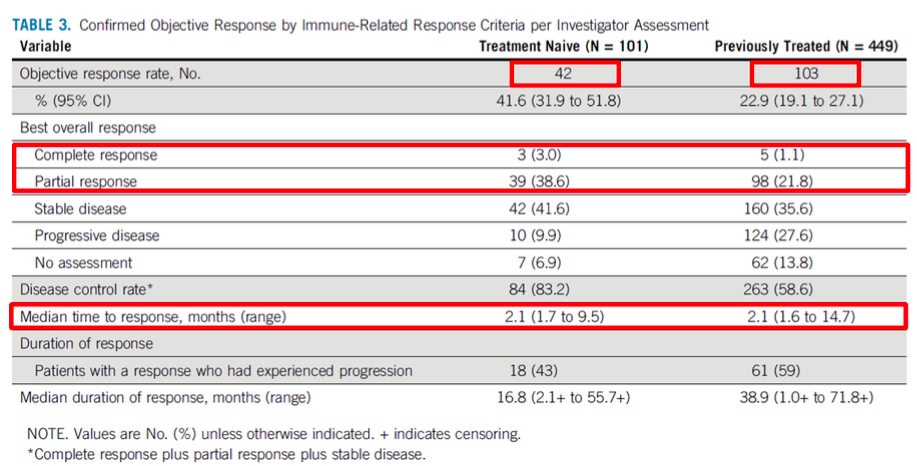
KEYNOTE-001研究5年随访的ORR分析结果
在KEYNOTE-181研究的中国人群结果分析中,帕博利珠单抗治疗PD-L1表达阳性(CPS≥10)食管癌、食管鳞癌和ITT人群的ORR分别为24.0%、16.7%和16.1%[2]。

KEYNOTE-181中国亚组人群的ORR分析结果[2]
在那些获得ORR的患者中,帕博利珠单抗中位起效时间在8~9周。所以,多数对于帕博利珠单抗会产生应答(完全缓解或部分缓解)的患者应该在12周的帕博利珠单抗治疗后"浮出水面" 。
这些患者若继续治疗则更有可能获得长期生存。而那些没有出现应答的患者可在权衡疗效和经济支出后,或选择继续使用帕博利珠单抗,或选择停止免疫治疗。
所有的PD-1/PD-L1免疫检查点抑制剂,无论是国产的还是进口的,目前显示只对一小部分患者人群有效,因为大量循证医学证据显示,PD-1/PD-L1单抗单药治疗多数实体瘤的ORR在10%~25%之间。
帕博利珠单抗的PAP项目设计显然不但可以降低患者的经济付出,而且可以用尽可能小的代价帮助医生找出最有可能从免疫治疗中获得持久疗效和长期生存的患者。而且针对使用帕博利珠单抗患者的这个判断是具有循证医学证据作为依据的,是一个目前最靠谱的结论。

[1] Shah M A, Adenis A, Enzinger P, et al. Pembrolizumab versus Chemotherapy as second-line therapy for Advanced Esophageal Cancer: Phase 3 KEYNOTE-181 Study[R]. 2019 ASCO, abstract 4010.
[2] Chen J, Luo S, Qin S, et al. Pembrolizumab versus Chemotherapy in Patients with Advanced/Metastatic Adenocarcinoma or Squamous Cell Carcinoma of the Esophagus as Second-line Therapy: Analysis of the Chinese Sub-group in KEYNOTE-181[R]. 2019 ESMO, Abstract 760P.
[3] 沈琳等. 帕博利珠单抗对比化疗二线治疗晚期/转移性食管腺癌或鳞状细胞癌:KEYNOTE-181 亚洲亚组分析, 2019 CSCO.
[4] Garon E B, Hellmann M D, Rizvi N A, et al. Five-Year Overall Survival for Patients With Advanced Non-Small-Cell Llung Cancer Treated With Pembrolizumab: Results From the Phase I KEYNOTE-001 Study[J]. J Clin Oncol . 2019,37(28):2518-2527.
排版编辑:DD















 苏公网安备32059002004080号
苏公网安备32059002004080号


