
乳腺癌患者发生骨转移的风险较高,临床上主要表现为骨痛、病理性骨折、碱性磷酸酶升高、脊髓压迫或脊神经根压迫、高钙血症等,乳腺癌骨转移综合治疗的主要目标是恢复功能、控制肿瘤进展、预防及治疗骨相关事件、缓解疼痛和改善生活质量, 乳腺癌骨转移治疗应以全身治疗为主。国内外指南一致推荐:对于激素受体阳性晚期乳腺癌患者(不伴有内脏危象),优选靶向治疗联合内分泌治疗。本文分享一例激素受体阳性HER2阴性转移性乳腺癌患者一线接受CDK4/6抑制剂联合内分泌治疗的成功案例,截止2020年1月PET/CT复查,PFS达30个月(2020年5月电话随访PFS已达34个月),耐受性好、生活质量佳。
病例介绍

福建省肿瘤医院
主治医师
硕士研究生
现主要从事乳腺内科治疗
以第一作者在国内发表论文数篇

福建省肿瘤医院乳腺内科副主任医师
CSCO乳腺癌专家委员会委员
CSCO药物安全管理委员会委员
中国抗癌协会乳腺癌专业委员会青年委员
中国医药教育协会乳腺疾病专业委员会委员
中国医师协会乳腺疾病培训专家委员会委员
福建省医师协会肿瘤内科医师分会常委
福建省抗癌协会肿瘤内科治疗专业委员会委员
基本情况
患者女性,1959年出生,2008年6月(49岁)因“发现左乳肿物3年”就诊当地医院。既往体健。家族史无特殊。月经史:48岁绝经(2007年)。
2008年初诊时检查结果
•体格检查:左乳内上象限触及一肿物,约10.0 cm × 7.0 cm大小,质地硬,活动度差,无红肿破溃,左腋窝触及肿大淋巴结,约2 cm × 3 cm,活动度差,质硬,余浅表淋巴结查体阴性。
•乳腺彩超示:1)左乳实性占位(倾向乳腺癌);2)左腋窝实性占位(转移待排)。
•左乳穿刺病理:左乳浸润性癌。
•免疫组化结果(IHC):ER(+),PR(+),HER2(+),ki67 25%。
•诊断:左乳腺癌cT3N2M0IIIB期
当地医院治疗过程
1. 新辅助治疗阶段:
•化疗方案:2008年6月14日至2008年8月17日予AT方案术前新辅助化疗4周期,计用:脂质体紫杉醇(力朴素) 1220 mg,表阿霉素960 mg。
•化疗后查体:左乳肿物大小约4 cm × 4 cm。疗效PR。
2.手术治疗:
•手术方案:2008年09年02日在全麻下行“左乳癌改良根治术(保留胸大小肌)”。
•术后病理示:(左乳内上象限)浸润性小叶癌(肿物大小4 cm × 3 cm),侵犯周围脂肪组织,轻度化疗反应。标本乳头未见癌。同侧腋窝LN3/4,“2组”LN 2/2,“3组”LN 1/1,“腋尖”LN 0/1见转移癌。“胸肌间”未见LN。
•免疫组化结果(IHC):ER(+++),PR少量(+),CerbB-2(-) ki67 28%。
3.术后辅助治疗阶段:
•辅助化疗:术后于2008年10月10日至2009年1月9日予以TC方案化疗5周期,计用紫杉醇1770 mg,环磷酰胺5.52。
•辅助放疗:2009年2月17日至2009年3月23日期间予补充放疗,辅助放疗:2009年2月17日至2009年3月23日期间予补充放疗,以左胸壁为CTV-T(4500cGy/25F)、左锁骨区淋巴引流区为CTV-N(5000cGy/25F)。
•术后内分泌治疗:2009年2月起至2017年7月,给予阿那曲唑(1mg/日)。
复发及我院的治疗、随访过程:
1. 复发:DFS为109个月:
•2017年7月18日因“腰背部及右髋部疼痛一月”,我院查PET-CT:1.考虑全身多发骨转移;2.右肺中叶钙化小结节,考虑陈旧性病变;右肺下叶背段磨玻璃密度小结节、中叶低代谢小结节。
•骨穿活检病理:(L1骨穿活检)转移性腺癌,结合病史及免疫组化,符合乳腺来源。IHC:ER 95%+, PR 80%+, HER2 0,Ki-67 5%+, GATA3 +。
2.解救治疗方案:
•全身系统性治疗:2017年8月16日开始接受“氟维司群(500mg)联合 CDK4/6抑制剂(哌柏西利,125 mg/日)”一线解救治疗,治疗期间有I度白细胞低下,间歇期白细胞可自行恢复,无肝功能等异常,顺利完成疗程,哌柏西利无减量。每月一次唑来磷酸治疗。
•局部止痛放疗:患者于2017年8月14日至2017年8月25日期间接受调强放疗,以T12、L1、右侧髂骨转移灶为GTV,GTV外扩5 mm为PTV,根据TPS计划结果,计划95%PTV照射3000 cGy/10F。
3.随访复查:
1)首次复查(治疗后3个月):2017年11月PET-CT复查评估,全身多发骨转移明显好转,成骨修复明显,SUV值下降(SUVmax 12.5 → SUVmax 4.1),肿瘤活性部分受抑制。疗效PR。
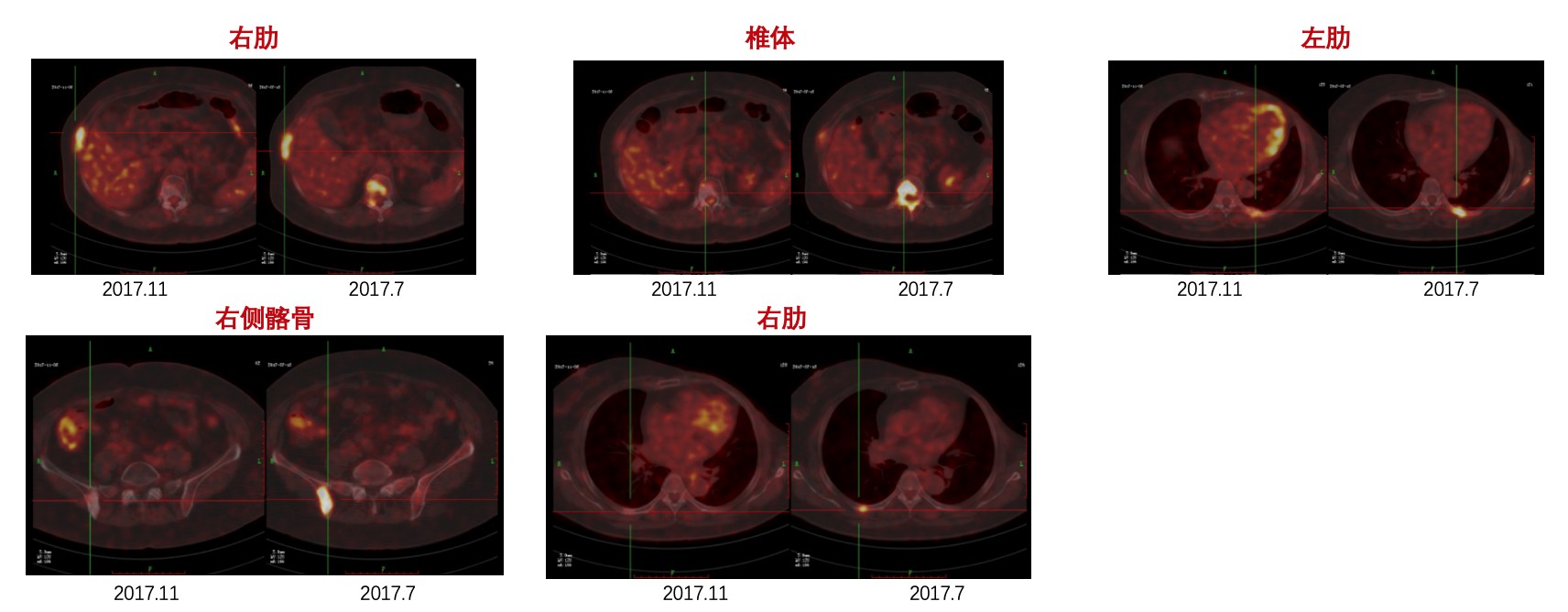
图1: 2017年11月PET-CT首次复查评估,综合疗效评价为PR
2)定期复查随访:(截止2020年1月PFS达30个月)
•2018年9月查PET-CT,左第7后肋、右第9侧肋病灶相应部位仍见片状代谢稍高,其余病灶成骨性修复较前明显,呈低代谢,SUV值下降(SUVmax 4.1 → SUVmax 3.2)考虑肿瘤活性受抑制。疗效PR。
•2019年5月复查PET-CT,左第7后肋、右第9侧肋病灶仍见片状代谢稍高,其余病灶呈低代谢,考虑肿瘤活性受抑制。
•2020年1月复查PET-CT,左第7后肋、右第9侧肋病灶代谢均较前减低,特别前者摄取增高现已消退(原SUVmax 1.9),其余病灶成骨性改变与前相仿,呈低代谢,考虑肿瘤活性受抑制。
•2020年5月电话随访:目前无明显骨痛等症状,生活自如,正常上班。截止2020年5月,PFS为34个月。
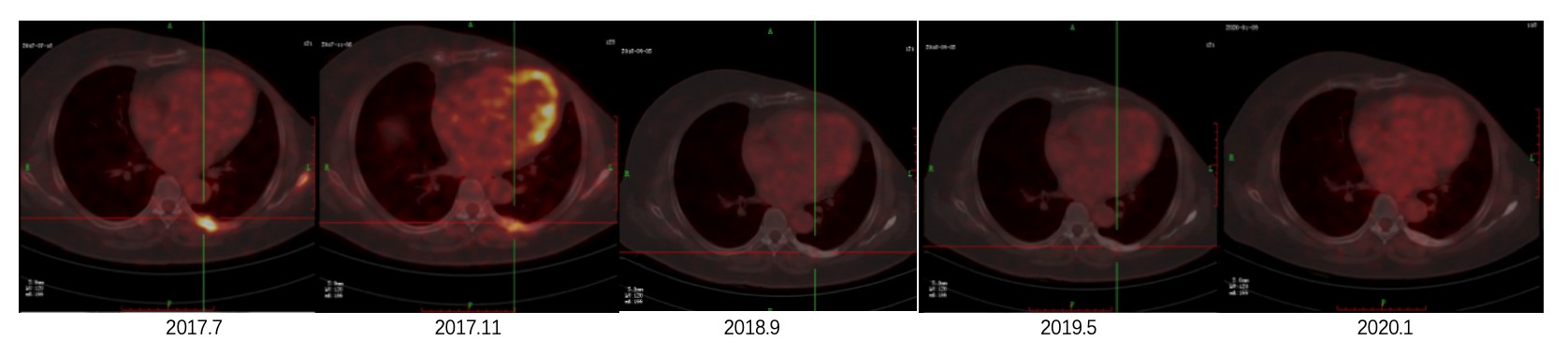
图2: 2017年7月至2020年1月的随访复查PET-CT结果

图3: 2017年7月至2020年1月的随访复查PET-CT结果
病例总结
•患者女性,初诊为局部晚期乳腺癌(Luminal B型),2008年09年02日新辅助化疗后行左乳房根治性切除术,术后接受了辅助化疗、放疗和内分泌治疗。 2017年7月出现全身多发骨转移,DFS达到109个月。作为内分泌治疗敏感的患者,一线解救方案为CDK4/6抑制剂(哌柏西利125mg)联合氟维司群(500mg)治疗,治疗期间有I度白细胞低下,间歇期白细胞可自行恢复,无肝功能等异常,顺利完成疗程,哌柏西利无减量,每月一次唑来磷酸治疗,初期曾配合止痛性放疗。截止2020年1月PET/CT复查,左第7后肋、右第9侧肋病灶代谢均较前减低,特别左第7后肋摄取增高现已消退,SUV值下降(原SUVmax 1.9),PFS已经达到30个月(2020年5月电话随访PFS已达34个月)。
专家点评

民进福建省委副主委、福建人大常委会委员
福建省肿瘤医院乳腺内科主任、硕导、省保健委专家
中国医师协会乳腺疾病专家培训委员会副主任委员
中国抗癌协会乳腺癌专业委员会常务委员
中国临床肿瘤学会(CSCO)乳腺癌专业委员会常务委员
国家卫生计生委合理用药专家委员会乳腺肿瘤组委员兼秘书
国家肿瘤质控中心乳腺癌专家委员会委员
中华医学会乳腺学组委员
中华预防医学会乳腺学组委员
福建省医师协会肿瘤内科医师分会主任委员
福建省抗癌协会乳腺癌专业委员会副主任委员
福建省抗癌协会内科治疗专业委员会副主任委员
福建省红十字会大病救助基金监委会副主任
《医学参考(乳腺频道)》常务编委
《JCO中文版乳腺肿瘤专刊》欧洲肿瘤年鉴中文版(乳腺癌)》编委
《中华内分泌外科杂志》编委
《中华肿瘤防治杂志》编委
《临床肿瘤学杂志》编委
《肿瘤学杂志》编委
《中国肿瘤》编委
1、患者首诊时为局部晚期乳腺癌(Luminal B型),有新辅助化疗适应症,经4周期AT方案化疗后疗效PR并接受左乳癌根治术,病理未达pCR,术后继续接受辅助化疗、放疗和内分泌治疗。
指南要求:乳腺癌新辅助化疗有效者应按计划完成6-8周期的新辅助化疗之后再予手术,乳腺癌新辅助治疗的规范需进一步推广落实。
2、患者在首诊9年后复发,病理再次证实是必要的。HR阳性HER2阴性型乳腺癌,仅有骨转移,无内脏危象,应该优先选择内分泌治疗。正如ESO/ESMO晚期乳腺癌共识(ABC4)中指出:对骨转移患者进行治疗选择的时候,应考虑HR和HER2状态、既往治疗方案和毒性、无病生存期(DFI)、肿瘤负荷(包括转移部位和转移数量)等;《中国晚期乳腺癌治疗专家共识(2018版)》[1] 推荐:对于HR阳性HER2阴性的晚期乳腺癌,若病变仅局限乳腺、骨和软组织以及无症状、肿瘤负荷不大的内脏转移患者,可以优先选择内分泌治疗。
3、自2016年以来越来越多的国内外指南与共识将HR+/HER2-晚期乳腺癌的内分泌治疗与靶向治疗联合。主要证据来自PALOMA-2研究[2] ,该研究纳入了666例绝经后、既往未接受针对复发或转移性肿瘤进行系统性治疗的晚期乳腺癌患者,按2:1随机分配至哌柏西利联合来曲唑组、或者安慰剂联合来曲唑组。结果显示,CDK4/6抑制剂哌柏西利联合来曲唑组患者的mPFS达到27.6个月(95% CI 22.4 ~ 30.3),对照组安慰剂联合来曲唑治疗的患者,其mPFS仅为14.5个月(95% CI, 12.3 ~ 17.1)(风险比为0.563; 95% CI, 0.461 ~ 0.687; P < 0.0001)。该研究提示,哌柏西利常见不良反应包括中性粒细胞减少、白细胞减少等血液学毒性,较少的非血液学毒性,例如疲劳、恶心等。我们注意到,PALOMA-2研究中仅骨转移的患者亚组分析显示,两组mPFS分别为36.2个月和11.2个月(风险比为0.41; 95% CI, 0.26 ~ 0.63; P < 0.0001)。PALOMA-2研究是第一个把HR+晚期乳腺癌患者的中位PFS延长到超过2年的Ⅲ期临床研究,是治疗HR+/HER2-晚期乳腺癌的重大突破。
4、目前指南与共识均推荐CDK4/6抑制剂联合内分泌治疗方案作为优选,而CDK4/6抑制剂哌柏西利联合氟维司群用于一线治疗的观念、改变体现在2018年V3和V4版的美国NCCN乳腺癌诊疗指南。2018年NCCN V3版指南明确提出CDK4/6抑制剂联合氟维司群用于HR+晚期乳腺癌一线治疗,证据源于MONALEESA-3研究,而2018年V4版则更新了相关证据,增加了PALOMA-3研究。PALOMA-3研究[3] 是前瞻性全球随机安慰剂对照的Ⅲ期对照研究,对比哌柏西利联合氟维司群和安慰剂联合氟维司群治疗既往接受过内分泌治疗进展后的HR+/HER2-晚期乳腺癌患者。研究共计入组521例患者,其中既往对内分泌治疗敏感的患者人群占79%。PALOMA-3研究结果显示,两组mPFS分别为11.2个月和4.6个月(风险比为 0.497;95%CI 0.398 ~ 0.62;P < 0.000001)。本例患者为对内分泌治疗敏感且仅骨转移的患者,而PALOMA-3研究中对既往内分泌治疗敏感的患者进行亚组分析,接受哌柏西利联合氟维司群和安慰剂联合氟维司群的mOS分别为39.7个月和29.7个月,(风险比为 0.72;95%CI 0.55 ~ 0.94;P = 0.0081),绝对获益10个月。研究中非内脏转移患者中多数为仅骨转移患者,对这类患者进行亚组分析,两组mPFS分别为11.2个月和5.6个月(风险比为 0.43;95%CI 0.28 ~ 0.67)。
5、乳腺癌骨转移临床上主要表现为骨痛、病理性骨折、碱性磷酸酶升高、脊髓压迫或脊神经根压迫、高钙血症等,有数据显示2/3的患者最终会发生骨骼相关事件。乳腺癌骨转移治疗的主要目标是恢复功能、控制肿瘤进展、预防及治疗骨相关事件、缓解疼痛和改善生活质量, 因此,乳腺癌骨转移治疗应以全身治疗为主。本例患者确诊为乳腺癌骨转移伴明显疼痛,在实施哌柏西利联合氟维司群一线解救同时予二磷酸盐和局部止痛性放疗,快速改善生活质量。符合国内外乳腺癌指南的治疗推荐。该患者在CDK4/6抑制剂哌柏西利联合氟维司群治疗三个月后疗效达PR,治疗过程中,毒性可耐受,剂量无调整,后续维持治疗中仍然使用125mg剂量至今。患者目前工作生活如常,对治疗非常满意,截止2020年1月PET/CT复查,PFS已经达到30个月(2020年5月电话随访PFS已达34个月)。本例患者的治疗效果再次证实:HR阳性HER2阴性型无内脏危象的转移性乳腺癌患者,一线选择CDK4/6抑制剂哌柏西利联合氟维司群治疗有效性高、安全性好。
[1]中国抗癌协会乳腺癌专业委员会.中国晚期乳腺癌治疗专家共识(2018年版).中华肿瘤杂志.2018,40(9):703-713.
[2]Rugo H S,Finn R S,Diéras V et al. Palbociclib plus letrozole as first-line therapy in estrogen receptor-positive/human epidermal growth factor receptor 2-negative advanced breast cancer with extended follow-up.[J] .Breast Cancer Res. Treat., 2019, 174: 719-729.
[3]Cristofanilli Massimo,Turner Nicholas C,Bondarenko Igor et al. Fulvestrant plus palbociclib versus fulvestrant plus placebo for treatment of hormone-receptor-positive, HER2-negative metastatic breast cancer that progressed on previous endocrine therapy (PALOMA-3): final analysis of the multicentre, double-blind, phase 3 randomised controlled trial.[J] .Lancet Oncol., 2016, 17: 425-439.
排版编辑:肿瘤资讯-细胞田















 苏公网安备32059002004080号
苏公网安备32059002004080号


