传统化疗作为晚期恶性肿瘤的治疗基石,给与细胞毒性药物的最大耐受剂量(MTD)直接杀伤肿瘤细胞,治疗过程中可能伤及正常人体细胞,因此某些化疗药物的不良反应相对较重,患者耐受性较差。不同于传统化疗,节拍化疗通过相对低剂量、高频度、持续应用的给药方式,在发挥抑制肿瘤作用的同时,其不良事件发生率更低、程度更轻。本文就节拍化疗的作用机制及在晚期乳腺癌和晚期非小细胞肺癌(NSCLC)领域的研究进展作一回顾。

中国科学院大学附属肿瘤医院(浙江省肿瘤医院)院长助理、乳腺肿瘤内科主任
国家卫健委合理用药专家组成员兼乳腺癌实践基地主任
国家肿瘤质控中心乳腺癌专家委员
浙江省肿瘤诊治质控中心副主任
CSCO乳腺癌专家委员会副主任委员
中国抗癌协会乳腺癌专业委员会常委
浙江省抗癌协会肿瘤内科专业委员会主任委员、乳腺癌专业委员会候任主任委员
浙江省省免疫学会副理事长
浙江省转化医学学会副理事长兼精准医学分会会长等
1.节拍化疗
化疗是多种晚期恶性肿瘤的治疗基石,常规化疗即所谓最大耐受剂量(maximum tolerated dose,MTD)化疗,是利用细胞毒性药物直接杀伤肿瘤细胞。MTD化疗对所有处于增殖期的细胞均有杀伤作用,不良反应相对较重,患者耐受性相对较差。节拍化疗在这一背景下应运而生。2000年,Browder等在动物实验中首次发现,通过低剂量、高频度方式给药,化疗药物可以促进肿瘤组织中的血管内皮细胞凋亡。在对常规化疗产生耐药的情况下,节拍化疗仍然可以达到减瘤效果[1]。Klemen等学者发现,持续低剂量长春花碱可以通过抑制肿瘤血管生成达到缩小肿瘤病灶的目的[2]。在这两项开创性的研究基础上,Hanahan提出了节拍化疗(metronomic chemotherapy)的概念[3]。通常情况下,节拍化疗采用的化疗药物剂量相对较小(通常为常规剂量的1/10-1/3),并且通过较高频率的给药方式来抑制肿瘤血管生成,节拍化疗也因此被称为抗肿瘤血管生成化疗。
2. 节拍化疗作用机制
通过低剂量、高频度、持续应用的给药方式,节拍化疗可以使药物能够长时间维持在相对较低、有效的血药浓度,以达到延长疾病控制时间,同时大大降低毒副作用的目的。节拍化疗主要通过以下机制增强抗肿瘤效应:抑制肿瘤血管生成、免疫激活、直接抑制肿瘤细胞。节拍化疗一方面可以在有效延长治疗周期的同时降低毒副作用,另一方面,不需要或很少需要使用生长因子来加速恢复患者的骨髓抑制,治疗指数较高[4-7]。
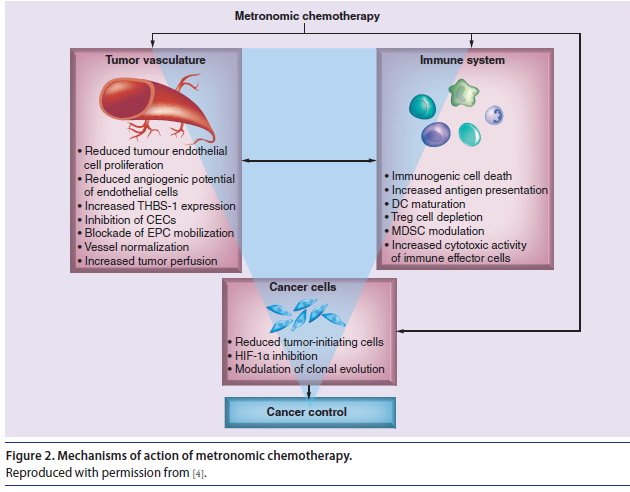
(图片来源于参考文献)
3. 节拍化疗在晚期乳腺癌中的应用
3.1 单药节拍化疗
卡培他滨单药常用于节拍化疗,在一项入组60例晚期乳腺癌患者的Ⅱ期临床研究中,给药方式为1500mg QD,中位OS达17个月,临床获益率达62%,极少发生3-4级不良事件,并且血液学毒性发生率仅为5%[8]。此外,一项针对不适合更强方案治疗的晚期乳腺癌研究中对卡培他滨间歇性或连续给药模式进行了探索,研究共入组323例患者,随机分配接受以下治疗模式:卡培他滨间断性给药1000mg/m2 BID, D1-14,Q3W;卡培他滨节拍化疗连续给药650mg/m2 BID;传统CMF化疗[7]。三组患者在无进展生存时间和ORR方面结果相似,但卡培他滨治疗组患者中位OS优于CMF化疗组(22 个月vs.18个月,P = 0.02)。上述研究表明,对于不能耐受更强化疗方案的晚期乳腺癌患者,间歇性或连续性卡培他滨一线治疗均可给患者带来生存获益。
长春瑞滨节拍化疗较早用于晚期乳腺癌的临床研究发表于2010年[9],用药剂量为周剂量70mg/m2,每周一、 三、五进行,研究共入组34例患者,ORR为 38%,中位PFS和OS分别为7.7和15.9个月。3级血液学不良反应为中性粒细胞减少(9%)和贫血(9%)。上述研究证实了长春瑞滨节拍化疗是耐受性良好且可行的化疗方案。另一项后续开展的针对老年晚期乳腺癌患者的Ⅱ期临床试验,采用长春瑞滨单药30mg隔天给药,DCR可达87.4%,并且没有3级或4级不良反应发生,再次证实了长春瑞滨单药节拍化疗的有效性及安全性[10]。
3.2 多药联合
环磷酰胺和甲氨蝶呤联合的CM方案是晚期乳腺癌领域中最早被研究和应用的节拍化疗方案。卡培他滨在节拍化疗中也常与环磷酰胺联合[7],一项Ⅱ期临床研究中共入组66例晚期乳腺癌患者,给药方式为:环磷酰胺65mg/m2 QD联合卡培他滨1000mg/m2 BID, D1-14,Q3W。中位OS为16.9个月,ORR为30.3%,临床获益率为53%。
VICTOR研究系以长春瑞滨为主的联合节拍治疗的系列研究,从VICTOR-0到VICTOR-6,从临床前研究到真实世界研究,逐步探索了长春瑞滨联合卡培他滨节拍化疗的最适剂量范围以及真实世界中节拍方案的疗效及安全性,其中也包括小样本研究探索长春瑞滨联合皮下曲妥珠单抗节拍疗法的安全性、小样本研究探索长春瑞滨联合卡培他滨对免疫调节的影响,为后续的进一步研究奠定了一定的基础。VICTOR-1 研究[11]对长春瑞滨联合卡培他滨节拍化疗治疗晚期乳腺癌进行了剂量探索,研究结果确定了NX节拍方案的给药剂量,同时观察了治疗方案的有效性和安全性,其中长春瑞滨的推荐剂量为40mg每周三次,该研究中患者的临床获益率(clinical benefit rate,CBR)为 58.1%,3 级及以上不良反应发生率为5.9%,疗效及安全性均体现出优势;≥70岁老年患者的ORR为33%,中位PFS为10.5个月,尽管在疗效方面未见明显统计学差异,但节拍化疗耐受性优于标准治疗方案。VICTOR-2临床研究[12]再次证实了VICTOR-1研究的结论,即NX方案在晚期乳腺癌患者中的有效性和安全性。VICTOR-6研究[13]系节拍化疗治疗晚期乳腺癌的真实世界研究,该研究数据显示,在一线治疗中,含长春瑞滨的治疗方案具有最高的ORR和CBR(单药化疗的ORR和CBR分别为44%和88%;联合化疗的ORR和CBR分别为36.7%和82.4%)。同时,在长春瑞滨联合治疗方案和卡培他滨单药治疗方案中观察到最长的中位PFS。
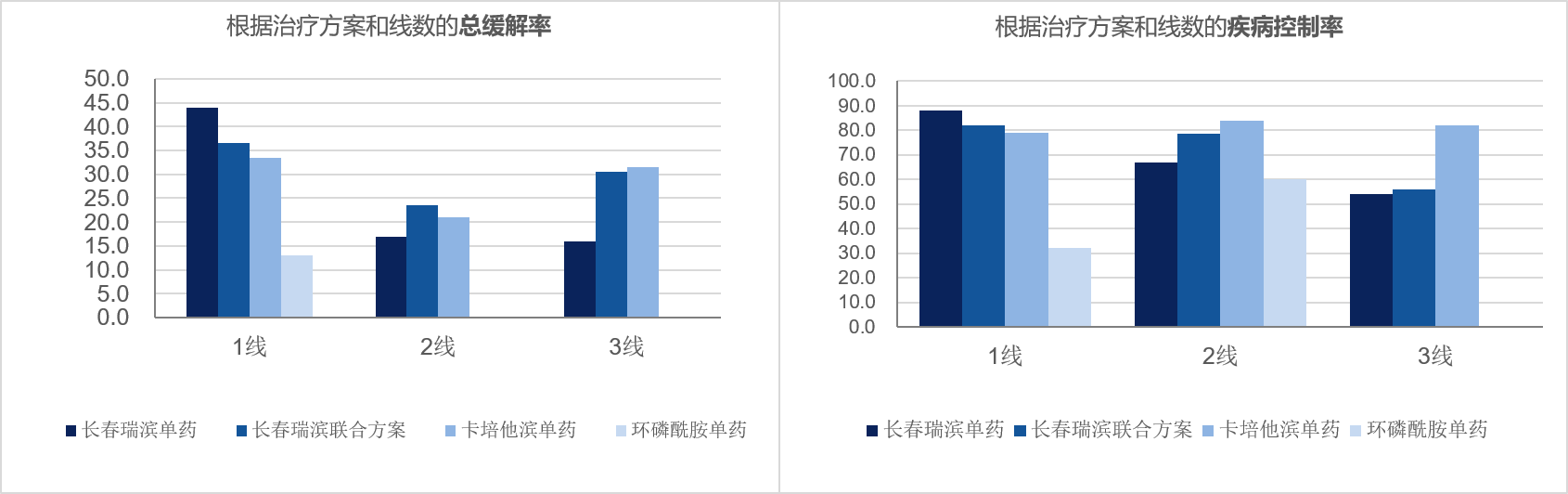
VICTOR-6中根据治疗方案和线数的总缓解率及疾病控制率
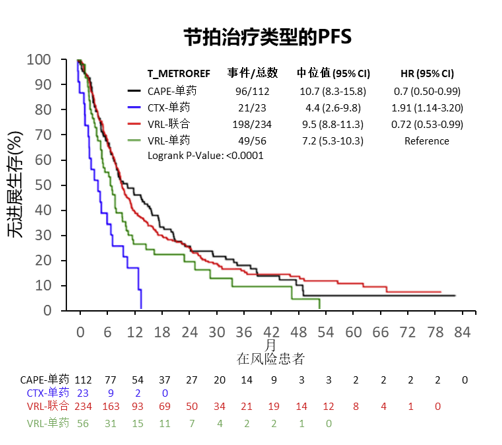
VICTOR-6中各治疗方案的PFS
另外一项长春瑞滨、卡培他滨和环磷酰胺联合(VEX方案)治疗激素受体阳性转移性乳腺癌的Ⅱ期临床试验[14]结果显示,一线及以上治疗患者的CBR分别为81%和74%,疾病进展时间分别为25.1和11.2个月,治疗耐受性良好,未发生4级不良反应。该研究作者也提到,在其早期开展的另一项临床研究中,节拍环磷酰胺(50mg每天)和卡培他滨(500mg每日三次)联合贝伐单抗治疗激素受体阳性晚期乳腺癌患者,临床获益率达到了74%,中位PFS达到6个月。另外一项VEX节拍化疗在三阴性乳腺癌[15]中的研究显示,具体治疗方案为:长春瑞滨采用40mg每周三次、环磷酰胺50mg每天、卡培他滨500mg每日三次口服节拍化疗。研究共入组25例患者,中位治疗到疾病进展时间(TTP)为6.4个月(95%CI 3.6-12.6)。最常见的1-2级毒性反应为恶心、腹泻、白细胞/中性粒细胞减少和可逆性肝功能改变。3级不良事件主要为手足综合症(9%)。该研究显示,VEX方案在三阴性转移性乳腺癌患者中作为一线治疗方案时可以表现出良好的抗肿瘤活性和耐受性。
节拍化疗还可联合内分泌治疗用于晚期乳腺癌的治疗[16-18],VICTORIANE研究旨在评估来曲唑或阿那曲唑联合或不联合长春瑞滨一线治疗ER阳性晚期乳腺癌的临床疗效,目前该Ⅲ期临床试验正在开展,期待后续研究结果公布。另外一项VENTANA研究[19]将未经治疗的I-Ⅲ期HR+/HER2-绝经后乳腺癌患者随机(1:1:1)分别接受来曲唑(2.5mg/天)或口服长春瑞滨50mg周疗(一周三次)或来曲唑+口服长春瑞滨周疗。研究共入组61例患者,初步结果显示,短期口服长春瑞滨节拍化疗具有良好的耐受性,单独或与来曲唑联合使用均具有抗增殖活性(− 19.1% vs. -73.2%性)。联合治疗组呈现高肿瘤淋巴细胞浸润,为研究该组合未来与免疫疗法联合应用提供了可能性。节拍化疗联合内分泌治疗有望进一步减少治疗相关不良反应,提高患者的生活质量,但结果有待于进一步研究证实。
4. 节拍化疗在晚期NSCLC中的应用
由Kontopodis等[20]主导的一项评估长春瑞滨单药节拍化疗(每次50mg口服,TIW,Q4W)对于一线治疗失败的晚期NSCLC临床疗效的研究发现,在入组46例患者中,5例患者疗效评估为部分缓解(PR),9 例疾病稳定(SD),客观缓解率(ORR)为 10.9%,疾病控制率(DCR)为 30.4%,中位肿瘤进展时间为2.2个月,中位OS为9.4个月,1 年生存率为 30.1%。Bilir等[21]采用长春瑞滨单药节拍化疗治疗35例老年(65~86岁)、体力状况较差(ECOG-PS 评分为2分)且不适合接受传统化疗的晚期NSCLC患者,用药方案为:长春瑞滨30mg,一周三次,9例患者达到PR,15例达到SD,总反应率为26%,DCR高达69%,1年和2年生存率分别为34%和8%。中位PFS和OS分别为4个月和7个月,所有患者均未发生治疗相关死亡事件,仅有1例患者因3级乏力和腹泻住院治疗。Camerini等[22]同样进行了一项长春瑞滨口服节拍化疗研究,入组患者接受50、40或30 mg长春瑞滨口服治疗,每周三次,研究共入组270例晚期NSCLC患者,就疗效而言,在持续服药12周后,46例患者PR,2例CR,119例SD,有效率17.8%,DCR为61.9%,中位OS为9个月,3-4级不良事件发生率为2%,没有发生治疗相关的死亡事件。上述研究表明节拍化疗可为无靶向药治疗指征且不能耐受传统化疗的患者提供一种安全、有效的治疗方案。
Tandon等[23]回顾性研究分析每周接受紫杉醇节拍化疗的100例经治或复发且一般状态较差的晚期转移性NSCLC患者,治疗方案为紫杉醇80mg/m2,每周一次,结果显示,3例患者达到CR,34例PR,35例SD,ORR为37%,DCR为72%,中位PFS和OS分别达5个月和12个月。上述研究表明每周紫杉醇节拍化疗方案治疗晚期 NSCLC 患者可能前景更广阔。遗憾的是,目前一些研究结果提示单药替莫唑胺、多西他赛节拍化疗对于一线治疗失败晚期NSCLC的临床疗效差强人意。
多药节拍化疗理论上可进一步提高抗肿瘤效果,但多药联合的耐受性仍需进一步研究证实。Correale等[24]探讨每周顺铂联合依托泊苷节拍化疗治疗31例晚期NSCLC患者疗效与安全性的研究,其治疗方案为:顺铂30mg/m2,每周一次,依托泊苷50mg,每日一次,服用21天,28天为一周期。其中,2例患者达到CR,12例PR,4例SD,ORR为45.2%,DCR达58.1%,3级中性粒细胞减少和贫血是最常见的不良反应,多药节拍化疗的临床疗效较好,且安全性良好。入组患者中位治疗周期数为20,3例患者死于肺栓塞,发生Ⅲ度白细胞降低和贫血分别为7例和10例。
HORG II期临床研究[25]共入组41例不可切除IIIB或IV期NSCLC患者,治疗方案为顺铂80mg/m2,口服长春瑞滨节拍给药60mg,隔日一次,21天为一周期。结果显示,13例患者疗效评估为PR,10例SD。中位PFS和OS分别为4.2和12个月,分别有5例(14.3%)和6例(17.1%)患者出现3、4级骨髓抑制,非血液学毒性反应中等。上述结果表明,尽管存在骨髓毒性,顺铂联合口服长春瑞滨节拍化疗一线治疗可以作为局部晚期和转移性NSCLC患者的一种有效治疗方法。
4.2.1 双药节拍化疗联合抗肿瘤血管生成药
双药节拍化疗联合抗肿瘤血管生成药能否进一步提高临床疗效有待于进一步研究证实。一项旨在评估一线紫杉醇和吉西他滨双药节拍化疗联合贝伐珠单抗治疗晚期NSCLC疗效和安全性的研究[26],其入组标准为:年龄≥组标岁;IV期;病理证实鳞状NSCLC;ECOG PS评分0-1;未接受系统化疗;没有明显器官损伤。其中,ORR为56%,中位PFS和OS分别可以达到8.5和25.5个月,耐受性良好。众所周知,在现阶段临床实践中,节拍化疗更多是用于二线及以上治疗,该研究虽不足以挑战晚期NSCLC的标准一线治疗方案,但至少为临床提供了一个新的方向,即对于体力状况较差、不能耐受常规化疗且无合适靶向药物治疗的晚期NSCLC患者,可以考虑双药节拍化疗联合抗肿瘤血管生成药物治疗。
4.2.2 TKI靶向药联合节拍化疗
由于潜在的抗肿瘤血管生成活性,替加氟/尿嘧啶更适合以节拍化疗的方式给药。Chen等[27]比较吉非替尼联合或不联合替加氟/尿嘧啶节拍化疗治疗一线治疗失败晚期NSCLC的临床疗效,结果显示,吉非替尼联合替加氟/尿嘧啶节拍化疗组患者的1年无进展生存率为36.7%,高于吉非替尼单药组患者的18.0%;进一步筛选EGFR敏感突变的患者,发现吉非替尼联合替加氟/尿嘧啶节拍化疗可明显延长有EGFR敏感突变患者的PFS(11.8个月 vs. 2.8个月)和中位OS(23.6个月 vs.18.3个月)。上述研究表明有EGFR敏感突变患者可应用靶向药联合节拍化疗,以进一步增强药物的抗肿瘤效应。
5. 口服节拍化疗
疫情期间,给肿瘤患者正常诊疗活动带来了极大不便,很多患者无法按时到医院复查、治疗。通常情况下,肿瘤患者免疫力相对较低,新冠肺炎感染风险相对较高,而对于感染新冠肺炎的肿瘤患者,死亡风险相对增高。在保证疗效的同时,可以对乳腺癌患者治疗方案进行调整,优先选择口服等能减少患者到医院就诊次数的治疗方案,降低新冠肺炎感染风险。口服节拍化疗应用方便,具备较好临床疗效和安全性,甚至对高龄或体力状况较差、无法耐受毒性较大化疗方案的晚期NSCLC也适用,对生活质量要求较高、不愿意频繁到医院接受静脉化疗的晚期乳腺癌患者更是合适之选。节拍化疗具有多重抗肿瘤作用,与传统化疗的作用机制有不同之处。另外,在传统药物耐药时,以节拍化疗给药仍可能敏感。除单独应用外,节拍化疗还可以与其他化疗药物、抗肿瘤血管生成药及靶向药联合应用,以增强抗肿瘤活性,并且耐受性良好,在提高疗效的同时改善患者生活质量。尽管节拍化疗已经取得了一定的成果,未来仍应进一步针对不同瘤种及人群继续探索的给药方案和剂量,以进一步明确适合节拍化疗的患者,实现精准施治。
[1] Browder T, Butterfield CE, Kräling BM, et al. Antiangiogenic scheduling of chemotherapy improves efficacy against experimental drug-resistant cancer. Cancer Res. 2000 Apr 1;60(7):1878-86.
[2] Klement G, Baruchel S, Rak J, et al. Continuous low-dose therapy with vinblastine and VEGF receptor-2 antibody induces sustained tumor regression without overt toxicity. J Clin Invest. 2000 Apr;105(8):R15-24. Erratum in: J Clin Invest. 2006 Nov;116(11):3084. J Clin Invest. 2006 Oct;116(10):2827.
[3] Hanahan D, Bergers G, Bergsland E. Less is more, regularly: metronomic dosing of cytotoxic drugs can target tumor angiogenesis in mice. J Clin Invest. 2000 Apr;105(8):1045-7.
[4] Cazzaniga ME, Camerini A, Addeo R, et al. Metronomic oral vinorelbine in advanced breast cancer and non-small-cell lung cancer: currentstatus and future development. Future Oncol. 2016 Feb;12(3):373-87.
[5] 冯宇,胡兴胜.节拍化疗在晚期非小细胞肺癌治疗中的研究进展[J].癌症进展,2019,17(3):264-266,276.
[6] 黎立喜,马飞.长春瑞滨在晚期乳腺癌节拍化疗中的研究进展[J].癌症进展,2019,17(23):2757-2760,2764.
[7] 夏雯.乳腺癌节拍化疗[C].第四届上海浦东乳腺癌高峰论坛论文集.2016:148-154.
[8] Fedele P, Marino A, Orlando L, et al. Efficacy and safety of low-dose metronomic chemotherapy with capecitabine in heavily pretreated patients with metastatic breast cancer. Eur J Cancer. 2012 Jan;48(1):24-9.
[9] Addeo R, Sgambato A, Cennamo G, et al. Low-dose metronomic oral administration of vinorelbine in the first-line treatment of elderly patients with metastatic breast cancer[J]. Clin Breast Cancer, 2010, 10(4): 301-306.
[10] De Iuliis F, Salerno G, Taglieri L, et al. On and off metronomic oral vinorelbine in elderly women with advanced breast cancer[J]. Tumori, 2015, 101(1): 30-35.
[11] Cazzaniga ME, Torri V, Villa F, et al. Efficacy and safety of the all- oral schedule of metronomic vinorelbine and capecitabine in locally advanced or metastatic breast cancer patients: the phase I- II VICTOR- 1 study[J]. Int J Breast Cancer, 2014, 2014: 769790.
[12] Cazzaniga ME, Cortesi L, Ferzi A, et al. Metronomic chemotherapy with oral vinorelbine (mVNR) and capecitabine (mCAPE) in advanced HER2-negative breast cancer patients: is it a way to optimize disease control? Final results of the VICTOR- 2 study[J]. Breast Cancer Res Treat, 2016, 160(3): 501-509.
[13] Cazzaniga ME, Pinotti G, Montagna E, et al. Metronomic chemotherapy for advanced breast cancer patients in the real world practice: final results of the VICTOR- 6 study [J]. Breast, 2019, 48: 7-16.
[14] Montagna E, Palazzo A, Maisonneuve P, et al. Safety and efficacy study of metronomic vinorelbine, cyclophosphamide plus capecitabine in metastatic breast cancer: a phase II trial[J]. Cancer Lett, 2017, 400: 276-281.
[15] Montagna E, Bagnardi V, Cancello G, et al. Metronomic Chemotherapy for First-Line Treatment of Metastatic Triple-Negative Breast Cancer: A Phase II Trial. Breast Care (Basel). 2018 Jul;13(3):177-181.
[16] Li JW, Zuo WJ, Ivanova D, et al. Metronomic capecitabine combined with aromatase inhibitors for new chemoendocrine treatment of advanced breast cancer: a phase II clinical trial[J]. Breast Cancer Res Treat, 2019, 173(2):407-415.
[17] Palazzo A, Dellapasqua S, Munzone E, et al. Phase II trial of bevacizumab plus weekly paclitaxel, carboplatin, and metronomic cyclophosphamide with or without trastuzumab and endocrine therapy as preoperative treatment of inflammatory breast cancer[J]. Clin Breast Cancer, 2018, 18 (4): 328-335.
[18] Schwartzberg LS, Wang G, Somer BG, et al. Phase II trial of fulvestrant with metronomic capecitabine for postmenopausal women with hormone receptor-positive, HER2-negative metastatic breast cancer[J]. Clin Breast Cancer, 2014, 14(1): 13-19.
[19] Adamo B, Bellet M, Paré L, et al. Oral metronomic vinorelbine combined with endocrine therapy in hormone receptor-positive HER2-negative breast cancer: SOLTI-1501 VENTANA window of opportunity trial. Breast Cancer Res. 2019 Sep 18;21(1):108.
[20] Kontopodis E, Hatzidaki D, Varthalitis I, et al. A phaseⅡstudy of metronomic oral vinorelbine administered in the second line and beyond in non- small cell lung cancer (NSCLC): a phase Ⅱ study of the hellenic oncology research group[J]. J Chemother, 2013, 25(1): 49-55.
[21] Bilir C, Durak S, Kızılkaya B, et al. Efficacy of metronomic vinorelbine in elderly patients with advanced non-smallcell lung cancer and poor performance status[J]. Curr Oncol, 2017, 24(3): e199-e204.
[22] Camerini A, Banna GL, Cinieri S, et al. Metronomic oral vinorelbine for the treatment of advanced non-small cell lung cancer: amulticenter international retrospective analysis. Clin Transl Oncol. 2019 Jun;21(6):790-795.
[23] Tandon N, Noronha V, Prabhash K, et al. Metronomic weekly paclitaxel in metastatic or recurrent non-small cell lung cancers[J]. J Clin Oncol, 2013, 31 suppl: e19095.
[24] Correale P, Cerretani D, Remondo C, et al. A novel metronomic chemotherapy regimen of weekly platinum and daily oral etoposide in high- risk non- small cell lung cancer patients[J]. Oncol Rep, 2006, 16(1): 133-140.
[25] Katsaounis P, Kotsakis A, Agelaki S, et al. Cisplatin in combination with metronomic vinorelbine as front-line treatment in advanced non-small cell lung cancer: a multicenter phase II study of the Hellenic Oncology Research Group (HORG). Cancer Chemother Pharmacol. 2015 Apr;75(4):821-7.
[26] 28. Jones BS, Jerome MS, Miley D, et al. Pilot phase Ⅱ study of metronomic chemotherapy in combination with bevacizumab in patients with advanced non-squamous non-small cell lung cancer[J]. Lung Cancer, 2017, 106: 125-130.
[27] Chen YM, Fan WC, Tsai CM, et al. A phase Ⅱ randomized trial of gefitinib alone or with tegafur/uracil treatment in patients with pulmonary adenocarcinoma who had failed previous chemotherapy[J]. J Thorac Oncol, 2011, 6(6):1110-1116.
排版编辑:肿瘤资讯-细胞田














 苏公网安备32059002004080号
苏公网安备32059002004080号


