2020年1月23~25日在旧金山举行了美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO-GI),本次大会共入选摘要855篇,【肿瘤资讯】择取了14篇来自中国学者的结直肠癌领域摘要,将其整理为三大部分内容,下文将主要介绍有关结直肠癌整体诊疗的相关研究内容。
【摘要222】全面基因组测序显示结直肠黏液腺癌独特的基因组特征
Distinct genomic landscape in colorectal mucinous carcinoma via comprehensive genomic profiling
第一作者:中山大学附属第六医院,广东省结直肠盆底疾病研究重点实验室 黄亮
背景
黏液性癌(MC)约占结直肠癌(CRC)的10%~15%,MC与治疗反应较差相关。早期CRC中,MC作为不良预后因素仍有待商榷。这项研究中,通过大型CRC队列研究定义了MC的基因组特征,并确定了具有预后作用的信息和可指导临床的相关信息。
方法
1226例CRC患者中包括997例腺癌(AC),129例MC和110例腺癌伴黏液成分(AMC)。所有病理切片由经验丰富的病理学家证实。FFPE肿瘤样本和匹配的外周血用于测序检查,共检测450个癌症相关基因。
结果
与AC相比,MC更多发生于右半结肠(P<0.001),并较多发生区域淋巴结转移(P=0.004)。与AC相比,MC具有更高的BRAF V600E突变率(10.9%和3.3%),PIK3CA突变率(28.7%和19.2%)、SMAD4突变率(34.1%和19.1%)、BRCA1/2突变率(16.3%和6.8%)和同源重组途径突变率(40.3%和22.7%),但以下基因突变率较低,如TP53(53.5%和79.5%)、APC(46.5%和75.1%)和HER2扩增(0%和2.1%)。MC较AC有更高比例的微卫星高度不稳定(MSI-H)肿瘤(22.5%和6.8%,P<0.001)。 此外,在MSI稳定肿瘤中,MC中POLE突变肿瘤的比例高于AC(7.0%和2.6%,P=0.094),尽而导致显著升高的肿瘤突变负荷(TMB,范围79.5~591.5 muts/Mb),因此高达30%的MC患者可能会获益于免疫治疗。MSI-H与Ⅱ/Ⅲ期MC CRC预后较好(5-y DFS,MSI-H 86.7%,MSS 56.7%)相关。重要的是研究还发现,AMC与MC的基因组改变特征更相似,而不是与AC更相似。
结论
首次通过全面基因组分析表明,MC具有独特的基因组特征,这些改变提示MC具有广阔的免疫治疗和靶向治疗的临床应用前景。由于MSI状态,早期MC具有不同的预后,应该予以不同解释。AMC和MC分子特征的相似性提示,应该使用MC的临床策略用于AMC的治疗。
【摘要98】 两项前瞻性研究的倾向得分匹配分析:局部进展期直肠癌mFOLFOXIRI新辅助化疗较CRT能更好的改善生存
Neoadjuvant mFOLFOXIRI chemotherapy-improved survival benefit comparing with CRT in locally advanced rectal cancer:A propensity score matched analysis from two prospective trials.
第一作者:中山大学附属第六医院 Jianwei Zhang
背景
新辅助放化疗(CRT)是局部进展期直肠癌(LARC)的标准治疗,但它会延迟全身化疗,导致远处转移的发生率增加。为了加强全身化疗,避免放疗损伤,对mFOLFOXIRI新辅助化疗在LARC中的作用进行了研究,但是目前尚缺少随机对照研究比较mFOLFOXIRI与CRT的疗效。
方法
Ⅲ期FOWARC研究(NCT01211210)中共有145例LARC患者接受了CRT作为新辅助治疗,另一项Ⅱ期研究(NCT02217020)中有103例患者只接受了mFOLFOXIRI作为术前治疗。采用倾向评分校正方法评估强化的新辅助化疗方案能否为生存和活性参数带来更多获益。
结果
初始队列中,mFOLFOXIRI组患者较 CRT组患者更年轻,中位年龄分别为48岁和56岁。mFOLFOXIRI组有更多患者的肿瘤长度超过5cm、cT3或N2疾病(P<0.05)。倾向评分校正匹配后,每组有73例可用于比较研究。mFOLFOXIRI组和CRT组的pCR率分别为23.3%和13.7%(P=0.14),yp 0~Ⅰ期患者比例分别为45.2%和39.7%(P=0.5),两组的局部复发率相似(5.5%和4.1%,P=0.70),但是mFOLFOXIRI治疗降低了远处转移发生率(8.2%和27.4%,P=0.002),mFOLFOXIRI组和CRT组的3年无病生存率分别为86.8%和75.8%(P=0.049)。mFOLFOXIRI组的吻合口瘘发生率低于CRT组(5.5%和17.8%,P=0.02),mFOLFOXIRI组较CRT组更常发生3/4级中性粒细胞减少(39.7%和8.2%,P<0.001)。
结论
与CRT相比,术前mFOLFOXIRI全身化疗能降低远处转移发生率并改善3年DFS,毒性较少且术后并发症更少。目前比较FOLFOXIRI和CRT的Ⅲ期随机研究正在进行中。
【摘要99】FOCULM研究:mFOLFOXIRI±西妥昔单抗作为 RAS/BRAF野生型不可切除肝转移结直肠癌的转化治疗
mFOLFOXIRI with or without cetuximab as conversion therapy in patients with RAS/BRAF wild-type unresectable liver metastases colorectal cancer: The FOCULM study
第一作者:中山大学附属第六医院 胡华斌
背景
不可切除结直肠癌肝转移(LM)通过转化治疗能够使肿瘤缩小,从而使患者有机会接受更多局部治疗,转变为无疾病证据状态(NED)。本研究评估了西妥昔单抗联合mFOLFOXIRI或单独mFOLFOXIRI作为转化治疗的有效性。
方法
FOCULM是一项前瞻性、多中心、2:1对照的Ⅱ期研究,由于没有免费药物以及考虑到患者对西妥昔单抗的支付能力,这项研究自2016年9月由随机化研究更改为非随机化研究。不可切除的LM患者接受西妥昔单抗(500mg/m2)+mFOLFOXIRI(奥沙利铂85mg/m2,伊立替康165mg/m2,亚叶酸400mg/m2,氟尿嘧啶2800mg/m2 46小时输注,每2周一次)(A组)或单独mFOLFOXIRI(B组)治疗。主要研究终点为NED率,次要研究终点为客观缓解率(ORR)、切除率、局部和消融治疗率(LAT)、总生存(OS)、无进展生存(PFS)和缓解深度(DpR)。
结果
自2014年2月至2019年7月期间,中国6家医学中心共招募114例患者,其中101例为ITT人群(组A 67例,组B 34例)。两组患者分布比较平衡,但A组有更多≥5个LM的患者。A组和B组的NED率分别为62.7%和38.2%(P=0.020)。中位随访19.4个月,A组患者的mOS较B组明显延长,ORR、LAT和DpR率增加(见下表)。无论是A组还是B组,NED患者都能获得显著的生存获益,分别为未达到和49.4个月(P=0.001),未达到和25.1个月(P=0.007)。
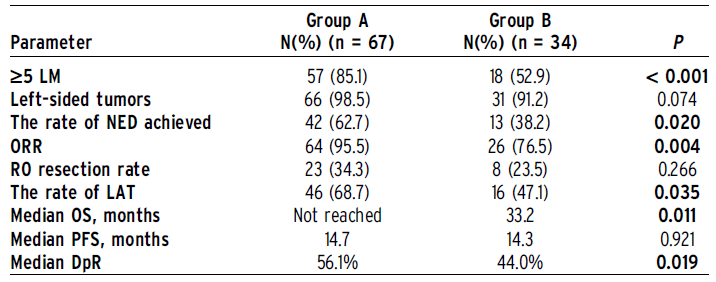
结论
RAS/BRAF野生型不可切除肝转移结直肠癌的转化治疗中,在mFOLFOXIRI基础上加入西妥昔单抗能明显改善NED率、ORR和OS。
【摘要97】系统综述和网状meta分析:比较FOLFOXIRI+贝伐珠单抗与双药化疗+抗EGFR抗体一线治疗转移性结直肠癌
Comparing FOLFOXIRI plus bevacizumab with doublet chemotherapy plus anti-EGFR antibody: A systemic review and network meta-analysis.
第一作者:中山大学附属第六医院 Jianwei Zhang
背景
转移性结直肠癌(mCRC)一线采用FOLFOXIRI+贝伐珠单抗(三药+Bev)治疗较双药+Bev治疗可改善生存获益。几项研究也比较了双药+EGFR抗体(EGFRi)治疗与双药+Bev治疗的疗效。然而,对于三药+Bev与双药+EGFRi治疗 mCRC的疗效差别知之甚少。
方法
检索PubMed、EMbase、Web of Science以及国际肿瘤学会议,进行系统综述和网状meta分析。纳入的Ⅱ期和Ⅲ期随机对照研究,主要是比较mCRC的一线治疗,包括FOLFOXIRI+Bev与双药+Bev或是比较双药+EGFRi与双药+Bev。通过Bayesian网状meta分析,比较总人群、RAS野生型人群、左半或右半肿瘤人群、左半或右半RAS野生型人群的PFS和OS的风险比(HRs),比较客观治疗反应率的相对风险(RR)。
结果
8项研究共3980例患者纳入研究。直接比较发现,无论是OS(HR=0.83,0.72~0.97)、PFS(HR=0.73,0.65~0.83)还是 ORR(RR=1.5,1.2~2.0),均是三药+Bev优于双药+EGFRi,双药+EGFRi较双药+Bev在OS(HR=1.2,1.1~1.5)和 ORR(RR=0.74,0.52~0.97)有更多获益,但PFS无显著获益。间接比较显示,三药+Bev与双药+EGFRi在总人群的OS(HR=1.0,0.84~1.4)和ORR(RR=1.1,0.73~1.6)无显著差异,但PFS有改善(HR=0.71,0.60~0.86)。左半RAS野生型亚组中,三药+Bev在OS(HR=1.2,0.6~2.5)、PFS(HR=1.6,0.59~4.3)和ORR(RR=0.63, 0.22~15)的疗效相似。右半亚组中,三药+Bev在OS(HR=0.41,0.18~0.93)和PFS(HR=0.55,0.34~0.92)均有获益。右半RAS野生型亚组中,三药+Bev较双药+EGFRi显示出更长OS(HR=0.37,0.12~1.1)和PFS(HR=0.43,0.18~1.1)的趋势。
结论
对于左半RAS野生型mCRC,FOLFOXIRI+Bev与双药+EGFRi具有相似的疗效,右半亚组或右半RAS野生型亚组中,三药+Bev应作为mCRC的优选初始治疗,但应注意治疗不良反应。
【摘要88】结肠癌含奥沙利铂化疗导致的脾脏增大
Splenomegaly during oxaliplatin-based chemotherapy in colon cancer.
第一作者:中国医学科学院北京协和医学院 Ruoyu Ji
背景
据报道,接受奥沙利铂治疗的患者可出现脾脏增大,但奥沙利铂所致脾脏增大的特点并无详细研究。本研究评估了脾脏体积的变化及其对奥沙利铂治疗患者的临床意义。
方法
对2016年1月至2017年12月在中国国家癌症中心接受奥沙利铂+卡培他滨治疗的Ⅱ-Ⅳ期原发性结肠癌患者进行回顾性研究,患者需有治疗前、治疗期间以及化疗结束后1.5年的完整实验室检查结果和CT检查结果。脾脏大小由AWVolumeshare5测量,脾脏增大定义为超过基线的30%,脾脏增大恢复定义为脾脏大小回落至基线的0.9~1.1倍范围内。
结果
总共144例患者,其中102例(70.8%)脾脏增加超过30%,72例(50.0%)脾脏增加超过50%,22例(15.3%)脾脏大小增加超过100%。102例脾脏增大患者中,5例(4.9%)在3个周期化疗内即出现脾脏增大,53例(53.0%)为 6个周期内,73例(71.6%)为9个周期内,末次奥沙利铂化疗后3个月内102例(100.0%)患者均出现脾脏增大。与没有脾脏增大的患者相比,脾脏增大的患者接受了更多周期的奥沙利铂治疗(中位数8和6,P<0.001)和较大的剂量强度(总剂量/m2的中位数为822.8mg/m2和629.3mg/m2,P<0.001)。 脾脏增大患者的血小板减少发生率更高(61.7%和38.1%,P=0.009),更有可能由于血小板减少而降低奥沙利铂使用剂量(21.6%和7.1%,P=0.038)。奥沙利铂末次治疗结束后0.5、1和1.5年内脾脏大小恢复率分别为23.2%、50.6%和74.3%。
结论
脾脏增大常见于奥沙利铂为基础的化疗患者中,多数在完成治疗后1.5年内恢复。脾脏增大患者更易发生血小板减少和奥沙利铂剂量减量。需要进一步研究揭示奥沙利铂诱发脾脏增大的作用机制。
排版编辑:肿瘤资讯-Jelly















 苏公网安备32059002004080号
苏公网安备32059002004080号


