2019年欧洲肿瘤内科学会亚洲峰会(ESMO ASIA)于11月22日—24日在新加坡盛大举办。来自全球肿瘤领域的专家齐聚一堂,共襄盛举,分享最前沿的研究进展。当地时间11月22日晚上,特别设置了“ESMO Asia Ask the Expert Session”环节,与专家面对面交流。本次会见的讨论主题为“征服HER2阳性早期乳腺癌的临床挑战”, 来自加拿大的Jane-Francois Boileau教授、来自台湾的黄俊升教授、来自中国北京大学人民医院的王殊教授和乳腺癌患者Ike de Rooij-van Haaren一起出席了本次会议,介绍了HER2阳性早期乳腺癌的系统治疗策略,并分别从内科、外科和患者的视角讨论新辅助治疗的利弊。大会同时展开专家面对面现场互动,为听众解答临床实践中的挑战和疑惑。
HER2阳性早期乳腺癌的系统治疗策略
讲者:王殊教授
 王殊教授是这次会议的首位演讲嘉宾,介绍了HER2阳性乳腺癌的系统治疗策略。
王殊教授是这次会议的首位演讲嘉宾,介绍了HER2阳性乳腺癌的系统治疗策略。
王教授指出,随着越来越多的药物的上市,我们已经从曲妥珠单抗一统天下的时代演变成了针对不同复发风险的患者,给予个体化治疗的时代。低风险的患者(T1/N0)可直接手术,术后进行一年的抗HER2+ 辅助治疗。APT结果表明,行紫杉醇+曲妥珠单抗单周方案12个周期序贯曲妥珠单抗满一年抗HER2的治疗方案的7年DFS也可以达到93.3%
对于高危患者,APHINITY研究提供了解决方案。APHINITY结果显示与曲妥珠单抗相比,曲妥珠单抗+帕妥珠单抗+化疗可使高复发风险患者(淋巴结阳性和激素受体阴性)的复发风险降低近25%。
对于T≥2cm或淋巴结阳性的早期乳腺癌患者,指南推荐6 ~ 8周期的PH为基础的新辅助治疗。新辅助治疗后实现pCR 的HER2阳性早起乳腺癌患者继续使用PH双靶一年的辅助治疗;而对于新辅助治疗后non-pCR 患者,则应该改为T-DM1 治疗14个周期。
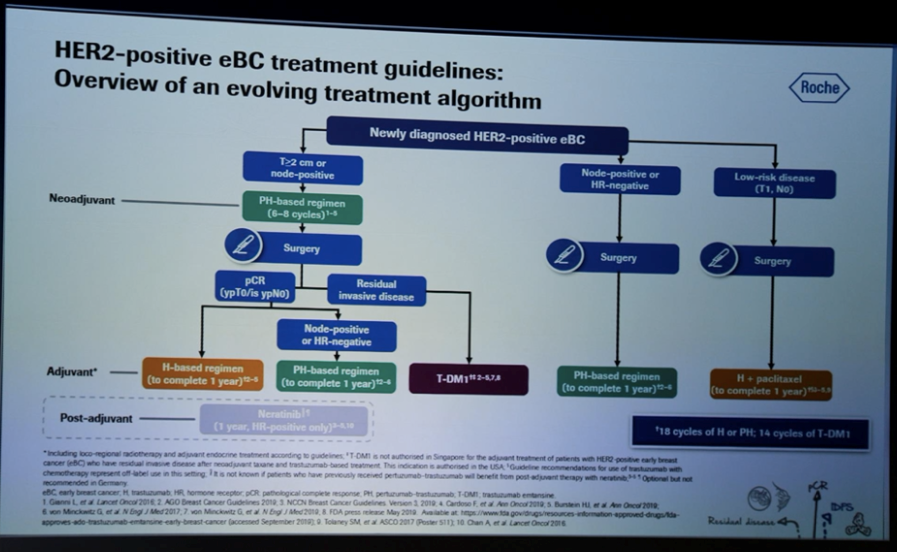
目前国际指南上关于HER2阳性早期乳腺癌的治疗推荐是一致的。强调根据每例患者及其疾病特征进行个体化治疗。早期乳腺癌作为可治愈的疾病,需要制定明确的管理决策,以期为患者提供最好的治疗。
目前对于HER2阳性早期乳腺癌,低风险的患者(T1/N0)建议直接进行手术治疗,术后予以1年曲妥珠单抗的辅助治疗,而对于T1 淋巴结阳性或激素受体阴性的患者则推荐术后PH双靶一年的辅助治疗。对于T ≥ 2cm或淋巴结阳性的患者,推荐首先进行PH为基础的新辅助治疗, 再根据术后是否实现pCR 给予PH或T-DM1 的辅助治疗。
随着Katherine 研究结果的公布,新辅助治疗正成为行业的热点话题,那么新辅助治疗能给患者带来哪些获益呢?
新辅助治疗的内外科视角
讲者:Jane-Francois Boileau教授

内科视角
过去新辅助治疗主要出于手术目的,将不可手术变为可手术, 将不可保乳变为可保乳。新辅助治疗方案与辅助治疗方案是一样的;而当代的新辅助治疗相较之前有了两大发展:一、新辅助治疗的手段从过去的化疗、内分泌治疗扩展为靶向、化疗和内分泌治疗,极大地提高了pCR 率。二、可通过新辅助治疗后是否实现pCR, 在辅助治疗筛选出预后不佳的non-pCR 患者,给予强化辅助治疗。
Dr. Boileau 介绍新辅助治疗可以带来多个关键的临床获益, 以实现早期乳腺癌治愈的目标:
尽早通过药物治疗控制病情发展
提供更全面的预后信息 (RCB 评估)
提供药物敏感信息,帮助辅助治疗方案选择,给予患者最合适的治疗方案,提高病人的长期生存
为更详尽的基因检测争取了时间, 比如BRCA1/2检测
pCR作为替代终点,能够帮助药物更快获批
外科视角
外科医生在决定病人是否需要新辅助治疗时扮演着关键角色。外科医生需要在获取了足够的影像学、病理活检和分子检测的结果后,结合病人的需求, 确定:何种手术术式? 是否需要新辅助治疗?新辅助治疗采用什么方案?何时手术? 以及术后辅助治疗方案?
Dr. Boileau认为可以通过新辅助治疗后来实现保腋窝,但是需要进行精细的前哨淋巴结活检,以降低复发,目前认为在以下情况下可以考虑在新辅助治疗后进行前哨淋巴结活检:新辅助治疗前为T1-3,N1-2,新辅助治疗后为cN0,采用双重示踪剂,至少切除2个前哨淋巴结,强烈建议在活检时切除更多的淋巴结,并且在手术时重新追踪切除的淋巴结,之后采用IHC检测淋巴结,对于N0(i+)的患者考虑定义为淋巴结阳性。
总体而言,从外科角度,新辅助治疗有如下益处:
对于手术的影响:
将不可手术的病人转变为可手术的病人;
提供保乳手术的可能性;
保腋窝, 避免腋窝清扫;
提高保乳手术以后整形的效果;
减少手术并发症;
为复杂的整形术式选择争取更多的时间
其他影响:
争取基因检测时间;
新辅助治疗肉眼可见的缩瘤效果提高了病人的治疗信心;
根据新辅助治疗的结果,为辅助治疗最佳方案选择提供了信息。
对于没有淋巴结转移的病人,Dr. Boileau以2cm 作为是否需要新辅助治疗的分界线。
那么对于新辅助治疗non-pCR的患者又该如何处理呢?
医患面对面:新辅助治疗患者视角

在此环节,黄教授与患者代表深入沟通治疗中的各项考量因素,了解到作为患者,他们的需求不仅是追求治愈,同时也希望提高生活质量。
残留疾病在HER2阳性早期乳腺癌诊疗决策中的价值
讲者:黄俊升教授
接下来,黄教授深度解读了KATHERINE研究,并指出,目前残留疾病已经成为优化辅助治疗方案的重要决策因素。在KATHERINE研究之后,对于所有合适的患者,都应该考虑使用新辅助治疗。T-DM1是目前唯一证实在新辅助治疗后合并残留疾病的HER2阳性早期乳腺癌患者的强化辅助治疗可以改善疗效的药物。
专家面对面

提问:临床上哪些HER2阳性患者会考虑使用新辅助治疗,肿瘤≥1 cm?2 cm?3 cm?
专家解答:指南中推荐对于肿瘤≥2 cm的患者就可以接受新辅助治疗。在临床实践中,对于ER阳性HER2阳性患者,肿瘤≥2 cm时考虑新辅助治疗;但对于ER阴性HER2阳性患者,肿瘤≥1 cm就考虑新辅助治疗。当然,非常期待2019年SABCS大会上公布的研究中提到关于1 ~ 2 cm ER阴性HER2阳性肿瘤,如何进行新辅助和辅助治疗。
提问:新辅助治疗有哪些好处?
专家解答:从外科医生、内科医生和患者角度而言,新辅助治疗可以达到不同的目的。总体而言,新辅助治疗的绝对适应证为降期保乳。Meta分析的结果证实新辅助治疗可以提高保乳率。此外,一些单中心前瞻性研究还发现新辅助治疗可以达到腋窝降期,保腋窝的目的。然而,Meta分析也显示新辅助化疗的局部复发率高,其原因为后续保乳手术比例高,在降低新辅助化疗的局部复发率应考虑更加仔细的病灶定位、详细的病理评估和增加适当的放射治疗。近年来,新辅助治疗后的保腋窝也成为趋势,但新辅助治疗后的前哨淋巴结活检,需要提高活检技术。在决定进行新辅助治疗时,需要和患者进行充分的沟通,让患者更好的参与治疗。
提问:对于不同大小的肿瘤,新辅助治疗方案是否应该个体化?
专家解答:单靶向新辅助治疗已经取得很好的疗效,但对于一些高危的患者,双靶向治疗可以进一步提高pCR率。NeoSphere研究评估了曲妥珠单抗联合帕妥珠单抗治疗HER2阳性早期乳腺癌。结果显示,曲妥珠单抗加帕妥珠单抗联合化疗显著提高pCR率并改善患者预后,pCR患者预后更佳。
提问:相对而言,ER阳性患者接受新辅助治疗的pCR率稍低。对于这类患者如果新辅助治疗未取得pCR,是否意味着预后更差?此外,对于新辅助治疗后不同大小的残留肿瘤患者,生存是否有差异?
专家解答:从KATHERINE研究中可知,即使是非常小的残留疾病,如微转移,接受T-DM1辅助治疗也可以获益。对于一些新辅助治疗前1-2cm的小肿瘤,如果新辅助治疗后未取得pCR,辅助治疗是否推荐T-DM1治疗,可以和患者进行充分的沟通。总体而言,KATHERINE研究为non-pCR的患者提供了机会,T-DM1强化辅助治疗有望降低患者疾病复发、死亡风险。











 苏公网安备32059002004080号
苏公网安备32059002004080号


