新加坡当地时间11月23日下午,吉林省肿瘤医院程颖教授在2019年欧洲肿瘤内科学会亚洲大会(ESMO Asia)大会上口头汇报了KEYNOTE-407研究中国人群数据。研究结果显示,相比传统化疗,一线帕博利珠单抗联合化疗为中国晚期肺鳞癌患者带来显著的临床获益,主要终点总生存期(OS)和无进展生存期(PFS)均取得阳性结果,与全球数据保持一致。【肿瘤资讯】在大会现场第一时间对程颖教授进行了专访。

程颖教授现场汇报KEYNOTE-407中国人群数据

享受国务院特殊津贴,卫生部突出贡献中青年专家
吉林省肿瘤医院党委书记
吉林省癌症中心主任
吉林省肺癌诊疗中心主任
中国临床肿瘤学会(CSCO) 副理事长
CSCO小细胞肺癌专业委员会主任委员
CSCO临床研究专家委员会候任主任委员
CSCO非小细胞肺癌专业委员会副主任委员
CSCO肝癌专家委员会副主任委员
CSCO肿瘤大数据专家委员会副主任委员
中国抗癌协会肺癌专业委员会副主任委员
中国抗癌协会肿瘤临床化疗专业委员会副主任委员
中华医学会肿瘤学分会委员
全国医师定期考核肿瘤专业编辑专业委员会副主任委员
国家卫生、计生委常见肿瘤规范化诊疗专家组成员
中国医师协会肺癌培训专业委员会副主任委员
吉林省医师协会肿瘤医师分会主任委员
吉林省医学会肿瘤专业委员会主任委员
担任《中华肿瘤杂志》等多家杂志编委
免疫治疗为肺癌的治疗带来突破,改写了肺癌治疗的格局,尤其是驱动基因阴性晚期非小细胞肺癌的一线治疗,能否首先请您谈谈当前晚期NSCLC一线免疫治疗的现状?
程颖教授:免疫治疗已经成为驱动基因阴性晚期NSCLC的一线标准治疗,既有去化疗的免疫单药疗法,也有免疫联合化疗,双免疫联合治疗等。在一线治疗中,临床常常根据患者肿瘤组织PD-L1表达情况选择治疗方案,对于PD-L1 TPS≥50%、EGFR/ALK阴性的患者,根据KEYNOTE-024和KEYNOTE-042研究结果,帕博利珠单抗单药是已经在国内获批的治疗选择。今年ESMO年会上公布了IMpower110研究的中期分析结果显示,在PD-L1高表达患者的中,与化疗相比,接受阿替利珠单抗一线治疗有更长的OS(中位OS:20.2个月 vs 13.1个月)和PFS(中位PFS:8.1个月和5.0个月),以及更高的ORR(38.3% vs 28.6%)。IMpower110研究结果已经递交美国FDA。除免疫单药治疗,对于体能状态较好的患者,免疫联合化疗也可以作为PD-L1高表达患者的治疗选择。
KEYNOTE-042研究的全球数据显示,在PD-L1 TPS 1~49%的患者中,帕博利珠单抗单药与化疗疗效相当,而KEYNOTE-042研究中国人群数据表明,与化疗相比,帕博利珠单抗单药治疗有OS获益(中位OS:19.9个月 vs 10.7个月),因此对于这部分患者,如果不愿意接受化疗或不能耐受化疗,可以考虑帕博利珠单抗单药治疗。除此之外,从CheckMate227研究Part1结果也观察到,对于PD-L1≥1%的患者,接受纳武利尤单抗联合低剂量伊匹木单抗的双免疫治疗与化疗相比也取得了OS获益(中位OS:17.1个月 vs 13.9个月),因此双免疫联合治疗也可作为PD-L1阳性患者一线治疗的另一个选择。
KEYNOTE-189和KEYNOTE-407研究结果表明,无论患者PD-L1表达如何,晚期非鳞癌和鳞癌患者,都能从帕博利珠单抗联合化疗中获益。目前国内依据KEYNOTE-189研究已经批准帕博利珠单抗联合化疗一线治疗晚期非鳞癌的适应证。在本次ESOM Asia会议上,我们也公布了KEYNOTE-407研究中国亚组数据,可以看到中国晚期肺鳞癌患者一线接受帕博利珠单抗联合化疗,获得了和总体人群一致的疗效和安全性。帕博利珠单抗联合化疗在中国晚期肺鳞癌一线治疗的适应证也即将获批。
此外IMpower150研究中阿替利珠单抗联合含铂化疗+抗血管生成治疗的四药方案,无论PD-L1表达水平如何均可使患者取得OS获益,尤其是对于存在肝转移的患者,在化疗的基础上增加免疫和抗血管治疗也获得了13.3个月的中位OS,与化疗相比能够降低48%的死亡风险,提示阿替利珠单抗联合含铂化疗+贝伐单抗可能是一些特殊人群,比如肝转移患者,更好的一线治疗选择。
KEYNOTE-407研究结果在2018年ASCO年会上的公布,从OS的亚组分析看到,免疫联合化疗似乎在东亚人群中有更好的获益。KEYNOTE-407研究中国人群数据公布,能否请您介绍下研究结果?中国人群数据与全球数据是否保持一致?
程颖教授:从先前公布的KEYNOTE-407研究全球OS数据,我们观察到免疫联合化疗在东亚人群中有更好的OS获益趋势(HR=0.44,图1),但因为样本量相对较小,所以需要更大样本量的数据证实,尤其是中国人群的数据。
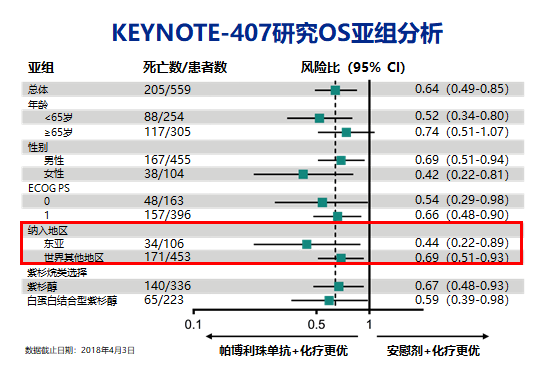
图1 KEYNOTE-407研究OS亚组分析
此次ESMO Asia大会,我代表中国的13家中心,报道了KEYNOTE-407中国人群扩展研究数据结果,共有125例大陆患者入组,其中15例进入全球研究,110例为中国扩展队列。这也是首次报道的中国晚期肺鳞癌人群一线免疫联合化疗的Ⅲ期研究数据。整体而言,与全球总人群数据相比,中国人群获得了一致的结果。
研究共纳入125例中国大陆患者,帕博利珠单抗+化疗组65例,对照组60例,对照组患者ECOG PS 1分的患者高于帕博利珠单抗+化疗组(82% vs 69%),其余基线特征均相似。数据截止时间2019年5月9日,中位随访时间为10.4个月,35例对照组患者交叉到帕博利珠单抗单药治疗,31例(48%)帕博利珠单抗+化疗患者和4例(7%)对照组患者仍在治疗中。
对研究共同主要终点OS和PFS进行分析,中国人群帕博利珠单抗联合化疗组和对照组的中位OS分别为17.3个月和12.6个月,联合组提高了4.7个月,死亡风险降低56%(HR=0.44),与全球总人群结果一致(KEYNOTE-407总人群中位OS为17.1个月和11.6个月,HR=0.71);12个月OS率为79%和55%,提高了24%(图2)。在中国人群的亚组分析中,所有的亚组(年龄,男性,ECOG PS状态,PD-L1表达)都可以从帕博利珠单抗联合化疗中获益。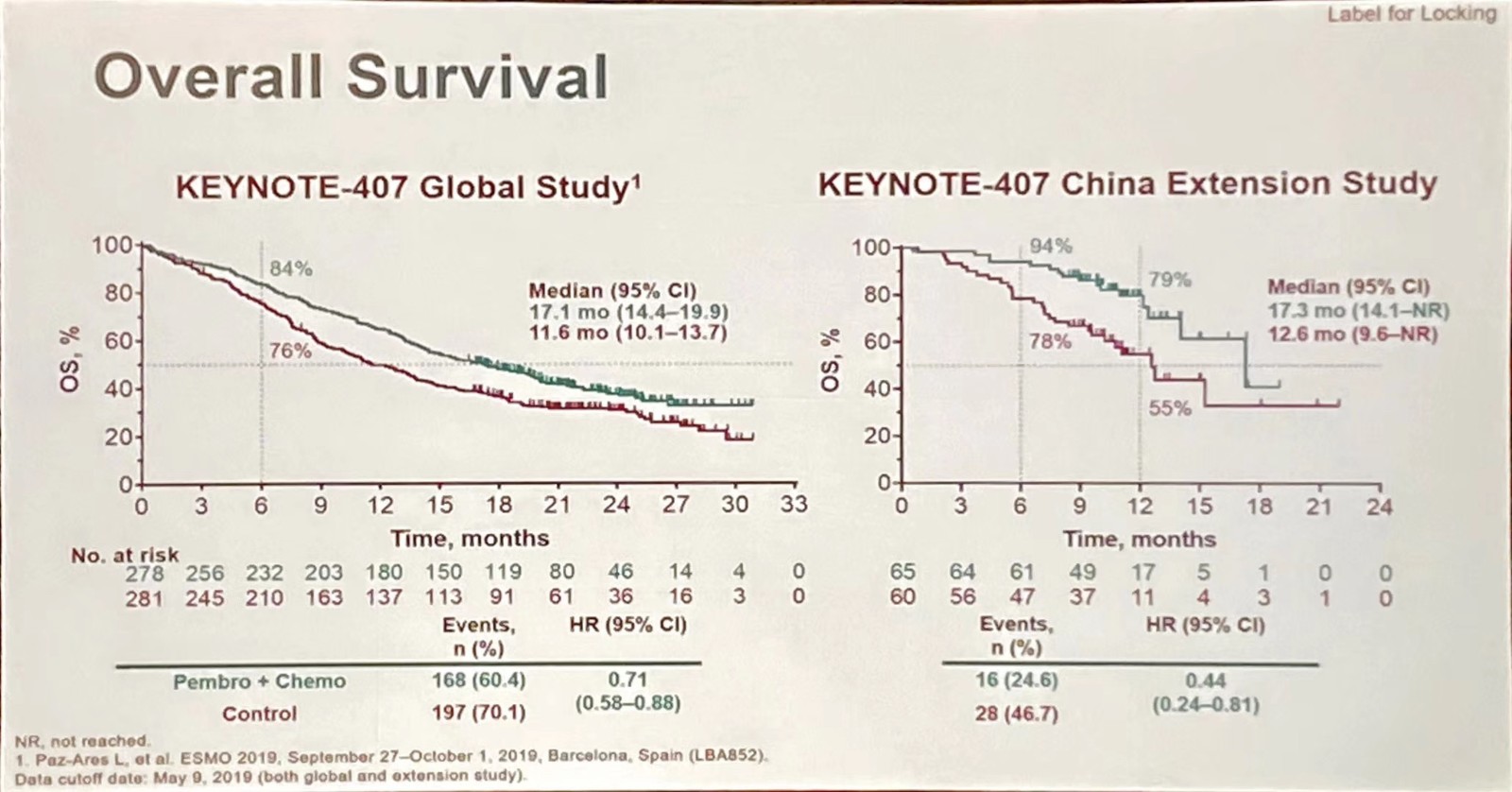
图2 KEYNOTE-407研究OS分析:全球数据和中国人群数据
帕博利珠单抗联合化疗同样显著改善患者的PFS,两组的中位PFS分别为8.3个月和4.2个月,疾病进展风险降低了68%,(HR=0.32,P<0.0001),与总人群结果相似(KEYNOTE-407总人群结果:中位PFS分别为8.0个月和5.1个月,HR=0.57)。6个月PFS为71%和34%,提高了37%(图3)。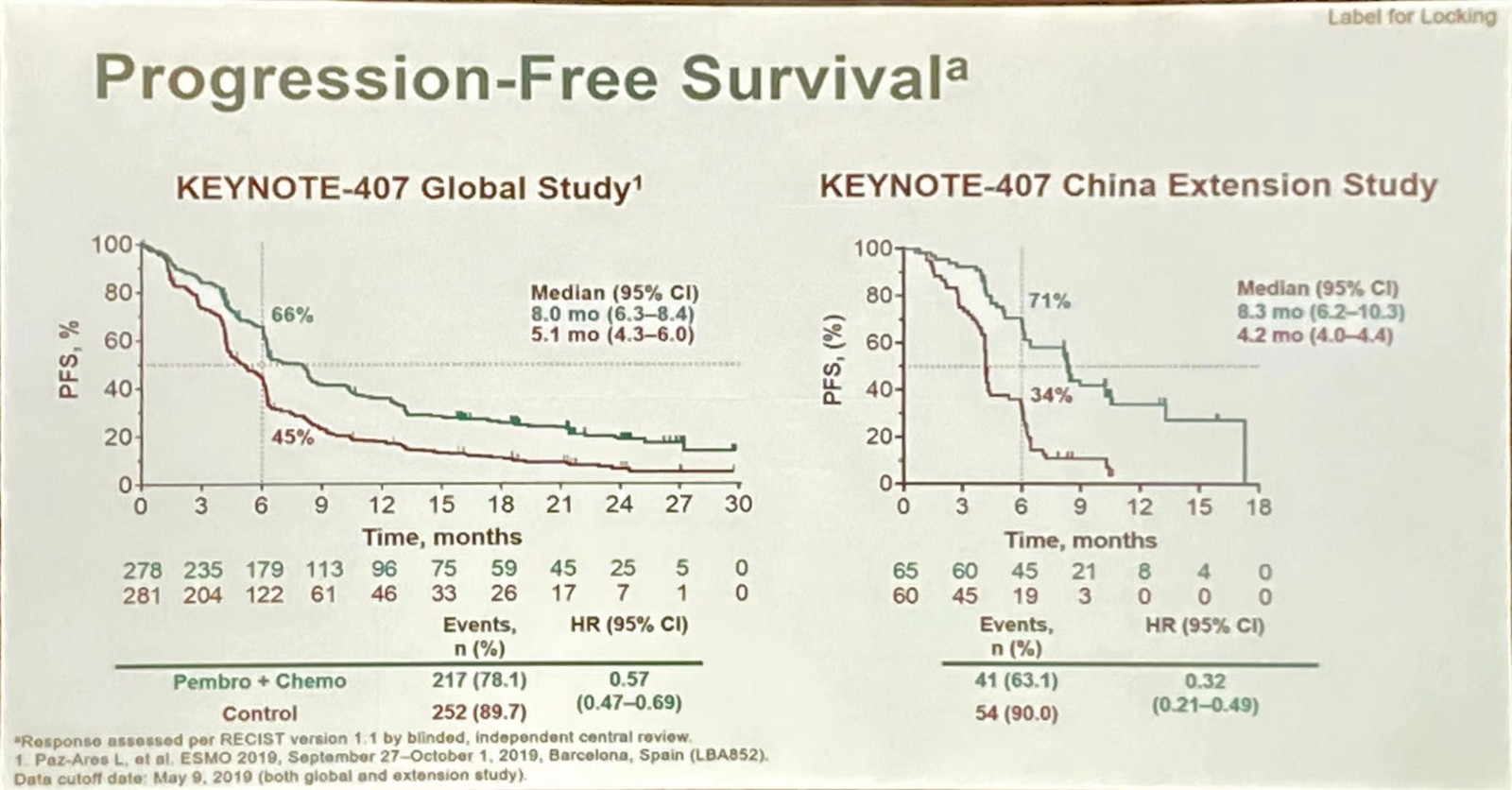
图3 图2 KEYNOTE-407研究PFS分析:全球数据和中国人群数据
除此之外,帕博利珠单抗联合化疗同样提高中国患者的ORR,分别为 78.5%和41.7%,提高了36.8%(总人群为62.6%和38.4%,提高了24.1%,图4)。
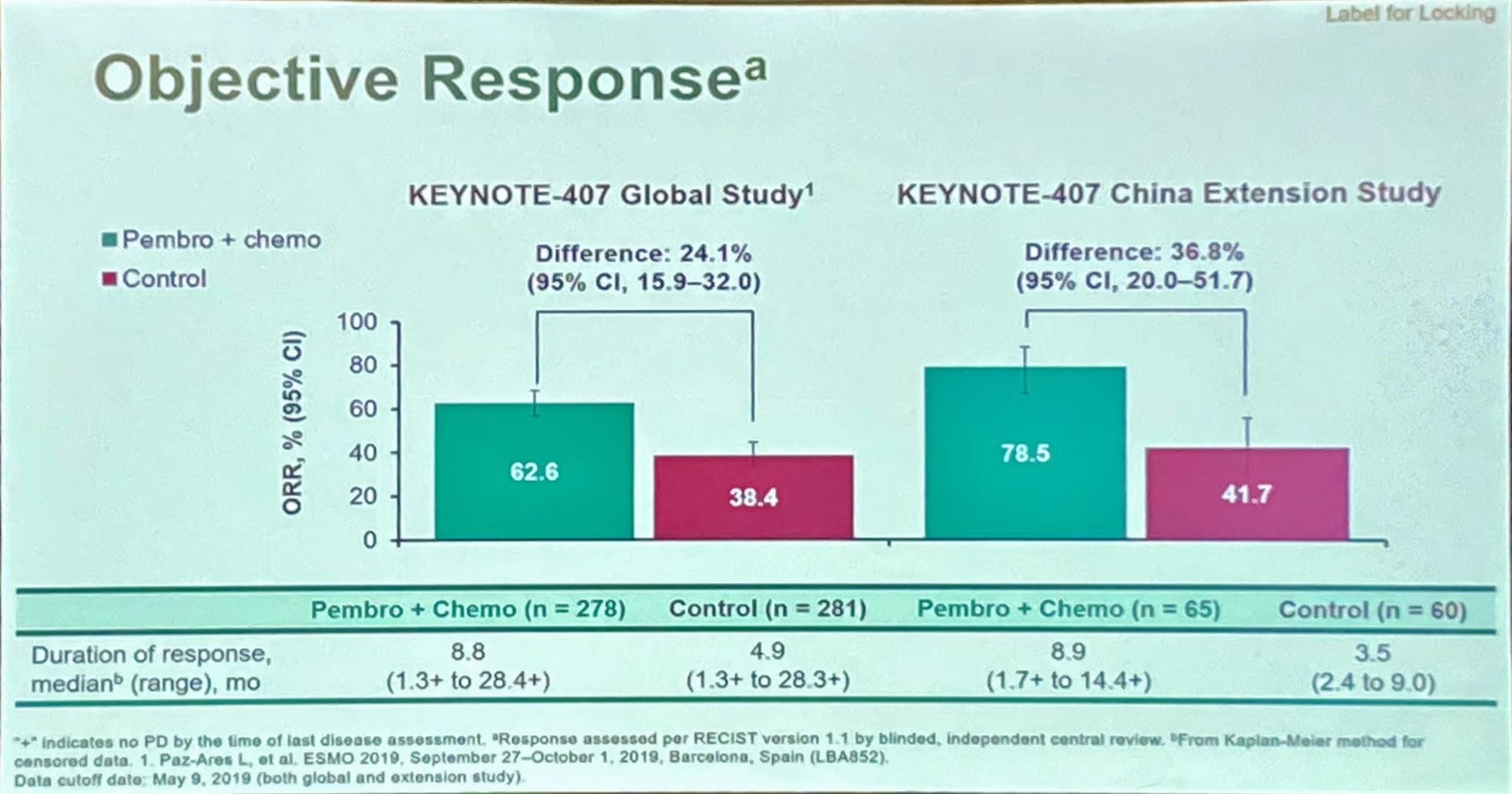
图4 KEYNOTE-407研究ORR分析:全球数据和中国人群数据
安全性方面,任何级别不良事件(AE)的发生率两组均为100%,3~5级AE两组相似,分别为89%和87%,中国人群最常见的免疫相关AE和输液反应为甲亢、甲减、输液反应、肌炎、肺炎、甲状腺炎、1型糖尿病,种类与总人群结果相似。
既往在晚期肺鳞癌的治疗上鲜有突破,能否请您介绍下晚期肺鳞癌的既往的治疗困境?KEYNOTE-407研究中国人群数据的公布将为中国晚期肺鳞癌患者的治疗带来怎样的影响?
程颖教授:2009年随着IPASS研究的正式发表,开启了人类抗肿瘤治疗的新篇章,也拉开了肿瘤精准靶向治疗的序幕。后续以EGFR、ALK和ROS-1等为靶点的靶向治疗药物相继出现,为晚期肺腺癌患者的治疗带来突破,腺癌患者生存期得到了极大的延长。但对于鳞癌患者,由于驱动基因尚不明确,极少有靶向治疗的机会。此外在一线治疗上,鳞癌患者也无法应用抗血管生成治疗。因此,长期以来,含铂双药化疗是晚期肺鳞癌患者的标准治疗,尽管有一些新的化疗药物,如奈达铂等药物的出现,但总体化疗疗效仍十分有限,有效率仅为30%左右,晚期肺鳞癌患者的中位生存时间仅1年左右,总体治疗停滞不前。
KEYNOTE-407研究的公布,帕博利珠单抗联合化疗作为一线治疗晚期肺鳞癌显著优于化疗,带来治疗的突破,这一研究结果也打破了肺鳞癌多年来没有进展的窘境,给肺鳞癌患者带来新的希望。而对于肿瘤内科医生而言,给肺鳞癌患者的治疗增加了一个新的治疗选择,可以说KEYNOTE-407是一个非常有价值、有意义的研究。
此次ESMO Asia会议上公布了KEYNOTE-407研究中国人群的数据,再一次证明了免疫治疗联合化疗在晚期肺鳞癌一线治疗中的疗效和安全性,为中国晚期肺鳞癌患者一线应用此方案提供了非常好的循证医学证据。如果中国药品监督管理局(NMPA)能够批准帕博利珠单抗联合化疗用于晚期肺鳞癌患者的一线治疗,对中国患者来说则具有重要的意义,中国肺鳞癌患者的一线治疗将进入免疫时代,在改变中国肺鳞癌患者治疗手段的同时,可以极大地延长鳞癌患者的生存时间,更好的获得生存获益,此外,也给中国医生提供一个新的治疗选择,为患者晚期肺鳞癌患者的一线治疗提供更好的治疗决策。
肺癌免疫治疗仍然是研究的热点和重点,对于免疫治疗未来的发展趋势,您又是如何看待的?
程颖教授:免疫检查点抑制剂的出现带来了肺癌治疗史上革命性突破,多次改写了临床指南,目前肺癌免疫治疗的主体格局基本形成。但是免疫治疗还有很多问题亟待解决,未来仍有很多需要探索的领域。
随着免疫治疗在临床应用越来越广泛,在关注疗效的同时,同样需要关注免疫相关性不良反应的管理;免疫治疗会产生超进展、假进展等特殊问题,需要制定免疫治疗相关的疗效评价标准;目前的标记物如PD-L1表达、TMB并不完美,对于免疫治疗,仍需要对最佳治疗人群、免疫治疗生物标记物进行探索;免疫治疗的耐药机制十分复杂,如何克服耐药也是需要更多探索的问题;不同的PD-1/PD-L1抑制剂,其疗效并不一样,临床医生应当依照循证医学证据用药;除了PD-1/PD-L1通路,对其他免疫治疗的相关通路也应当进行积极探索。
在精准医学指导下的免疫联合治疗可能是未来的发展趋势,通过biomarker筛选免疫治疗获益人群,重视肿瘤微环境因素,利用基因组学、免疫组学针对肿瘤细胞和肿瘤微环境中多个生物标记物的联合检测,可以加深对癌症免疫治疗的了解。免疫联合治疗策略可以通过增强肿瘤免疫原性、降低抑制性细胞活性、增强TILs浸润等来克服耐药,根据不同的耐药机制采用相应的联合治疗策略。目前免疫联合化疗、放疗、抗血管生成治疗等治疗模式已在临床中应用,PD-1/PD-L1单抗与其他免疫检查点抑制剂如CTLA-4单抗或OX40单抗、LAG-3单抗等联合应用是未来重要的研究方向。同时动态监测耐药机制对临床治疗决策有重要参考价值,在治疗过程中(治疗前、治疗期间和进展时)对肿瘤组织、血液、排泄物的微生物组学进行纵向评估、深入分析,可以揭示耐药的潜在机制,提前预知可能发生的获得性耐药并及时干预。免疫治疗未来需要基础医学、转化医学以及临床医生深入合作,共同深入挖掘耐药机制,寻找可靠生物标记物,采用最佳的联合模式并动态监测其疗效,实现免疫精准治疗。











 苏公网安备32059002004080号
苏公网安备32059002004080号


