2019年9月27日—10月1日,2019年欧洲肿瘤内科学会(ESMO)年会在西班牙巴塞罗那盛大召开。为了更好地照护癌症患者,诸多临床专家潜心钻研。2019年9月28日,媒体发布会公布三大研究的重磅结果,【肿瘤资讯】小编从前线带来最新报道。

LBA2——新诊断晚期卵巢癌患者含铂化疗+贝伐珠单抗治疗后以奥拉帕利+贝伐珠单抗维持治疗

报告者:Isabelle Ray-Coquard教授
贝伐珠单抗联合化疗序贯贝伐珠单抗维持治疗是多数新诊断晚期卵巢癌患者的一线标准治疗。奥拉帕利用于BRCA突变的晚期卵巢癌的一线维持治疗显示出前所未有的无进展生存(PFS)获益,而在铂敏感复发患者中,非BRCA突变者也有获益。PAOLA-1/ENGOT-ov25研究旨在一线接受含贝伐珠单抗标准治疗的晚期卵巢癌患者中(无论BRCA突变状态如何)评估PARP抑制剂的疗效和安全性,这是这方面的第一项Ⅲ期临床试验。
研究共计入组新诊断FIGO Ⅲ~Ⅳ期高级别浆液性卵巢癌、输卵管癌或原发性腹膜癌患者806例,这些患者经标准治疗后获得无疾病状态(NED)/完全缓解(CR)/部分缓解(PR),按2∶1随机入组接受奥拉帕利+贝伐珠单抗或安慰剂+贝伐珠单抗维持治疗。主要研究终点是研究者按RECIST V1.1评估的PFS,并由盲法独立审查委员会(BICR)进一步评估PFS,以进行敏感性分析。次要研究终点包括:至首次后续治疗的时间(TFST)、至二次进展时间(PFS2)、至二次后续治疗的时间(TSST)、总生存(OS)、健康相关生活质量(HRQoL)、安全性和耐受性。探索性终点包括根据BRCA突变状态和HRD评分进行的亚组PFS分析。
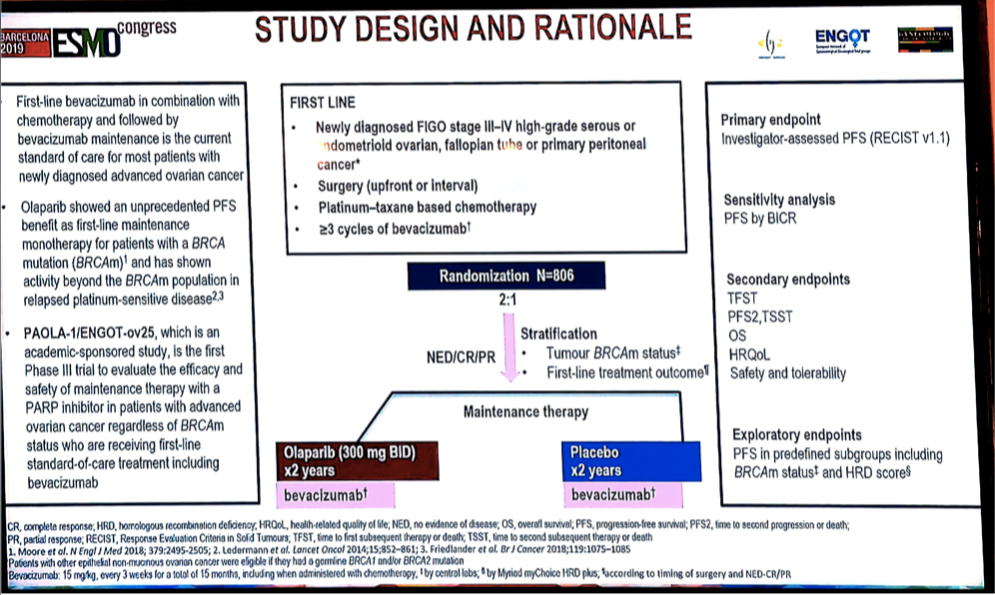
图1 研究设计
结果显示:奥拉帕利+贝伐珠单抗组对比安慰剂+贝伐珠单抗组,中位PFS分别为22.1个月和16.6个月(HR 0.59;95%CI 0.49~0.72;P<0.0001)。根据tBRCA突变状态进行亚组分层,奥拉帕利+贝伐珠单抗对比安慰剂+贝伐珠单抗,中位PFS分别为37.2个月和21.7个月(HR 0.31;95%CI 0.20~0.47);HRD阳性,包括tBRCA突变的亚组分析显示,两组PFS分别为37.2个月和17.7个月(HR 0.33;95%CI 0.25~0.45);HRD阳性,排除tBRCA突变的亚组分析显示,两组PFS分别为28.1个月和16.6个月(HR 0.43;95%CI 0.28~0.66)。
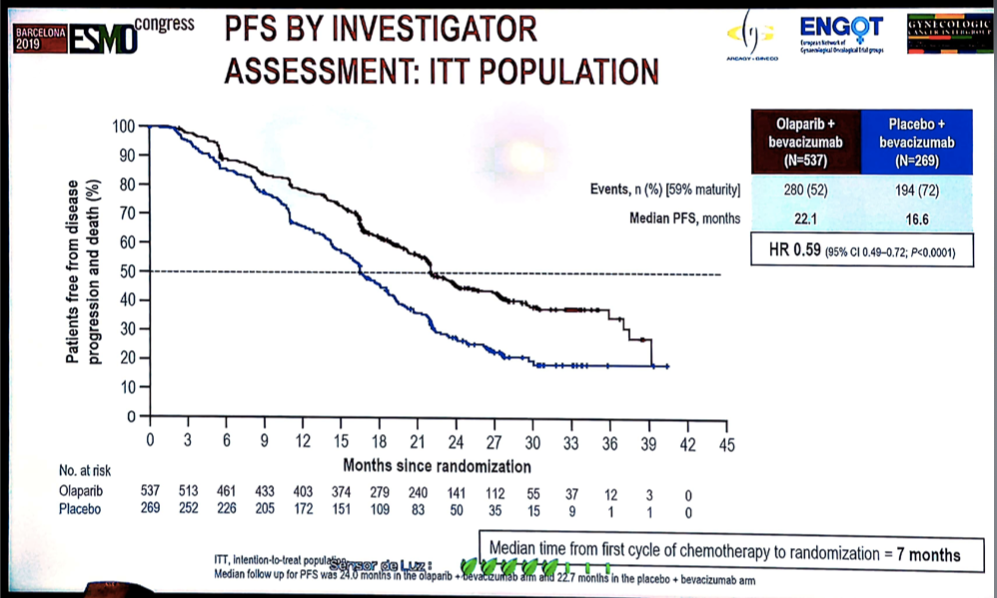
图2 ITT人群中位PFS结果
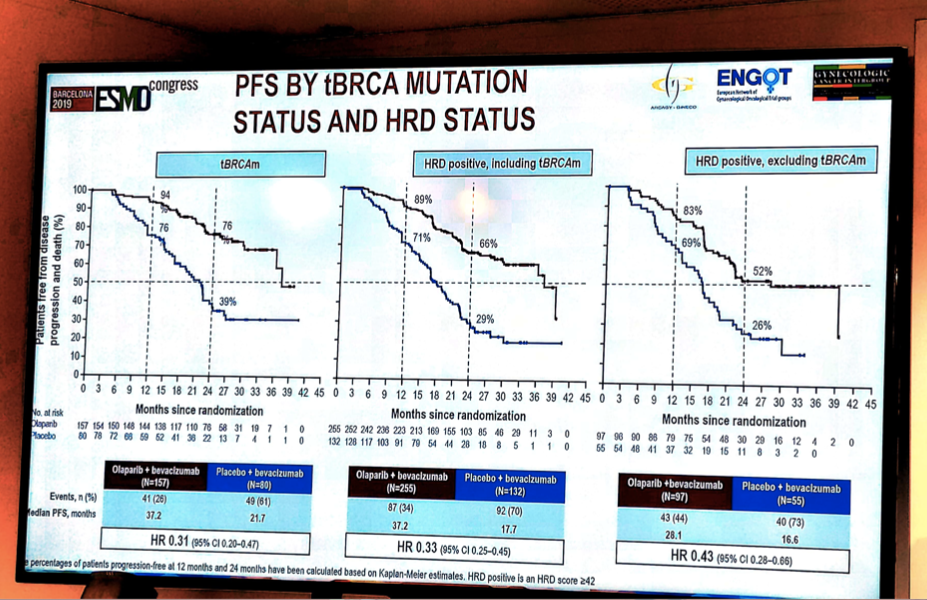
图3 不同tBRCA突变和HRD状态亚组分析
PAOLA-1/ENGOT-ov25研究达到主要研究终点,无论手术结果或者BRCA突变状态如何,ITT人群中,在标准的贝伐珠单抗一线维持治疗基础上加用奥拉帕利显著延长PFS。亚组分析显示tBRCA突变和HRD阳性患者PFS获益更多。奥拉帕利+贝伐珠单抗联合用药的安全性与以往试验结果基本一致,加用奥拉帕利并未影响患者对贝伐珠单抗的耐受性和生活质量。
LBA5——FLAURA研究:奥希替尼对比第一代EGFR-TKI(吉非替尼/厄洛替尼)用于EGFR突变阳性晚期NSCLC患者一线治疗的最终OS分析

报告者:Suresh S Ramalingam 教授
FLAURA研究设计:
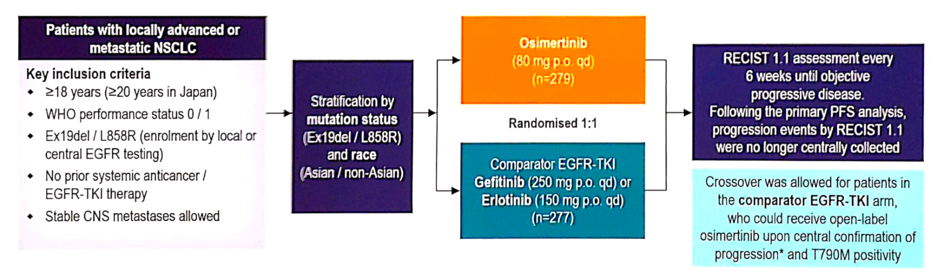
图4 FLAURA研究设计
研究结果显示,奥希替尼组和对照组的中位OS分别为38.6个月和31.8个月(HR 0.799,95%CI 0.641~0.997;P=0.0462)。
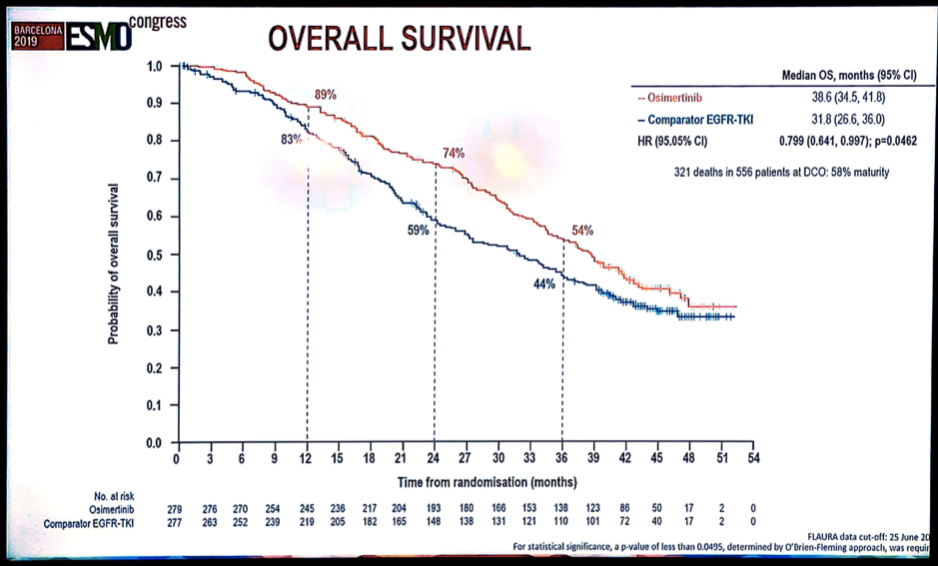
图5 FLAURA研究OS结果
研究者同样对各亚组OS结果进行了分析。如下图所示分别为OS亚组分析结果森林图以及亚洲、非亚洲患者的OS结果分析。
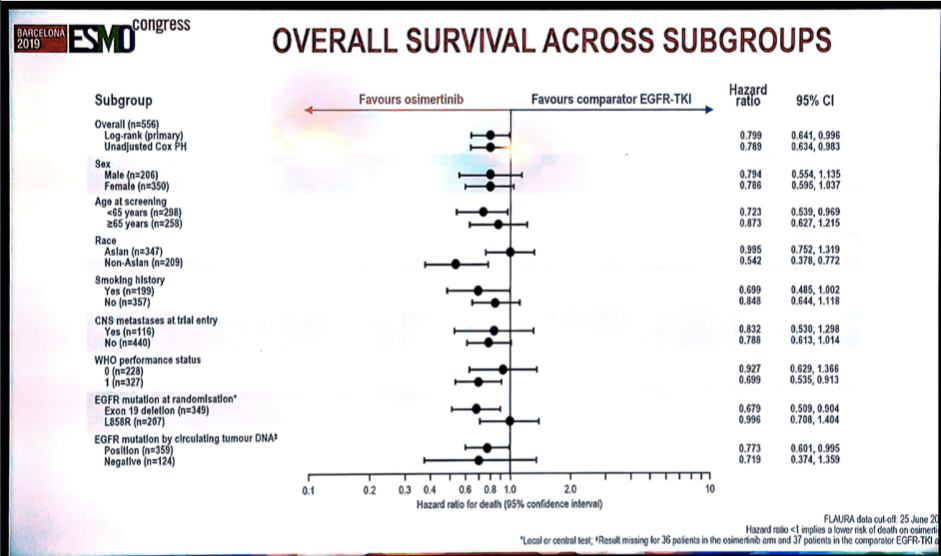
图6 FLAURA研究亚组分析森林图
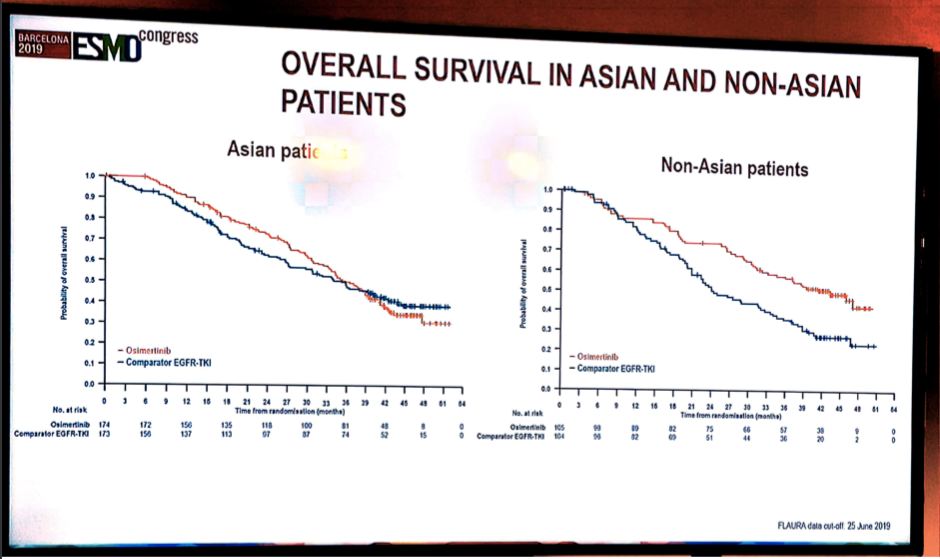
图7 FLAURA研究亚洲与非亚洲患者OS结果分析
FLAURA研究显示,奥希替尼对OS改善具有统计学意义及临床意义,奥希替尼组的中位OS显著延长6.8个月。对比其他EGFR-TKI,奥希替尼是首个能够获得显著OS改善的EGFR-TKI单药。目前随访时间超过3年,奥希替尼组的28%的患者和对照组9%的患者仍然在接受一线治疗。尽管经过了长时间的用药,奥希替尼仍显示出更好的安全性,未观察到意外的毒性。
LBA4——纳武利尤单抗联合低剂量ipilimumab对比含铂双药化疗一线治疗晚期非小细胞肺癌:CheckMate 227 Part 1最终分析

报告者:S. Peters教授
CheckMate 227研究是一项随机、开放标签Ⅲ期临床试验,研究以纳武利尤单抗为基础的治疗对比化疗,有两项独立的联合研究终点。既往结果显示,在TMB≥10mut/Mb人群中,与PD-L1表达无关的纳武利尤单抗+ipilimumab组的PFS终点达到。本次ESMO公布纳武利尤单抗+ipilimumab组对比化疗在肿瘤PD-L1≥1%人群中的主要终点OS,同时发布含纳武利尤单抗治疗患者,无论PD-L1表达水平的分析。
研究设计:入组患者为IV期或复发性NSCLC,未经系统治疗,无中枢神经系统转移,无EGFR突变或ALK突变,ECOG评分0~1分。第一部分,1a部分在PD-L1表达≥1%的患者中,评估纳武利尤单抗+低剂量ipilimumab、纳武利尤单抗单药与化疗的疗效;1b部分在PD-L1表达<1%的患者中,评估纳武利尤单抗+低剂量ipilimumab、纳武利尤单抗联合化疗与化疗的疗效。治疗直至疾病进展、不可接受的毒性或免疫治疗达到两年。
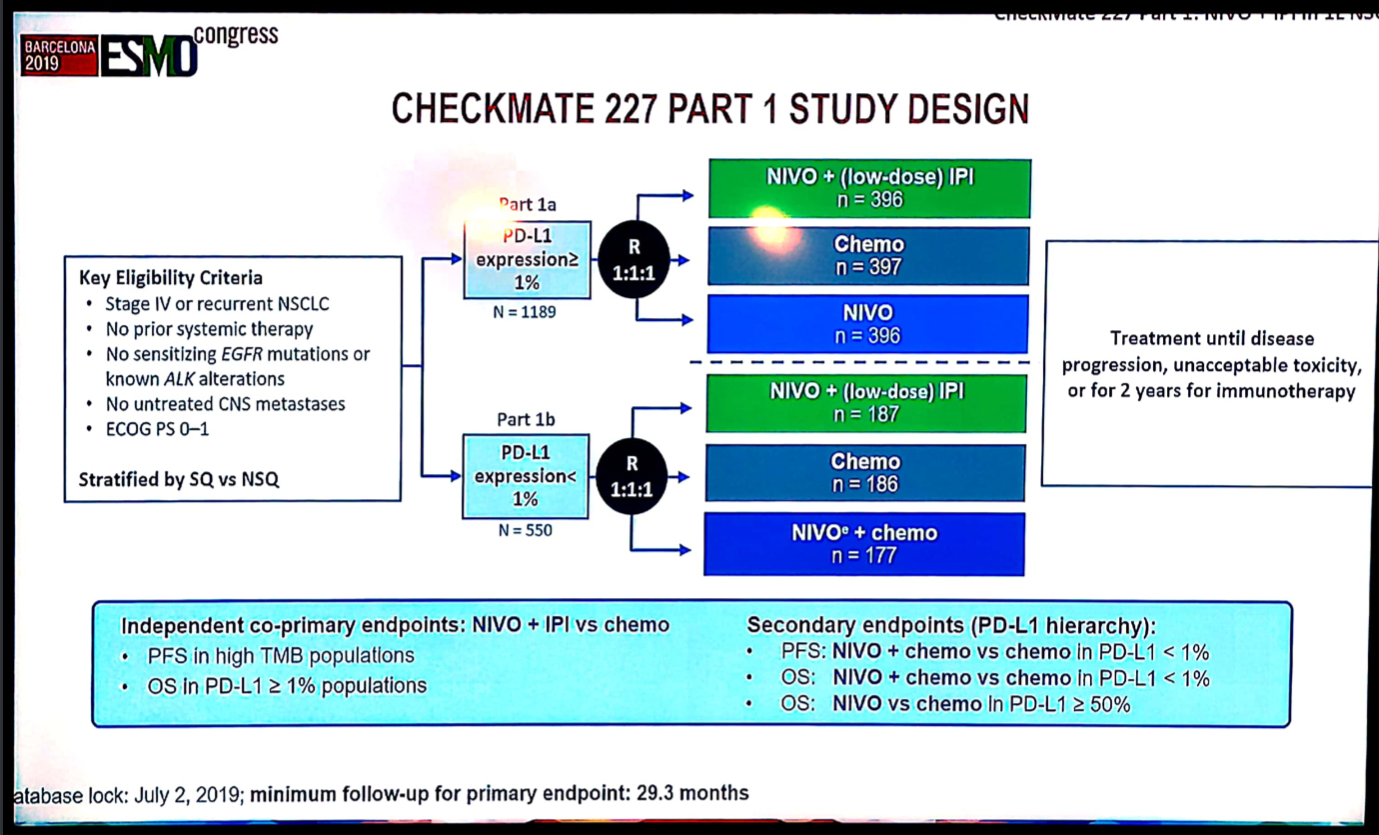
图8 CheckMate 227研究第一部分研究设计
主要终点:PD-L1表达≥1%的患者中,纳武利尤单抗+低剂量ipilimumab对比化疗,两组中位OS分别为17.1个月和14.9个月(HR=0.79;95%CI 0.65~0.96;P=0.007)。在PD-L1≥1%的患者中,纳武利尤单抗+ipilimumab、纳武利尤单抗单药和化疗组的中位OS分别为17.1个月、15.7个月和14.9个月,中位DOR分别为23.2个月、15.5个月和6.2个月。
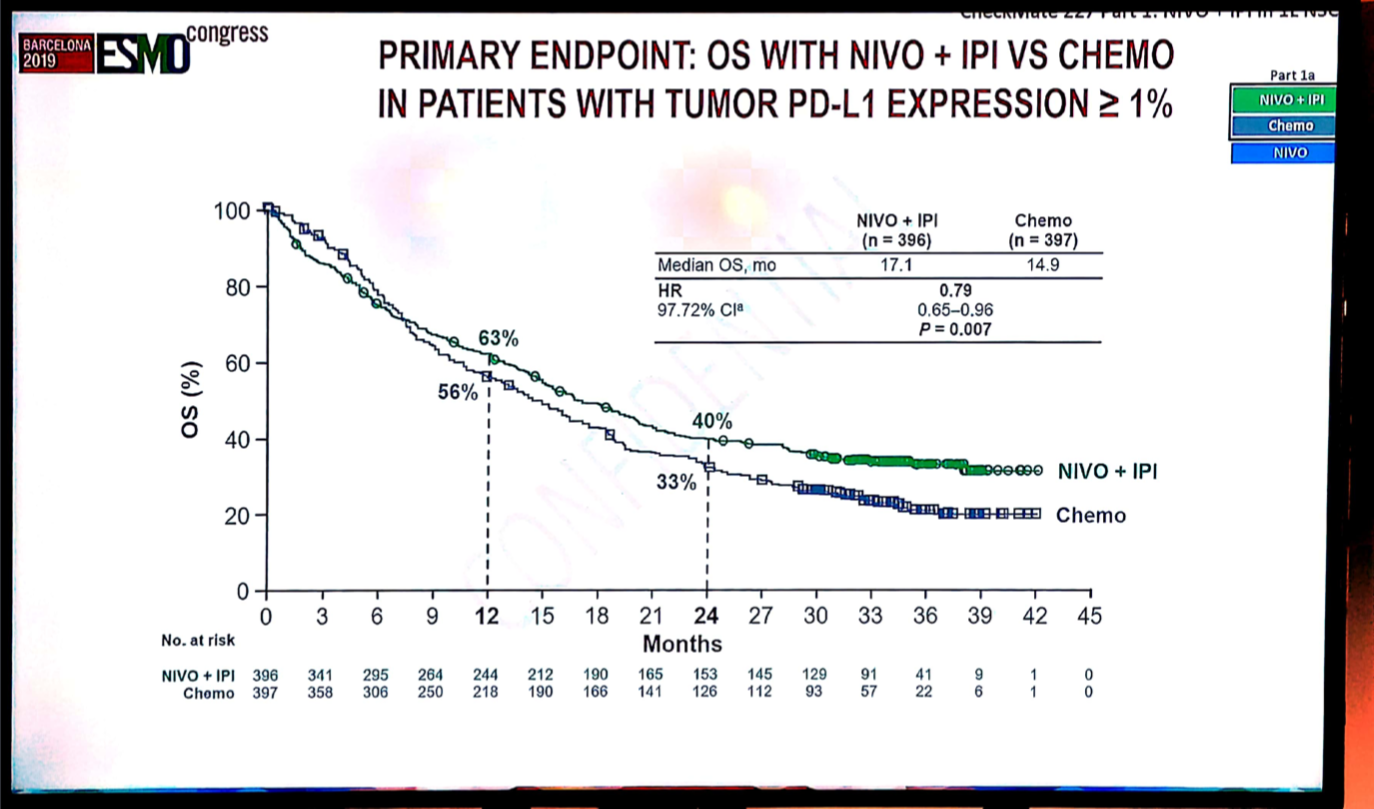
图9 CheckMate 227研究第1部分PD-L1表达≥1%的患者中,纳武利尤单抗+ipilimumab对比化疗
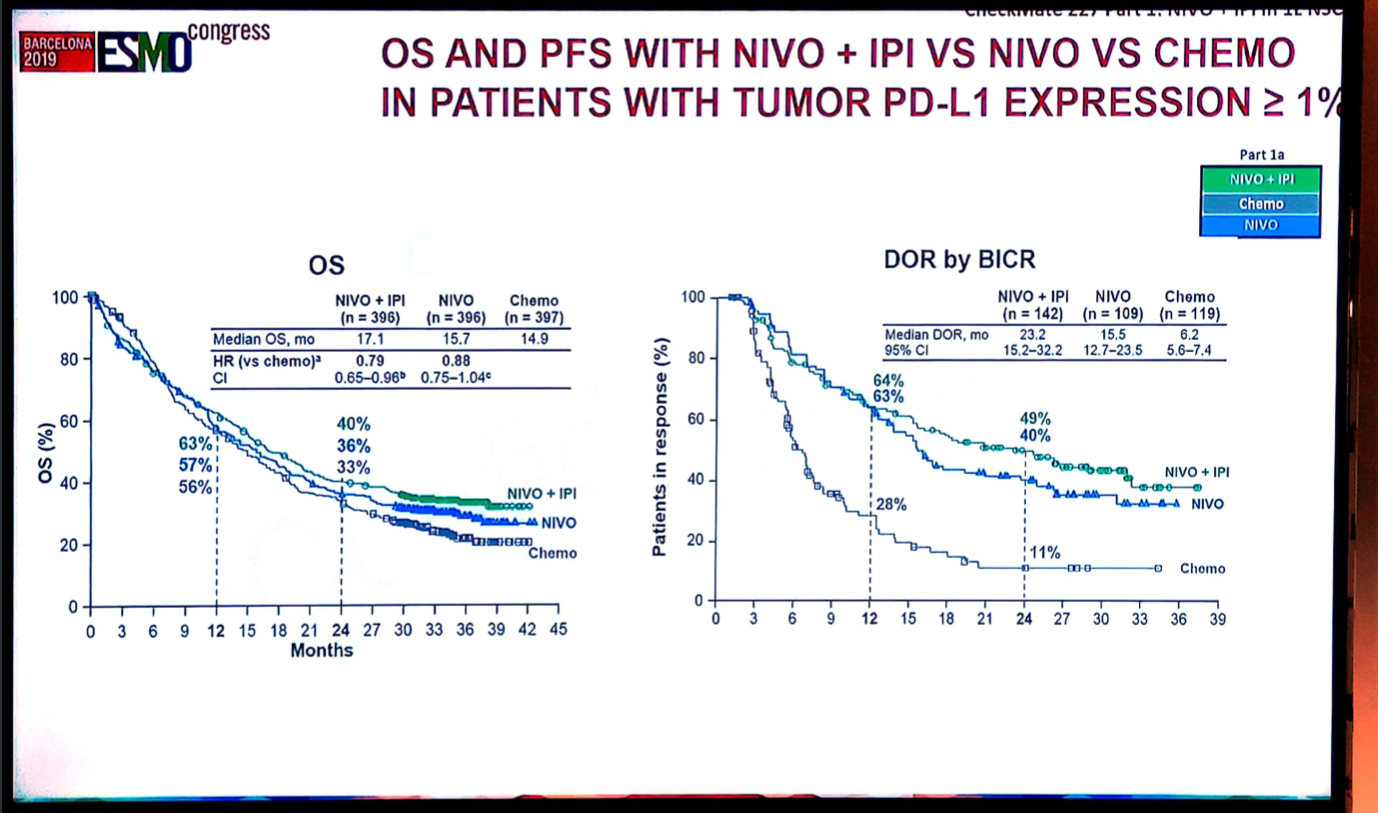
图10 CheckMate 227研究第一部分PD-L1表达≥1%患者比较
在PD-L1<1%的患者中,纳武利尤单抗+低剂量ipilimumab、纳武利尤单抗联合化疗和化疗组的中位OS分别为17.2个月、15.2个月和12.2个月。
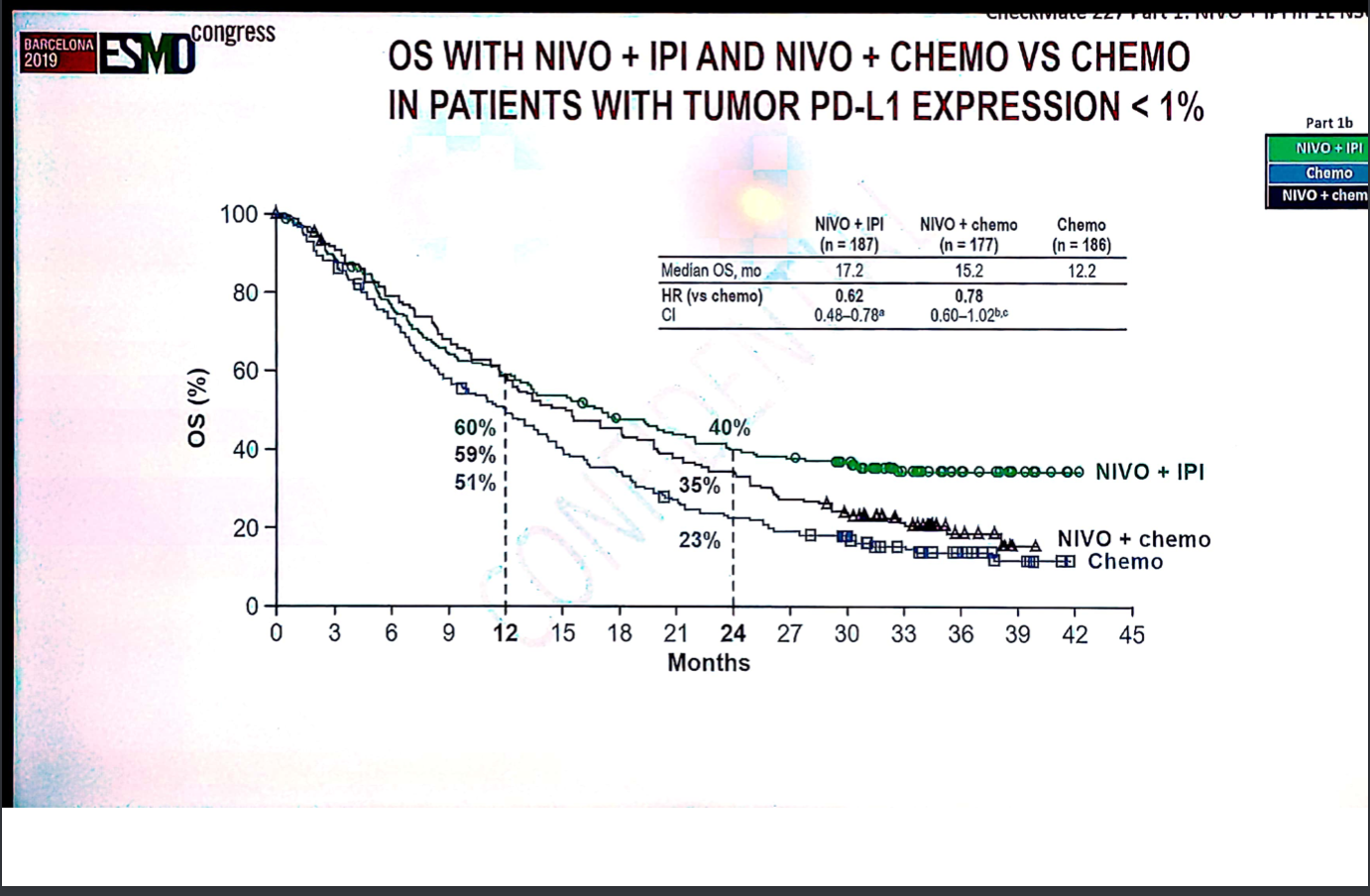
图11 CheckMate 227研究第一部分PD-L1<1%的患者三组OS比较
CheckMate 227研究中PD-L1≥1%的患者人群达到主要研究终点OS,这是第一项显示PD-1单抗与CTLA-4单抗联合一线治疗NSCLC有效的III期临床试验。根据PD-L1状态的不同,对比化疗,PD-1单抗联合CTLA-4单抗能够带来具有临床意义的OS延长。这种免疫联合给晚期NSCLC患者一线治疗带来新的选择机会。
【肿瘤资讯】小编将持续从西班牙巴塞罗那为您报道2019 ESMO盛况,敬请关注!
责任编辑:肿瘤资讯-Ervin












 苏公网安备32059002004080号
苏公网安备32059002004080号


