
随着中国女性乳腺癌发病率的持续性升高,晚期乳腺癌患者的人群也逐年增加。其中很大一部分人群是HR+/HER2-的患者,内分泌治疗是这类患者重要的,并且非常有效的治疗手段。近年来,HR+/HER2-晚期乳腺癌内分泌治疗领域的最大进展,无疑是CDK4/6抑制剂联合内分泌治疗。

重庆大学附属肿瘤医院/重庆市肿瘤医院/乳腺肿瘤中心副主任
中华医学会肿瘤学分会乳腺肿瘤青年学组委员
重庆市医学会肿瘤学专业委员会乳腺癌学组委员兼秘书
重庆市抗癌协会肿瘤心脏病学专业委员会委员
重庆市医院协会肿瘤学管理专业委员会委员
德国杜塞尔多夫欧洲乳腺中心访问学者
背景
目前国外已经上市三种CDK4/6抑制剂(Palbociclib、Ribociclib及Abemaciclib),大量的研究已经显示CDK4/6抑制剂联合内分泌治疗,可以给患者带来明显的PFS获益,但是尚未观察到整体OS的获益。在2018年ESMO大会上,PALOMA-3研究公布了OS数据,首次报道了CDK4/6抑制剂用于HR+/HER2-晚期乳腺癌Ⅲ期临床试验的OS数据。但遗憾的是,PALOMA-3研究中接受CDK4/6抑制剂联合内分泌治疗的患者,与单用内分泌治疗的患者相比较,整体OS呈获益趋势,但差异尚未达到统计学意义。最近,MONALEESA-7研究结果显示:Ribociclib联合内分泌治疗带来显著的整体OS获益。本文将对PALOMA-3和MONALEESA-7研究进行联合分析。
PALOMA-3研究
PALOMA-3研究是一项前瞻性、全球、随机、安慰剂对照的III期研究,对比氟维司群+Palbociclib和氟维司群+安慰剂,治疗既往接受过内分泌治疗进展后的HR+/HER2-晚期乳腺癌。患者按2:1的比例随机分配接受氟维司群+Palbociclib或氟维司群+安慰剂治疗。分层因素包括既往内分泌治疗敏感性、内脏转移状态、月经状态。研究者评估的PFS(既往已有报道)是主要终点,而OS是既定的次要终点,定义为随机至任意原因导致的患者死亡。
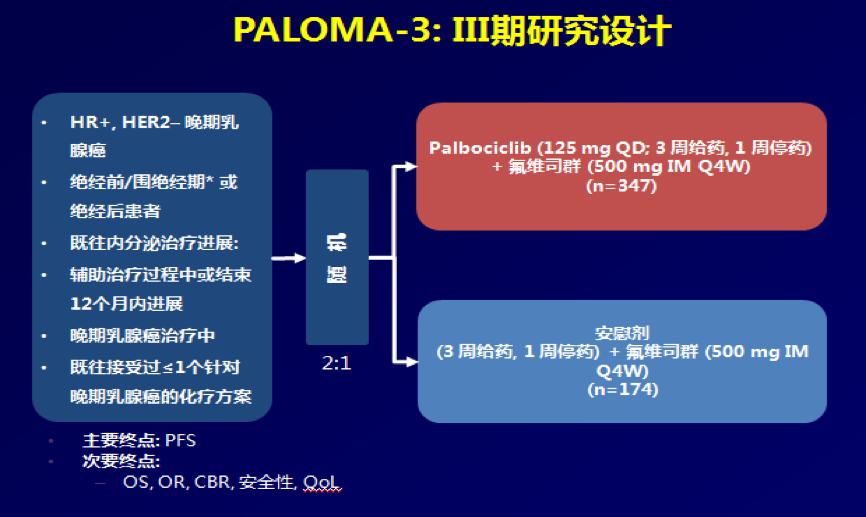
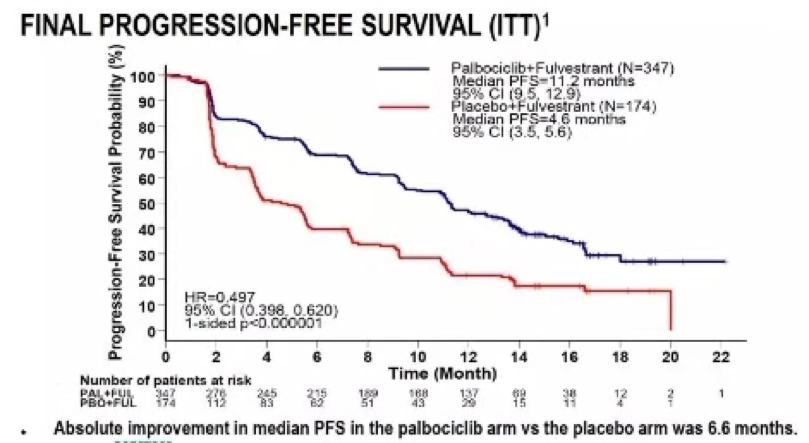
PALOMA-3研究共入组521例患者(定义为ITT人群),其中氟维司群+Palbociclib组347例,氟维司群+安慰剂组174例。更新的PFS结果与既往报道结果一致,与氟维司群+安慰剂组相比,氟维司群+Palbociclib组PFS得到显著延长,mPFS分别为11.2个月、4.6个月,HR 0.497;95%CI:0.398~0.620,P<0.000001(见下图)。
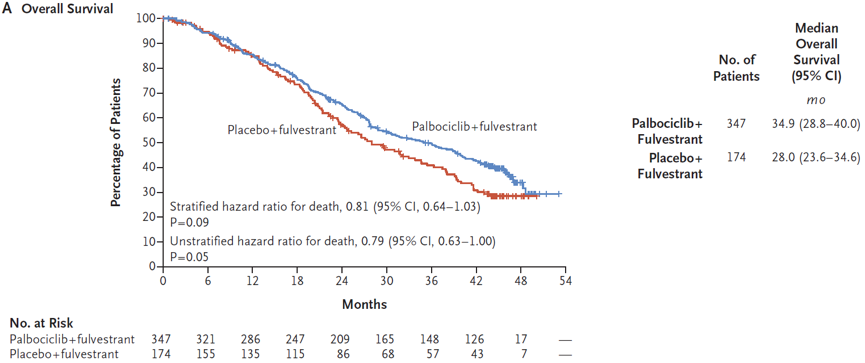
 OS分析的截止日期为2018年4月13日,中位随访时间为44.8个月,入组的521例患者中,310例患者死亡。氟维司群+Palbociclib组和氟维司群+安慰剂组分别有201例和109例患者死亡,两组的mOS分别为34.9个月、28.0个月,HR 0.81;95%CI:0.64~1.03;P=0.09,OS绝对获益6.9个月(见下图)。预计的3年OS率,两组分别为50%和41%。
OS分析的截止日期为2018年4月13日,中位随访时间为44.8个月,入组的521例患者中,310例患者死亡。氟维司群+Palbociclib组和氟维司群+安慰剂组分别有201例和109例患者死亡,两组的mOS分别为34.9个月、28.0个月,HR 0.81;95%CI:0.64~1.03;P=0.09,OS绝对获益6.9个月(见下图)。预计的3年OS率,两组分别为50%和41%。
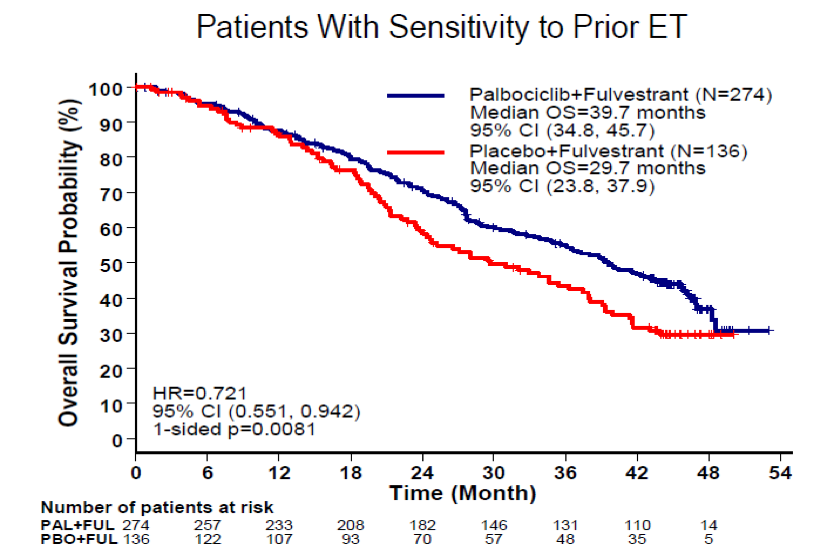
 根据既往内分泌治疗敏感性、内脏转移状态、和绝经状态3个既定的分层因素进行亚组分析。既往内分泌治疗敏感的410例患者中,氟维司群+Palbociclib组和氟维司群+安慰剂组的mOS分别为39.7个月、29.7个月,HR 0.72;95%CI:0.55~0.94,OS绝对获益达到10个月。既往内分泌耐药的患者有111例,mOS分别为20.2个月、26.2个月,HR 1.14;95%CI:0.71~1.84;P=0.30。
根据既往内分泌治疗敏感性、内脏转移状态、和绝经状态3个既定的分层因素进行亚组分析。既往内分泌治疗敏感的410例患者中,氟维司群+Palbociclib组和氟维司群+安慰剂组的mOS分别为39.7个月、29.7个月,HR 0.72;95%CI:0.55~0.94,OS绝对获益达到10个月。既往内分泌耐药的患者有111例,mOS分别为20.2个月、26.2个月,HR 1.14;95%CI:0.71~1.84;P=0.30。
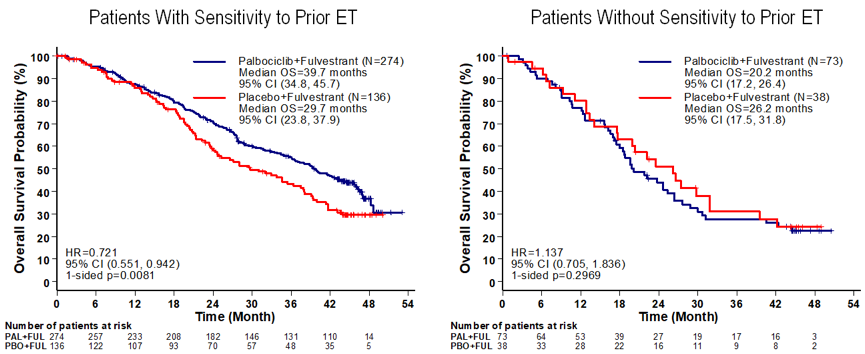
在PALOMA-3的研究结果显示,氟维司群+Palbociclib较之氟维司群+安慰剂可以带来6.9个月的OS绝对延长。这与氟维司群+Palbociclib治疗显著延长的PFS结果相符,而在既往内分泌治疗敏感的人群中,则观察到OS有10个月的延长,HR=0.72,单侧P=0.0081。
MONALEESA-7研究
MONALEESA-7研究是一项全球、随机、双盲、安慰剂对照的III期研究,对比了Ribociclib和安慰剂联合内分泌治疗用于绝经前或围绝经期HR+/HER2-晚期乳腺癌。患者1:1随机分配接受Ribociclib(600mg,每天口服,连续使用21天后停药7天,28天为1个周期)或安慰剂治疗。两组患者均同时接受戈舍瑞林治疗,并且同时接受非甾体类AI(阿那曲唑或来曲唑)或他莫昔芬治疗,两组患者不允许交叉。
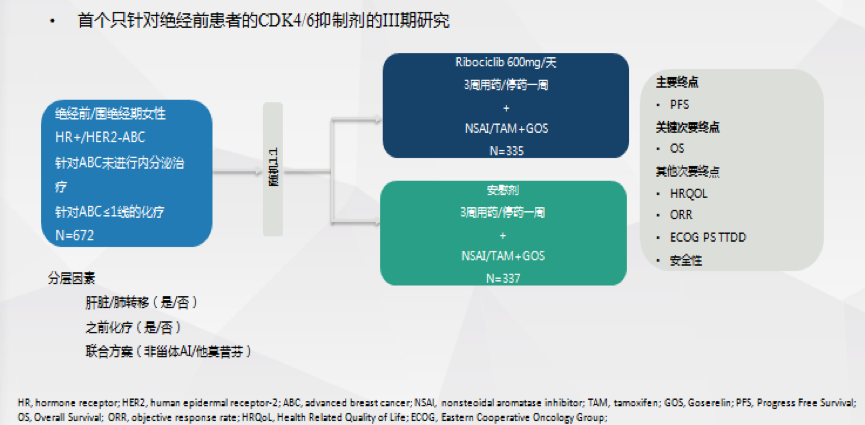
研究共入组晚期患者672例,1:1随机分配进入Ribociclib组(n=335)或安慰剂组(n=337),两组均以他莫昔芬(20 mg/d)+OFS或NSAI(来曲唑2.5mg/d,阿那曲唑1mg/d)+OFS为基础用药。分层因素包括是否合并肝脏或肺转移、晚期阶段是否接受过化疗以及入组后的内分泌治疗方案(他莫昔芬或非甾体AI)。主要研究终点为研究者评估的PFS,既往已经报道,重要的次要终点为OS。
研究结果显示,ribociclib组和安慰剂组42个月的OS率分别为70.2%和46.0%(表1)。ribociclib组对比安慰剂组,可以显著延长患者OS,两组的mOS分别为NE、40.9个月;降低了29%的死亡风险(HR 0.71;95%CI:0.54~0.95;P=0.00973;图1A)。在495例接受AI治疗的患者中,ribociclib组和安慰剂组分别有24.6%(61/248)和32.4%(80/247)的患者死亡,预估42个月的OS率,两组分别为69.7%和43.0%(HR 0.70;95%CI:0.50~0.98;图1B)。在177例接受他莫昔芬治疗的患者中,ribociclib组和安慰剂组分别有25.3%(22/87)和32.2%(29/90)的患者死亡,预估42个月的OS率,两组分别为71.2%和54.5%(HR 0.79;95%CI:0.45~1.38;图1C)。
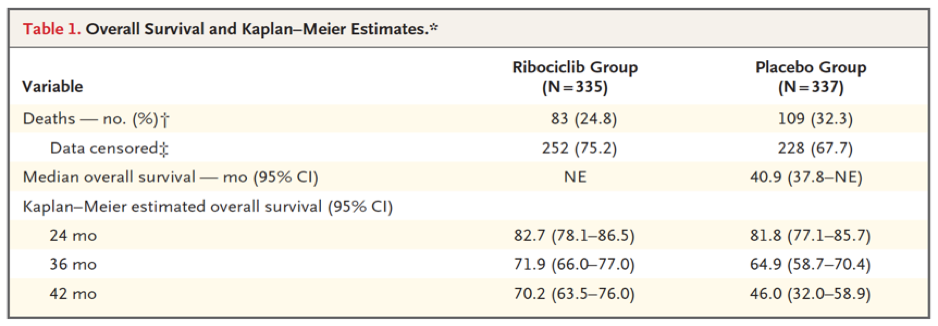
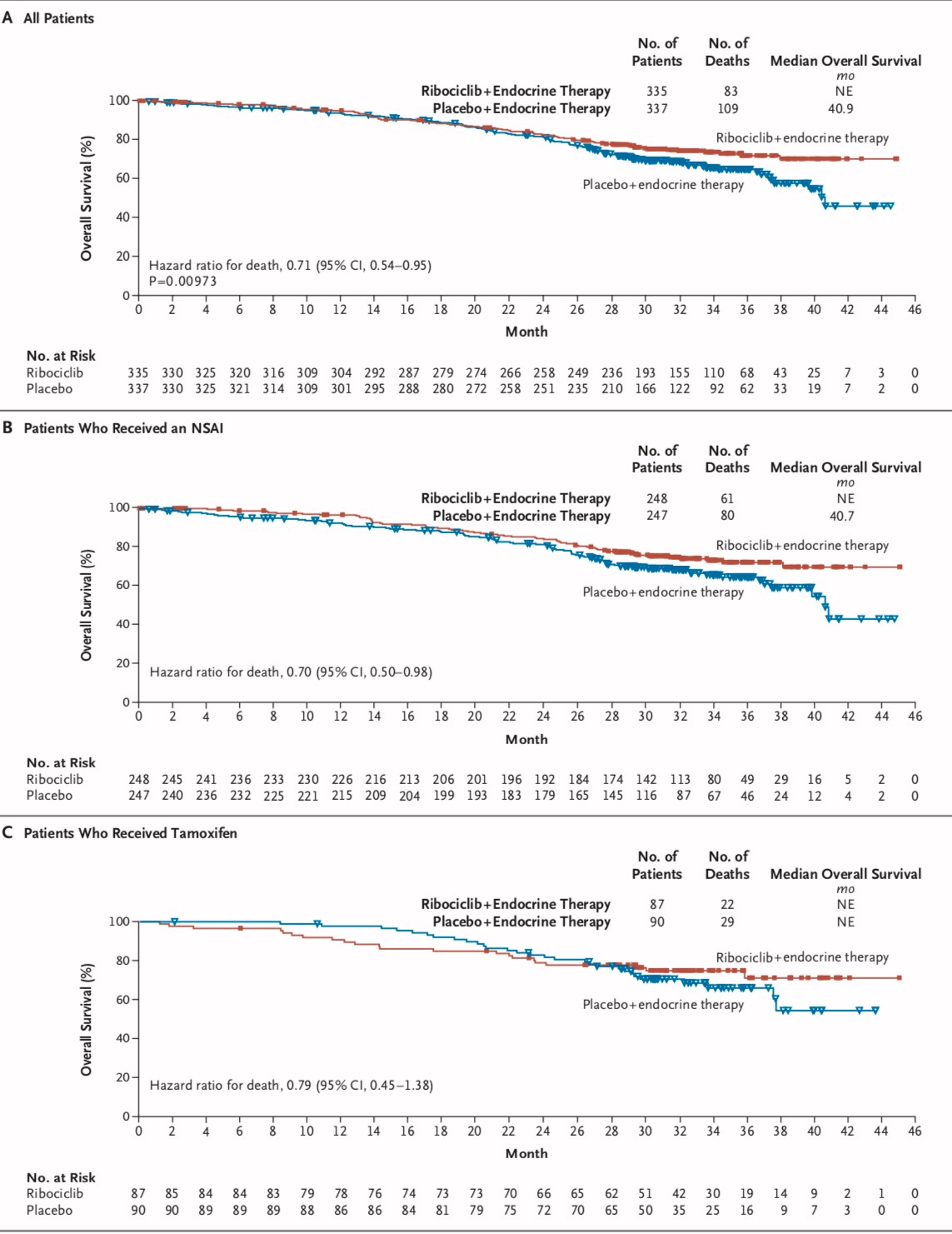
MONALEESA-7研究显示,ribociclib+内分泌治疗相比于单纯内分泌治疗,可以显著延长HR+/HER2-晚期乳腺癌的OS。在接受AI治疗的亚组中,ribociclib+内分泌治疗带来的获益与总体人群相似。
联合分析PALOMA-3和MONALEESA-7研究
为什么以上两个研究会得出不同的结果呢?我们知道,不同的入组人群及后续治疗情况会导致迥异的OS研究结果。为了深入分析导致不同结果的原因,我们将两个研究的后续治疗情况及入组人群进行了仔细的对比!
首先就入组人群而言:两个研究分别入组521例和672例HR+/HER2- 晚期乳腺癌。PALOMA-3研究的入组人群是既往内分泌失败的患者【辅助治疗(AI或他莫昔芬)期间或辅助治疗结束≤12个月进展,晚期疾病进展或AI/其他内分泌治疗结束≤1个月】,也就是说包含内分泌治疗原发性耐药和继发性耐药的患者(表2);而MONALEESA-7研究纳入的人群是针对晚期乳腺癌未进行内分泌治疗的患者,也就是一线内分泌解救的患者(表2)。另外,PALOMA-3研究的入组人群中有34%的患者接受过解救化疗(表2),而MONALEESA-7研究纳入的人群中仅仅只有14%的患者接受过解救化疗(表2)。因此,我们得出的结论是:PALOMA-3研究纳入的人群病期更晚,并且均为内分泌治疗耐药,包括原发性(辅助内分泌治疗2年内复发)和继发性内分泌耐药;而MONALEESA-7研究的入组人群均是一线内分泌解救的患者,病期较早。从两个研究对照组的mOS数据也可以得到验证(PALOMA-3对照组:mOS为28月,MONALEESA-7对照组:mOS为40.9月)
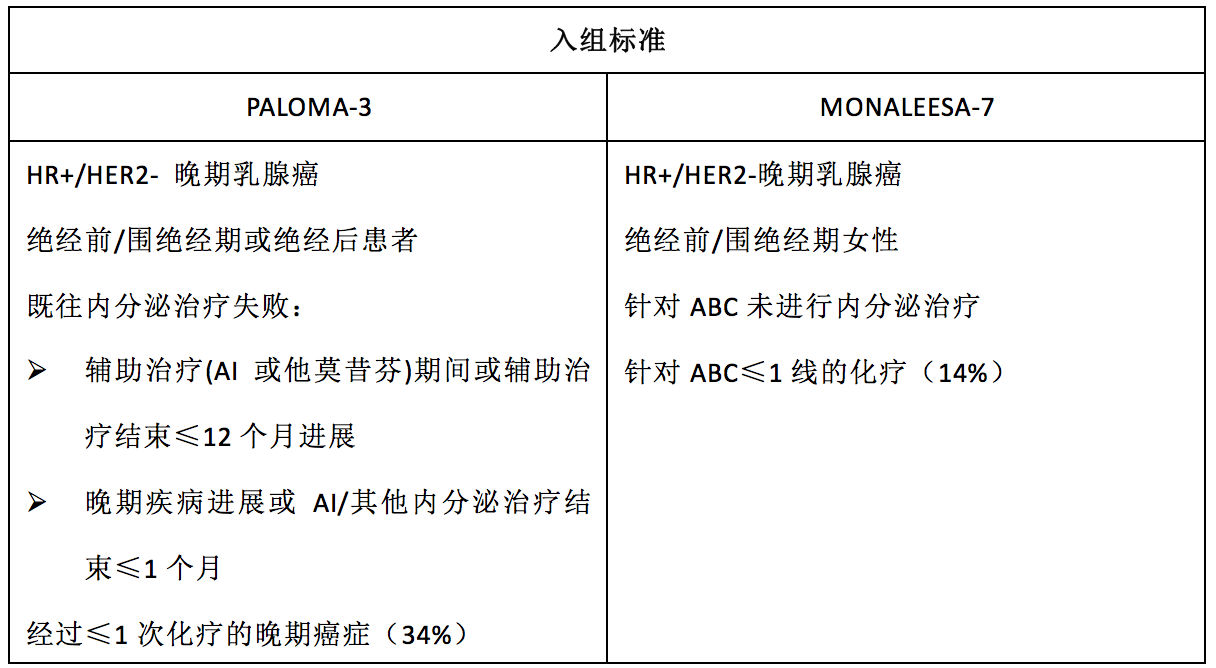
表2 PALOMA-3和MONALEESA-7研究入组标准对比
发现两个研究入组人群的差异后,我们再对两个研究的结果进行联合分析。PALOMA-3研究中定义的既往内分泌敏感是在辅助性内分泌治疗的24个月后复发,或晚期治疗阶段对先前的疗法有临床获益的患者,更类似于内分泌治疗继发耐药的患者。氟维司群+Palbociclib较之氟维司群+安慰剂,在整体人群中带来6.9个月的OS绝对延长,但差异并没无统计学意义。在既往内分泌治疗敏感的人群中,氟维司群+Palbociclib较之氟维司群+安慰剂,OS有10个月的延长(39.7月 vs 29.7月),差异有统计学意义(HR 0.72,95%CI:0.55~0.94,P=0.0081)。(见下图)
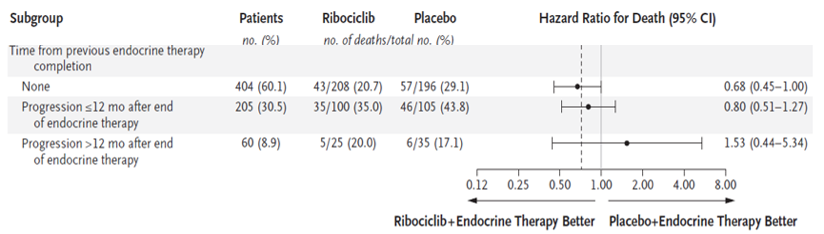
 而MONALEESA-7研究中定义的既往内分泌敏感是完成辅助内分泌治疗后12个月后复发。结果显示:ribociclib+内分泌治疗相比于单纯内分泌治疗,可以显著延长HR阳性HER2阴性晚期乳腺癌的总体人群的OS,差异有统计学意义;并且在接受AI治疗的亚组中,ribociclib+内分泌治疗带来的获益也与总体人群相似。我们再依据距以前内分泌治疗结束时间进行分层,发现未经过任何内分泌治疗(包括辅助治疗阶段)的亚组有404例(60.1%)、辅助内分泌治疗结束12月以内复发(继发性耐药)的亚组有205例(30.5%)、辅助内分泌治疗结束12个月后复发(内分泌敏感)的亚组有60例(8.9%)。分层分析发现:仅未经过任何内分泌治疗的亚组,OS获益具有统计学意义;辅助内分泌治疗结束12个月以内复发的亚组,ribociclib+内分泌组OS仅有获益趋势;而辅助内分泌治疗结束12个月后复发的亚组,ET+OFS组OS有获益趋势,当然这可能与亚组样本量较小有关。(见下图)
而MONALEESA-7研究中定义的既往内分泌敏感是完成辅助内分泌治疗后12个月后复发。结果显示:ribociclib+内分泌治疗相比于单纯内分泌治疗,可以显著延长HR阳性HER2阴性晚期乳腺癌的总体人群的OS,差异有统计学意义;并且在接受AI治疗的亚组中,ribociclib+内分泌治疗带来的获益也与总体人群相似。我们再依据距以前内分泌治疗结束时间进行分层,发现未经过任何内分泌治疗(包括辅助治疗阶段)的亚组有404例(60.1%)、辅助内分泌治疗结束12月以内复发(继发性耐药)的亚组有205例(30.5%)、辅助内分泌治疗结束12个月后复发(内分泌敏感)的亚组有60例(8.9%)。分层分析发现:仅未经过任何内分泌治疗的亚组,OS获益具有统计学意义;辅助内分泌治疗结束12个月以内复发的亚组,ribociclib+内分泌组OS仅有获益趋势;而辅助内分泌治疗结束12个月后复发的亚组,ET+OFS组OS有获益趋势,当然这可能与亚组样本量较小有关。(见下图)
 其次就后续治疗情况而言,PALOMA-3中安慰剂+氟维司群组有16%的患者在后续治疗中接受了CDK4/6抑制剂的治疗(见下表),即CDK4/6抑制剂对安慰剂+氟维司群组的OS存在一定贡献,从而影响最终的结果。
其次就后续治疗情况而言,PALOMA-3中安慰剂+氟维司群组有16%的患者在后续治疗中接受了CDK4/6抑制剂的治疗(见下表),即CDK4/6抑制剂对安慰剂+氟维司群组的OS存在一定贡献,从而影响最终的结果。
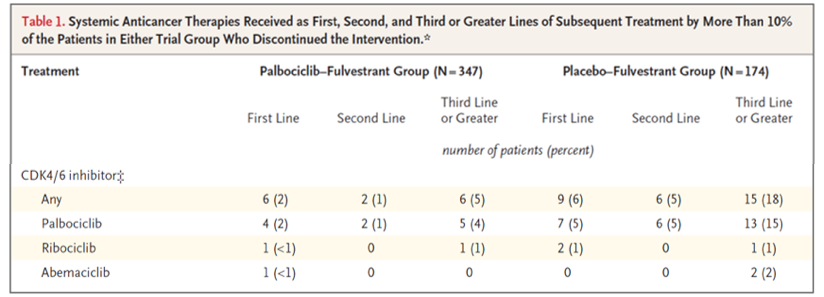
将PALOMA-3和MONALEESA-7研究进行联合分析后发现,两个研究OS获益结果的差异主要来自于研究入组人群的差异。既往涉及3个CDK4/6抑制剂的临床试验显示,接受CDK4/6抑制剂治疗的患者均有明显的PFS获益;就像3个AI类药物一样,MONALEESA-7研究显示的总体人群的OS获益应该可以视为所有CDK4/6抑制剂均能起到的作用。目前,CDK4/6抑制剂+内分泌治疗已经作为一线内分泌解救的首选方案,以上两项研究的结果显示,给HR+/HER2-晚期乳腺癌带来的PFS的获益,最终能够转化为总体人群的OS获益,HR+/HER2-晚期乳腺癌的内分泌治疗已经正式进入“靶向+内分泌治疗”的新时代。











 苏公网安备32059002004080号
苏公网安备32059002004080号


