当地时间2019年5月31日—6月4日,美国临床肿瘤学会(ASCO)年会在芝加哥盛大举行。ASCO年会是世界上规模最大,学术水平最高,最具权威的临床肿瘤学会议。本届年会的主题为“Caring for Every Patient, Learning from Every Patient”。【肿瘤资讯】已经抵达会议现场,将第一时间对本次大会发布的重磅研究进行报道! 2019 ASCO年会6月3日的新闻发布会,由ASCO首席医学官Richard Schilsky主持,四项重磅研究公布,以下带来详细报道。

1. 扩大受试申请,肿瘤领域的两方需求
讲者:Richard Pazdur教授

图:Richard Pazdur教授
来自FDA的血液和实体肿瘤产品执行总监Richard Pazdur教授介绍了扩大受试申请(EA),旨在帮助更多患者得到机会接受研究药物的治疗。目前对于扩大受试申请,我们已知的是,由于患者获取信息的能力差异,因此在申请上存在一定不公平性,此外,需要比较繁琐的申请过程。当然,我们也面临众多未知,如需要EA的患者人数、赞助商拒绝的原因、从申请到获得研究药物的时间、患者的获益和不良反应。
2. 调查显示超过60%的妇科肿瘤学家经历过性骚扰
讲者/研究者:Marina Stasenko教授

图:Marina Stasenko教授
这一研究旨在评估在培训和执业期间,性骚扰的发生率以及性别和骚扰在职业发展上的影响。本研究在2018年10月匿名调查了1566名美国妇科肿瘤学会中的内科医师。其中共402名(26%)调查者反馈了调查问卷,女性和男性分别为255例和147例。结果显示:在培训或执业期间,64%的被访者经历过某种形式的性骚扰,女性和男性被访者发生率分别为71%和51%;仅10% 的被访者将性骚扰报告给行政人员,其中女性和男性被访者比例无显著差异。未报告性骚扰的最常见原因为被访者认为这一事件并不是非常重要 (40%)或即使报道了也无计可施 (37%)或害怕打击报复(34%)。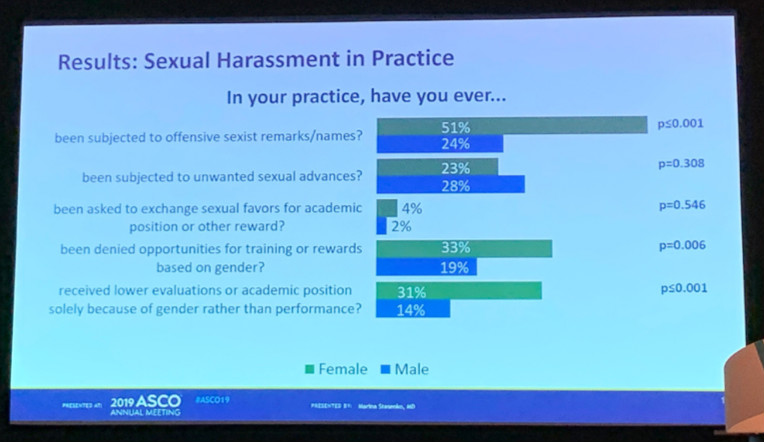
图:职业过程中性骚扰发生率
ASCO观点
ASCO专家组Merry-Jennifer Markham 教授介绍道,“性骚扰是一个广泛的社会问题,目前我们越来越强烈的意识到,性骚扰会影响医疗行业的女性。此外,如这一研究显示的,一些男性在培训或工作期间也会遭受性骚扰。基于这一研究数据,我们有责任提高这方面的意识,在更广泛层面解释性骚扰和其他与性别偏见相关的问题,期望最终可以让我们工作的环境更为安全和平等。”
作者感言
来自纪念斯隆凯瑟琳癌症中心的Marina Stasenko教授谈到,性骚扰是大众媒体广泛热议的话题,在影视和体育行业,这一话题被广泛报道,但在医疗领域,仅限于小众讨论。医疗领域一直存在着性别差异,尽管近年来女性内科医生队伍不断壮大。我们期望通过这一研究来增加妇科肿瘤医生对性骚扰和性别不平等的意识和认知,期望未来能针对这一不平等采取相应的措施。
3. 结直肠癌肝转移患者腹腔镜和开腹肝转移瘤切除术后患者的长期生存对比
讲者/研究者:Åsmund Avdem Fretland教授

图:Åsmund Avdem Fretland教授
结直肠癌是美国第4大瘤种,其中约一半的患者会出现肝转移,且越来越多的肝转移患者可以进行手术切除。开放手术是肝转移切除的标准治疗方案,在美国仅22%的结直肠癌肝转移患者接受腹腔镜手术。本研究是第一项对比腹腔镜和开腹切除结直肠癌肝转移的研究,旨在评估腹腔镜肝转移灶切除术是否优于开腹手术,主要终点为术后并发症(30天)。该研究2012年至2016年共纳入280例患者。既往对这一研究的短期疗效进行过对比,结果显示,腹腔镜肝转移切除术较开腹手术耐受性更好,并发症发生率更低(19% vs 31%)、住院时间更短(2 vs 4天)、患者生活质量更优。两者在治疗花费上没有显著差异,且腹腔镜手术性价比更高。
本次报道长期生存结局
目前中位随访时间为45个月,两组患者的生存结果相似,开腹手术和腹腔镜手术的中位OS分别为81个月和80个月,5年生存率分别为57%和56%,无显著统计学差异,即超过一半的患者可以存活超过5年;两组疾病复发率也相似。

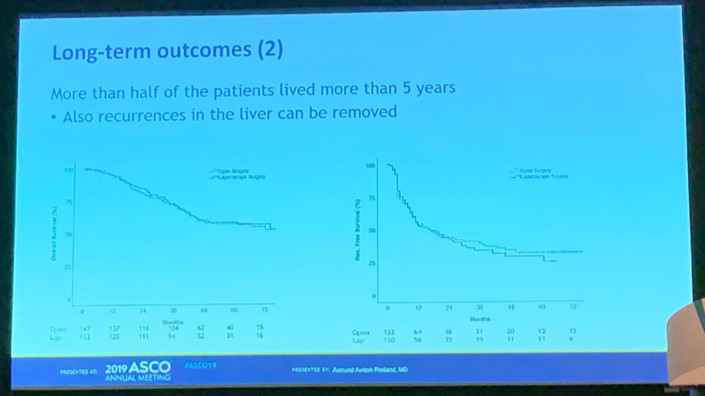
图:开腹和腹腔镜肝转移灶切除术生存对比
ASCO专家Nancy N. Baxter教授评论道:“腹腔镜手术已经广泛用于很多腹部实体瘤中,因为手术恢复快,且并不复杂。然而,对于那些技术上有挑战的手术,如肝脏肿瘤手术,仍会对患者的术后存活时间存在担忧。本研究是第一项在结直肠癌合并肝转移的患者中,显示腹腔镜手术对比开放手术可以取得相似长期疗效的研究,这就为患者在进行手术方式选择时增加了信心。但我们也需要关注进行手术医生的技能。
4. 更为宽松的入组标准可以成倍增加肺癌入组患者
讲者/研究者: R. Donald Harvey教授

图:R. Donald Harvey教授
ASCO和其他一些癌症研究协作组推荐临床研究应该放宽入组标准。更为宽松的入组标准不仅可以纳入更多患者,也可以让研究人群更具代表性,研究结果适用性更广,且能够加速入组。目前,FDA、NCI、NCTN协作组和ASCO发起的相关研究已经在这方面进行了相应举措,如ASCO TAPUR研究采用更为广泛的入组标准;FDA宣布可以入组更广泛的人群,并对更广泛人群进行单独分析;NCI更新了方案模版,采用了更为宽泛的入组标准;FDA正在起草相关指导文件。本研究旨在评估采用更为广泛的标准对比传统标准,对入组晚期NSCLC的影响。终点指标包括:传统 vs 更广泛标准排除的患者人数,传统 vs 更广泛标准纳入的患者的临床特征对比。
这是一项基于真实世界数据的回顾性研究,筛选了电子病例系统2011年1月至2018年12月的数据。选择NSCLC作为研究瘤种的原因是,这类疾病晚期患者更多,且通常合并并发症;此外NSCLC近年来进展较多,开展了很多临床试验。纳入标准为诊断为晚期NSCLC后患者接受的治疗。
通过电子病历库数据,研究者评估了采用传统标准和扩大标准的两组患者的差异。扩大标准指的是ASCO以及其他癌症协作组提出的新标准,如允许脑转移患者、既往或目前诊断为癌症和肌酐清除率为30 ml/min的患者入组,而传统标准则不允许有这些合并症或肌酐清除率低于60ml/min的患者入组。

图:传统标准和扩大标准的对比
研究显示,60%的患者为晚期或IV期患者,80%为既往或当下吸烟者。患者的中位年龄为67.6岁,女性和男性分别占56%和44%。当研究者采用传统标准入组时,5005例(47.7%)患者满足入组标准。然而,如果采用扩大标准入组,仅154例(1.5%)患者不满足入组标准。采用扩大标准,可以让额外4851例患者满足入组标准,即符合入组标准的患者人数增加一倍。此外,采用扩大入组标准后,相比于传统标准,患者的临床特征也会发生一些变化:如入组患者更为年老,中位年龄从66.1岁增加至67.5岁,女性患者比例从40%增加到44%,IV期患者比例从55%增加到60%,非鳞NSCLC患者比例从45%增加至47%,非吸烟者从13%增加至16%。
ASCO观点
ASCO专家David L. Graham教授评论道,“目前在美国仅3%的癌症患者参加了临床研究,限制性的入组标准导致很多患者不能参加研究,仅采用支持疗法。这一研究评估了采用扩大入组标准后,更多的肺癌患者有机会安全的参加有可能改善他们生存的临床研究。
作者感言
主要研究者,来自爱默里大学医学院I期临床研究中心的R. Donald Harvey教授分享到,如果基于安全性考虑,继续采用既往比较严格的入组标准,可能会使入组人群产生不必要的限制,使得我们很难加速进行相关临床研究,以评估新药的疗效和安全性。入组标准的改变对加速推荐靶向治疗和免疫治疗的相关研究非常重要,而这些药物相比于传统化疗具有更好的安全性。
小结
采用扩大入组标准可以成倍增加符合入组标准的NSCLC患者,且更广泛的入组标准可以让研究人群更具代表性,提高研究结果的适用性。我们期望研究赞助者都可以采用这一标准。
5. EV201研究:Enfortumab Vedotin单药治疗既往接受过铂类和免疫检查点治疗的转移性尿路上皮癌
讲者/研究者:Daniel Petrylak教授

图:Daniel Petrylak教授
晚期或转移性尿路上皮癌的一线治疗为铂类为基础的化疗,然而大多数患者会出现进展或需要后续治疗。二线PD-1/PD-L1单抗治疗的ORR较低,为13-21%,大多数患者因为免疫治疗无效或进展,仍需要接受后续治疗。目前,对于铂类化和免疫治疗进展后的患者,缺乏标准治疗方案。Enfortumab Vedotin是一个在研的抗体药物偶联剂,靶向Nectin-4,这是在多个实体瘤中高表达的治疗靶点,包括尿路上皮癌。
EV201研究是一个单臂的关键II期研究,入组了经治的晚期或转移性尿路上皮癌患者,队列1中入组了既往接受过PD-1/ PD-L1单抗和含铂化疗的患者,入组结束日期为2018年7月,入组了128例患者。队列2入组了既往接受过PD-1/ PD-L1单抗,但未接受过铂类或顺铂不耐受的患者,目前这一队列仍在入组。所有入组患者接受Enfortumab Vedotin 1.25mg/kg治疗,第1、8、15天用药,28天为一个治疗周期。主要研究终点为独立评估委员会采用RECSIT 1.1标准评估的ORR,次要终点包括DOR、PFS、OS和安全性。
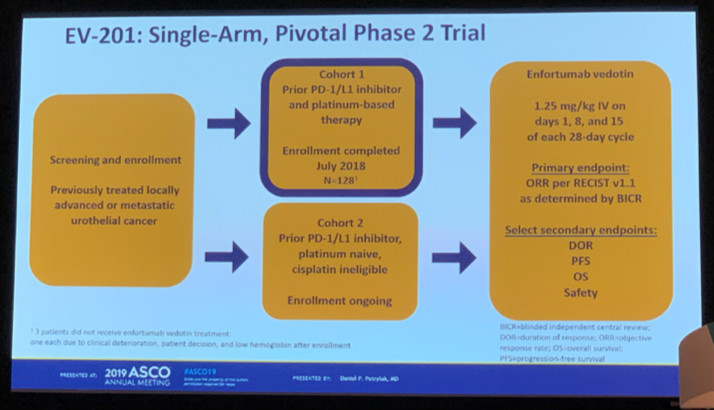
图:EV201研究设计
本次大会报道了队列1的研究结果。结果显示:接受Enfortumab Vedotin治疗后,大多数患者在第一次疗效评估时即观察到疗效,中位起效时间为1.8个月,中位疗效持续时间为7.6个月,中位PFS为5.8个月,中位OS为11.7个月。
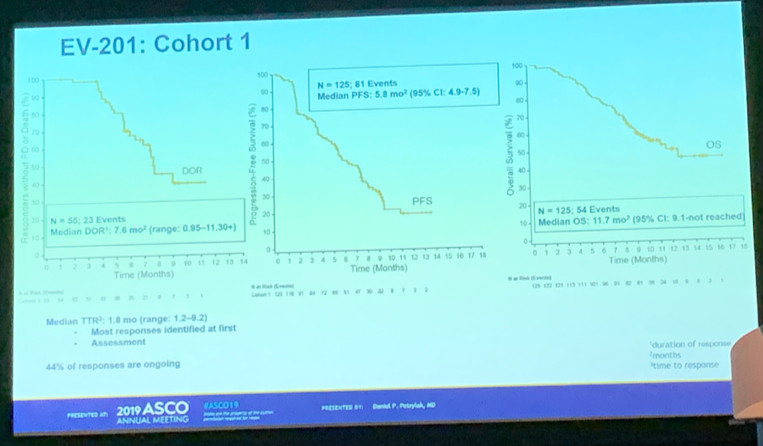
图:患者的疗效数据
常见的不良事件包括疲劳、脱发、食欲减退、味觉障碍、外周神经病变、恶心、呕吐等。大多数AE为1-2级,3级AE发生率较低。
小结
EV-201研究队列1的结果满足了晚期或转移性尿路上皮癌未被满足的需求。Enfortumab Vedotin是第一个在铂类和免疫治疗进展后的转移性尿路上皮癌患者中显示出显著临床活性的新型药物。基于这一研究结果,这一药物有望获批用于这类患者的标准治疗。











 苏公网安备32059002004080号
苏公网安备32059002004080号


