美国临床肿瘤学会(ASCO)成立于1964年,ASCO年会是世界上规模最大,学术水平最高,最具权威的临床肿瘤学会议。2019年ASCO年会即将于5月31日至6月4日在美国芝加哥举办,今年的主题为“Caring for Every Patient,Learning from Every Patient”。替雷利珠单抗(Tislelizumab,BGB-A317)是百济神州自主研发的PD-1单抗,作为国产创新药的代表之一,有多项研究将在ASCO年会上展示,【肿瘤资讯】特做整理,一睹国产创新药的风采。
替雷利珠单抗治疗中国鼻咽癌患者的初步结果(Abstract 2556)
主要研究者:王思阳 教授|中山大学附属第五医院
中国是全球鼻咽癌发病率最高的国家之一,先前Ⅰ/Ⅱ期的研究(CTR20160872)已经证明,替雷利珠单抗单药在中国晚期实体瘤患者中显示出良好的抗肿瘤活性和耐受性,替雷利珠单抗推荐的治疗剂量为200mg IV,Q3W。本次ASCO会议中,研究者公布了替雷利珠单抗在晚期鼻咽癌患者亚组中的结果。研究入组了20例经组织学或细胞学确诊的晚期或转移性鼻咽癌患者(WHO分型为Ⅱ型[非角化型癌]和Ⅲ型[未分化癌]),19例(95%)患者既往接受≥1线全身治疗。
在数据截止时,中位随访时间5.5个月,仍有15例患者在接受治疗,在15名可评估疗效的患者中,3例患者被确认为部分缓解(PR),9例患者疾病稳定(SD),1例患者未最终确认PR。不良反应方面,7例患者出现了≥1次治疗相关不良事件(TRAE),甲状腺功能减退(n=3)是唯一在≥2名患者中发生的TRAE,同时研究中没有报告≥3级或更严重的TRAE。研究表明,替雷利珠单抗在经治的晚期鼻咽癌患者中显示出抗肿瘤活性和良好的耐受性。(临床试验信息:CTR20160872)
替雷利珠单抗联合化疗一线治疗晚期肺癌(Abstract e14067)
主要研究者:王洁 教授|中国医学科学院肿瘤医院
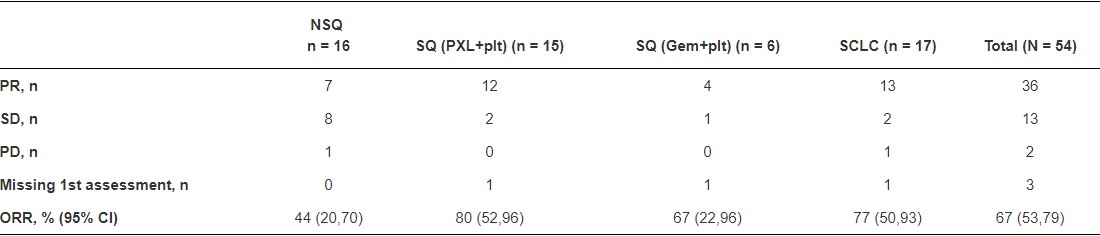
在该项Ⅱ期临床试验(NCT03432598)中,评估了替雷利珠单抗(200mg,Q3W)联合含铂化疗方案一线治疗中国晚期肺癌的疗效和安全性。所有患者均接受4~6个周期的替雷利珠单抗+含铂化疗方案治疗,直至疾病进展。其中非鳞非小细胞肺癌患者化疗方案为培美曲塞+铂类(4个周期),然后使用培美曲塞维持治疗;鳞癌患者接受方案A:紫杉醇+铂类,或方案B:吉西他滨+铂类。小细胞肺癌患者接受依托泊苷+铂类。最终评估肿瘤应答(RECIST v1.1)和药物安全性,同时研究中对患者进行肿瘤PD-L1表达检测。
截止2018年10月15日,54例患者中仍有24例在接受治疗。36例患者疗效评价为部分缓解,所有患者的客观缓解率为67%,无进展生存(PFS)数据尚未成熟。研究表明替雷利珠单抗联合含铂化疗方案治疗晚期肺癌患者耐受性良好,显示出抗肿瘤活性(临床试验信息:NCT03432598)。
除了已经公布的研究结果,每年ASCO摘要还有很特别的一类,那就是"正在进行的研究",代码为TPS(trial in progress),每个瘤种大约在16篇以内,部分瘤种甚至更少,编号为TPSxxxx,对于了解本领域内目前全球正在进行的研究是一个很好的窗口。在今年ASCO会议中,替雷利珠单抗有3项研究入选TPS。
在替雷利珠单抗+同步放化疗后继续替雷利珠单抗单药治疗新诊断的局部晚期不可切除NSCLC:Ⅲ期RATIONALE 001研究(Abstract TPS8574)
主要研究者:Luis G. Paz-Ares 教授| Hospital Universitario 12 de Octubre, CiberOnc, Universidad Complutense and CNIO, Madrid, Spain
RATIONALE 001研究是一项随机双盲、安慰剂对照的Ⅲ期临床研究,评估替雷利珠单抗+同步放化疗治疗局部晚期不可切除非小细胞肺癌的疗效和安全性。主要入组标准为:患者诊断为Ⅲ期不可切除非小细胞肺癌,先前未接受治疗,ECOG PS≤1分。同时随机化前不需要对患者进行PD-L1表达的评估。
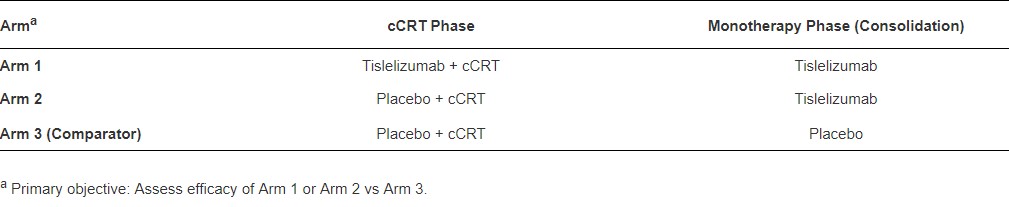
在这项3臂的研究中,计划约840例患者将按1∶1∶1随机分配,第1组在给予替雷利珠单抗+同步放化疗后继续予替雷利珠单抗巩固治疗;第2组给予安慰剂+同步放化疗,后续使用替雷利珠单抗巩固治疗;第3组给予安慰剂+同步放化疗,后续继续安慰剂对照。对靶病灶放疗的剂量为60Gy(2Gy/30F),化疗方案包括依托泊苷+顺铂和紫杉醇+卡铂。研究主要终点为无进展生存(PFS),次要终点包括客观缓解率(ORR)、总生存期(OS),2年生存率和安全性。临床试验信息:NCT03745222。
替雷利珠单抗+化疗治疗局部晚期或转移性胃癌或胃食管结合部腺癌的Ⅲ期研究(Abstract TPS2655)
主要研究者:徐瑞华 教授|中山大学肿瘤防治中心
以氟尿嘧啶和铂类为基础的联合化疗是局部晚期或转移性胃癌或胃食管结合部腺癌的一线标准治疗。尽管化疗方案有所改善,但患者的治疗效果较差,生存率很低。本研究是一项全球性随机双盲的Ⅲ期研究,旨在比较替雷利珠单抗+氟尿嘧啶和铂类与安慰剂+氟尿嘧啶和铂类一线治疗局部晚期或转移性胃癌或胃食管结合部腺癌患者的疗效和安全性。
来自全球160个中心的大约720例患者将入组,并按1∶1随机分配接受替雷利珠单抗(200mg IV,Q3W)或安慰剂(IV,Q3W)联合化疗治疗,以个体为基础的基本化疗方案包括奥沙利铂(130mg/m2,IV,Q3W)联合卡培他滨(1000 mg/m2,口服,BID,持续2周)或顺铂(80mg/m2,IV,Q3W)联合5-氟尿嘧啶(800mg/m2/d,IV,D1-5,Q3W)。化疗将长达6个周期,对于接受卡培他滨和奥沙利铂的患者,可以选择卡培他滨维持治疗。研究同时将使用VENTANA PD-L1(SP263)来测定评估患者PD-L1表达水平。PFS和OS是研究的主要终点,包括意向治疗人群和PD-L1表达阳性亚组患者,其他次要研究终点包括总反应率、缓解持续时间、生活质量以及联合治疗的安全性/耐受性,探索性终点包括疾病控制率、应答时间和潜在预测性生物标志物的分析(包括但不限于PD-L1的表达)。临床试验信息:NCT03777657。
替雷利珠单抗+化疗一线治疗不可切除、局部晚期/转移性食管鳞癌的疗效和安全性(Abstract TPS2656)
主要研究者:徐建明 教授|解放军总医院第五医学中心
早期的研究显示替雷利珠单抗在包括食管鳞癌在内的实体瘤中表现出抗肿瘤活性,在本项随机双盲、安慰剂对照的Ⅲ期临床研究中,旨在评估替雷利珠单抗+化疗一线治疗不可切除、局部晚期/转移性食管鳞癌的疗效和安全性。经组织学确诊为食管鳞癌的成人患者,首次诊断为转移性疾病,或间隔治疗≥6个月,同时患者具有可测量/评估的病灶,ECOG PS评分≤1份,且患者在治疗前≤4周内未接受PD-1/PD-L1、PD-L2抑制剂进行一线治疗或姑息性放疗。
研究预计将入组大约480例患者,1∶1随机接受研究者选择的化疗加替雷利珠单抗(200mg,IV Q3W)或化疗加安慰剂。化疗可选方案包括:铂类(顺铂60~80mg/m2或奥沙利铂130mg/m2,IV,Q3W)加5-氟尿嘧啶 750~800mg/m2,IV,D1-5,Q3W;或铂类加卡培他滨1000mg/m2,口服,BID,连续14天,Q3W;或铂类+紫杉醇175mg/m2,IV,Q3W。研究主要终点为PFS和OS,次要终点包括客观缓解率,缓解持续时间,与健康相关的生活质量。研究将通过监测不良事件、体格检查、生命体征和心电图来评估安全性。研究目前正在积极招募,临床试验信息:NCT03783442。
以上摘要信息均可在ASCO大会官网查询,点击阅读全文直达查询页面:
ASCO 2019 摘要查询:http://abstracts.asco.org/239/IndexView_239.html
ASCO Meeting Library 链接:https://meetinglibrary.asco.org/















 苏公网安备32059002004080号
苏公网安备32059002004080号


