2018年12月1-4日,第60届美国血液学年会(ASH)将于美国圣地亚哥隆重召开。作为全球最顶级的血液学术会议之一,每年的ASH无疑是众咖齐聚、精彩纷呈。骨髓增殖性肿瘤(MPN)是一组异质性疾病,代表性疾病包括原发性骨髓纤维化、真性红细胞增多症和原发性血小板增多症。该组疾病发病率相对较低,诊断与治疗进展相对缓慢。本届ASH上有多项研究涉及MPN的预后评估、对比干扰素和羟基脲的疗效差别,小编接下来将其中较为重要的几项研究结果作以详细介绍。

基因突变与临床因素结合可更好的预测原发性血小板增多症和真性红细胞增多症的生存和纤维化进展风险
时间:2018年12月3日7:15 AM
讲者:AyalewTefferi
类型:Oral Abstract(578)
地点:Grand Hall D (Manchester Grand Hyatt San Diego)
链接:https://ash.confex.com/ash/2018/webprogram/Paper109715.html
研究详情
原发性血小板增加多症(ET)和真性红细胞增多症(PV)生存的预测目前主要依赖临床因素如年龄、血栓和白细胞计数。基因改变的作用在ET和PV诊疗中的作用越来越不容忽视,因此有必要明确遗传学和临床变量的联合对预测总生存(OS)、无白血病生存(LFS)和无骨髓纤维化生存(MFFS)是否更优,以指导更精细的治疗。
这项研究由梅奥诊所和佛罗伦萨大学共同进行, NGS测序,基因改变根据ExAC数据库定义为突变或意义不明变体(VUS)。共有906例患者,502例 ET,404 例PV,均为分子水平诊断,梅奥诊所/佛罗伦萨ET270/232,中位年龄57/54岁,60%/59%女性,PV146/258,中位年龄63/58,52%/44%女性,中位随访ET和PV分别9.9/12.9和10.7/12.4年,死亡、白血病和纤维化进展ET组分别为39%/38%、4.4%/6.5%和16%/33%,PV组分别为50%/26%、4.8%/3% 和13%/36%。
分析显示,剪接体突变对OS(ET为SF3B1和SRSF2 ,PV为SRSF2 )和MFFS有不良影响(ET为U2AF1 和SF3B1),TP53突变与ET的白血病转化有关。只在一个队列中得到证实与预后有关突变包括EZH2和IDH2。OS独立风险因素,ET包括SRSF2/SF3B1突变,年龄>60岁和男性;PV包括SRSF2突变,年龄>67岁和白细胞≥11×109/L。只在一个队列中得到证实的OS风险因素是,ET与白细胞增多,PV与异常核型有关。根据上述指标确定了4分法含有突变的国际预后评分,MIPSS-ET包括突变、年龄和性别(图1a),MIPSS-PV包括突变、核型、白细胞和年龄(图1b),二个评分系统均显示了高的预测精确性并经拔靴法证实,进一步证实TP53突变对LFS的影响(图1C)和U2AF1/SF3B1突变对ET的影响。
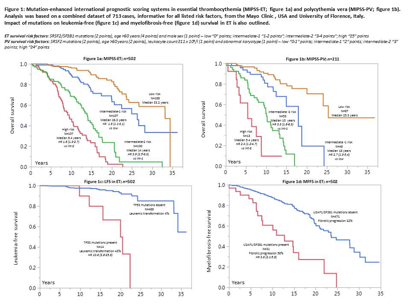
研究结论
剪接体突变可进一步增加对ET和PV生存的预测能力,并能鉴定发生纤维化进展的风险,TP53突变可预测ET的白血病转化。
原发性骨髓纤维化异基因移植的临床-分子风险模型
时间:2018年12月3日11:30AM
地点:Grand Hall A (Manchester Grand Hyatt San Diego)
讲者:NicoGagelmann教授
类型:Oral Abstract(689)
链接:https://ash.confex.com/ash/2018/webprogram/Paper114636.html
研究详情
动态国际预后评分系统(DIPSS)可预测原发性骨髓纤维化(PMF)的生存,对继发骨髓纤维化(SMF)和移植后的生存预测能力较差。MIPSS和MYSEC-PM已确认基因突变对生存的预测作用,因此有必要建立含有临床和分子因素的新的预后系统用于预测MF移植后的生存。
对MF相关基因测序( CALR1/2、JAK2、MPL、ASXL1、SRSF2、EZH2IDH1/2、DNMT3A、TET2、TP53),对OS相关变量进行选择,模型建立后进一步确认。骨髓纤维化移植评分系统(MTSS)中, 白细胞增高,血小板减少、KPS<90、年龄>57、受者/供者CMV血清状态(+/-)、ASXL1 突变均为1分, JAK2/三阴和不匹配无关供者均为2分。根据评分分为4个风险组:低危(0-2)、中危(3-4)、高危(5-6)极高危(7-9),5年OS分别为88%、71%、50%和20%(图1),死亡风险比(低危作参考)中危组2.36,高危组4.65,极高危组9.72。该评分对PMF和SMF的OS预测能力相同,对不同预处理和芦可替尼治疗患者均具有预测作用。
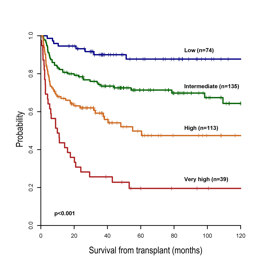
研究结论
MTSS评分中包括了疾病本身和移植治疗的相关风险因素,对PMF和SMF有一致的预测能力,对不同预处理和芦可替尼治疗患者均有预测作用,可用于指导临床治疗决定。
重组干扰素α-2与羟基脲治疗真性红细胞增多症的长期有效性和安全性:随机对照III期Daliah研究的3年结果
时间:2018年12月3日7:45AM
地点:Grand Hall A (Manchester Grand Hyatt San Diego)
讲者:rine Alma Knudsen教授
类型:Oral Abstract(580)
链接:https://ash.confex.com/ash/2018/webprogram/Paper111255.html
研究详情
重组干扰素α-2(r-IFNα)用于真性红细胞增多症(PV)治疗已30余年,可诱导临床血液和分子缓解,但几无研究比较r-IFNα与羟基脲(HU)的有效性与安全性,这项研究采用低剂量r-IFNα治疗≤ 60 或> 60岁的PV患者,与HU治疗>60岁的患者相比较。
DALIAH研究中共有90例新诊断或只行过放血治疗的PV,≤60岁患者1:1进入r-IFNα-2a或r-IFNα-2b治疗,>60岁患者1:1:1接受r-IFNα-2a、 r-IFNα-2b或 HU治疗, r-IFNα-2a和r-IFNα-2b剂量 45或35µg/w,HU剂量500-2000 mg/d。
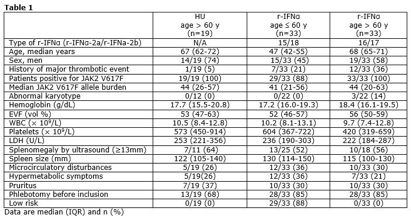
共有85例患者符合分析要求(表1),HU组、≤60岁r-IFNα组和>60岁r-IFNα组总的临床血液学反应率(ORR)68%、42%和39%,部分临床血液学反应率(PHR)和完全临床血液学反应率(CHR)分别为53%和16% ,9%和33%,9%和30%,各组ORR、CHR 和PHR无显著差别。各组维持治疗中保持CHR者分别为11%、21%和18%。
47例JAK2V617F阳性患者,部分分子反应(PMR),HU组、≤60岁r-IFNα组和>60岁r-IFNα组分别为21%、24%和18%,≤60岁r-IFNα组患者7%获得完全分子反应(CMR),PMR无显著差别,中位减少量分别为38%、79%和73%。各组停用治疗率分别为21%、52%和45%,毒性相关停用率分别为5%、30%和30%,3-4级副反应率32%、27%和42%,严重副反应率21%、9%和24%。
研究结论
经过3年治疗,不论年龄,r-IFNα和HU治疗PV的CHR无显著差别,但r-IFNα维持CHR更长。ORR无显著差别,PMR也几近相同,但JAK2V617F减少量在r-IFNα组更明显,毒性相关停药在 r-IFNα组更高。
骨髓增殖性肿瘤-研究组合(MPN-RC)112随机研究结果:聚乙二醇干扰素 Alfa-2a(PEG)和羟基脲(HU)治疗高风险真性红细胞增多症(PV)和血小板增多症(ET)
时间:2018年12月3日7:00AM
地点:Grand Hall D (Manchester Grand Hyatt San Diego)
讲者:John Mascarenhas教授
类型:Oral Abstract(577)
链接:https://ash.confex.com/ash/2018/webprogram/Paper111946.html
研究详情
HU一直用于高危ET/PV治疗,但有认为PEG可作为另一治疗选择。MPN-RC 112研究的中期分析未显示12个月时二者治疗的CR与PR差别,以下为长期随访结果。
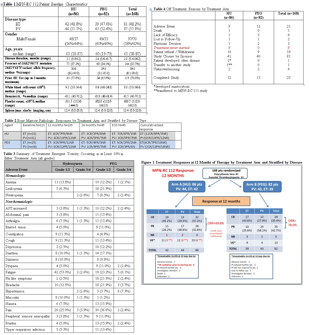
MPN-RC 112是随机、开放式、3期临床研究,采用HU和PEG治疗高风险ET/PV达12个月以获得PR或CR(ELN/IWG-MRT标准)。获PR/CR者继续治疗达6年。共招募168名患者,86例HU,82例PEG,基线特征见表1。12个月时,HU和PEG的总反应率((ORR= PR+CR)69.8%和78%,图1示不同疾病类型的反应分布。24个月时,HU组仍在治疗患者的ORR22/54(40.7%),PR 11(20.4%)和CR11(20.4%),PEG组仍在治疗患者的ORR31/52(59.6%),PR15(28.9%),CR16(30.8%),二组任何时间的最佳ORR分别是70.9%和81.7%,上述指标均无显著差别。此外脾容积的最大变化二组亦无差别。
骨髓形态学反应见表2。ET患者接受HU和PEG治疗的CR率分别为52%(12/23)和32%(8/25),PV患者接受HU和PEG治疗的CR率分别为19% (6/31)和6% (2/34)。86%患者有细胞遗传学分析,异常核型15%,5例PV和1例ET染色体异常消失,3例1年后,3例2年后。
副作用见表3。60例患者发生≥3级副反应,HU22(27.5%),PEG38(46.3%),28例PV有≥3级副反应,HU10(24.4%)和 PEG18(41.9%),32 例ET有≥3级副反应,HU12(30.8%)和 PEG20(51.3%)。停药原因见表4。
研究结论
MPN-RC 112 研究显示,高风险ET/PV患者接受HU和PEG治疗,12个月和24个月时的CR率均相似,PEG组有较高的3/4级毒性发生率。二种药物均对疾病病程有改变作用,用于评估的参数包括脾缩小、核型异常消失、组织病理学参数改善、低血栓发生率和低疾病进展率。
时间:2018年12月3日7:30AM
地点:Grand Hall D (Manchester Grand Hyatt San Diego)
讲者:Heinz Gisslinger教授
类型:Oral Abstract(579)
链接:https://ash.confex.com/ash/2018/webprogram/Paper118715.html
研究详情
Ropeg干扰素Alfa-2b(Ropeg)是一种新型干扰素,可减少剂量使用频度、改善耐受性。III期PROUD/CONTI-PV研究采用Ropeg和羟基脲/最佳支持治疗,对比患者3年的临床数据,其中包括 JAK2V617F在内多种基因的动态改变以及染色体的变化。
共纳入254例PV,Ropeg 组83例和HU/BAT组70例符合36个月时的分析条件,Ropeg组较HU/BAT组有更高的反应率,分别为70.5%和51.4%,更高的CHR+症状改善率,分别为52.6% 和37.8%,而且Ropeg组的反应率在24个月内稳定增加,在36个月后仍继续维持。二组的副反应事件相似,治疗相关最常见副反应贫血、血小板减少和白细胞减少在HU组更多,而GGT增高主要见于Ropeg组。Ropeg和HU/BAT组分别有66.0%和27.0%的患者获得 JAK2V617F的MR,具有显著差异,且MR显著相关CHR。最常见的非JAK突变有DNMT3A、 TET2、ASXL1、CUX1、CEBPA和 EZH2,除JAK相关9号染色体异常,亦有其它细胞遗传学改变。二种治疗对基因水平改变的影响有显著差别,HU似乎只对JAK2V617F有抑制作用且作用只发生在治疗初期,对其它突变缺少抑制作用。除JAK2V617F外,Ropeg还能减少TET2负荷。细胞遗传学方面,只有HU组患者发生新的基因损害,也只有HU组患者发生治疗或疾病相关继发肿瘤,Ropeg组的新发肿瘤似与治疗无关。
研究结论
Ropeg可致高效可持续血液学反应、症状控制且耐受良好。干扰素对JAK2V617F等多个与骨髓增殖性肿瘤相关的基因突变和细胞遗传学异常有改善作用。Ropeg有望成为 一种新的治疗选择。
号外!号外!!号外!!!2018 ASH征稿啦!如果你在2018 ASH现场,如果你发现了重磅研究,如果你擅长文字撰写……欢迎给【良医汇-肿瘤资讯】投稿!投稿邮箱oncologynews@163.com,肿瘤资讯小编-Amiee期待您的来稿!











 苏公网安备32059002004080号
苏公网安备32059002004080号


