【35 under 35】风采展示第二轮已经开始啦!本轮正经名叫“病例实战分析”,不正经名叫“互相伤害”,哈哈哈~100位入围选手每人提交一个有意思的病例,并就病例提出一个问题,形成一个病例库!然后100位入围选手从病例库中任意选择一个非自己提供的病例进行解读并回答问题!最后,我们将呈现病例+别人的点评+病例提供者自己的点评,同步展示!
 100位小伙伴已将自己的病例提交,并提出了问题,让我们一起先阅读下精彩病例吧!
100位小伙伴已将自己的病例提交,并提出了问题,让我们一起先阅读下精彩病例吧!
患者病史摘要
患者,女,65岁,因“反复上腹痛4月”入院。曾于当地医院就诊,查腹部CT示“胰体尾部肿块,胰腺癌考虑”,未治疗。
一般情况:
BMI 28.45 kg/m2,营养评分0分。
体格检查:
未见异常。
入院实验室检查:
肝功能:TB 16.4umol/L,ALB 43.7g/L,ALT 12U/L,r-GT 17U/L。
肿瘤标志物:
CA19-9 659.5 U/mL,CEA 2.4ng/mL,AFP 6.0ng/mL,CA125 29.5U/ml,CA242 109.7U/ml,细胞角蛋白211 0.7ng/ml,神经元特异性烯醇化酶13.3ng/ml,鳞状上皮细胞癌相关抗原0.5ng/ml,CA153 10.5U/ml,β-HCG 2.1U/L。
影像学评估:
腹部CT(图1):胰体部占位,考虑胰腺癌伴周围淋巴结肿大,累及脾动脉近段、肝总动脉及胃左动脉起始部。

图1
腹部CTA(图2):肿块包绕腹腔干,门静脉无明显狭窄中断征象。
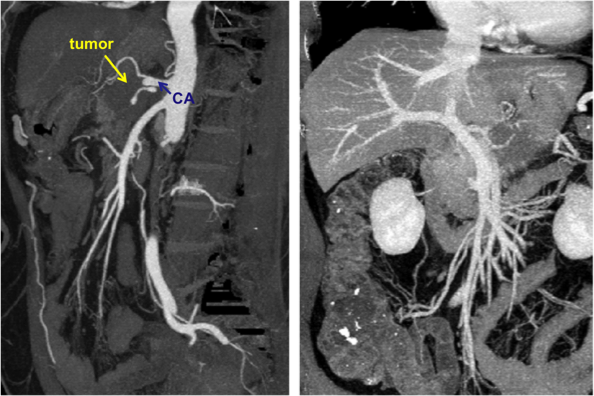
图2
PET-CT(图3):未见远处转移。
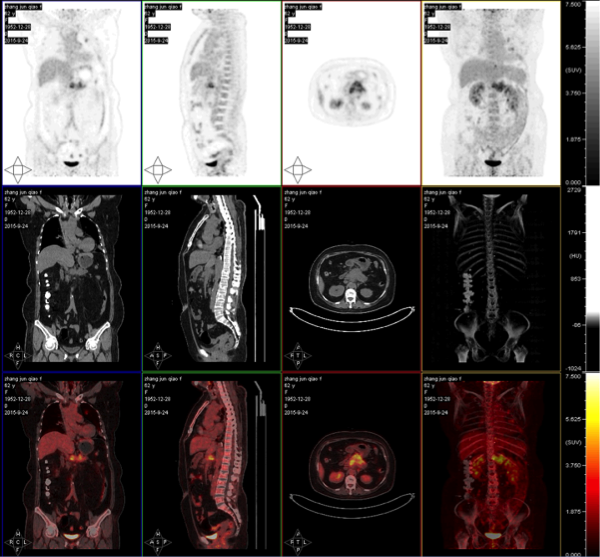
图3
超声引导下肿块FNA(图4):涂片见成巢异型细胞,考虑导管腺癌。
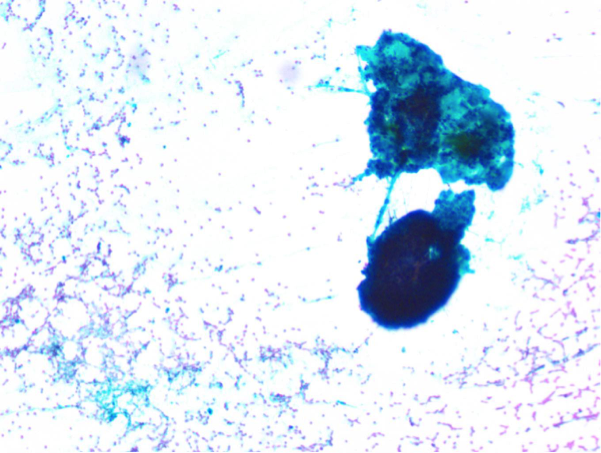
图4
肝脏MRI:肝脏未见明显异常。附见:胰腺体部胰腺癌,肿瘤侵犯腹腔干(360度包埋)及肝总动脉。
诊断
胰腺恶性肿瘤:T4NxM0(局部进展期胰腺癌——不可切除)
治疗经过
SBRT放疗(5*5Gy)
序贯接受7次的modified-Folfirinox化疗(根据推荐剂量调整为伊立替康75%, 5-FU 100%,奥沙利铂80%,亚叶酸钙100%),耐受性可。
放化疗后评估:
血清CA19-9水平下降明显(图5),复查腹部CTA示“对照前片肿块略有缩小伴有明显坏死,血管侵犯情况略有好转;肿块可能仍包绕腹腔干(>180°),门静脉无明显狭窄中断征象”。
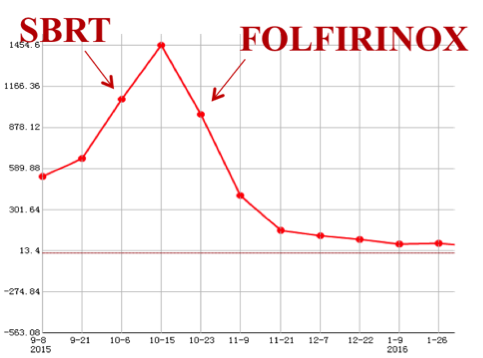
图5 放化疗后血清CA19-9变化
行胰腺癌扩大根治术(胰体尾切除+脾切除+肿瘤活检+腹腔干切除重建+后腹膜淋巴结扩大清扫术)
术后病理报告:低分化腺癌,伴大片坏死,大小3*2.5cm,神经侵犯阳性,脉管内可见瘤栓形成,胰腺断端切缘阴性,周围淋巴结均阴性。胰腺切缘、脾静脉内膜、肝动脉鞘、肝动脉壁均未见肿瘤细胞。
问题:该患者术后辅助治疗方案?
此病例共有2位入围选手点评,分别为59-谢蕊、74-李伟 ;病例提供作者为:63-章琦。详情如下:
点评医生简介:59-谢蕊
 点评内容分享:
点评内容分享:
胰腺癌是临床上常见的恶性肿瘤之一,手术是唯一潜在可治愈患者的治疗手段,但约80%的患者在确诊时已为中晚期癌。该患者初诊为胰腺恶性肿瘤:T4NxM0,局部进展期胰腺癌,不可手术切除。多数胰腺癌对放疗的敏感性较差,胰腺癌根治剂量大,且胰腺周围的器官对放射线耐受性低。给于此患者体部立体定向放疗(SBRT)治疗,此技术可明显增加肿瘤靶区的局部照射剂量,降低靶外正常组织的照射剂量,使患者接受治疗的同时减少对周围正常组织的影响。伊立替康对晚期胰腺癌患者有效,伊立替康在氟尿嘧啶和亚叶酸钙之前使用有协同增效作用,奥沙利铂仅在与氟尿嘧啶联用时对胰腺癌有效,体外研究显示奥沙利铂与伊立替康联用有协同增效作用,氟尿嘧啶、亚叶酸钙、伊立替康和奥沙利铂联用不会出现毒性叠加效果,因此Folfirinox化疗方案(亚叶酸钙、5-FU、伊立替康和奥沙利铂)诞生了。PRODIGE协作组的随机对照试验ACCORD,探究Folfirinox对比吉西他滨在PS评分较好的转移性胰腺癌一线治疗中的有效性及安全性。Folfirinox组的18月生存率为吉西他滨组的3倍,该研究让临床医生在转移性胰腺癌患者中广泛应用该方案。而且自结果公布以后,Folfirinox在新辅助化疗中的应用也越来越多,不仅为了手术降期,也为了治疗微转移病灶。Forrone等发布了潜在可切除的胰腺癌和局部晚期胰腺癌应用Folfirinox方案新辅助治疗胰腺癌的回顾性分析,与未接受新辅助治疗相比,接受Folfirinox治疗明显降低了淋巴结阳性率和周围神经浸润的比例。Folfirinox新辅助治疗组的潜在可切除的胰腺癌患者的中位总生存期比与可手术切除的,未接受新辅助治疗直接手术的患者要高。有的队列研究中,接受新辅助治疗后,R0切除率可达90%。对于治疗前CA19-9 明显升高的患者,CA19-9 在治疗过程中的变化对预测治疗疗效具有一定的意义。在该患者应用SBRT的治疗过程中,虽有血清CA19-9的升高,但在接受序贯的modified-Folfirinox化疗的过程中,患者血清CA19-9水平明显下降,复查腹部CT显示与之前相比肿块缩小并伴坏死,患者后续并行胰腺癌扩大根治术。此本病例是应用新辅助放化疗结合手术对局部进展期胰腺癌患者进行治疗的一值得学习的病例。
--------------------------------------
点评医生简介:74-李伟
 点评内容分享:
点评内容分享:
国内外研究表明,约60%的胰腺癌患者在确诊时已发生远处转移;25%患者为局部晚期,如不能行根治性切除术,中位生存仅为6~9个月;初治可手术切除的仅15%,中位生存期约15个月。以往研究证实,R0切除是影响生存的关键。对于初治不可手术,但新辅助治疗或转化治疗后完成R0手术切除的患者,仍可获得长期生存。随着以FOLFIRINOX(氟尿嘧啶+奥沙利铂+伊立替康)或吉西他滨联合白蛋白结合型紫杉醇为代表的化疗方案,以及立体定向放疗(SBRT)的广泛应用,为实现R0切除奠定了解剖学和病理学基础,显著延长了局部进展期胰腺癌患者的生存期。本病例是一例不可切除的局部进展期胰腺癌,经SBRT和FOLFIRINOX方案化疗后,成功转化,实现R0切除的典型病例。由于缺乏高级别循证医学证据,目前治疗指南尚无对此类患者术后辅助治疗的明确推荐。
胰腺癌生物学行为独特,普遍认为初治时即可能存在肉眼不可见的亚临床微小转移灶,故术后复发率极高。即使是初治可切除的患者,术后复发率仍高达80%。对于本例初治不可切除的局部进展期患者,虽然经转化治疗获得了R0切除,但病理已证实神经侵犯阳性,脉管内可见瘤栓形成,亚临床微小转移不可避免。即使给予术后辅助治疗,彻底治愈的可能性依然微乎其微。因此,术后辅助治疗不应以治愈为目的,而应以长期生存为目标。治疗过程中,需要综合考虑治疗风险与获益比,任何治疗都不应以损失OS为代价。
化疗时机方面,以往研究发现影响可手术患者术后生存的独立因素是其能否顺利完成6 个周期的规律化疗,而并非是否能尽可能早地接受术后辅助化疗。病人的体能状态被认为是影响胰腺癌预后的独立危险因素,并可以预测病人对化疗的耐受程度。无论是ASCO 指南推荐的“术后完全恢复前提下,8 周以内”,还是NCCN 指南推荐的“术后充分恢复前提下,12 周以内”,均强调了术后体能状态完全恢复的重要性,体现了循证医学证据对于临床诊治规范制定的重要价值。对于本例的老年女性患者来说,术前接受过毒副作用相对强烈的FOLFIRINOX方案化疗,术后需要更长的恢复时间,化疗切不可操之过急。如果患者体能状态较差,化疗可能弊大于利时,应考虑延迟化疗甚至不化疗,而以观察等待为主。待患者体能状态恢复,重新评估后再制定进一步治疗方案。
化疗方案上,参考新辅助治疗的建议,NCCN指南推荐结合临床实际及其他方面评估,优选术前化疗效果良好的方案。制定辅助化疗方案前,首先仍要对患者的体能状态进行评估。如果患者体能状态好,根据指南推荐,仍可考虑原方案化疗。但由于FOLFIRINOX方案严重的毒副反应和治疗的累积毒性,应随时评估体能状态,及时调整治疗方案。如果患者体能状态一般或不能耐受FOLFIRINOX,可考虑在原氟尿嘧啶+奥沙利铂+伊立替康三药联合方案的框架内适当删减,采用单药或两药联合化疗。单药方案选择氟尿嘧啶类,可参考2017 NCCN指南中胰腺癌的术后辅助治疗方案,包括氟尿嘧啶/LV(1类推荐)、氟尿嘧啶持续输注、卡培他滨(2B类推荐),也可参考《胰腺癌综合诊治中国专家共识(2016 年版)》选择S-1(Grade A)。含吉西他滨的方案虽然也是辅助治疗的1类推荐,但在术前方案有效、无疾病复发进展,且无可评价病灶的情况下,术后的辅助治疗显然不适合改换为含吉西他滨的方案。如采用两药联合化疗方案,氟尿嘧啶+奥沙利铂,或氟尿嘧啶+伊立替康均可考虑,两种方案都已证实在胰腺癌中有效。2017 NCCN指南中,氟尿嘧啶+奥沙利铂的方案可用于晚期患者的一线(2B类推荐)或二线治疗,而氟尿嘧啶+伊立替康可用于晚期患者的二线治疗。两种方案在胰腺癌中孰优孰劣,目前尚无定论。上海交通大学医学院附属仁济医院王理伟教授团队建立了国内最大的胰腺癌PDX移植瘤库和预测平台,研究发现目前胰腺癌常用五大类药物(氟尿嘧啶、吉西他滨、奥沙利铂、紫杉醇以及伊立替康)在疗效上存在显著差异,该研究目前正在总结当中,让我们共同期待。另外值得注意的是,NCCN指南中特别提及氟尿嘧啶+伊立替康用于二线治疗时,需要患者KPS≥70,提示氟尿嘧啶+伊立替康的方案对患者体能状态的要求相对较高。
至于化疗时程,ASCO 指南对于已行术前化疗者,建议辅助化疗(术前+术后)总计达6 个月(表1,建议4.3)。但由于缺乏相应RCT 证据支持,该建议仅为“推断性的”专家共识性建议。实际应用中,应根据患者的体能状态随时进行调整。
 综上所述,由于胰腺癌极差的预后、FOLFIRINOX方案严重的毒副作用,以及手术的巨大创伤,这些胰腺癌不同于其他癌种的独特之处,决定了术后辅助治疗方案必须考虑到患者的体能状态以及对风险获益比的评估。虽然NCCN指南和ASCO指南都针对新辅助化疗后的术后辅助化疗给出了一定的建议,但并未给出详细的治疗方案,实际操作中有必要针对患者的个体差异制定个体化的治疗方案。对于以本病例为代表的成功转化的胰腺癌患者,术后辅助治疗的目的在于长期生存,在治疗时机、治疗方案,以及治疗时程的选择上均需要慎重,不能冒着损失OS的风险,也不能以降低生活质量为代价。
综上所述,由于胰腺癌极差的预后、FOLFIRINOX方案严重的毒副作用,以及手术的巨大创伤,这些胰腺癌不同于其他癌种的独特之处,决定了术后辅助治疗方案必须考虑到患者的体能状态以及对风险获益比的评估。虽然NCCN指南和ASCO指南都针对新辅助化疗后的术后辅助化疗给出了一定的建议,但并未给出详细的治疗方案,实际操作中有必要针对患者的个体差异制定个体化的治疗方案。对于以本病例为代表的成功转化的胰腺癌患者,术后辅助治疗的目的在于长期生存,在治疗时机、治疗方案,以及治疗时程的选择上均需要慎重,不能冒着损失OS的风险,也不能以降低生活质量为代价。
除了术后辅助治疗方案的选择,本病例的治疗过程也带给我们诸多思考。本例患者化疗后复查腹部CTA示肿块可能仍包绕腹腔干(>180°),根据NCCN指南对可切除状态的定义(表2),此时患者仍属于不可切除。那么对于化疗有效,但影像学再评估仍为不可切除的患者,该不该手术?值得注意的是,影像学报告中用了“可能”一词,也就意味着从影像学上并不能明确肿瘤的侵犯程度。事实上,类似的情况并不罕见。原因在于CT无法很好地区分炎性粘连和癌性浸润。尤其是经过新辅助治疗或转化治疗后,仅凭影像学检查往往难以区分治疗导致的粘连与肿瘤侵犯,此时影像学检查作为评估手段不再可靠。以往有研究证实,术前化疗虽然不能在影像学上达到降期的目的,但明显提高了手术切除率。对于转化成功并完成R0切除的病人,其存活率甚至接近可切除胰腺癌。因此,对于化疗后肿瘤指标明显下降,影像学提示化疗有效,但血管侵犯程度不明确的患者,不能轻易放弃手术探查。
 胰腺癌手术难度高,需要术者拥有丰富的手术经验。NCCN指南推荐胰腺癌的诊断处理及手术切除应当是在一个有一定规模的中心,经多学科讨论并有恰当的影像学资料情况下作出的临床决策。近年来随着手术技术的进步,血管切除重建使得胰腺癌的切除率得到了很大提高。部分大型胰腺中心已常规开展胰腺癌联合静脉的切除与重建,但联合动脉切除由于近、远期并发症等因素仍存在争议。联合动脉切除的胰腺癌根治术的总手术死亡率高达10%~20%,从而抵消了手术所带来的获益。但目前普遍认为,只要可以实现R0切除,仍然应对可能切除胰腺癌尝试行联合血管切除。正如本病例中,针对受侵犯的腹腔干进行了动脉重建,获得了R0切除。在动脉受侵的处理方式上,南京医科大学第一附属医院胰腺中心苗毅教授团队进行了开拓性的探索。该中心研究发现,>90%的病人动脉壁侵犯仅局限于动脉外膜而很少突破由致密结缔组织组成的外弹力层。在外膜与外弹力层之间存在相对疏松的组织结构,利用动脉鞘剥除技术沿此解剖平面,可将受侵犯的动脉外膜连同肿瘤一并剥除。此方法虽然没有切除动脉,但仍可达到根治的目的。单中心研究证实,施行动脉鞘剥除病人的生存期与没有动脉侵犯的病人相近,同时避免了动脉切除所引发的严重并发症。该研究建立的基于动脉壁侵犯深度的评价体系,可能会颠覆指南中对胰腺癌可切除状态的定义,从而指导未来的临床实践。
胰腺癌手术难度高,需要术者拥有丰富的手术经验。NCCN指南推荐胰腺癌的诊断处理及手术切除应当是在一个有一定规模的中心,经多学科讨论并有恰当的影像学资料情况下作出的临床决策。近年来随着手术技术的进步,血管切除重建使得胰腺癌的切除率得到了很大提高。部分大型胰腺中心已常规开展胰腺癌联合静脉的切除与重建,但联合动脉切除由于近、远期并发症等因素仍存在争议。联合动脉切除的胰腺癌根治术的总手术死亡率高达10%~20%,从而抵消了手术所带来的获益。但目前普遍认为,只要可以实现R0切除,仍然应对可能切除胰腺癌尝试行联合血管切除。正如本病例中,针对受侵犯的腹腔干进行了动脉重建,获得了R0切除。在动脉受侵的处理方式上,南京医科大学第一附属医院胰腺中心苗毅教授团队进行了开拓性的探索。该中心研究发现,>90%的病人动脉壁侵犯仅局限于动脉外膜而很少突破由致密结缔组织组成的外弹力层。在外膜与外弹力层之间存在相对疏松的组织结构,利用动脉鞘剥除技术沿此解剖平面,可将受侵犯的动脉外膜连同肿瘤一并剥除。此方法虽然没有切除动脉,但仍可达到根治的目的。单中心研究证实,施行动脉鞘剥除病人的生存期与没有动脉侵犯的病人相近,同时避免了动脉切除所引发的严重并发症。该研究建立的基于动脉壁侵犯深度的评价体系,可能会颠覆指南中对胰腺癌可切除状态的定义,从而指导未来的临床实践。
--------------------------------------病例提供作者简介:63-章琦

病例提供作者自评:
对比NCCN指南2015/2016/2017版本较2014版本之变化,放宽了对局部进展期胰腺癌(local advanced pancreatic cancer, LAPC)诊断的动脉受侵标准,即胰头或钩突肿瘤侵犯腹腔干不足180度的情况不认为是LAPC;与此同时增加了肿瘤侵犯空肠动脉第一支的判断(侵犯即为LAPC)。而对胰体尾肿瘤,亦增加了对肿瘤同时侵犯腹腔干及腹主动脉情况的判断(侵犯即为LAPC)。本病例入院时腹部CT及CTA提示胰体尾肿瘤侵犯腹腔干(360度包埋),同时PET-CT未见远处转移,LAPC诊断应无争议。经MDT讨论,认为目前不可切除;但可考虑新辅助治疗降期后争取手术机会。行超声引导下肿块穿刺见导管腺癌。患者彼时一般情况尚可,体力评分较好,且无明显黄疸,根据最新NCCN指南,可首选 FOLFIRINOX或吉西他滨+白蛋白紫杉醇方案。由于副作用较大,经过药物减量的不同方案mFOLFIRINOX更常用,以提高患者的耐受性。国外小样本研究显示,新辅助mFOLFIRINOX化疗可使44%的LAPC实现切除,并且R0切除率达到91%。笔者所在科室在国内率先开展了mFOLFIRINOX的胰腺癌临床研究,约40%LAPC患者实现降期接受手术,R0切除率达到82%(数据未发表)。另一方面,已有证据显示,新辅助立体定向放疗(Stereotactic body radiation therapy, SBRT)联合化疗在LAPC中的客观响应率高达82.6%,亦有助于降期切除并减少切缘阳性率[1]。因此针对本病例,我们制定了SBRT联合mFOLFIRINOX的新辅助方案。治疗后CA19-9下降至正常水平,CTA复查亦见肿瘤缩小、血管侵犯好转,可惜肿块包绕腹腔干仍>180°,仍属于LAPC,未能实现降期的目标。然而,研究显示FOLFIRINIOX新辅助化疗后影像学明显低估LAPC的可切除性[2]。经MDT讨论后行胰腺癌扩大根治术,术后病理证实各切缘均阴性。由于患者对mFOLFIRINOX方案敏感,术后一月开始继续予该方案进行辅助治疗1次,因患者术后耐受性不佳,遂改为吉西他滨单药化疗。术后8月时复查见CA19-9再次升高,CT示“右肺转移灶、后腹膜淋巴结肿大”。再次予mFOLFIRINOX方案化疗7次,CA19-9下降至接近正常水平,肺转移灶缩小。目前患者术后生存20个月,一般情况良好。
综合而言,本例患者新辅助治疗较为成功,为患者争取到了R0切除的机会。对新辅助治疗最大的担忧来自方案不敏感可能造成的疾病进展,但这在不可切除的LAPC中并不是个问题;况且,目前胰腺癌化疗方案也非常有限,在新辅助和辅助治疗中的应用尚无严格的区分。对于LAPC,通过新辅助治疗降期并争取R0切除是切实可行的近期目标。以转移性胰腺癌作为参考,对比FOLFIRINOX和吉西他滨+白蛋白紫杉醇两种方案,前者在各项疗效评估指标上均略好于后者,且价格更为便宜[3]。此外,笔者科室发现在中国人群中mFOLFIRINOX对胰腺癌中的客观缓解率可达32.5%,疾病控制率达到60%[4]。因此,在患者耐受性良好的情况下,以mFOLFIRINOX作为新辅助治疗方案是可以首先考虑的。其次,手术时机的掌握在整体治疗中非常关键,对放化疗后影像学评估的“失真”要有足够的认识,对手术各切缘需仔细分析,准确评判R0/R1/R2切除。因降期成功患者对新辅助化疗方案至少具有部分响应,术后辅助治疗在条件允许的情况下可以继续使用新辅助化疗方案,将吉西他滨等作为二线方案备用。幸运的是,患者对mFOLFIRINOX的敏感性一直保持得较好,没有因为复发而变得抵抗;另一方面,患者在吉西他滨应用短期内出现复发,提示对吉西他滨的敏感性可能不佳。当然,对该病例术后治疗的总结和反思中,值得商榷的一点是,mFOLFIRINOX的时机。2015年NCCN指南将术后辅助治疗的起始时间由原来的4-8周调整为4-12周,有适度延迟以便保障患者术后康复利于承受标准化疗的意图。本例患者术后化疗起始较早(4周),且mFOLFIRINOX毒性相对较大,不得已因耐受性换用吉西他滨单药,这可能在一定程度上缩短了患者PFS。此外,术后辅助使用毒性较小的S-1也是一种选择。总之,LAPC的综合治疗是个系统工程,放化疗和手术选择的考量均需贯穿始终并提前计划,在力争保障生存质量的前提下实现延长患者生存的最终目标。
-------------------------------------
以上为【35 under 35】的观点,您怎么看?欢迎广大肿瘤医生在下方留言发表您的观点!
以上所有点评参考文献略。














 苏公网安备32059002004080号
苏公网安备32059002004080号


