【35 under 35】风采展示第二轮已经开始啦!本轮正经名叫“病例实战分析”,不正经名叫“互相伤害”,哈哈哈~100位入围选手每人提交一个有意思的病例,并就病例提出一个问题,形成一个病例库!然后100位入围选手从病例库中任意选择一个非自己提供的病例进行解读并回答问题!最后,我们将呈现病例+别人的点评+病例提供者自己的点评,同步展示!

患者病史摘要
性别:女
年龄:58岁
主述:确诊肺癌2年10月,腹痛4月,停止排气排便5天于2015.8.24第一次入湖南省肿瘤医院肺胃肠肿瘤内科
体能状态评分:2分
既往史:否认高血压、糖尿病及心脏病,否认肺结核。
家族史:无
入院查体:PS=2,全身浅表淋巴结未扪及,左胸壁可见一10cm手术瘢痕。左下肺呼吸音稍低,右肺呼吸音清,双肺未及明显干湿罗音;腹部膨隆,上腹部轻压痛,无反跳痛,肝脾未及,移动性浊音阳性,肠鸣音活跃,约7-8次/分
入院实验室检查:
1) 血常规检查:未见明显异常。
2) 尿常规:未见明显异常。
3) 便常规:未见明显异常。
4) 肝、肾功能:未见明显异常。
5) 肿瘤标志物:CEA、CA199、CA125等,未见明显异常。
肠镜检查
肠镜:直肠距肛门7cm可见一直径约2cm带蒂肿物,表面大量坏死物包裹,活检质脆;
病理诊断:分化差的癌。
影像学检查
入院时胸、腹、盆腔等影像学检查及CT/MRI片子:2015.8.28胸腹部CT提示1.左肺癌术后改变,左侧胸膜增厚、左侧胸腔少量积液;双肺多发结节,2.腹腔积液(腹腔引流后);局部腹膜不规则增厚、网膜浑浊,3.部分小肠扩张积液积气,考虑不全肠梗阻,4.直肠左侧壁占位性病变
腹部平片:肠梗阻。
入院前治疗史
2012.10因“ 体检发现左肺结节3月余”就诊于外院,并于2012.10.25 行“肺癌根治术”,术后病理诊断为:原发性支气管肺癌 左下肺 周围型 腺癌 pT2aN2M0 IIIA期 (N2为第9组淋巴结1/1)EGFR野生型(ARMS) ALK未知
2013.11-2014.1术后于外院行DP方案化疗4周期。
2013.12 复查肺部CT发现左上肺结节,左侧胸腔积液,于外院行PC方案化疗2周期,治疗后左上肺较前缩小,左侧胸腔积液较前吸收,后拒绝治疗。
2014.4.出现左股骨疼痛,未检查,未治疗。
2014.9.18复查CT:双肺内、左侧胸膜转移,并左颈部及锁骨上窝淋巴结转移,左侧胸腔积液,左股骨转移,并于2014.9-2014.12行培美曲塞 +卡铂 化疗4周期,期间于2014.12-2015.1行左侧股骨头姑息放疗,4周期化疗后,双肺内、左侧胸膜及左锁骨上窝淋巴结转移较前改善,左侧胸腔积液较前减少。
2015.8.21院外基因检测结果(血液):EGFR、ALK、ROS、KRAS、NRAS、BRAF、HER2、RET、MET、PIK3CA、DDR-2 均未见突变。
入院诊断
原发性支气管肺癌 左下肺周围型 腺癌pT2aN2M0 IIIA, rcT4N3M1 IV期(双肺、胸膜、胸腔积液) EGFR 野生型 ALK- 双肺、腹水
腹腔积液查因
直肠占位查因,性质待定
肠梗阻
患者各阶段影像资料、检测报告
2012.10 肺部CT

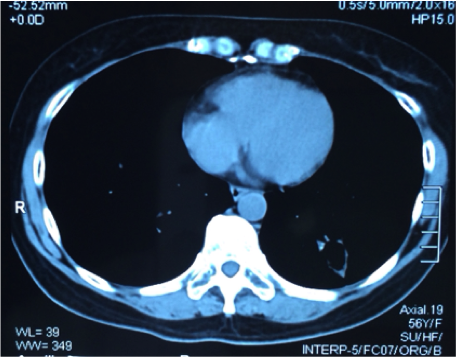 2013.12 肺部CT
2013.12 肺部CT
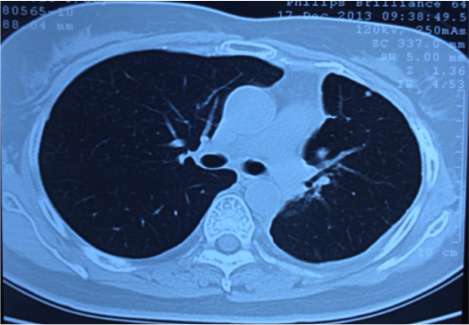
 2014.2 肺部CT
2014.2 肺部CT
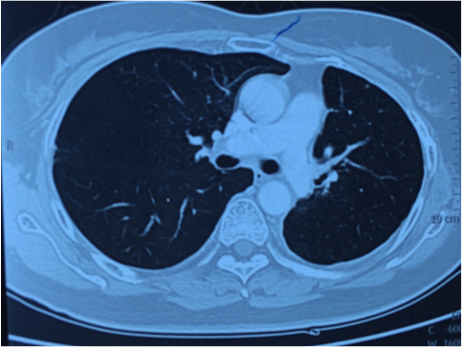

2014.9 肺部CT
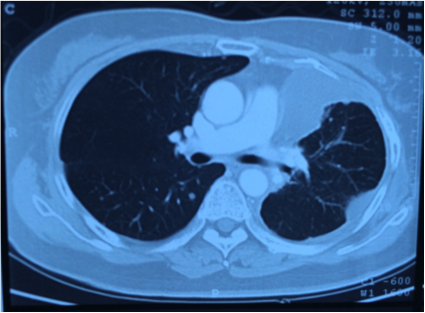

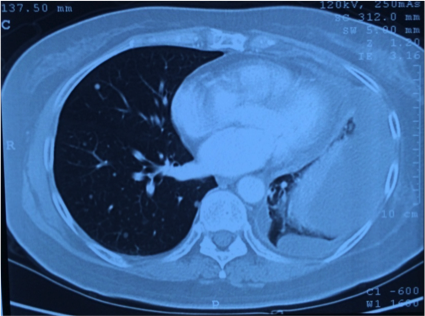
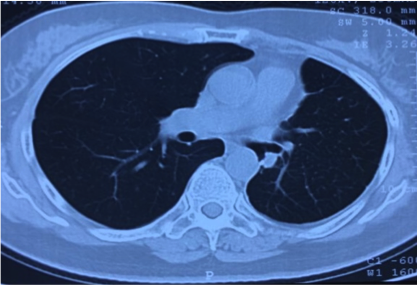
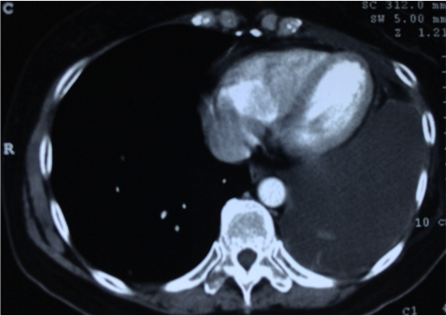 2014.12 肺部CT
2014.12 肺部CT


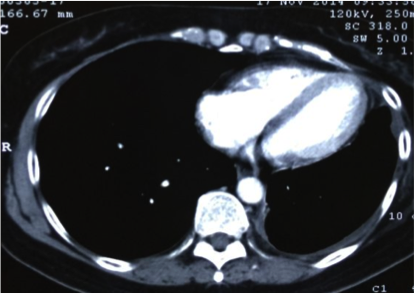 2015.8.21 外院基因检测结果
2015.8.21 外院基因检测结果

2015.8.27 入院急诊腹部X线
 2015.8.28 肺部及腹部CT
2015.8.28 肺部及腹部CT



2015.8.28 肺部及腹部CT

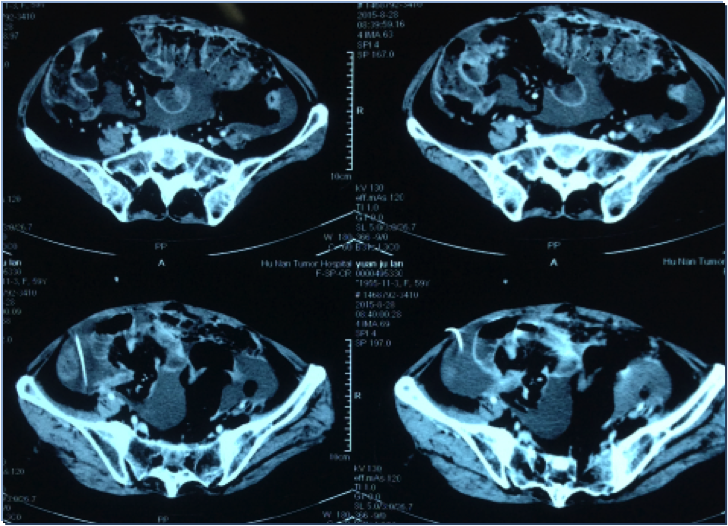 2015.8.28 肺部及腹部CT
2015.8.28 肺部及腹部CT
 2015.9.1 肠镜
2015.9.1 肠镜
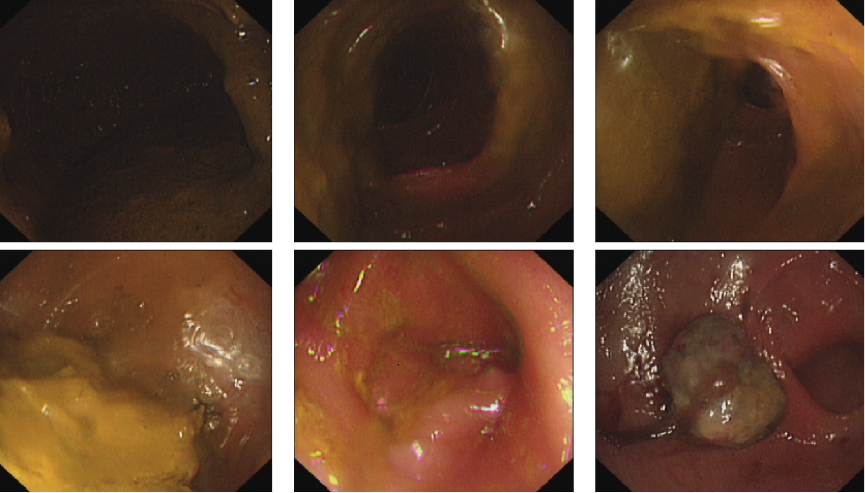 2015.9.3 肠镜病理诊断
2015.9.3 肠镜病理诊断

问题:请提出下一步诊疗方案?
此病例共有1位入围选手点评:95-张乐蒙 ;病例提供作者为:99-张永昌 。详情如下:
点评医生简介:95-张乐蒙
 点评内容分享:
点评内容分享:
概括病例特点,中年女性患者,肺癌术后两年,肺部原发病灶为腺癌,行“肺癌根治术”,术后分期IIIA期,无EGFR、ALK突变。术后病理证实第9组淋巴结转移,术后辅助化疗,但未行辅助放疗。术后1年肺部病灶复发,可疑骨新发病灶(未检查,已行姑息放疗),颈部淋巴结、锁骨上淋巴结复发,液体活检未发现驱动基因突变。
此次入院以腹痛和肛门停止排气排便为主要临床表现。体查腹水征阳性,肠鸣音活跃。影像学提示双肺多发结节,胸腔积液,胸膜增厚,腹腔积液,不完全性肠梗阻,直肠占位。肠镜可见直肠肿物,病理检查为分化差的癌。我将重点从患者就诊的主要原因,不完全性肠梗阻、直肠占位和腹腔积液入手分析。
1、肿瘤患者合并不完全性肠梗阻的常见原因分析及处理。
患者有肺癌病史,术后肺部病灶复发,骨出现新发病灶,此次以腹痛和肛门停止排气排便为主要临床表现。体查胸部呈术后改变,腹腔积液,肠鸣音活跃。肠镜可见直肠肿物,病理检查为分化差的癌。影像学提示双肺多发结节,腹腔积液,不完全性肠梗阻,直肠占位。
不完全性肠梗阻的原因,除了明确的直肠肿物导致机械性梗阻外,还需考虑化疗药物、腹腔积液、腹腔感染等相关因素。不完全性肠梗阻的治疗,包括原发疾病的治疗,以及禁食、胃肠减压、生长抑素抑制消化液分泌、肠外营养支持、抗感染、维持水电解质平衡等综合治疗,也可以给予石蜡油鼻饲、腹部按摩、热敷等处理,发生绞窄性肠梗阻或急腹症时可以行急诊手术治疗。
2、原发性支气管肺癌直肠转移,原发性支气管肺癌合并直肠癌的鉴别诊断。
肠镜发现直肠占位,究竟是原发性支气管肺癌少见肠道转移,还是双原发癌,建议完善直肠活检病灶的免疫组化检测及多基因检测,以明确直肠病灶的病理类型、原发部位及基因状态。需行免疫组化包括:CKpan、EMA、CK20、CK7、CD3、CDX-2、TTF-1、Ki-67、P40、CgA、Syn、LCA等,以鉴别原发性支气管肺癌直肠转移和原发性支气管肺癌合并直肠癌。
3、对原发灶和转移灶进行二代测序的重要性。
患者PS评分2分,肺部原发病灶可以采用单药化疗。该患者肺部原发灶仅检测EGFR和ALK状态,液体活检行多基因检测未发现驱动基因突变。但原发灶可能存在罕见驱动基因突变,液体活检也有一定的假阴性率。因此,建议对肺部原发灶和直肠转移灶(或直肠原发灶)进行二代测序。如果原发灶和转移灶能发现驱动基因突变,进行靶向治疗,仍可临床获益,且改善患者的生活质量。
4、腹腔积液的形成原因及处理。
第一,引流腹腔积液,行腹水常规、生化、肿瘤标志物、细胞学、革兰氏染色及细菌学培养。明确腹腔积液性质是渗出液还是漏出液。第二,结合病例,腹腔积液形成的可能原因包括,癌细胞腹膜转移、腹腔感染、不完全肠梗阻、低蛋白血症、肝脏基础疾病等。第三,腹腔积液的治疗包括对于原发疾病的全身治疗,以及局部治疗,会在第五点讨论。
5、抗血管生成治疗在胸腔积液和腹腔积液中的应用。
第一、联合治疗。从ECOG4599到BEYOND,从Avial到REVEL,贝伐珠单抗联合化疗的疗效,已经得到公认。第二、抗血管生成制剂在控制胸腔积液、腹腔积液中的应用。前瞻性随机对照Ⅱ期研究提示贝伐珠单抗对恶性胸腔积液控制率高,可采用静脉联合化疗或胸腔局部灌注等方式,通过降低血管通透性,减少胸水生成(1)。这位患者可以考虑采用贝伐珠单抗或重组人血管内皮抑制素进行局部或全身治疗。第三,解除肠梗阻后,如果排除感染性因素,还可以考虑化疗药物局部灌注。
6、手术相关问题。
第一、N2阳性患者术后辅助治疗。这是一个“老生常谈”的问题,对于IIIA期NSCLC患者,术后辅助放疗可以改善IIIA-N2患者的总生存(2),对于该患者,除了术后辅助化疗,还需要辅助放疗。根据ADJUVANT研究(3),如果存在EGFR敏感突变,可以考虑术后辅助靶向治疗。
第二,医生手术技巧个体差异的影响。手术本身就是影响预后的最大不确定因素。手术不是流水线生产出来的标准化“商品”,手术是外科医生日积月累、匠心仁心打造的“艺术品”。虽然按照“完全性切除标准”执行,但是“完全性”的执行程度难以标准化和评估,可能影响患者预后。
点评医生简介:1-蔡修宇
 点评内容分享:
点评内容分享:
病例特点:
1、中年女性患者,既往无其他慢性病病史。
2、12年行左肺癌根治术,术后诊断为肺腺癌,pT2aN2M0,IIIA期,EGFR-,ALK未知。
3、术后行多程DP、PC方案辅助化疗。术后1年出现双肺、胸膜转移,多发淋巴结及左股骨转移。后行多程AC方案化疗及骨转移灶姑息放疗。液体活检未见明显相关基因突变。
4、本次入院主症为腹痛伴停止排便排气。查体上腹轻压痛,移动性浊音+,肠鸣音活跃。CT示双肺多发占位,胸腔积液,腹腔积液,不完全性肠梗阻,直肠占位。肠镜示直肠肿物,病理示分化差。
下一步需要解决以下几个问题:
1、肺癌术后患者合并不完全性肠梗阻原因及处理办法:进一步明确直肠肿瘤来源,如果为第二原发可以考虑手术切除解除梗阻,如果考虑转移,则保守治疗为主,考虑全身治疗。
2、胸腔积液及腹腔积液性质检查及处理办法:抽取胸腔及腹腔积液离心取沉渣包埋行免疫组化及相关基因检测。可以考虑加上抗血管药物减少胸腹水。
3、直肠占位查因决定下一步治疗方案:肺癌肠M?原发性直肠Ca?完善病理检查及免疫组化。
4、肺癌原发病灶及直肠病灶二次基因检测,避免假阴性结果。
病例提供作者简介:99-张永昌
 病例提供作者自评:
病例提供作者自评:
1、肠梗阻明确?
明确,一旦穿孔,后果严重,首先对症支持治疗。禁食、胃肠减压、清洁灌肠、肠外营养、腹水引流、生长抑素等对症支持治疗。
2、其次,直肠占位性质如何?决定治疗方案差异!
肠镜提示直肠占位,考虑原发性直肠癌,不排除转移,必须行免疫组化检测,病理结合免疫组化(CK+ EMA+ CK7± CK20- CD3- CD20- CDX-2- TTF-1+ Ki-67约30% ALK-),分析病史,考虑转移性腺癌,肺来源可能性大,符合肺癌直肠转移(虽然极其罕见)。
3、 还不够,基因检测结果可靠不可靠?
根据WCLC 2015 ORAL03.05关于罕见突变使用培美曲塞的研究,该患者使用培美曲塞(虽治疗中断)PFS明显长于JMDB等其他研究的数据,且根据IPASS、FAST-ACTII、EUTAC、BENEFIT等研究,关于组织与血浆基因突变一致性的亚组分析,发现可靠度80%左右,最高88%,仍然有一部分患者假阴性。该患者极有可能属于基因突变假阴性,或者属于罕见突变。因此,将直肠转移灶再送基因检测非常有必要。奇迹出现了,ROS1融合阳性(CD74/ROS1)。
4、下一步治疗方案?
无论是EUROS1 cohort. J Clin Oncol, 2015. 33(9): p. 992-9.还是Shaw et al, N Engl J Med. 2014 Nov 20;371(21):1963-71,充分证明使用crizotinib的必要性与重要性,故治疗方案为:1、克唑替尼 250mg po bid,2、唑来膦酸抗骨转移,3、对症支持治疗
5、预后如何?
服药2周,腹痛缓解,大便通畅;服药1月,肺部及腹部CT:复查CT:双肺内/左侧胸膜转移灶较前缩小,直肠肿块较前缩小,盆腹腔及腹膜后淋巴结较前缩小,腹膜转移灶较前缩小,盆腔积液较前减少,疗效评价PR。PFS 12月,后出现局部孤立脑转移,局部放疗等处理后继续口服克唑替尼,PFS 6月。
治疗前/治疗1月后
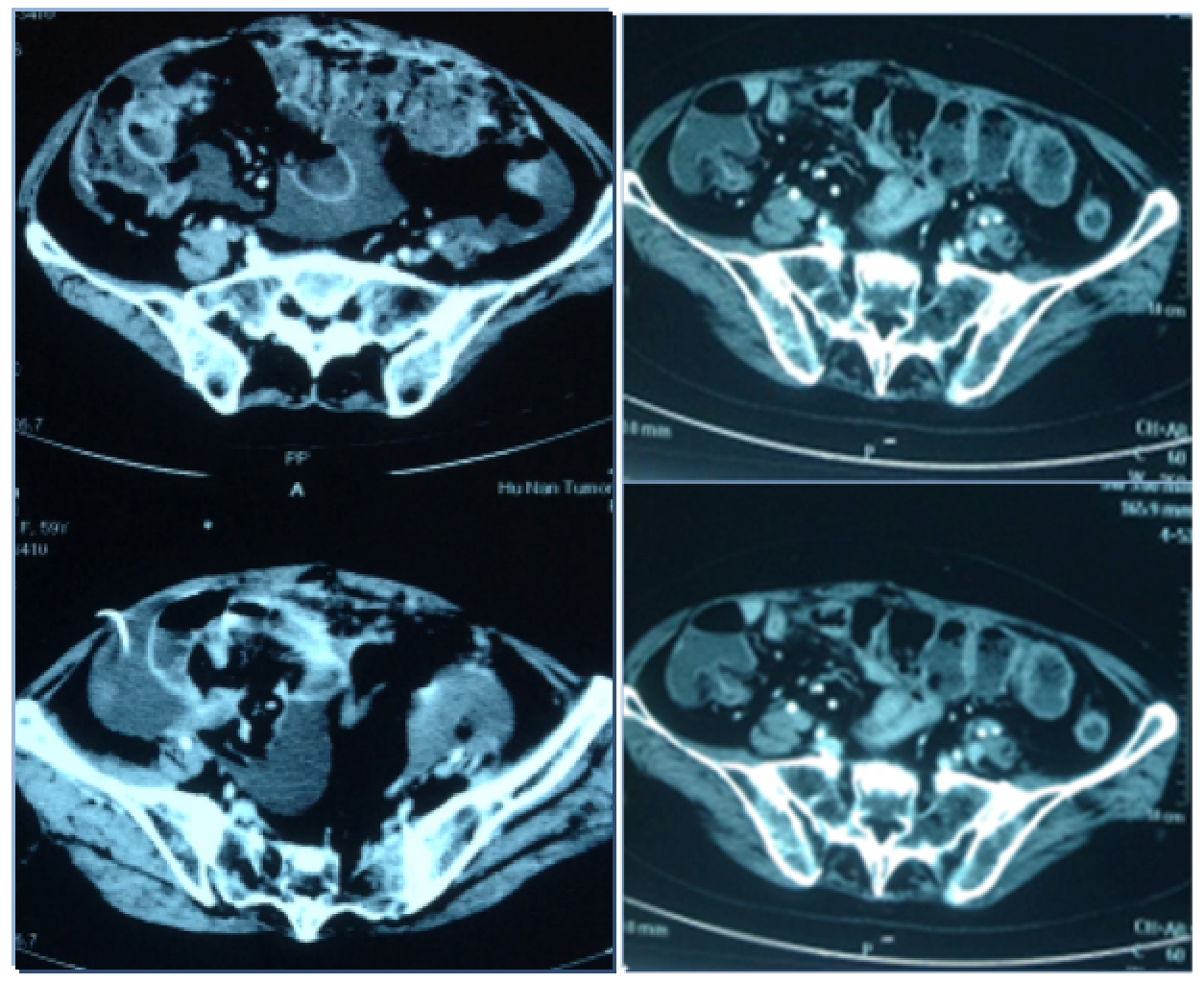
治疗前/治疗1月后

以上为【35 under 35】的观点,您怎么看?欢迎广大肿瘤医生在下方留言发表您的观点!
















 苏公网安备32059002004080号
苏公网安备32059002004080号


