【35 under 35】风采展示第二轮已经开始啦!本轮正经名叫“病例实战分析”,不正经名叫“互相伤害”,哈哈哈~100位入围选手每人提交一个有意思的病例,并就病例提出一个问题,形成一个病例库!然后100位入围选手从病例库中任意选择一个非自己提供的病例进行解读并回答问题!最后,我们将呈现病例+别人的点评+病例提供者自己的点评,同步展示!
 100位小伙伴已将自己的病例提交,并提出了问题,让我们一起先阅读下精彩病例吧!
100位小伙伴已将自己的病例提交,并提出了问题,让我们一起先阅读下精彩病例吧!
患者病史摘要
患者,女性,31岁,于2016年12月21日收治入院。
主诉:升结肠癌术后近9个月,发现腹膜后淋巴结转移2月余
现病史:
患者近9个月前无诱因出发右下腹痛,为绞痛,逐渐加重,后持续不缓解,后于外院行急诊剖腹探查术(2016-03-31),术中见右半结肠巨大肿物(6x6cm),肠管呈闭袢性肠梗阻,遂行根治性右半结肠切除术。
术后病理示(升结肠)溃疡型印戒细胞癌(图1),侵出浆膜,浆膜外可见癌结节,神经侵犯(+),脉管癌栓(+),淋巴结(20/21)。免疫组化示MLH1(-),MSH2(-),MSH6(+),PMS2(-),PD-L1(-)。
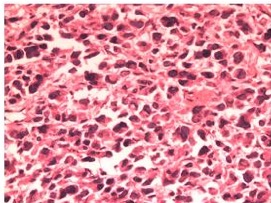 图1:手术病理,印戒细胞癌,侵透浆膜层,可见脉管癌栓。
图1:手术病理,印戒细胞癌,侵透浆膜层,可见脉管癌栓。
基因检测示KRAS、NRAS和BRAF均野生型。术后3周(2016-04-21)患者CT发现腹主动脉周围见数个小淋巴结,较大约6x5mm,余未见异常。
后患者于2016-05-03至2016-09-28行奥沙利铂联合替吉奥方案辅助化疗共8周期。2月余前(2016.10.13)患者血肿瘤标志物出现升高(CEA:66.28ng/ml,CA199:169.5U/ml),复查CT发现腹膜后淋巴结较前明显增多、增大,考虑肿瘤复发转移明确。后患者来我院就诊,并于2016年11月9日参加PD-L1单抗I期临床研究,具体为PD-L1单抗 1200mg静脉滴注 d1 Q21d,共2周期,末次用药时间为2016年11月30日。5天前患者复查CT提示肿瘤较前继续增多、增大,为进一步治疗入院。患者近2个月来进食尚可,精神好,无恶心呕吐、无腹痛腹泻、无明显手足麻木等,体重无明显变化。
入院评估:
一般情况:体重指数(BMI)23.5kg/m²,营养风险评分0分,东部肿瘤协作组(ECOG)评分0分,体表面积(BSA):1.87m²。
体格检查:生命体征均正常,皮肤巩膜无黄染。右腋下可及肿大淋巴结,大小约2.5*1.5cm,固定,质地硬,无明显压痛。心肺无殊,腹平软,未及明显肿块,无压痛及反跳痛,肝脾下界未触及。肛门指诊:肛门外观无特殊,指诊未见异常。
辅助检查:血尿粪3大常规、肝肾功能、凝血谱、肿瘤标志物等检查发现以下异常:癌胚抗原(CEA)175.4ng/ml,癌抗原(CA199)258.3U/ml。
胸部及腹部CT(2016-12-15,图2)示:新发多脏器转移(右侧腹壁、附件等),淋巴结转移较前增多、增大(双腋下、腹腔、腹膜后、髂血管旁、腹股沟淋巴结等),最大淋巴结为25*15mm。
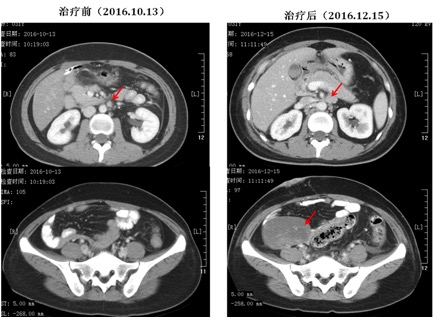 图2:PD-L1治疗2周期后CT显示腹膜后淋巴结较前明显增大,且右侧附件可见新发转移(76*51mm)。
图2:PD-L1治疗2周期后CT显示腹膜后淋巴结较前明显增大,且右侧附件可见新发转移(76*51mm)。
目前诊断:升结肠印戒细胞癌术后,右腹壁及右附件转移,双腋下、腹腔、腹膜后、髂血管旁、腹股沟淋巴结转移
问题:患者下一步的诊疗计划和治疗依据?
此病例共有1位入围选手点评:37-李咏生 ;病例提供作者为:81-鲁智豪。详情如下:
点评医生简介:37-李咏生
 点评内容分享:
点评内容分享:
1. 患者术后一线辅助化疗方案使用不规范
根据NCCN指南,结肠癌患者术后辅助化疗方案首选FOLFOX方案或者CAPEOX (XELOX)方案,可以联合贝伐珠单抗,延长患者PFS。本病例虽然患者KRAS、NRAS和BRAF均为野生型,但不推荐右侧结肠癌在一线使用西妥昔单抗,二线或者更晚线可以考虑使用;该患者采用奥沙利铂加替吉奥不符合指南,虽然替吉奥也是氟尿嘧啶衍生物,但没有相关的研究表明其可以替代5-氟尿嘧啶或者卡培他滨。
2. PD-L1作为该病例二线治疗方案注定失败
尽管在治疗皮肤癌和肺癌方面取得了显著的成功,但是免疫检查点抑制剂并没有在结肠癌方面产生相同的效果。关于为什么只有少数结肠癌患者受益,霍普金斯大学研究结果证实,这些少数结肠癌患者的MMR基因中存在缺陷(dMMR)。2017年5月23日美国FDA将免疫药物PD-1抑制剂Keytruda(派姆单抗)批准用于dMMR亚型的实体瘤患者,包括结肠癌,否则不建议使用。该病例患者MMR蛋白免疫组化提示dMMR,按说dMMR的患者可以从PD-L1/PD-1的治疗中获益,然而值得注意的是,该患者的术后病理还提示PD-L1阴性,因此该患者的二线方案使用PD-L1抗体治疗没有任何依据和意义,治疗注定无效。但需要指出的是,该患者肿瘤的快速进展和转移应该并非PD-L1抗体治疗导致,而是由于印戒细胞癌本身是高度恶性肿瘤,具有极强的侵袭转移能力。
3. 下一步诊疗计划
患者目前PS评分0分,血常规、肝肾功正常,因此可以继续考虑二线规范化化疗,同时可以加或不加靶向治疗。建议下一步治疗方案可以使用标准FOLFOX±贝伐珠单抗/西妥昔单抗,或者FOLFORI±贝伐珠单抗/西妥昔单抗。
另外,由于患者具有多种高危因素:①年轻;②T4期肿瘤;③梗阻;④神经侵犯;⑤脉管癌栓;⑥印戒细胞为主,虽然可以继续治疗,但基于这些高危因素的存在,此患者预后欠佳。
结语:
肿瘤免疫治疗是近年来最被看好的有望攻克肿瘤的治疗方法。免疫治疗的方法有许多,目前最被推崇的是免疫检查点阻断(如PD-1、PD-L1抗体)和嵌合抗原T细胞(CAR-T)。这些免疫疗法在血液系统肿瘤和部分实体瘤如黑色素瘤和肺癌中取得了令人振奋的功效,其中不乏有些患者得到了彻底治愈。然而免疫疗法也需要精准化、个体化,并常常需要联合放化疗,甚至几种免疫疗法联合。采用免疫疗法的患者需符合入组标准,比如检测PD-1、PD-L1的表达以判断患者是否会对相应抗体应答;体内DC细胞、T细胞的数量及活性的检测;前期是否采用了规范化的放化疗等等。此外,绝大多数实体瘤采用免疫治疗的效果还有待提高,因此肿瘤免疫治疗任重道远,让我们拭目以待!
--------------------------------------
病例提供作者简介:81-鲁智豪
 病例提供作者自评:
病例提供作者自评:
这是一名青年女性患者,右半结肠印戒细胞癌,以急性肠梗阻起病。在根治性术后,辅助化疗期间迅速出现腹膜后淋巴结转移,提示肿瘤生物学行为差,预后欠佳。本例患者免疫组化显示MLH1、MSH2、PMS2均为阴性,按照Bethesda标准属于MSI-H,所以参加PD-1/PD-L1单抗临床研究能给本例患者带来最大生存获益的机会。
本例患者在PD-L1单抗治疗2周期后,虽然未出现明显的症状加重,但CT发现肿瘤明确增大和增多,根据RECIST 1.1标准,应该评效为疾病进展。然而我们不能忽略的是,肿瘤免疫治疗中会存在延迟效应、假进展效应,甚至为致命的超进展效应。所以如何正确地进行诊断和鉴别诊断,是目前该患者治疗中噬待解决首要问题。
一. 患者目前的诊断和鉴别诊断:
免疫治疗后疾病超进展(Hyper -progressive disease, HPD)的发生率在8-10%左右,目前尚无统一诊断标准(表1)。Champiat等[1]使用TGR评价肿瘤生长情况,TGR为在1个月的时间内肿瘤体积增加的百分比。Kato等[2]则使用进展速率,即一定时间内靶病灶SPD增加的百分比。Saada-Bouzid等[3]则使用TGK,即一定时间内靶病灶最长径之和的变化除以此段时间。在目前的研究中,TGR的应用相对多见,但仍需要大样本的研究确定合适的临界值。另外,由于此标准需要比较治疗后TGR及基线TGR,故不能将新出现的病灶包含在内。所以,HPD的诊断标准仍需进一步完善。
 本例患者免疫治疗之前无可测靶病灶,免疫治疗1个月余后新出现广泛、多发脏器转移及淋巴结转移,其中右侧卵巢病灶最大为76x51mm。虽然,此例患者的病情变化无法用文献报道的标准来判读,但患者的病变在1月内广泛、快速进展,综合判断应属于HPD。
本例患者免疫治疗之前无可测靶病灶,免疫治疗1个月余后新出现广泛、多发脏器转移及淋巴结转移,其中右侧卵巢病灶最大为76x51mm。虽然,此例患者的病情变化无法用文献报道的标准来判读,但患者的病变在1月内广泛、快速进展,综合判断应属于HPD。
另外,本病例需要与假进展进行鉴别:假进展是指患者在接受免疫治疗之后,病灶的体积可表现为暂时性增大,甚至出现新发病灶,但而随着肿瘤细胞被清除,增大的病灶可继而缩小或消失的现象[4].。这与病灶处聚集大量T细胞及其他免疫细胞等相关。关于超进展和假进展的区别见表2 。
虽然本患者一般状况在治疗后无明显恶化,但根据目前肿瘤的生长范围和发展速度,诊断为免疫治疗后超进展明确。后续可行腋窝淋巴结活检,进一步协助鉴别诊断。
 二、下一步治疗:
二、下一步治疗:
患者出现超进展后,往往生物学行为非常差,预后极度不良,中位生存时间仅2-5个月左右[1-4]。所以本患者治疗的目的是尽可能控制肿瘤生长,延长生存。治疗上应(1)立即停用PD-L1单抗治疗,(2)积极联合应用抗肿瘤药物治疗,比如靶向药物联合伊立替康为基础的化疗等,尽快控制肿瘤生长。该患者肿瘤起源于右半结肠,虽然K-ras为野生型,但根据2017年NCCN指南,可首先考虑应用贝伐珠单抗联合FOLFIRI或XELIRI等方案治疗[5]。
总之,肿瘤超进展对临床医生来说无疑是巨大的考验之一,因为这关系着患者后续的治疗抉择,并与患者的预后明确相关。未来,我们应(1)规范HPD的诊断标准;(2)探索能提前预测HPD的标志物,这需要更多研究机构、更多患者参与的大样本研究,探索能预测HPD的肿瘤标志物;(3)需要进一步探究HPD的发生机制,从分子水平上解释HPD的发生、发展过程,进一步探索能否通过联合用药或其他途径预防和治疗HPD患者。
--------------------------------------
以上为【35 under 35】的观点,您怎么看?欢迎广大肿瘤医生在下方留言发表您的观点!
以上所有点评参考文献略。















 苏公网安备32059002004080号
苏公网安备32059002004080号


