KRAS突变广泛存在于多种癌症中,其中G12C突变占NSCLC总突变的12%左右,而G12D突变则在胰腺癌和结直肠癌中更为常见。很长一段时间内,KRAS都被医学界视为“不可成药”的靶点。如今,这一僵局已被打破。除了传统的小分子抑制剂,未来的KRAS治疗正大步迈向更加前沿的非小分子领域。
细胞疗法:重塑免疫系统
肿瘤浸润淋巴细胞疗法
肿瘤浸润淋巴细胞疗法的核心优势在于不需要寻找特定的抗原,也不需要进行HLA配型。其制备与治疗流程如下:
提取与扩增:通过手术切除患者的肿瘤组织,提取其中的肿瘤浸润淋巴细胞,并在GMP级别的实验室中进行体外大规模扩增。
清淋预处理:患者需入院接受低剂量化疗(通常为氟达拉滨和环磷酰胺)。这一步至关重要,旨在清除体内的免疫抑制细胞(如Treg细胞和MDSC),为肿瘤浸润淋巴细胞留出发挥作用的空间。
回输与刺激:将扩增好的肿瘤浸润淋巴细胞回输给患者,并联合注射白细胞介素-2,以刺激T细胞在体内长期存活和扩增。
需要注意的是,该疗法的主要毒性往往来源于白细胞介素-2注射,而非CAR-T疗法中常见的细胞因子释放综合征或神经毒性。
临床进展:Lifileucel是首个获批的肿瘤浸润淋巴疗法,已在黑色素瘤领域应用约两年。在NSCLC的早期研究中,该药物也展现出巨大潜力:在23例患者的小样本研究中,ORR达到27%,DCR高达近80%。此外,美国Moffitt癌症中心的一项研究表明,对于免疫检查点抑制剂耐药的患者,使用纳武利尤单抗联合肿瘤浸润淋巴疗法,能够带来深度且持久的肿瘤缓解。需要强调的是,肿瘤浸润淋巴疗法并不特异性针对KRAS,而是适用于各类难治性肺部肿瘤,但目前的临床试验排除具有典型EGFR、ALK或ROS1突变的患者。
CAR-T疗法
CAR-T是经过基因工程改造的T细胞,无需HLA配型即可直接识别肿瘤表面的抗原。其结构包含胞外抗原识别结构域、铰链区、跨膜区以及胞内信号传导结构域(如CD3 zeta)。随着技术迭代,第二代和第三代CAR-T加入CD28或4-1BB等共刺激分子,而第四代和第五代(被称为“TRUCKs”)甚至加入细胞因子来增强杀伤力。
在实体瘤方面,靶向SCLC表面抗原DLL3的CAR-T疗法已在I期临床中展现出极佳的耐受性和显著的疗效。然而,将CAR-T应用于KRAS突变面临巨大挑战,因为KRAS是胞内蛋白,而传统CAR-T只能识别胞外表面抗原。
应对策略与未来方向:
新抗原CAR:类似于TCR疗法,通过设计CAR结构来识别由HLA递呈到细胞表面的KRAS胞内蛋白片段。
异体“现货型”CAR-T:针对晚期患者因身体虚弱无法提供足够健康T细胞或等待时间过长的问题,通过CRISPR-Cas9技术敲除供体T细胞表面的TCR和HLA,解决移植物抗宿主病和免疫排斥问题,实现即用即取。
体内CAR-T生成:利用纳米载体包裹mRNA或使用病毒载体,直接注射入患者体内,在体内完成T细胞的转染与改造。这免去了体外扩增的繁杂步骤,目前主要在血液瘤和肝癌等少数实体瘤中进行探索。
TCR疗法
在滑膜肉瘤中,针对MAGE抗原且受HLA-A 02(覆盖30%-40%人群)限制的TCR疗法已经获批。
NEJM曾报道过一例结直肠癌患者接受TCR治疗后获得极好的初步缓解,但随后因肿瘤病灶丢失HLA亚型而产生耐药性,这也提醒我们在开发该疗法时需警惕肿瘤的免疫逃逸机制。
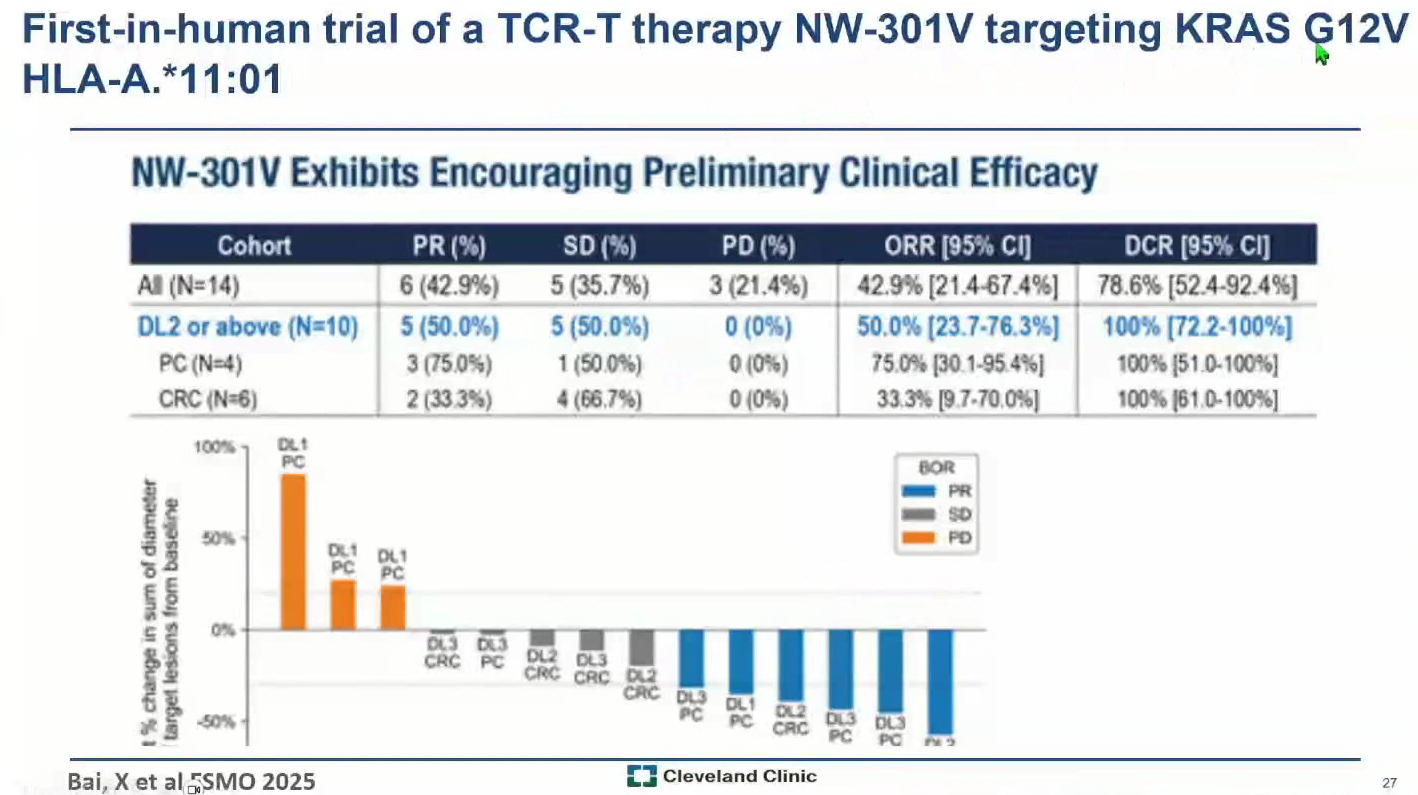
在去年的ESMO大会上,一项研究展示靶向KRAS G12V突变(受HLA-A 11 01限制)的TCR疗法数据。在14例胰腺癌和肠癌患者中,ORR达到近43%,且耐受性良好。
癌症疫苗:激活免疫系统的靶向向导
癌症疫苗可以分为三大类:利用粗提肿瘤组织的非特异性疫苗、基于预定突变的共享抗原疫苗,以及为个人量身定制的个性化疫苗。疫苗的核心组件包括抗原本身、递送系统以及用于刺激免疫反应的免疫调节剂。
研发现状与挑战:
Moderna曾推出针对KRAS G12/G13的共享抗原mRNA疫苗,虽然第一代产品已停止开发,但第二代产品即将问世。
个体化RNA疫苗通常需要对患者的肿瘤进行全外显子组测序,以寻找特异性突变。
临床落地的难点:疫苗试验的患者筛选极具挑战。患者需要签署知情同意、送检组织样本,不仅要确认肿瘤中存在特定突变(如KRAS或TP53),还必须满足严格的HLA配型条件。这导致大量患者在筛选阶段被淘汰。
此外,疫苗激发的免疫反应往往需要面对肿瘤微环境中各种免疫抑制分子的阻碍。因此,目前的疫苗研究已全面转向与PD-1或PD-L1抑制剂联合使用的策略,以克服这一耐药机制。
蛋白质降解剂:从源头清除致病蛋白
蛋白质降解是截然不同的非传统信号抑制路径。人体细胞内主要有两种降解途径:处理大分子和细胞器的溶酶体(通过自噬机制),以及处理短寿命或错误折叠蛋白的蛋白酶体(通过泛素-蛋白酶体系统)。目前进入临床视野的主要基于蛋白酶体途径,分为PROTAC和分子胶两类。
PROTAC:结构复杂,包含靶向致病抗原的弹头、连接子,以及结合E3泛素连接酶的结构域。由于分子体积较大,递送存在一定难度。目前已有多种靶向KRAS的PROTAC药物进入临床阶段,例如 ASP3082(靶向G12D) 和 CFT8919(靶向G12C)。
分子胶:机制更为简单,直接促使致病蛋白与E3泛素连接酶结合。它主要通过高通量筛选获得,具有极佳的小分子成药性。在多发性骨髓瘤治疗中广泛使用的来那度胺和泊马度胺(或沙利度胺)均属于此类。
结语与未来展望
通过非传统的信号机制直接抑制或清除KRAS突变蛋白,具有极高的临床吸引力。从肿瘤浸润淋巴细胞疗法、CAR-T、TCR到癌症疫苗和蛋白质降解剂,这些早期的概念验证数据令人振奋,为攻克KRAS提供丰富的治疗策略。
当然,未来的道路仍充满挑战。一方面,我们需要开展大规模的临床试验来进一步验证这些疗法的确切疗效;另一方面,细胞因子风暴等潜在毒性问题也不容忽视。更为现实的是,大多数细胞疗法流程高度复杂,需要完备的GMP制造设施和医疗基建支持,这在许多地区尚无法普及,是未来需要全行业共同克服的壁垒。
排版编辑:肿瘤资讯-Bear











 苏公网安备32059002004080号
苏公网安备32059002004080号


