随着精准肿瘤学的发展,针对KRAS突变的治疗已经迈入全新的阶段。在探讨KRAS突变疾病的未来时,我们的视野必须超越单一的G12C突变。为更好地指导临床开发和深入理解肿瘤生物学,我们可以将KRAS突变疾病的未来发展划分为三大核心前沿领域:生物学前沿、基因组学前沿以及临床前沿。
生物学前沿:解码KRAS的内在机制与微环境
不同KRAS变异体的存在意味着我们需要采取差异化的靶向策略。这种多样性不仅暗示肿瘤生物学的差异,也揭示肿瘤微环境和通路可塑性的不同。
划时代的生物学发现:Jonathan Ostrem 和 Kevan Shokat团队的开创性研究表明,KRAS蛋白会在结合GTP(活性状态)和GDP(失活状态)之间不断循环。在这一循环过程中,会暴露出结合口袋,药物可以嵌入该口袋,抑制这种循环,从而下调通路并导致肿瘤细胞死亡。正是由于这一循环机制具有可成药性,才使得靶向KRAS成为可能。
靶向模板的解锁:这一发现不仅为开发针对G12C的抑制剂提供模板,也为针对其他多种KRAS突变甚至Pan-KRAS(泛KRAS)和Pan-RAS靶向治疗奠定基础。例如,目前已有利用Cyclophilin A等其他分子参与这一过程的新型药物。
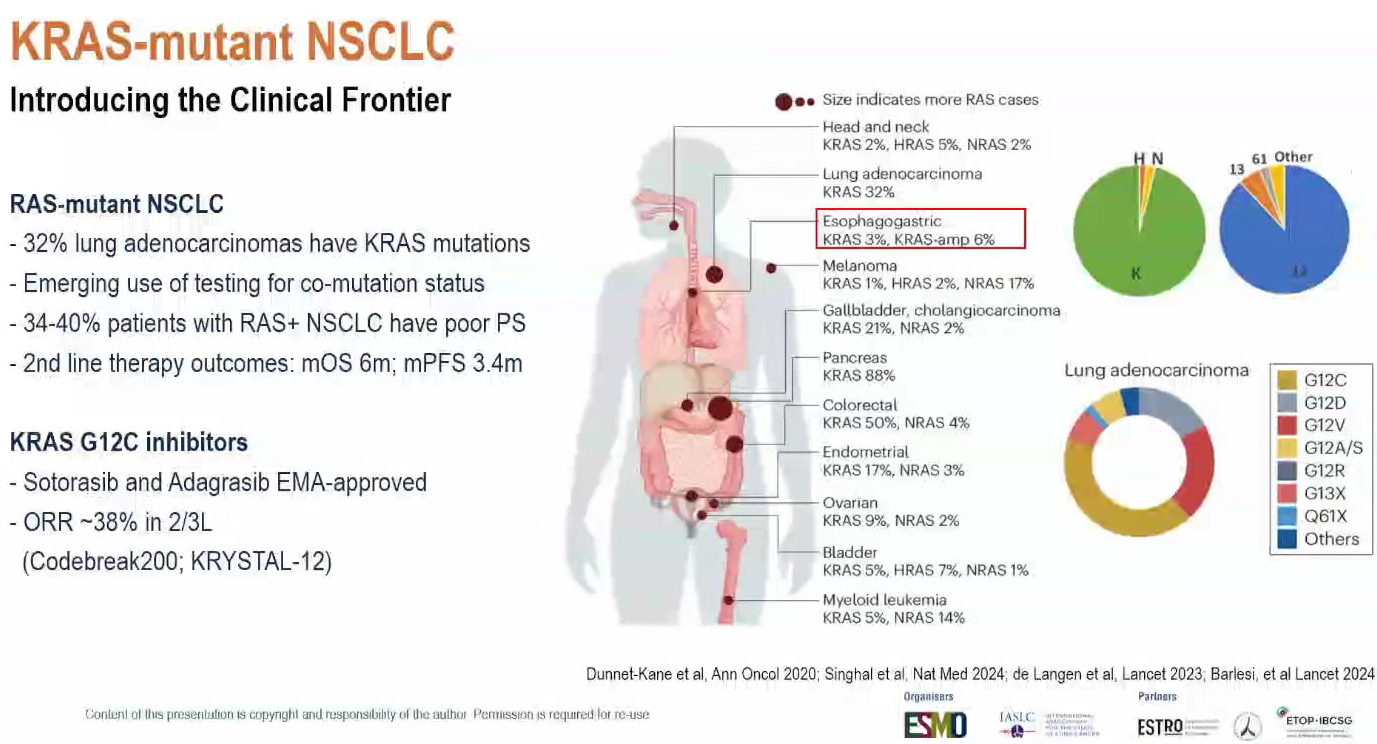
非G12C突变的统计数据:在肺癌中,超过一半的KRAS突变NSCLC属于非G12C突变。具体而言,G12C突变约占40%;在G12变异中,G12A、G12D和G12V合计占比约45%;此外还有G13和Q61突变。总体来看,非G12C突变在KRAS突变NSCLC中占据约58%的高比例。
通路抑制策略:临床开发中目前包含垂直通路抑制(如抑制SOS、SHP2和EGFR)以及水平/平行通路抑制(如联合抑制PI3K或MAPK通路),旨在最大程度地阻断KRAS信号传导。
重塑肿瘤微环境:抑制KRAS不仅影响肿瘤细胞本身,还能显著改变肿瘤微环境。它能减少免疫抑制细胞,增加促炎细胞因子,促进活化T细胞的浸润,并增强肿瘤的免疫原性。这为KRAS抑制剂与免疫疗法的联合使用奠定坚实的生物学基础。
基因组学前沿:共突变的临床意义
在临床决策中,我们不能将KRAS突变孤立看待。MD Anderson癌症中心的Nando Skoulidis团队在这一领域做出杰出贡献。
三大临床相关亚型:基于回顾性数据,研究人员识别出三个生物学和临床表现截然不同的KRAS共突变亚型:
KL亚型:KRAS合并STK11/LKB1突变。这类肿瘤通常呈现“免疫冷”表型,预后较差,且患者通常无法从免疫单药治疗中获益。
KP亚型:KRAS合并TP53突变。这类肿瘤往往表现为“免疫热”表型。
KC亚型:KRAS合并CDKN2A或SMARCA4突变。这通常预示着肿瘤具有极强的侵袭性和较差的预后。
指导免疫治疗方案:STK11/KEAP1阳性且TMB低的NSCLC患者预后最差。然而,通过分析Poseidon数据集发现,采用CTLA-4抑制剂联合PD-1抑制剂及化疗的组合方案,可以在一定程度上逆转这种劣势,这在各类型KRAS突变NSCLC患者中表现得尤为明显。
临床前沿:策略整合与患者管理
肺癌KRAS突变基线数据:约32%的肺腺癌患者携带KRAS突变。值得注意的是,34%至40%的RAS突变肺癌患者体能状态较差,这导致他们可能无法满足许多要求良好ECOG评分的临床试验入组标准。
传统治疗瓶颈:目前二线标准化疗的疗效堪忧,中位OS仅约6个月,PFS仅约3至3.5个月。虽然已获EMA批准的Sotorasib和Adagrasib在二/三线治疗中提供约38%的ORR,但临床仍需要更多元化的治疗选择。
多样化的抑制策略:
直接选择性等位基因抑制剂:如Zoldonrasib、TSN 1611等,专门针对特定突变。
降解剂:旨在降解整个通路的母体蛋白。
泛抑制剂:包含Pan-KRAS和Pan-RAS抑制剂。
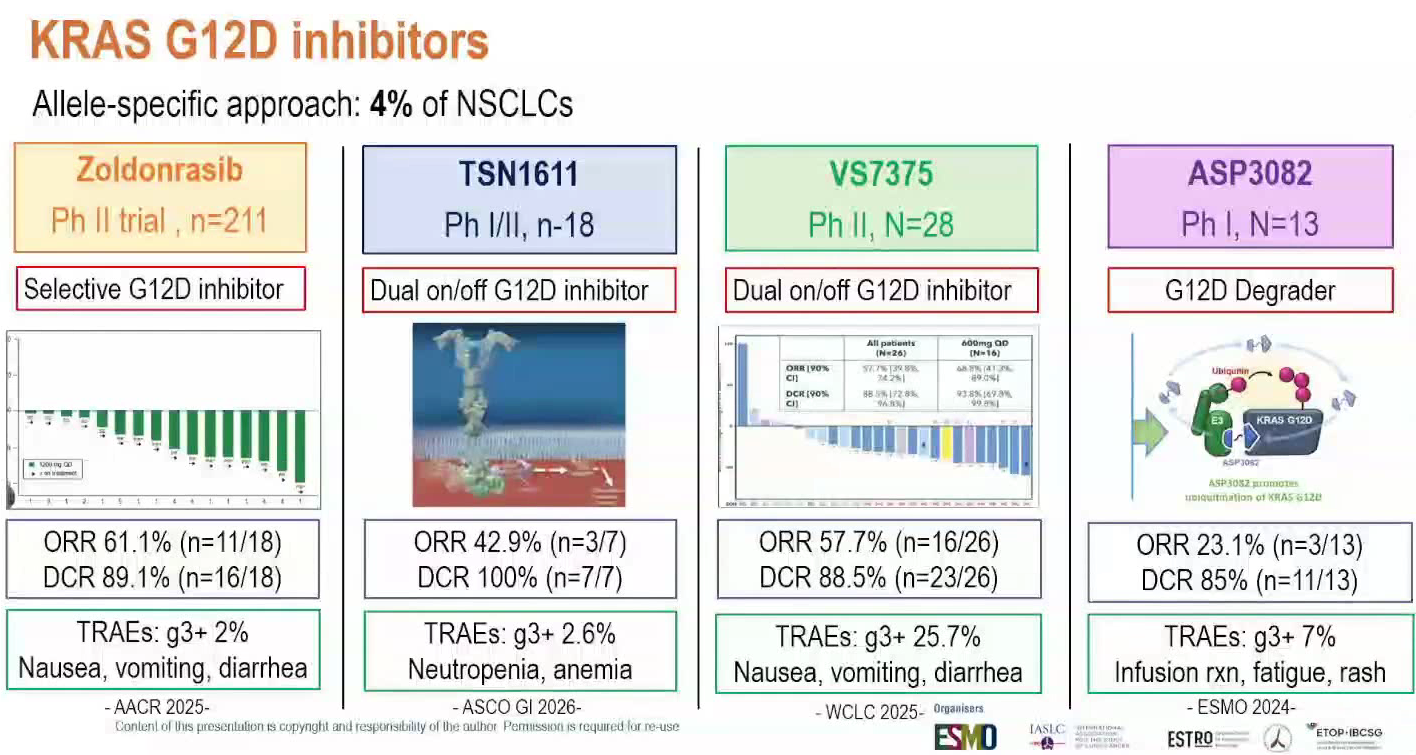
G12D抑制剂进展:G12D约占NSCLC的4%。Zoldonrasib在一项1/1b期临床试验中展现出约61%的ORR,且3级毒性(主要为胃肠道毒性)仅约2%。双重阻断剂的ORR在40%至57%之间。而新型降解剂ASP 3082(静脉给药)虽然ORR为23%,但DCR达到85%,且具有独特的毒性特征(输液反应、疲劳和皮疹)。
Pan-RAS抑制剂临床数据:首个利用亲环蛋白机制的直接Pan-RAS抑制剂在1期试验(未纳入G12C患者,包含KRAS/HRAS/NRAS突变)中,确定200mg的推荐剂量。该队列患者中29%存在脑转移。数据显示ORR为38%,中位DoR达15个月,PFS为9.8个月,OS为17.7个月。虽然89%的患者出现皮疹(3级以上仅7%),但通过剂量调整可有效管理。
联合治疗方案:Pan-RAS抑制剂联合帕博利珠单抗±化疗的数据显示潜力。在TPS>50%的患者中(联合帕博利珠单抗),ORR高达86%,DCR达100%;在联合化疗队列中,ORR为60%,DCR为90%。
未满足的临床需求与未来展望
面对如此丰富的临床试验选项和靶向策略,临床医生在决策时必须综合考量患者的年龄、体能状态、转移部位、共突变特征以及预期的毒副反应。未来,该领域需要重点关注以下四大方向:
关注弱势患者群体:填补ECOG PS评分为2分及老年患者的临床数据空白。例如,ETOP组织正在开展针对这一群体的Adagrasib的2期临床试验。
攻克获得性耐药:深入解使用泛抑制剂与等位基因特异性抑制剂后,下游获得性耐药机制的差异,从而指导后续的治疗排兵布阵。
向早期肺癌推进:将KRAS抑制剂引入新辅助和辅助治疗阶段,不仅有助于提升手术切除率,也为探索耐药机制提供绝佳的“机会之窗”。
生物学引导的精准治疗:在ctDNA时代,利用可检测的KRAS突变等位基因丰度来预测和监测疗效。已有数据显示,对Zoldonrasib产生响应的患者,其ctDNA中的VAF水平会出现显著下降。
排版编辑:肿瘤资讯-Bear











 苏公网安备32059002004080号
苏公网安备32059002004080号


