KRAS G12C突变是驱动NSCLC等肿瘤生长的关键“开关”。尽管第一代靶向药物(如Sotorasib)打破传统化疗的局限,为患者带来新希望,但其毒性与耐药问题仍是亟待克服的临床痛点。当前,新一代具备更高效价的“ON/OFF”抑制剂及联合治疗方案正强势崛起。
KRAS G12C的生物学机制
生物学通路与“开关”机制
在生理状态下,KRAS蛋白位于细胞内,负责将来自跨膜受体(如EGFR)的生长信号传递至细胞核。这一过程主要通过MAPK通路,以及PI3K-mTOR等其他通路来实现,最终诱导细胞分裂。
当发生激活性的KRAS突变时,来自KRAS的生长信号会持续处于“ON”状态,从而驱动肿瘤生成和细胞分裂,此时它表现为一种致癌基因。通常,KRAS G12C会在“ON(GTP结合态)”和“OFF(GDP结合态)”之间不断切换。
抑制剂的分类机制
针对这种切换机制,目前开发多种不同作用方式的抑制剂:
“OFF”抑制剂:将KRAS G12C锁定在关闭状态(GDP结合态)。
“ON”抑制剂:将KRAS锁定在开启状态(GTP结合态)。
双重抑制剂:同时抑制KRAS G12C的“ON”和“OFF”两种异构体。
突变特异性:这些抑制剂通常具有突变特异性,能够避开对KRAS野生型的抑制,这与Pan-RAS抑制剂有显著区别。
此外,还有一种特殊机制的药物(如Eleronrasip),它利用细胞内负责蛋白质折叠的Cyclophilin A,将KRAS锁定在开启状态(GTP结合态)。该药物形成三元复合物,阻断KRAS与RAF的结合口袋,从而有效阻断MAPK通路的信号传导。
KRAS G12C抑制剂在现有治疗体系中的潜力
目前,对于KRAS G12C突变阳性的NSCLC患者,一线标准治疗主要是化疗联合帕博利珠单抗,或根据PD-L1状态使用帕博利珠单抗单药。
然而,现有标准治疗存在明显局限性:即使是体能评分为0或1的患者,在接受标准治疗9个月后,也有高达50%的患者出现疾病进展。在临床实践中,大量患者的体能评分在2分或以上,伴有体重减轻,其身体状况根本无法耐受全剂量的化疗加免疫治疗。
这正是靶向治疗展现巨大潜力的地方。正如我们在EGFR突变、ALK融合、ROS1等其他疾病背景中所见,靶向药物起效极快,且潜在毒性低于传统化疗。这种特性使得更多身体条件较差的患者能够接受全身性治疗并获得缓解。
第一代抑制剂的疗效与局限:Sotorasib与 Adagrasib
目前,Sotorasib和Adagrasib均已获得EMA和FDA的批准。与化疗药物多西他赛相比,两者的临床数据如下:
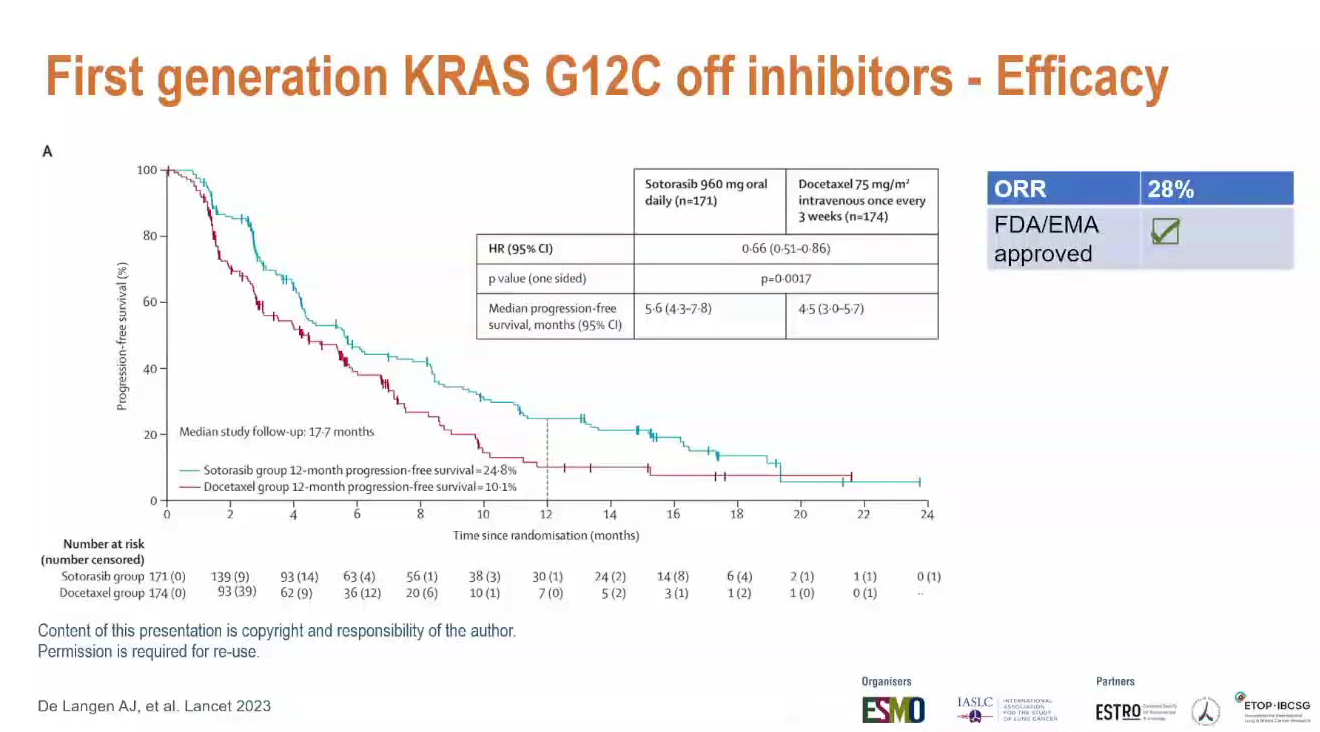
Sotorasib数据:中位PFS为5.6个月(多西他赛为4.5个月),ORR为28%,HR为0.66。
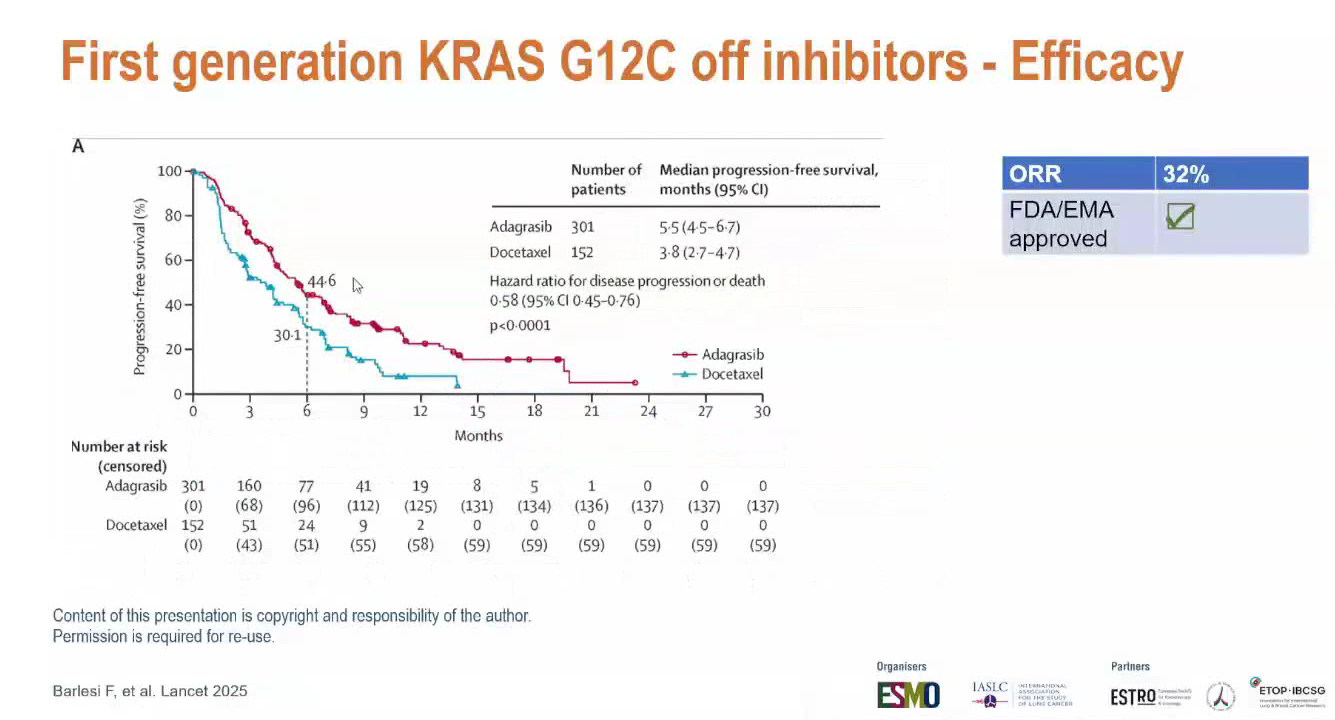
Adagrasib数据:中位PFS为5.5个月(多西他赛为3.8个月),ORR为32%,HR为0.58。
这两种药物的毒性相当严重,且与多西他赛的毒性谱完全不同。Sotorasib的3级及以上TRAE发生率为33%,而Adagrasib则高达47%。
耐药机制及新一代高潜力抑制剂的崛起
关于耐药性,令人瞩目的是约有55%的患者并未发现明确的获得性耐药机制。这意味着这些肿瘤可能依然依赖于KRAS G12C通路,更强效的抑制剂或许仍然能够发挥作用。另一方面,我们也观察到熟悉的耐药机制,包括:靶点结合口袋突变及其他继发性突变、垂直或水平通路的旁路耐药机制,以及组织学转化。
新一代抑制剂在抑制KRAS G12C的效价(通过测量磷酸化ERK的纳摩尔浓度评估)、中枢神经系统(CNS)活性、以及作为单药或联合用药的耐受性方面存在明显差异。
其中,Divorasib和Olomorasib表现突出。在1/2期数据中,它们展现极佳的疗效-毒性比,3级及以上TRAE的发生率较低,且缓解持久。尽管需要警惕3期临床试验数据可能会有所回落,但初步证据显示:在先前接受过Sotorasib或Adagrasib治疗后发生进展的39例NSCLC患者中,使用更强效的KRAS G12C抑制剂可获得41%的ORR,且中位PFS远高于单纯“再治疗”的预期效果。
KRAS G12C“ON”抑制剂(如Eleronrasip)利用亲环蛋白A机制的“ON”抑制剂展现极具前景的数据:
在未接受过KRAS G12C抑制剂治疗的患者中:确定的ORR高达56%,中位PFS为10.3个月,3级及以上TRAE仅为19%。
在既往接受过抑制剂治疗的患者中:确定的ORR仍有42%,毒性较低。这进一步证明部分肿瘤依然依赖于该通路,需要3期试验来进一步验证。
联合治疗的探索:机遇与挑战
SHP2蛋白在KRAS G12C从关闭状态切换到开启状态的过程中起推动作用。理论上,阻断SHP2联合KRAS G12C抑制剂可以产生更好的抗肿瘤作用。然而,临床数据显示这种联合会导致毒性大幅上升。虽然在初治患者中看到不错的缓解率,但在经治患者中,缓解率仅约为10%(甚至低于强效KRAS抑制剂单药的疗效)。目前来看,联合SHP2抑制剂带来高毒性,却尚未释放出明显提高疗效的信号。
EGFR上调是已知的耐药机制之一,这在结直肠癌中更为普遍,但也在NSCLC的临床前模型中被观察到。KRAS G12C抑制剂联合西妥昔单抗的一线治疗1/2期数据非常具有前景(3期数据等待中)。对于那些不适合化放疗,或者PD-L1阴性/伴随STK11突变、对免疫治疗反应率极低的患者而言,这也是不错的治疗选择。
总结
目前,Sotorasib和Adagrasib在大多数国家已可用于二线治疗。随着更强效的“OFF”、“ON”以及双重机制抑制剂进入临床开发阶段,我们需要时间去验证谁将成为“同类最佳”药物。未来的临床研究重点将集中在:如何对这些药物进行序贯使用、探讨“ON”加“OFF”抑制剂的联合、以及与泛RAS抑制剂的联合。当前,大量KRAS G12C抑制剂联合帕博利珠单抗(联合或不联合化疗)的一线研究正在进行中。
排版编辑:肿瘤资讯-Bear











 苏公网安备32059002004080号
苏公网安备32059002004080号


