分子诊断已成为NSCLC精准治疗的绝对基石。在2025年,全面且及时的NGS筛查是制定最佳一线方案的核心前提。当前,打破EGFR单药“舒适区”的联合疗法、针对罕见驱动基因的创新药,以及向早期推进的靶向治疗,正全面重塑治疗格局。然而,新型ADC与双抗等策略的涌现也让临床决策空前复杂。在疗效与毒副作用之间寻求最优解,亟需依托高质量的循证数据、多学科协作以及医患间的共享决策。
分子诊断:精准治疗的基石
广泛的生物标志物筛查
在做出1L治疗决定之前,指南建议对肿瘤组织(初始活检)进行全面的生物标志物检测。
免疫组化:用于检测PD-L1表达水平。
基因突变:必须涵盖EGFR、BRAF、HER2、METex14以及 KRAS G12C。
基因融合:必须涵盖ALK、ROS1、RET、NTRK1-3和 NRG1。
初始NGS面板中的其他标志物:通常还包括KEAP1、STK11、TP53和MTAPdel等,它们多用于预后评估、探索性研究或临床试验入组。
检测方法的选择与耐药后重检
NGS的作用:鉴于组织样本有限且治疗靶点不断增加,NGS是必不可少的。
DNA与RNA结合:同时进行DNA和RNA-NGS非常重要,其中RNA-NGS对于高敏感度的融合基因检测是必不可少的。
液体活检与组织活检:液体活检具有高特异性,但敏感性有限,因此组织活检仍然是金标准。
进展后检测:在疾病进展时,通过组织再活检检测MET扩增、HER2扩增等耐药机制变得日益重要。
等待检测结果的临床意义
一项关于晚期NSCLC的真实世界OS研究强调基于分子图谱指导治疗的重要性。
在基因突变报告出具后才开始治疗的患者(Group A),其中位OS为28.8个月。
在报告出具前就开始治疗,但未在35天内切换至TKI的患者(Group C),中位OS骤降至15.3个月。
核心建议:如果必须在分子分析完成之前开始治疗,应考虑先进行1个周期的化疗,且不应加入免疫治疗。
晚期/转移性NSCLC:经典与罕见靶点的突破
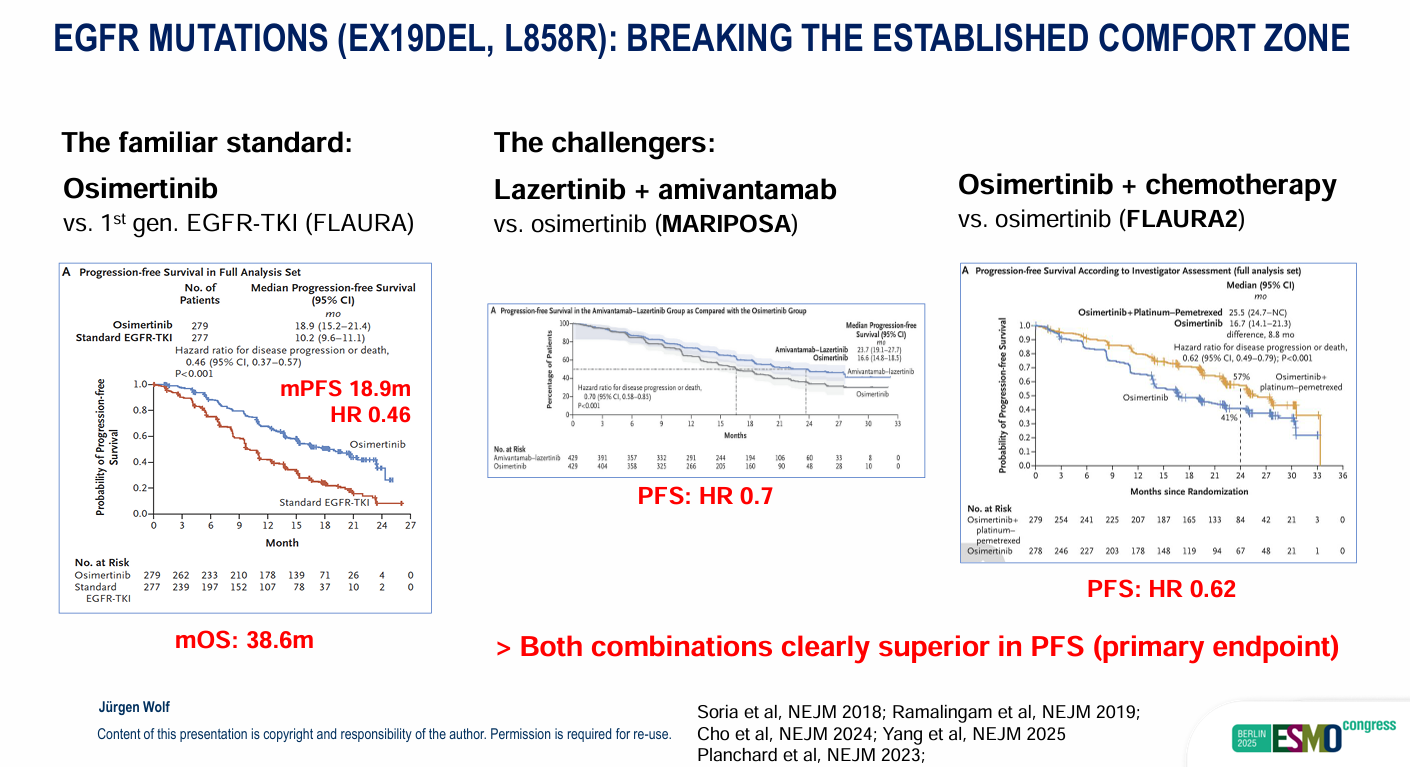
EGFR突变(ex19del, L858R):打破既定“舒适区”
长期以来,奥希替尼单药相较于第一代EGFR-TKI(FLAURA研究,中位PFS18.9个月,HR 0.46,中位OS 38.6个月),一直是大家熟悉的标准治疗。然而,两项关键的联合疗法挑战这一“舒适区”。
Lazertinib联合amivantamab (MARIPOSA研究):相比于奥希替尼,该联合方案将中位PFS从16.5个月提升至23.7 个月(HR 0.70)。3年OS率也从51%提升至60%(OS HR 0.75)。
奥希替尼联合化疗(FLAURA2研究):相比于奥希替尼单药,联合化疗的中位PFS为25.5个月(HR 0.62)。其中位 OS达到47.5个月(OS HR 0.77),3年OS率为63% vs 51%。
个体化决策:对于高龄(>80岁)、有合并症、无脑转移或无TP53突变的患者,第三代EGFR-TKI单药治疗仍可能是首选。治疗必须纳入患者偏好,进行医患共享决策。
融合驱动基因:ALK, ROS1, RET, NTRK, NRG1
对于融合驱动的肿瘤,新一代TKI设定极高的疗效基准。
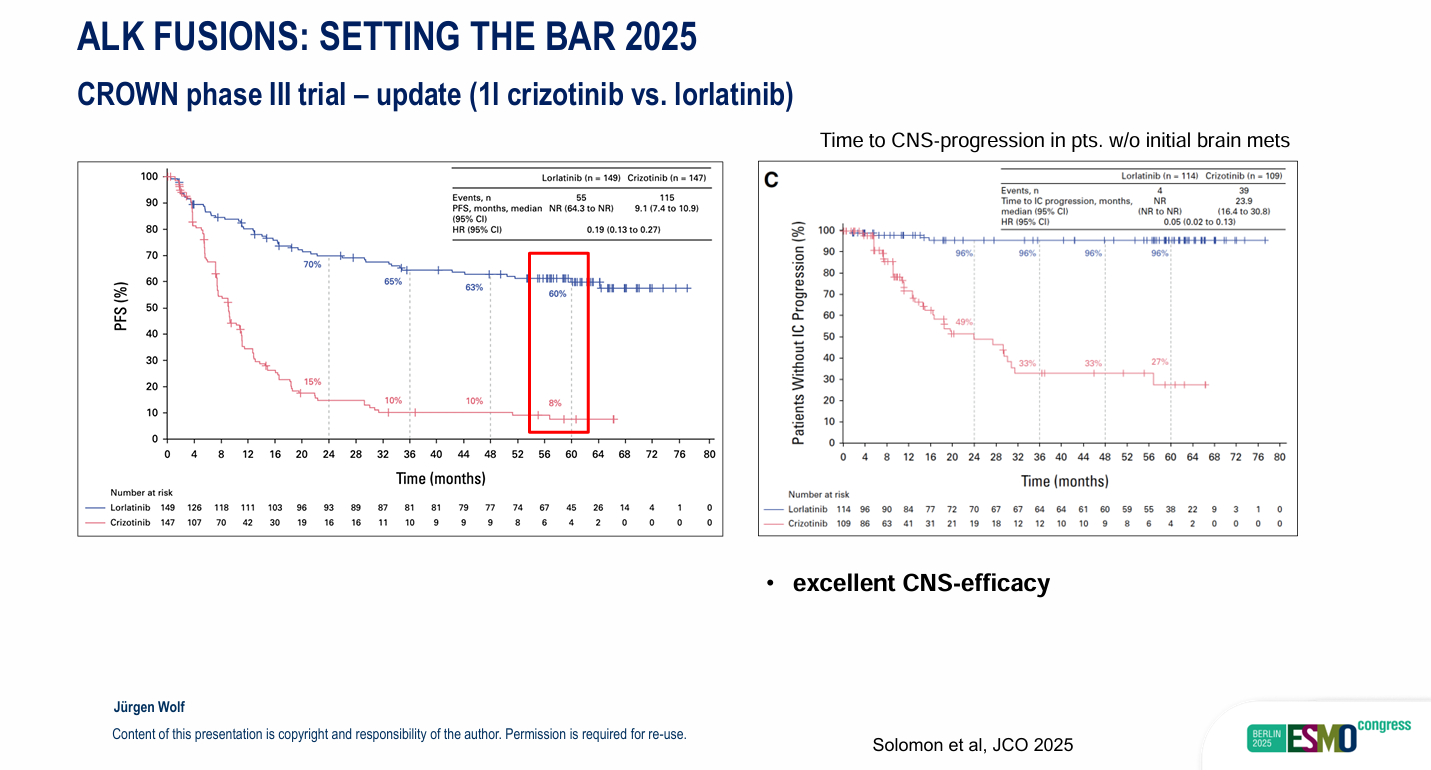
ALK融合:在CROWN Ⅲ期研究中,相较于克唑替尼,洛拉替尼展示出显著的优势。其3年PFS率为65%,5年PFS 率高达60%(HR 0.19)。此外,洛拉替尼展现出卓越的CNS疗效,在无基线脑转移的患者中,其发生颅内进展的风险极低(HR 0.05)。
ROS1融合:这是一种罕见突变,但拥有多种活性药物。目前的证据支持“最佳药物优先”的策略。例如,新一代 ROS1-TKI Repotrectinib作为一线治疗,ORR达79%,中位PFS为35.7个月,且对耐药突变(如G2032R)和脑转移均有极高活性。
RET和NTRK融合:拥有明确的1L治疗标准,Selpercatinib治疗RET融合的ORR达84%,中位PFS为25 个月。NTRK融合则首选Entrectinib或Larotrectinib。
NRG1融合:对于这一极罕见靶点,双特异性抗体 Zenocutuzumab(靶向HER2/HER3)是标准治疗失败后的有效选择。
罕见突变与KRAS
BRAF V600E:目前有Dabrafenib/trametinib和 Encorafenib/binimetinib两款获批的靶向联合方案。然而,最佳一线策略仍存在争议。真实世界数据显示,一线使用TKI或免疫(联合或不联合化疗)的OS几乎完全相同(均为28个月,HR 1.1)。
METex14与EGFRex20ins:METex14跳跃突变患者一线首选Capmatinib或Tepotinib。EGFR ex20ins的标准一线方案则是卡铂/培美曲塞联合Amivantamab。
HER2突变:目前抗体偶联药物Trastuzumab-deruxtecan(T-DXd)已获批用于含铂化疗后的二线治疗。同时,新型TKI(如Zongertinib和Sevabertinib)正在开展一线Ⅲ 期临床试验。
KRAS突变:目前获批的G12C抑制剂(Sotorasib和 Adagrasib)在化疗/免疫后二线治疗中的疗效相对适中(ORR约30%,PFS约5.5个月)。目前包括针对G12D、G12V的抑制剂、KRAS(ON)抑制剂(针对活性GTP结合形式)、泛KRAS抑制剂以及各种联合疗法正在探索中,部分联合免疫疗法展现出令人印象深刻的初期疗效。
早期和局部晚期NSCLC的靶向治疗
靶向药物正在迅速向早期和局部晚期推进,证据不断积累,但某些领域的数据仍不够成熟。
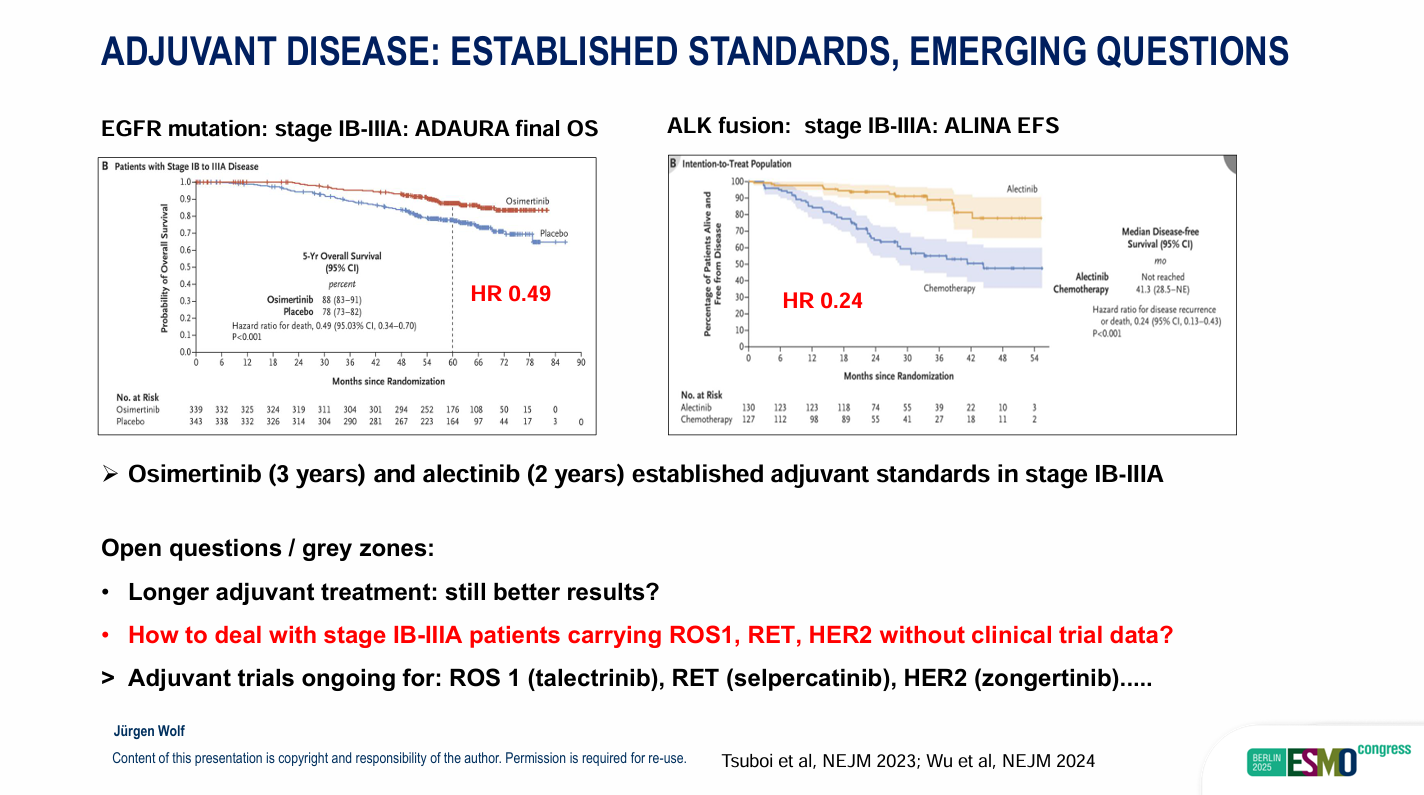
辅助治疗:在完全切除的IB-IIIA期患者中,目前已确立明确的标准。ADAURA试验证明,EGFR突变患者术后使用 3年奥希替尼可显著改善生存(5年OS HR 0.49)。ALINA 试验证明,ALK融合患者术后使用2年阿来替尼可显著延长DFS(HR 0.24)。
不可切除的III期:对于放化疗后的EGFR突变患者,LAURA 试验确立使用奥希替尼维持治疗直至进展的新标准(PFS HR 0.16)。
新辅助治疗 (Neoadjuvant):在可切除的II-IIIB期EGFR突变患者中,NEOADAURA试验探索新辅助奥希替尼联合化疗的效果。结果显示其具有很高的R0切除率(>90%)和良好的耐受性,且在新辅助治疗期间仅有1%的患者发生疾病进展。然而,其EFS数据目前仍不成熟,需要更长期的随访。
多学科讨论:对于携带ROS1、RET或HER2等其他驱动基因的局部晚期患者,目前缺乏明确的临床试验数据支持,因此将这些疗法推广到其他靶点的做法尚不明朗,临床决策必须依赖个体化的多学科团队讨论。
不断丰富的治疗策略
ADC药物:除了在HER2突变中获得成功的T-DXd,目前正在开发针对TROP2(如Datopotamab-deruxtecan和 Sacituzumab-tirumotecan)和MET(如Telisotuzumab-adizutecan)等靶点的新型ADC药物,并在EGFR突变患者中展现出活性。
双特异性抗体:除了已获批的Amivantamab(靶向 EGFR/MET),靶向PD-1和VEGF的双抗Ivonescimab在 HARMONI Ⅲ期研究中对比化疗也展现出潜力。在该研究中,对于EGFR-TKI治疗后进展的患者,Ivonescimab联合化疗组的PFS HR达到0.46。然而,尽管HR令人印象深刻,但其绝对PFS获益仅为中等的2.4个月(7.06个月 vs 4.6 个月),且OS差异不具有统计学意义。
总结
在2025年,NSCLC的精准肿瘤学已经达到新的成熟度水平。然而,随着生物标志物和治疗选择的增多,临床决策的复杂性也在不断增加,且真正的革命性突破依然罕见。持续的创新不仅需要更好的药物,更需要高质量的数据、智能的协作网络,以及与患者真诚的伙伴关系,只有这样,才能在日常临床实践中指引最佳的治疗决策。
排版编辑:肿瘤资讯-Bear











 苏公网安备32059002004080号
苏公网安备32059002004080号


