长期以来,SCLC因其极高的侵袭性、易早期转移及极高的复发率,被公认为预后最差的恶性肿瘤之一。在过去的30余年里,受限于患者复杂的合并症与极短的PFS,该领域的治疗手段几近停滞,生存数据令人沮丧。然而,历史的转折点在2025年全面到来。随着多项重磅Ⅲ期临床数据的集中爆发,这不仅打破多年的生存期瓶颈,还为SCLC患者带来更多的治疗新选择。
在2025年之前,SCLC的预后极差。它是一种起源于神经内分泌细胞的侵袭性肿瘤,生长迅速、有丝分裂率高且极易发生早期转移,因此需要快速干预。SCLC几乎全部发生在吸烟者中,患者通常伴有慢性阻塞性肺疾病、缺血性心肌病和高血压等严重合并症。尽管患者最初对化疗高度敏感,但大多数患者会在2年内复发并死亡。在2025年之前,LS-SCLC的中位PFS仅为15个月,中位OS为30个月;ES-SCLC的中位PFS仅为5个月,中位OS为12个月。在长达30多年的时间里,该领域几乎没有重大治疗进展。
然而,在2025年,临床数据迎来历史性突破。对于LS-SCLC,ADRIATIC试验将中位PFS提升至16.6个月,中位OS大幅延长至55.9个月。对于ES-SCLC一线治疗,IMFORTE试验将中位PFS提升至5.4个月,中位OS达到13.2个月。即使在ES-SCLC的二线治疗中,DeLLphi 304试验也实现5.3个月的中位PFS和13.6个月的中位OS。
放疗领域的探索
在放疗方面,中国进行一项针对局限期SCLC的大型多中心III期试验,比较常规放疗(ConvRT,60Gy/2Gy/30F)与大分割放疗(HypoRT,45Gy/3Gy/15F)的疗效。该试验纳入年龄在18-70岁、ECOG PS评分为0-1的患者。ConvRT组和HypoRT组的中位OS分别为47.9个月和40.2个月(P=0.752,HR=1.04)。HypoRT组未能达到OS的非劣效性界值,两组在PFS上也没有显著差异。但是,HypoRT显著降低放射性肺炎和淋巴细胞减少症的发生率。
LS-SCLC:同步放化疗后的免疫巩固治疗
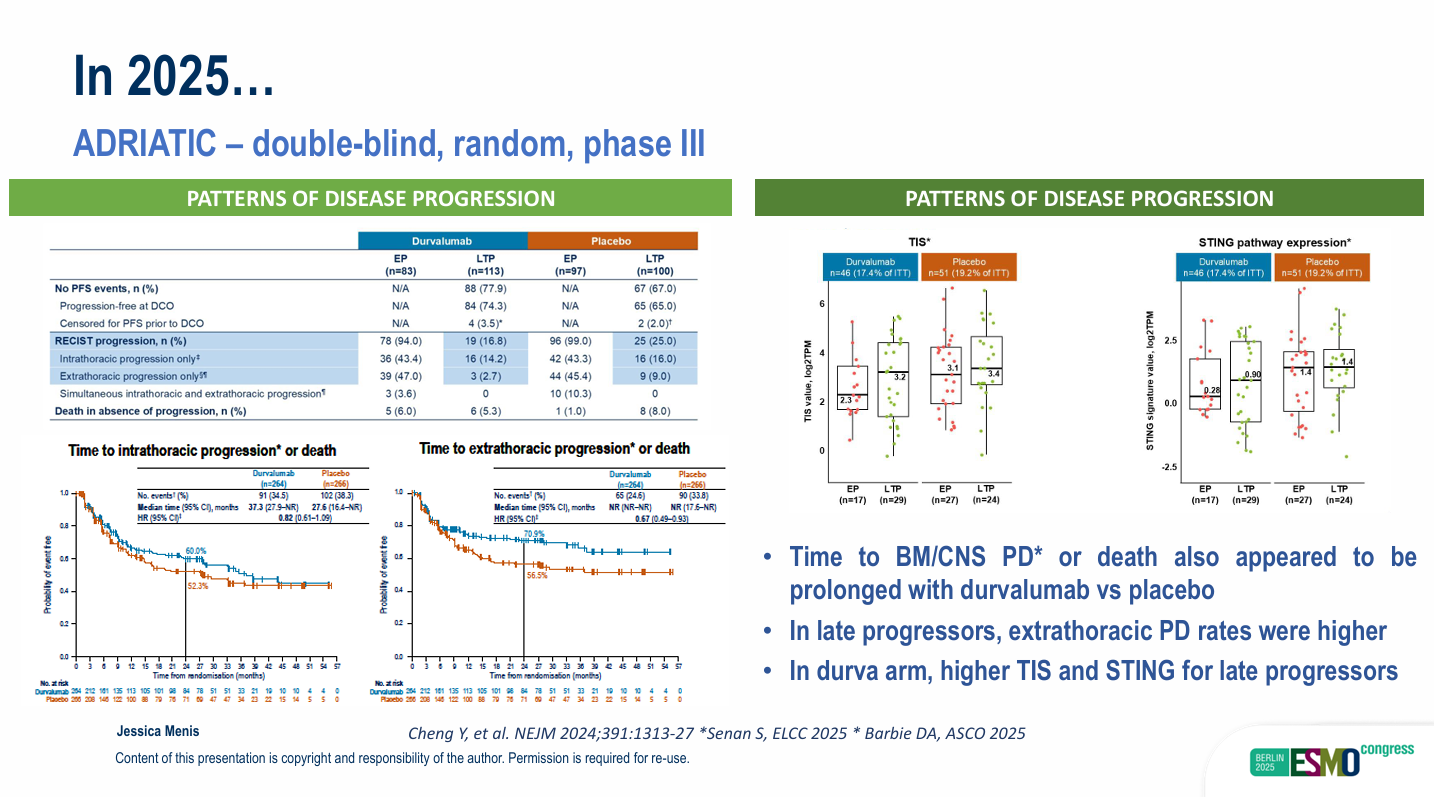
ADRIATIC试验显示,Durvalumab组对比安慰剂组,实现OS和PFS的双重主要终点获益。
OS显著延长:55.9个月对比33.4个月(P=0.01)。
PFS显著延长:16.6个月对比9.2个月(P=0.02)。
在亚组分析中,接受PCI的患者,Durvalumab组的PFS和OS分别为19.8个月和45.5个月;未接受PCI的患者则为10.4个月和24.5个月。
使用顺铂的患者中,Durvalumab组的PFS为11.4个月(安慰剂组为9.7个月),OS为41.9个月(安慰剂组为34.3个月)。使用卡铂的患者中,Durvalumab组的PFS为27.9个月(安慰剂组为9.2个月),OS为未达到(NR,安慰剂组为33.4个月)。
发生晚期进展的患者在Durvalumab组中表现出更高的肿瘤炎症特征和STING通路表达。同时,Durvalumab也延长脑转移/中枢神经系统进展或死亡的时间。
ES-SCLC:一线维持与后线治疗的突破
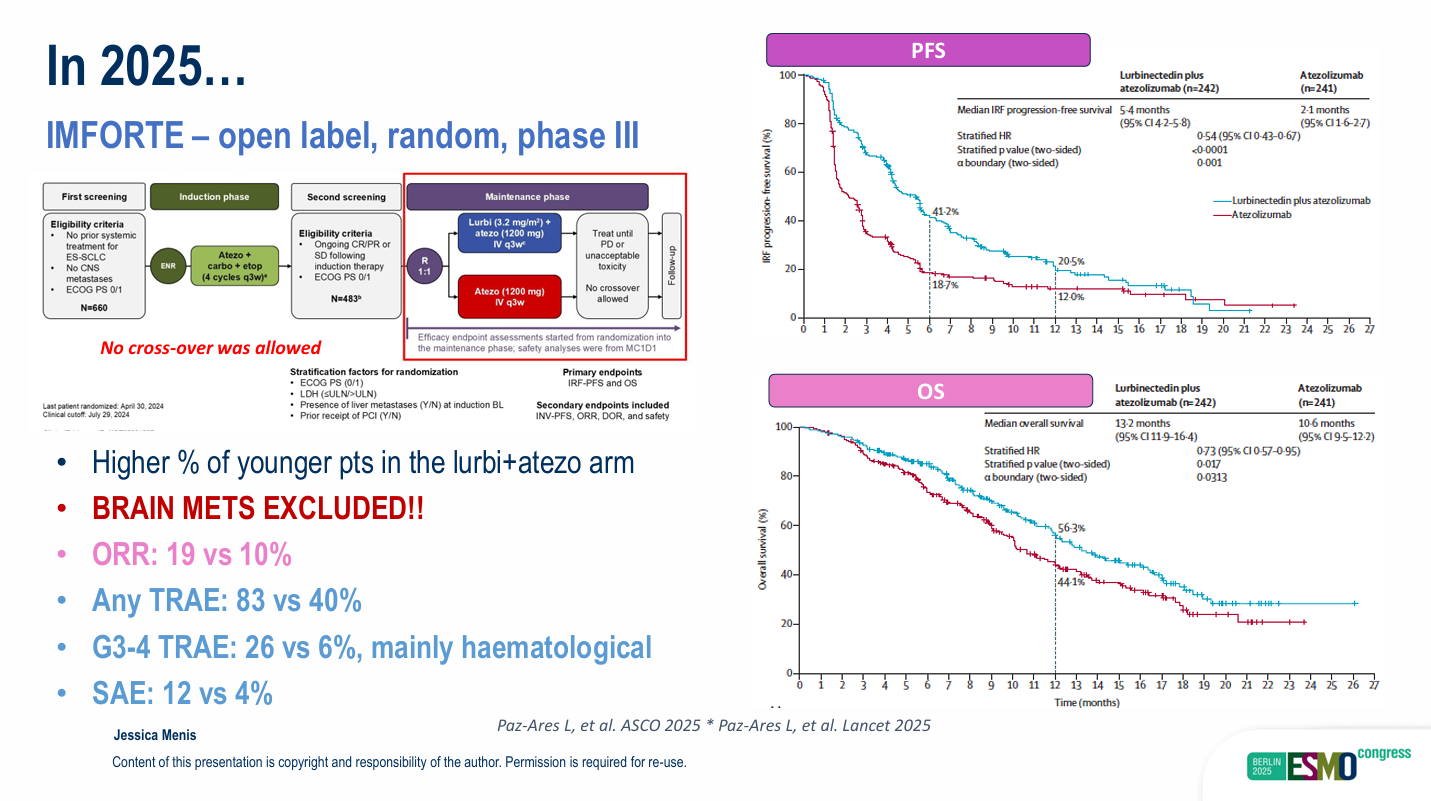
一线维持治疗:IMFORTE试验
IMFORTE是一项开放标签、随机的III期试验,针对在4个周期Atezolizumab+卡铂+依托泊苷诱导治疗后未出现进展的ES-SCLC患者。
患者被随机分配接受Lurbinectedin+Atezolizumab或单药Atezolizumab的维持治疗,且不允许交叉用药。联合治疗组的中位PFS为5.4个月,显著优于单药组的2.1个月(HR 0.54,P<0.0001)。联合治疗组的中位OS为13.2个月,优于单药组的10.6个月(HR 0.73,P=0.017)。联合治疗组的ORR更高(19% vs 10%)。
然而,联合治疗组的安全性挑战更大,任意级别治疗相关不良事件发生率为83%(单药组为40%),G3-4 不良事件发生率为26%(单药组6%,主要为血液学毒性)。不良事件的发生率主要集中在治疗的前9周。
二线及以上治疗:Tarlatamab的应用
DeLLphi-303试验:在ES-SCLC一线化学免疫治疗后探索Tarlatamab的联合应用,显示出24%的ORR。
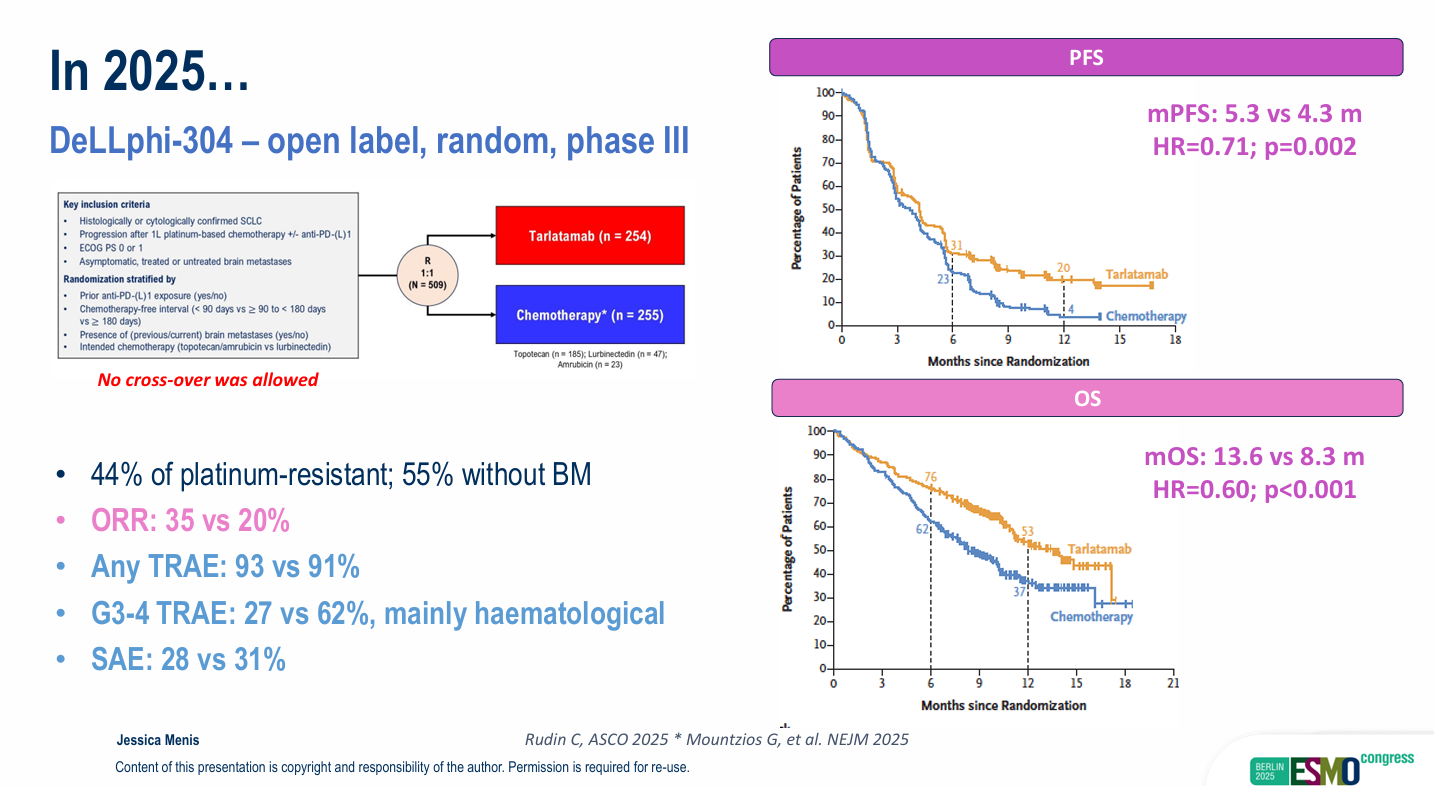
DeLLphi-304试验(III期):针对一线铂类化疗失败的患者,比较Tarlatamab与标准或研究者选择的化疗(如Topotecan、Lurbinectedin、Amrubicin)。Tarlatamab组的中位PFS为5.3个月(化疗组4.3个月,HR=0.71,P=0.002),中位OS达到13.6个月(化疗组8.3个月,HR=0.60,P<0.001)。
安全性方面,Tarlatamab组出现CRS和ICANS。总体CRS发生率为37%,主要为1级(28%),没有观察到4级CRS或ICANS。
新兴疗法与转化医学展望
在2025年,各类新型药物在SCLC中展示巨大潜力:
双特异性T细胞衔接器/T细胞接合剂:包括Obrixtamig(正进行I-II期剂量评估)、Gocatamig、ZG006(Alveltamig,II期试验中10mg和30mg剂量的ORR分别达到62.5%和58.3%)、Pumitamig和Ivonescimab。
抗体偶联药物:针对DLL3靶点的SHR-4849在所有线数的ORR达73.2%。针对B7-H3靶点的I-DXd(DS7300)在总人群中确认的ORR为48.2%。其他靶点还包括SEZ-6(ABBV-706)和TROP2(Sacituzumab Govitecan)。
CAR-T细胞疗法:靶向DLL3的LB2102在早期研究中ORR为13.3%,且未观察到剂量限制性毒性或ICANS。
放射性药物疗法:如225Ac-DOTATATE(RYZ101,靶向SSTR)和225Ac-ABD147(靶向DLL3),通过释放α粒子导致细胞死亡。
转化医学与精准治疗:
未来的试验如SWOG S2409(PRISM)正在引领SCLC进入精准医学时代。该试验基于四种SCLC分子亚型(A亚型:ASCL1上调;N亚型:NEUROD1过表达;P亚型:POU2F3过表达;I亚型:炎症通路上调)对患者进行分层,并在此基础上分配特定的靶向药物(如Saruparib、Ceralasertib、Monalizumab)联合Durvalumab进行维持治疗。此外,真实世界证据表明“一刀切”的治疗并不适用,对于老年、体能状态差或伴有自身免疫疾病的患者,剂量的调整至关重要。
总结
展望未来,SCLC的治疗已正式告别“一刀切”的传统模式,全面迈入精准医学与多元化干预的新纪元。双特异性抗体、ADC、CAR-T及放射性药物等前沿疗法的蓬勃发展,正不断拓宽生命的边界。更重要的是,基于四种分子亚型的精准分层(如PRISM试验)让量身定制靶向方案成为现实。在追求极致生存获益的同时,临床也将更加注重个体化差异,通过精细的剂量调整与安全性管理,护航各类复杂体质患者走向真正的“慢病化”长生存。
排版编辑:肿瘤资讯-Bear











 苏公网安备32059002004080号
苏公网安备32059002004080号


