2026年3月,国际知名医学期刊Nature Medicine(IF 50)在线发表了II期ILUSTRO研究队列4的最终分析结果。这是系统评估佐妥昔单抗(一种靶向CLDN18.2的单克隆抗体)联合mFOLFOX6化疗及纳武利尤单抗免疫治疗“三联方案”在CLDN18.2阳性、HER2阴性不可切除或转移性胃/胃食管结合部腺癌一线治疗中的前瞻性临床研究。研究结果显示,这一生物标志物引导的三联方案在中位无进展生存期(PFS)、客观缓解率(ORR)及缓解持续时间(DOR)等重要终点上均表现出色,尤其在CLDN18.2高表达合并PD-L1阳性的优势人群中疗效更为突出。该研究不仅为三联方案的合理性提供了重要临床证据,也推动了正在进行中的全球随机III期LUCERNA研究的设计落地,标志着晚期胃癌精准治疗进入全新阶段。
晚期胃癌治疗困境犹存,佐妥昔单抗+化疗+纳武利尤单抗三联方案应运而生
胃癌是全球癌症死亡的重要原因,2022年新发病例近100万例,死亡超65万例。在当前III期临床研究中,转移性胃/胃食管结合部腺癌患者接受一线治疗后的中位总生存期(OS)约为14个月,整体预后仍不乐观。
当前一线标准方案为铂类联合氟尿嘧啶的双药化疗,而基于生物标志物(PD-L1、HER2、CLDN18.2)的靶向联合方案已逐渐改写治疗格局。其中,CLDN18.2作为胃黏膜细胞特异性紧密连接蛋白,在肿瘤发生过程中因细胞极性丧失而暴露于细胞表面,成为抗体药物的理想靶点,35%~45%的胃癌患者存在CLDN18.2阳性表达。
佐妥昔单抗是全球首个靶向CLDN18.2的嵌合IgG1单克隆抗体,通过抗体依赖性细胞毒性(ADCC)和补体依赖性细胞毒性(CDC)两种机制杀伤肿瘤细胞。此前,佐妥昔单抗联合化疗已在III期SPOTLIGHT和GLOW研究中证实可显著改善CLDN18.2阳性、HER2阴性转移性胃/胃食管结合部腺癌患者的PFS与OS,为临床实践确立了重要基石。
ILUSTRO研究队列4进一步探索的核心假设在于:佐妥昔单抗介导的肿瘤细胞裂解可促进抗原释放与树突状细胞致敏,而联合PD-1通路阻断则有望维持并放大肿瘤特异性T细胞应答,从而协同激活固有免疫与适应性免疫,实现“1+1+1>3”的三联增效。这一假设已在CLDN18.2表达的小鼠模型中得到验证——三联方案的抗肿瘤活性明显优于任一两联方案。
从安全导入到扩展分析:ILUSTRO队列4的研究设计
ILUSTRO(NCT03505320)是一项全球多中心、开放标签的II期多队列研究。队列4分为两个子队列:4A(安全性导入阶段)和4B(扩展阶段),共纳入77例接受佐妥昔单抗 800 mg/m²起始剂量治疗的患者(4A,n=6例;4B,n=71例)。
入组人群为既往未接受全身治疗、经影像学确认的局部晚期不可切除或转移性CLDN18.2阳性(高表达或中等表达)、HER2阴性的G/GEJ腺癌患者。CLDN18.2高表达定义为≥75%肿瘤细胞呈现中到强的膜染色,中等表达定义为≥50%且<75%。PD-L1状态通过中心实验室检测CPS确定。
队列4的主要疗效终点为研究者评估的PFS(依据RECIST v1.1标准),这一终点的选择与III期SPOTLIGHT和GLOW研究保持一致。基线分析与安全性评估在4A+4B合并集中进行,主要疗效分析在4B队列中开展。数据截止日期为2025年9月2日。
靶免化三联方案在多个关键疗效终点上表现亮眼
CLDN18.2高表达且PD-L1 CPS≥1人群,中位PFS 23.6个月
77例患者的中位年龄61.0岁(37~86岁),62.3%为男性。在肿瘤分子特征方面,85.5%的患者为CLDN18.2高表达,14.5%为中等表达;65.3%的患者PD-L1 CPS≥1。Lauren分型以弥漫型为主(70.7%),肿瘤原发部位以胃体居多(86.5%)。基线可测量病灶比例为81.8%,整体入组人群的临床基线特征具有良好代表性。
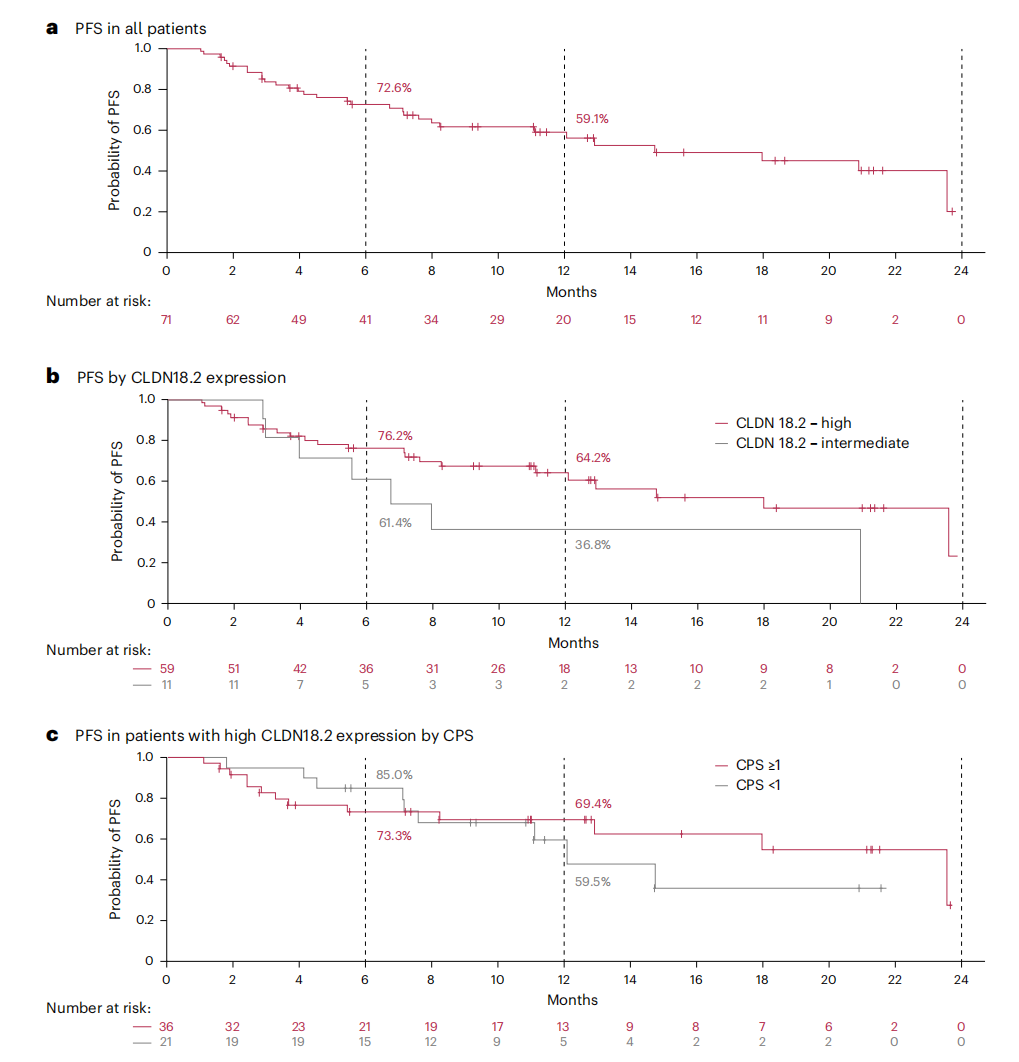
4B队列的中位随访时间为11.5个月,全人群中位PFS为14.8个月(95%CI:8.3~未达到);6个月及12个月的PFS率分别为72.6%和59.1%。在CLDN18.2高表达人群(n=59例)中,中位PFS达18.0个月(95%CI:11.1~未达到),95%CI下限(11.1个月)明显超过研究预设的历史对照阈值8.5个月,充分体现了三联方案的增效潜力。
进一步按PD-L1状态分层分析揭示了更具临床意义的规律:在CLDN18.2高表达且PD-L1 CPS≥1的患者(n=36例)中,中位PFS高达23.6个月;CLDN18.2高表达、PD-L1 CPS<1的患者(n=21例)中位PFS为12.1个月。这一差距提示,双生物标志物阳性(CLDN18.2高表达+PD-L1 CPS≥1)可能是从三联方案中获益最大的优势人群,为未来研究的入组标准优化提供了重要依据。
超六成患者肿瘤缩小,应答持久
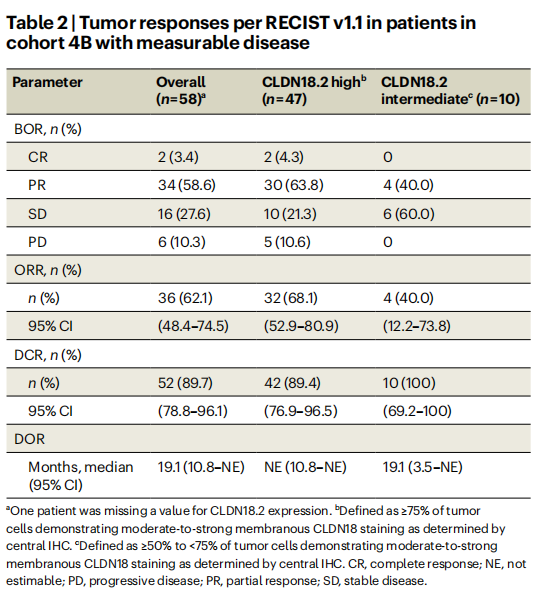
在4B队列可评估可测量病灶的患者(n=58例)中,ORR为62.1%(95%CI:48.4%~74.5%),其中完全缓解(CR)2例(3.4%),部分缓解(PR)34例(58.6%),疾病控制率(DCR)达89.7%(95%CI:78.8%~96.1%)。
在CLDN18.2高表达的可测量病灶患者(n=47例)中,ORR升至68.1%;而中等表达患者(n=10例)ORR为40.0%,进一步印证了CLDN18.2表达水平与疗效的正相关关系。
在CLDN18.2高表达且PD-L1 CPS≥1的可测量病灶患者(n=31例)中,ORR达74.2%,而CPS<1的高表达患者(n=15例)ORR为60.0%,再次凸显双生物标志物共阳性人群的疗效优势。
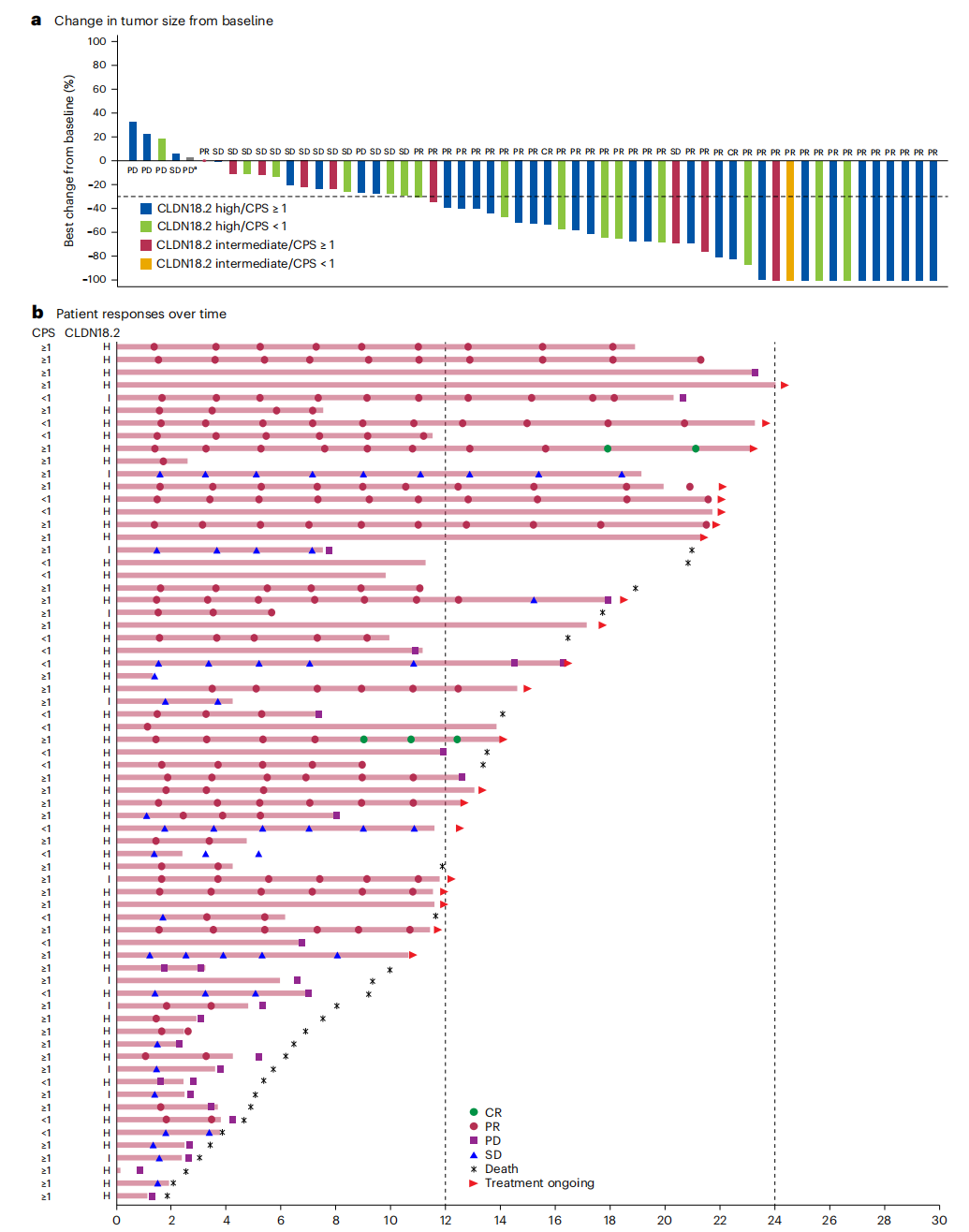
4B队列可测量病灶患者的中位DOR为19.1个月(95%CI:10.8~未达到);CLDN18.2高表达患者的中位DOR未达到(95%CI:10.8~未达到),提示应答一旦建立,患者或可长期从治疗中获益。
可测量病灶患者的肿瘤缓解情况
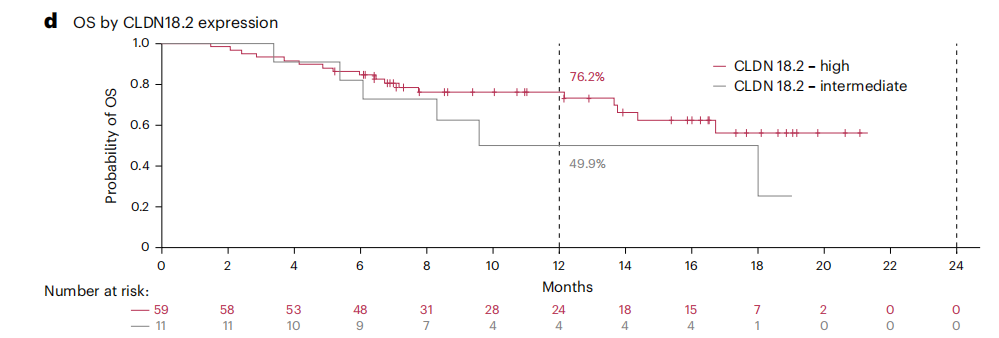
OS数据尚未成熟,已显现积极信号
OS数据在本次分析时尚不成熟,4B队列仅35.2%的患者发生OS事件。在中位随访15.4个月时,全人群的中位OS为18.0个月(95%CI:13.6~未达到);CLDN18.2高表达患者的中位OS未达到(95%CI:13.7~未达到),最终数据值得期待。
安全性可控,毒性特征与已知一致
77例患者中,98.7%发生至少一项TEAE,≥3级TEAE发生率为66.2%。最常见的任意级别TEAE包括恶心(80.5%)、食欲减退(72.7%)、中性粒细胞计数降低(45.5%)、外周感觉神经病变(45.5%)和呕吐(37.7%)。
值得关注的是,高级别胃肠道不良事件总体少见:≥3级呕吐见于3.9%患者,无≥3级恶心报告。免疫相关不良事件(包括药物超敏、对比剂过敏及超敏反应)发生率为9.1%,均可控。与既往佐妥昔单抗联合化疗研究相比,三联方案中加入纳武利尤单抗未出现新的安全性信号。
循证递进:II期ILUSTRO奠定基础,III期LUCERNA将给出最终答案
ILUSTRO 4B队列的结果表明,佐妥昔单抗+mFOLFOX6+纳武利尤单抗三联方案在CLDN18.2阳性晚期胃癌一线治疗中展现出具有临床意义的疗效信号:全人群中位PFS达14.8个月,ORR为62.1%,而CLDN18.2高表达患者的获益更为突出(中位PFS 18.0个月,ORR 68.1%),这与FAST试验中表达水平越高、疗效越佳的规律高度吻合。尤为值得关注的是,在CLDN18.2高表达且PD-L1 CPS≥1的双阳性患者中,中位PFS进一步延伸至23.6个月,ORR达74.2%,提示两种生物标志物的协同筛选可能实现最优的患者富集。研究者认为,CLDN18.2靶向治疗与PD-1阻断之间存在互补而非重叠的抗肿瘤机制——因为现有数据显示CLDN18.2状态本身对免疫联合化疗预后并无预测价值,这进一步佐证了三联方案中佐妥昔单抗的贡献具有独立的靶点驱动性。在终点选择上,PFS被设定为主要疗效终点,与III期SPOTLIGHT和GLOW研究保持一致,而本研究实际观察到的疗效结果也明显优于预设的历史对照阈值(8.5个月),疗效信号的强度值得肯定。
安全性方面,三联方案的毒性谱与各药物已知特征一致,无新发安全性信号,虽然恶心、呕吐发生率较高,但均以低级别为主,通过预防性止吐方案可有效管理;外周感觉神经病变则主要与累积奥沙利铂暴露相关,可通过剂量调整加以应对,整体治疗依从性良好。
研究者同时客观指出了本研究的局限性:非随机单臂设计缺乏直接对照、OS数据尚不成熟、中等表达亚组样本量偏小,这些均需在解读结论时保持科学审慎。正因如此,ILUSTRO队列4的结果已为正在进行的全球随机III期LUCERNA试验的设计提供了依据——该试验在CLDN18.2阳性、PD-L1 CPS≥1、HER2阴性局部晚期不可切除或mG/GEJ腺癌患者中,评估佐妥昔单抗联合化疗与PD-1抑制剂三联方案疗效(NCT06901531)。若LUCERNA研究获得阳性结果,三联治疗方案有望成为CLDN18.2阳性、PD-L1阳性、HER2阴性局部晚期mG/GEJ腺癌患者合理的、基于生物标志物指导的一线治疗策略。
Shitara K, Shoji H, Fazio N, et al. First-line zolbetuximab plus mFOLFOX6 and nivolumab in unresectable CLDN18.2-positive gastric or gastroesophageal junction adenocarcinoma: a phase 2 trial. Nat Med. 2026 Mar 16.
排版编辑:肿瘤资讯-Marie











 苏公网安备32059002004080号
苏公网安备32059002004080号


