胆道恶性肿瘤(BTC)是一类高度恶性的实体肿瘤,50%的BTC患者在确诊时已为进展期,生存期低于1年。近年随着对BTC的分子生物学特征、基因组异常及致癌机制不断的深入理解,靶向及免疫治疗在BTC领域的临床研究不断前行,也在逐步改变临床实践。为深入解读BTC的前沿进展,医脉通特邀请江苏省肿瘤医院孙小峰教授对近期BTC领域发表的研究进行学术点评,以期为临床实践和研究方向提供更多借鉴。
专家简介
江苏省肿瘤医院 肿瘤内科 主任医师
胆道胰腺肿瘤MDT首席专家 神经内分泌肿瘤MDT领衔专家
中国抗癌协会中西整合神经内分泌肿瘤专业委员会常务委员
中国临床肿瘤学会(CSCO)胰腺癌专家委员会委员
中国临床肿瘤学会(CSCO)神经内分泌肿瘤专家委员会委员
中国医疗保健国际交流促进会胰腺病学分会委员
江苏省老年医学学会肿瘤整合医学分会主任委员
杭州临床肿瘤研究会(HACO)胰腺癌研究分会常务委员
长三角肝胆肿瘤内科联盟委员会委员
江苏省抗癌协会肝癌专业委员会委员
江苏省医学会胰腺病学分会委员
江苏省医师协会胰腺病专业委员会委员
中国医师协会胃肠间质瘤专业委员会委员
中国抗癌协会胃肠间质瘤专业委员会常务委员
中国临床肿瘤学会(CSCO)胃肠间质瘤专家委员会委员
江苏省抗癌协会胃肠间质瘤专业委员会副主任委员
江苏省抗癌协会肉瘤·恶性黑色素瘤专业委员会副主任委员
江苏省研究型医院学会核医学及临床转化专业委员会常务委员
江苏省医学会神经内分泌学组委员
南京医学会老年医学分会委员
获江苏省卫生厅新技术引进一等奖1项
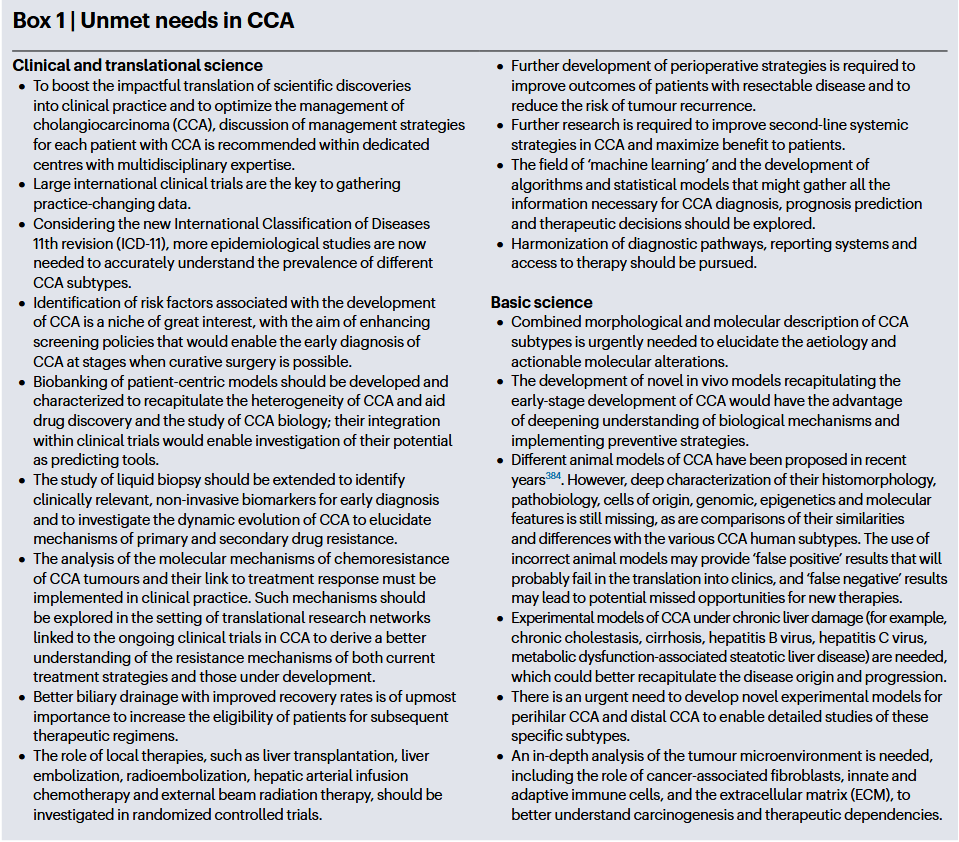
2026 胆管癌:现状、未满足的需求和优先事项
Cholangiocarcinoma 2026: status quo, unmet needs and priorities[1]
这篇文章是由欧洲胆管癌研究网络(ENS-CCA)牵头,联合全球多学科专家制定的最新国际共识,旨在为未来几年的临床实践和研究方向定调。文章首先更新了流行病学数据,指出全球范围内胆管癌(CCA)的发病率和死亡率呈上升趋势,特别是在西方国家,这可能与对“原发灶不明癌症”的重新分类有关。
在临床管理方面,共识明确了顺铂、吉西他滨联合免疫检查点抑制剂(如度伐利尤单抗或帕博利珠单抗) 为晚期胆管癌的一线标准治疗方案(SoC)。对于二线治疗,若无驱动基因突变,FOLFOX方案仍是推荐的治疗选择。
文章强烈建议对所有晚期BTC患者进行分子分型。对于iCCA患者,必须关注的高频突变包括FGFR2融合/重排和IDH1突变,此外还包括BRAF V600E突变、HER2扩增/过表达等。针对这些靶点,佩米替尼、福巴替尼、艾伏尼布以及双特异性抗体泽尼达妥单抗等药物已在二线及以上患者治疗中显示出疗效。
III期研究ClarIDHy试验表明,在IDH1突变型胆管癌患者中,IDH1抑制剂艾伏尼布相较于安慰剂,显著改善了主要终点PFS。在调整了70%患者从安慰剂组交叉至艾伏尼布治疗的影响后,OS亦得到改善。这些结果促使美国食品药品监督管理局(FDA)和欧洲药品管理局(EMA)批准了艾伏尼布的临床应用。
多项Ⅱ期试验初步验证了FGFR抑制剂在FGFR2基因组重排突变患者中的疗效,客观反应率(ORR)从21%到42%不等,疾病控制率(DCR)超过80%,中位PFS从7到9个月不等,中位OS从12到22个月不等。为了进一步评估FGFR抑制剂在胆管癌一线治疗中的疗效,三项Ⅲ期临床试验(FIGHT-302、FOENIX-CCA3、PROOF301)先后启动,但均因入组困难而提前终止。新一代FGFR抑制剂如lirafugratinib和tinengotinib作为克服因获得性FGFR2突变导致的耐药患者二线治疗方案的研究正在进行。
曲妥珠单抗与帕妥珠单抗的双抗体疗法疗效已在MyPathway和TAPUR研究中得到验证。与之类似的是泽尼达妥单抗,IIb期Herizon-BTC-01显示其在二线患者中的缓解率超过40%。目前一项III期临床试验(NCT06282575)正在进行,以验证泽尼达妥单抗的治疗潜力。II期试验DESTINY-PanTumour02公布了德曲妥珠单抗的结果,在经治且HER2免疫组化3+阳性的胆道癌患者中,该药物的ORR达56%。
对于BRAF V600E、NTRK、RET等更为罕见的靶点,疗效数据往往出自篮子实验,FDA也基于此进行审批。
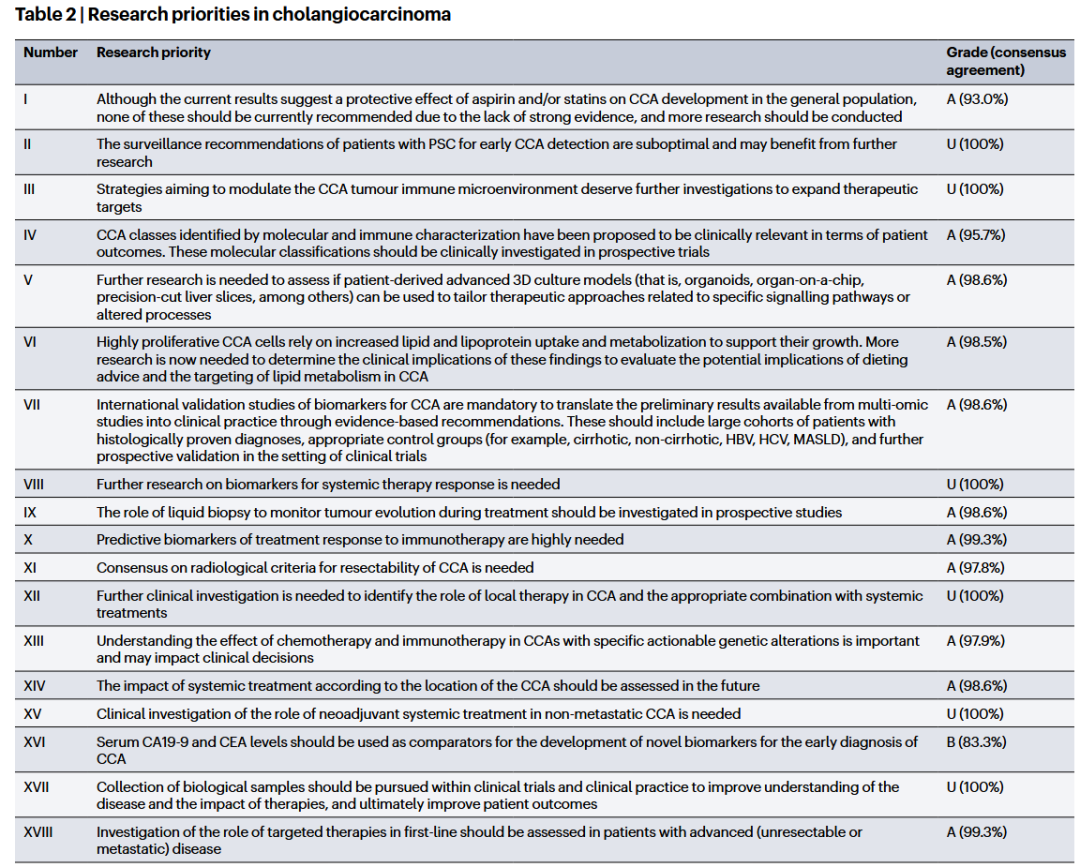
未来探索的方向:
肿瘤免疫微环境(TIME)调节: 需要进一步研究旨在调节胆管癌(CCA)肿瘤免疫微环境的策略,以扩展治疗靶点
脂质代谢: 高增殖的CCA细胞依赖脂质和脂蛋白摄取及代谢增加来支持其生长。需要研究这些发现的临床意义,以评估饮食建议和靶向脂质代谢在CCA治疗中的潜在作用
一线靶向治疗: 应在晚期(不可切除或转移性)疾病患者中,评估靶向治疗作为一线治疗的作用
新辅助治疗: 需要对非转移性CCA的新辅助系统治疗的作用进行临床评估
生物样本库: 应在临床试验和临床实践中进行生物样本的收集,以提高对疾病的理解和疗法的影响,并最终改善患者预后
孙小峰教授:
这份共识不仅是临床指南的更新,更是对我们诊疗思维的一次升级。
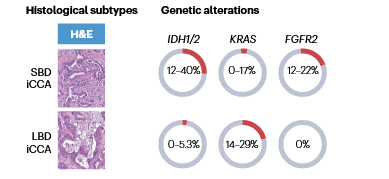
1. 分子分型的必要性: 我非常认同共识中提出的观点“Reflex Test”,即基于确诊的病理报告进行后续的分子检测。如病理分型为小胆管型的CCA患者,携带可靶向治疗突变的可能性更高。除了指导靶向治疗,分子分型还能提示疾病的分子亚型特征。
2. 标准之外的思考: 在FGFR抑制剂一线研究进行期间,免疫联合化疗基于3期研究TOPAZ-1的阳性结果成为新的一线标准治疗方案。由于FGFR抑制剂的三项Ⅲ期临床试验(FIGHT-302、FOENIX-CCA3、PROOF301)均采用化疗作为标准对照,因此都在入组缓慢的困境中走向研究终止。尽管免疫联合化疗确立了一线地位,但中位OS仅在12个月左右。共识中提到的针对TME的调节、代谢通路的干预以及新辅助治疗的探索,提示我们未来的突破点可能在于“联合中的联合”,即在免疫化疗基础上叠加靶向药物或抗血管生成药物的四药联合模式。NCT04088188是较早开始的探索性1期研究,但并未得出结论,目前已终止。另一项研究1b/2期研究NCT06501625(评估艾伏尼布联合度伐利尤单抗及吉西他滨/顺铂作为IDH1突变胆管癌一线治疗方案)在2026 ASCO GI刚刚披露数据:入组7例患者,1例PR,4例SD。也有一些去化疗的尝试,如NCT06439485(佩米替尼联合阿替利珠单抗和贝伐珠单抗治疗FGFR2融合的晚期胆管癌)正在进行中。
3. 中西方差异:中西方胆管癌患者的基因突变谱和疾病危险因素都存在差异,如亚洲胆管癌更多被提及与肝吸虫、肝结石等风险因素相关。而西方国家胆管癌常见的风险因素包括酒精相关肝病、二型糖尿病、烟草使用、代谢功能障碍相关脂肪肝等代谢综合征风险因素。对于存在代谢综合征相关风险因素的亚洲胆管癌患者而言,其胆管癌发病机制通路、基因突变谱以及可能的靶向治疗选择方案上可能也与西方胆管癌患者更为相似。
胆道癌靶向治疗的事实与误区、需求与挑战
Targeted therapy for biliary tract cancer: facts and fictions as well as demands and challenges[2]
这篇综述指出当前BTC靶向治疗领域存在的“理想丰满,现实骨感”的反差。尽管我们在实验室看到了令人振奋的数据,但在真实世界中,靶向药物的疗效往往受到诸多限制。
1.患者层面:高龄、体能状态差以及合并症等因素都可能影响疗效。作者认为在BTC研究应当引入老年综合评估(CGA),将其作为患者分层的工具,以便在追求精准靶向治疗的同时,为老年患者制定更安全、更个体化的治疗方案。
2. 肿瘤层面:肿瘤相关因素包括胆道肿瘤的内在异质性、多种耐药机制的存在以及肿瘤微环境的复杂性。胆道肿瘤常存在基因共突变,例如在FGFR依赖性肿瘤中出现的PIK3CA突变,这些突变会削弱单药靶向治疗的疗效。此外,癌症干细胞(CSCs) 也是肿瘤耐药和复发的常见特征。CSCs具有自我更新能力,被认为是化疗和靶向治疗后复发的根源。它们通过激活NOTCH、WNT、YAP/TAZ等通路,在治疗压力下存活并导致肿瘤复发。
3. 研究层面:传统上,肝吸虫感染一直被视为通过慢性炎症、胆汁淤积和氧化损伤导致胆道肿瘤发生的主要病因驱动因素,尤其是在东南亚流行地区。随着全球胆道肿瘤发病率不断上升,其他因素在其发病机制中的决定性作用日益凸显。分子特征分析已显示地域和病因异质性:肝吸虫相关肿瘤更多携带TP53、SMAD4或ARID1A突变,而其他肿瘤则与IDH1/2突变或FGFR2融合更相关。考虑到大多数胆道肿瘤实际与肝吸虫无关,目前将其作为主要致病驱动因素的观点似乎过于牵强。由于肝吸虫相关肿瘤具有独特的分子和免疫原性特征,专注于此类研究模型会给新治疗方法的发现带来偏差。因此,研究工作必须多元化,纳入其他潜在驱动因素,如代谢综合征、炎症(包括病毒性肝炎)以及更多遗传和表观遗传因素。整合包括miRNA组学和蛋白质组学在内的多组学研究方法,将成为更好识别治疗靶点的关键。
4. 转化层面:胆道肿瘤是一种具有高度解剖学和分子异质性的罕见癌症。其低发病率限制了开展大规模随机临床试验的可行性,因此需要通过创新的试验设计,最大限度地从小型队列中获取信息。在胆道肿瘤研究中,篮式试验和伞式试验均已得到应用,以提高试验可行性、统计效力,并实现适应性试验设计,包括采用贝叶斯模型纳入先验数据。这些方法能够加速有效剂量和治疗方案的识别。另一项提高研究成功率的策略是采用共同临床试验,即使用患者来源异种移植模型或患者来源类器官作为转化模型来预测治疗效果。
孙小峰教授:
BTC分子分型的突破为靶向治疗奠定了核心基础,但将其转化为显著的生存获益仍面临巨大挑战。
1. 耐药后的应对: 临床上我们常看到FGFR2融合患者使用靶向药后6-8个月出现进展。这篇文章提醒我们,耐药不仅仅是靶点本身的二次突变,还可能涉及旁路激活(如PI3K通路)或CSCs的富集。因此,未来的治疗策略不能仅是更换新一代抑制剂,更应考虑联合治疗,例如靶向药联合化疗或联合针对WNT/NOTCH通路的干预,以清除肿瘤干细胞。
2. 个体化模型的应用: 文中提到的PDO(类器官)药敏测试从目前来看非常有前景。对于多线治疗失败的患者,如果条件允许,建立类器官模型进行体外试药,可能比盲目尝试昂贵的靶向药更具性价比和科学性。
3. 老年患者管理: 胆管癌患者往往年龄偏大,合并症多。我们在追求精准靶向的同时,必须重视CGA评估。CGA 通过量化老年患者的功能储备和脆弱性,帮助医生识别出那些能够耐受标准治疗的“健康”老年人,以及那些需要减量或接受支持治疗的脆弱人群,从而避免过度治疗带来的严重毒性,实现疗效与生活质量的最佳平衡。
皮质类固醇对晚期BTCs患者(接受顺铂、吉西他滨和度伐利尤单抗治疗)结局的影响:一项全球大型真实世界人群研究
Negative impact of corticosteroid use on outcome in patients with advanced BTCs treated with cisplatin, gemcitabine, and durvalumab: A large real-life worldwide population[3]
研究回顾了全球12个国家、41个中心的666名晚期BTC患者,评估了在接受标准一线治疗——顺铂+吉西他滨+度伐利尤单抗(CGD)方案时,基线伴随药物对预后的影响。研究得出的结论是在启动CGD治疗前,使用皮质类固醇(定义为泼尼松 >10 mg/天或同等剂量)与显著缩短的总生存期(OS)独立相关。
• 未使用类固醇组的中位OS为 14.8个月;
• 使用类固醇组的中位OS仅为 5.0个月。 多变量分析证实,类固醇的使用是预后不良的独立危险因素(HR 0.37, P=0.04)。
其他合并用药(如降压药、他汀类、非甾体抗炎药等)未显示对OS或PFS的显著影响。值得关注的是,两组ORR与DCR无差异,提示皮质类固醇主要通过免疫抑制削弱长期生存获益,而非影响短期治疗响应。
生物学机制上,类固醇作为免疫抑制剂,会减少促炎细胞因子,影响淋巴细胞的迁移,并削弱CD8+ T细胞的抗肿瘤反应,从而拮抗免疫检查点抑制剂(ICIs)的疗效。
孙小峰教授:
这是一项极具临床指导意义的真实世界数据回顾性分析。
1. 预处理的调整: 许多化疗方案(如含紫杉类或培美曲塞)需要激素预处理以预防过敏或呕吐。但在CGD方案中,吉西他滨和顺铂的致吐风险相对可控。临床医生应尽量通过优化5-HT3受体拮抗剂和NK-1受体拮抗剂的使用来控制恶心呕吐,从而减少或避免激素预处理,或者在免疫药物输注完成后再给予必要的低剂量激素,以最大程度保护免疫治疗的微环境。
2. 缓解症状的药物选择:在免疫治疗时代,我们必须改变过去使用地塞米松或泼尼松来改善患者皮疹、腹泻等症状的习惯,特别是在启动一线“免疫+化疗”的前期,除非是为了处理脑转移水肿或脊髓压迫等急症,否则应严格限制高剂量激素的使用。
3. 患者沟通: 对于基线状态较差(如ECOG PS评分较差)且依赖激素缓解症状的患者,我们需要坦诚地沟通:激素可能会大幅削弱昂贵的免疫药物的疗效,需要权衡利弊,甚至考虑先进行激素减量,待病情平稳后再启动免疫治疗。
总而言之,临床医生应当在使用激素改善患者症状与使用免疫药物治疗肿瘤之间取得一个平衡,尽量避免治疗前使用皮质类固醇,确需应用时需采用最低有效剂量,以优化CGD方案的临床获益。
艾伏尼布在治疗IDH1突变的胆管癌和急性髓性白血病中的安全性与疗效:系统综述与荟萃分析
Safety and efficacy of ivosidenib in the treatment of isocitrate dehydrogenase 1 mutant cholangiocarcinoma and acute myeloid leukemia: a systematic review and meta-analysis[4]
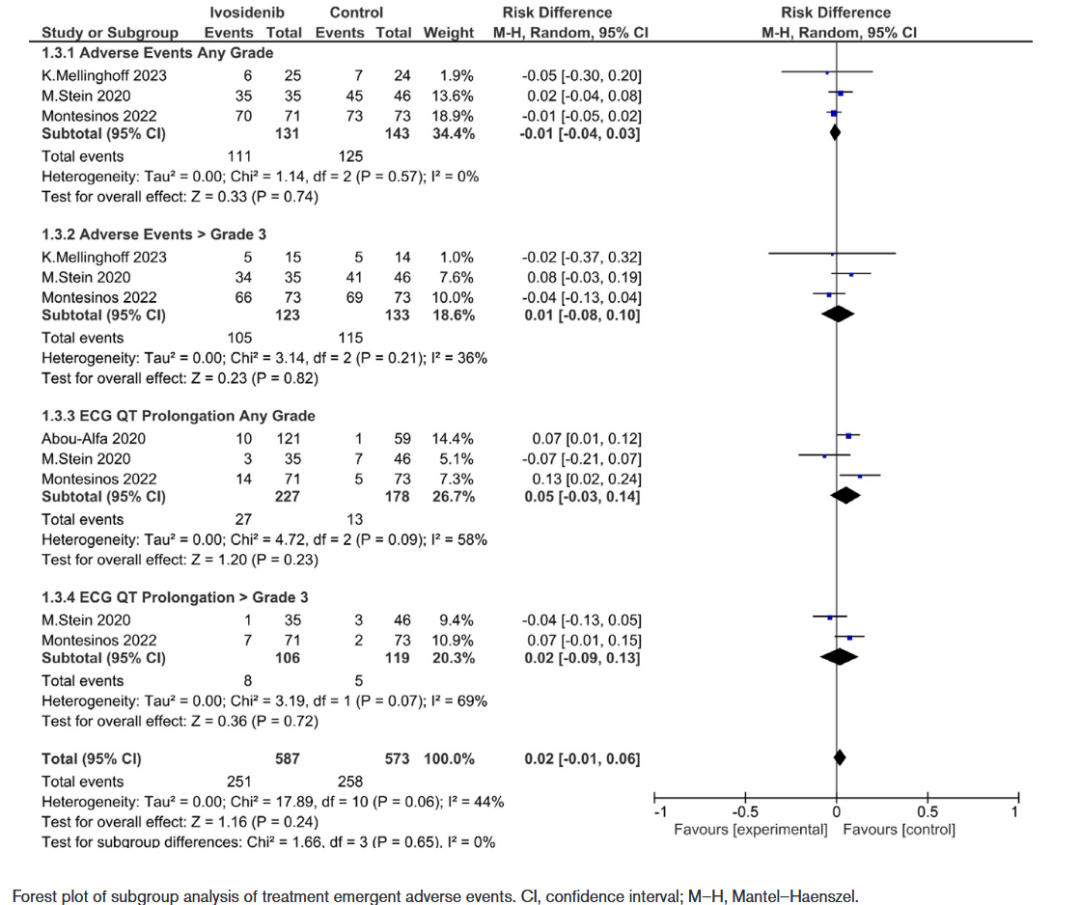
IDH1突变与胆管癌、急性髓系白血病(AML)等恶性肿瘤密切相关,艾伏尼布作为IDH1突变选择性抑制剂,可阻断D-2-羟基戊二酸的合成、恢复细胞正常分化,并抑制肿瘤发生。本研究旨在通过系统评价与荟萃分析,综合评估艾伏尼布在治疗IDH1突变癌症中的整体疗效与安全性。最终纳入4项RCT,共533例患者,其中艾伏尼布组281例,对照组252例,以肝内胆管癌和原发性AML为主。结果显示:艾伏尼布组与对照组的整体治疗中出现的不良事件(TEAE)发生率无统计学差异。对于任意级别的QT间期延长风险,艾伏尼布组与对照组相比,总体效应的风险差(RD)为 0.05,95%置信区间为 -0.03 至 0.14,P值为0.23,I 2= 58%, P = 0.09。3级以上(> Grade 3)的QT延长风险:风险差(RD)为 0.02,95%置信区间为 -0.09 至 0.13。Z值为0.36,P值为0.72,I 2= 69%, P = 0.07。QT间期延长在两组间无统计学差异。
孙小峰教授:
该综述虽然2025年底新近发表,但数据检索工作截止到2024年7月,并且作者在进行研究文章选择时忽略了最终OS发表相关文章(如ClarIDHy最终OS结果在2021年发表,但并未纳入)。肿瘤领域的研究进展日新月异,青年医生在投稿文章时应检查是否有遗漏新近发表的文章。此外,虽然IDH1突变在多个肿瘤中都有出现,且艾伏尼布作为IDH1突变选择性抑制剂,在携带该突变的急性髓系白血病以及实体瘤如胆管癌治疗中展现出获益(如本文纳入的NCT03173248(AGILE)研究,其最终OS 为HR= 0.44( 95% CI, 0.27-0.73)。但是药物疗效可能由于不同疾病本身通路不同而存在差异,而药物的安全性往往在不同的疾病治疗中差异会更小一些,本文更值得关注的是泛瘤种中艾伏尼布的安全性。它基于4项研究533例患者的数据,明确量化了QT间期延长的风险。艾伏尼布与对照组相比,增加了5%的任意级别QT间期延长的风险,增加了2%的3级以上的QT间期延长风险。整体而言,虽然两组间无统计学差异,临床也并不常见。但在使用艾伏尼布时,我们必须在基线及治疗期间定期监测心电图,特别是对于合并使用其他可能延长QT间期药物(如某些抗生素、止吐药)的患者,需格外警惕心脏毒性。
总结
综合这四篇文献,我们可以看到晚期胆管癌的治疗正在向精细化和全程化发展。一线治疗要“稳”,在确立免疫联合化疗地位的同时,需警惕激素等伴随用药的负面影响;后线治疗要“准”,基于NGS检测的靶向治疗(如针对FGFR2、IDH1)能为患者争取宝贵的生存时间,但需关注耐药监测和特定副作用的管理。希望这些点评能为广大医生朋友们的临床决策提供有益的参考。
1. Banales, J. M. et al. Nat Rev Gastroenterol Hepatol 23, 65–96 (2026)
2. Neureiter, D. et al. Expert Review of Anticancer Therapy 1–5 (2025)
3. Prinzi, F. L. et al. Intl Journal of Cancer 157, 2092–2102 (2025)
4. Qasim, R. et al. Anticancer Drugs 36, 812–821 (2025)
免责声明:
本资料由临床专家制作,内容仅作为科学信息参考,仅用于医疗卫生专业人士的学术交流,请勿用于任何其他用途。若您不是医疗卫生专业人士,请勿观看和/或传播此资料。
本资料可能会出现某些药品信息,但该药品/适应症可能尚未获得国家药品监督管理局的注册批准。医疗卫生专业人士做出的任何与治疗有关的决定应根据患者的具体情况并应参照国家药品监督管理局批准的药品说明书。对于本资料可能提到的相关诊断、治疗方法,请遵守国家卫生健康委员会以及相关部门批准使用的指南或规定。审批号:M-TIBSO-CN-202601-00021











 苏公网安备32059002004080号
苏公网安备32059002004080号


