胆管癌作为高度异质性的恶性肿瘤,长期以来面临治疗手段有限、预后不佳的困境。尽管免疫联合化疗已确立为一线标准,但患者中位生存期仍徘徊在12个月左右,二线治疗更是面临FOLFOX方案疗效有限的严峻挑战。值得欣慰的是,随着精准医疗时代的到来,胆管癌治疗正迎来重大转折,约半数患者携带可靶向的驱动基因变异,为个体化治疗提供了坚实基础。值此契机,中国医学论坛报特邀解放军总医院苟苗苗教授聚焦这一领域的最新突破进行系统介绍,解放军总医院戴广海教授进行深度点评,以期为临床实践提供参考。
专家简历
解放军总医院 肿瘤内科副主任医师,副教授
日本国立癌研医院高级访问学者
北京癌症防治学会胃癌防治青年委员会常务委员
北京抗癌协会胃癌专委会常委
CSCO胰腺癌、胆道癌、抗肿瘤药物安全、老年肿瘤防治专委会委员
中国研究型医院学会精准医学与肿瘤MDT专委青年委员、肿瘤外科委员会委员
中国医师协会结直肠肿瘤MDT学组委员、医工融合与智能医学学组委员
中国抗癌协会头颈肿瘤整合康复专委会委员
长期以来从事消化道肿瘤的综合治疗,以第一作者发表15余SCI
多次参与ASCO和ASCO-GI及国内会议交流
CSCO化疗安全管理大赛第一名,个人风采奖
主持一项青年成长课题,参与2项国自然课题和2项重大课题的研究
撰写中国胆管肿瘤多学科综合治疗专家共识、2023人卫出版社《结肠癌肿瘤学》、中国胃癌肝转移诊断与综合治疗中国专家共识(2024版)
亚洲年轻肝内及肝门部胆管癌患者中的FGFR2融合或重排:泛亚洲研究的关键遗传学见解
FGFR2 Fusions or Rearrangements in Young Intrahepatic and Perihilar Cholangiocarcinoma Patients: Key Genetic Insights From a Pan‐Asian Study1
针对特定基因变异的胆管癌靶向治疗,例如针对成纤维细胞生长因子受体2(FGFR2)融合或重排的FGFR抑制剂,在携带相应变异的胆管癌患者中展现出潜力,已成为二线治疗选择。然而,亚洲人群,特别是东南亚地区,关于FGFR2阳性率及其临床特征的数据仍然有限,个性化医疗和基因检测的普及也相对滞后。基于此,本研究旨在评估亚洲多国肝内胆管癌(ICC)和肝门部胆管癌(PCC)患者中FGFR2融合或重排的发生率,并探讨其临床意义。
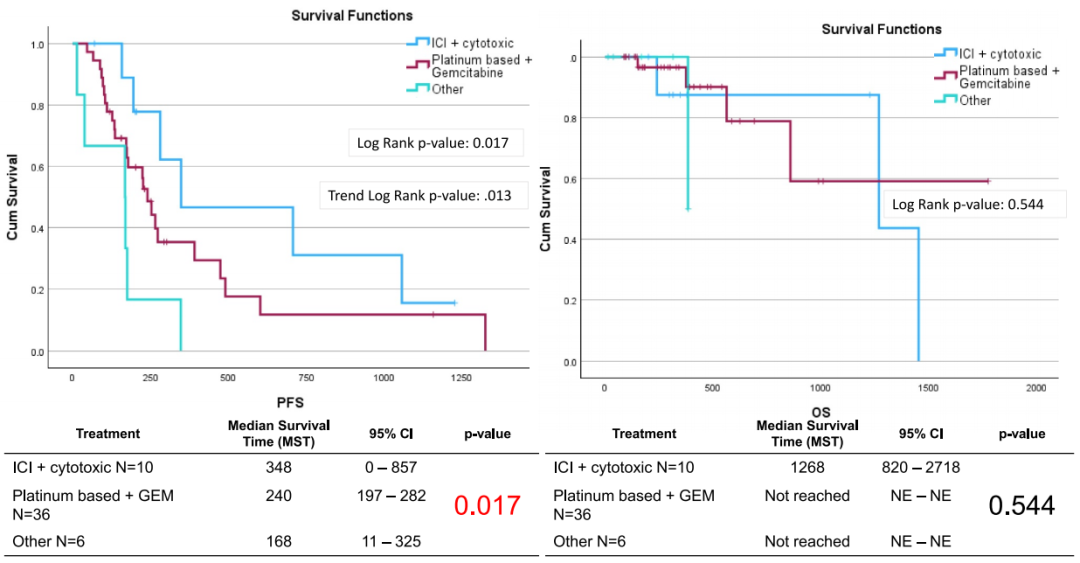
研究结果显示,在最初纳入的113例患者中,经中心病理复核后有102例符合条件。100例样本成功完成FISH检测,其中发现4例(3.9%)FGFR2 FISH阳性病例,4例均为ICC患者,占全部ICC患者的4.7%。88例患者成功完成基于TOP2的全面基因组测序分析,其结果与FISH完全一致,确认了这4例FGFR2融合,并鉴定出融合伴侣基因分别为TSC22D3、INA和G3BP2,均为可产生功能性嵌合蛋白的框内融合。值得注意的是,更年轻的年龄是与FGFR2阳性显著相关的临床因素:阳性患者平均年龄为34.5 ± 3.17岁,显著低于阴性患者的62.69 ± 1.04岁(P=0.0003)。此外,FGFR2阳性患者表现出显著更低的肿瘤突变负荷(TMB)(0.925 ± 0.46 mut/Mb vs 5.347 ± 13.96 mut/Mb, P=0.003)。基因组分析显示,TP53(26.9%)、KRAS(25.8%)、ARID1A(15.7%)等是常见的突变基因,且存在地区异质性。45.45%的样本中发现了可靶向的基因改变变异。生存分析显示,在接受一线姑息化疗的患者中,接受ICI+细胞毒药物治疗的患者PFS最长(中位PFS 348天),优于铂类+吉西他滨(240天)和其他治疗(168天),组间差异显著(P=0.017),但OS无显著差异。
IDH1/2抑制剂LY3410738在携带IDH1或IDH2突变的晚期实体瘤中的首次人体1期研究的最终结果
Final Results from a First-in-Human Phase 1 Study of the Dual Isocitrate Dehydrogenase (IDH) 1/2 Inhibitor, LY3410738, in Advanced Solid Tumors Harboring IDH1 or IDH2 Mutations2
本研究是一项全球多中心、开放标签的1期研究,旨在评估LY3410738在IDH突变实体瘤患者中的安全性、药代动力学和初步抗肿瘤活性。研究分为剂量递增阶段(LY3410738单药治疗晚期实体瘤,包括复发性/难治性胆管癌和胶质瘤)和剂量扩展阶段[LY3410738联合顺铂-吉西他滨(CISGEM)用于初治的胆管癌,或联合度伐利尤单抗用于复发性/难治性胆管癌]。主要目标是确定最大耐受剂量(MTD)、推荐2期剂量(RP2D)和初步抗肿瘤活性。研究同时还评估了药代动力学、D-2-羟基戊二酸(D-2-HG)抑制情况以及循环肿瘤DNA(ctDNA)的动态变化。
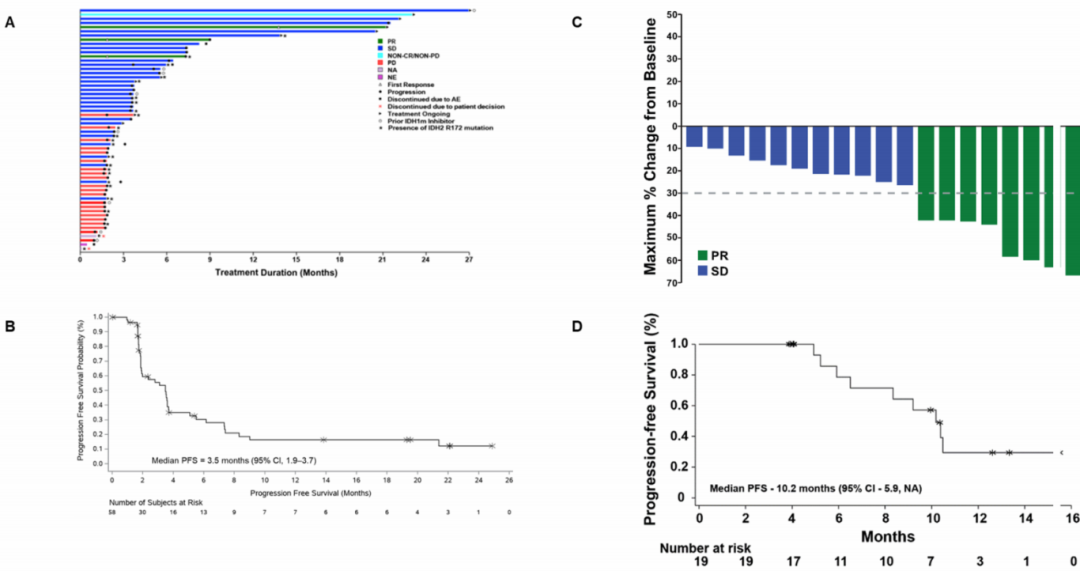
图. LY3410738单药治疗在复发性/难治性胆管癌患者中以及LY3410738联合CISGEM在初治胆管癌患者中的抗肿瘤活性
注:(A) 游泳图,显示接受LY3410738单药治疗的复发性/难治性IDH1或IDH2突变胆管癌患者的治疗持续时间和反应;(B) 接受LY3410738单药治疗的复发性/难治性IDH1或IDH2突变胆管癌患者的中位PFS的Kaplan-Meier曲线;(C) 瀑布图,显示接受LY3410738联合CISGEM治疗的初治胆管癌患者的反应程度;(D) 接受LY3410738联合CISGEM治疗的初治胆管癌患者的中位PFS的Kaplan-Meier曲线
研究结果显示,共有119例患者入组并接受治疗(单药94例,联合CISGEM 19例,联合度伐利尤单抗6例)。单药治疗未观察到剂量限制性毒性,MTD未达到,耐受性良好,最常见的不良事件包括恶心、呕吐和食欲下降。药效学方面,LY3410738能快速、持久地使血浆D-2-HG水平正常化,但抑制IDH2突变所需的剂量(≥150 mg BID)高于IDH1突变。抗肿瘤活性方面,单药治疗复发性/难治性IDH1或IDH2突变胆管癌的ORR为5.2%,DCR为56.9%;单药治疗复发性/难治性IDH1突变胶质瘤的ORR为11.1%,DCR为63.0%。最重要的发现之一在于联合治疗:LY3410738联合CISGEM用于初治IDH突变胆管癌患者,ORR达到42.1%,中位PFS为10.2个月,显示出令人鼓舞的疗效。而LY3410738联合度伐利尤单抗组未观察到客观缓解,所有患者达到疾病稳定。转化研究显示,ctDNA中mIDH的清除与治疗反应相关,未发现亚型转换或经典二次位点突变,但共存KRAS/PIK3CA突变可能与较短的LY3410738单药治疗持续时间相关。
新型抗HER2双特异性抗体泽尼达妥单抗治疗胆道癌的评价
An evaluation of zanidatamab, a novel, anti-HER2 biparatopic antibody, for the treatment of biliary tract cancer3
人表皮生长因子受体2(HER2)是成熟的抗癌治疗靶点,其在BTC中的过表达和/或ERBB2基因扩增发生率为9-20%,尤其在胆囊癌中更为常见,这为HER2靶向治疗胆道癌提供了理论基础。本文系统回顾了目前晚期BTC的治疗格局,重点聚焦HER2作为治疗靶点的意义,并详细评述了新型HER2靶向药物泽尼达妥单抗的现有临床试验数据。泽尼达妥单抗是一种人源化双特异性IgG抗体,通过同时靶向HER2胞外结构域II和IV的两个非重叠表位,独特地促进HER2交联、内吞和降解,并诱导形成"HER2帽"结构,从而增强补体依赖性细胞毒作用等抗肿瘤机制。关键II期研究HERIZON-BTC-01评估了泽尼达妥单抗单药用于经治、HER2扩增的不可切除局部晚期或转移性BTC患者。
研究结果显示,在HER2 IHC 2+或3+的患者队列(Cohort 1, n=80)中,经独立中心审查确认的ORR为41.3%,包括2例完全缓解和31例部分缓解,DCR为68.8%;中位持续缓解时间(DoR)达14.9个月,中位PFS为5.5个月,中位OS为15.5个月。值得注意的是,疗效与HER2表达水平显著相关,在HER2 IHC 3+患者中ORR高达51.6%,中位PFS和OS分别达7.2个月和18.1个月,而在IHC 2+患者中疗效有限。安全性方面,泽尼达妥单抗耐受性良好,最常见治疗相关不良事件为腹泻(37%)和输注相关反应(33%),多数为1-2级;3级及以上治疗相关不良事件发生率为18%,因不良事件导致停药的比例低(2.3%),且患者报告的生活质量在应答者中得到改善。基于这些令人鼓舞的数据,泽尼达妥单抗已于2024年11月获美国FDA加速批准,并于2025年6月获欧洲EMA批准,用于治疗既往经治的HER2阳性(IHC 3+)晚期BTC。
精准治疗的演进:胆道癌靶向治疗新进展
Evolving Precision: Updates in Targeted Therapy for Cholangiocarcinoma4
胆道癌是一组来源于胆道上皮细胞的异质性恶性肿瘤。尽管其整体发病率相对较低,但在亚洲部分地区及西方国家的年轻人群中呈上升趋势。多数患者确诊时已属晚期,失去手术机会,传统一线治疗为吉西他滨联合铂类化疗,近年来,联合免疫检查点抑制剂虽带来生存获益,但中位无进展生存期仍仅约7–8个月。二线治疗长期以来缺乏标准,直至ABC-06研究确立FOLFOX方案作为治疗选择,但其客观缓解率仅5%,中位总生存期仅6.2个月,且仅约40%患者有机会接受二线治疗。
随着下一代测序技术的广泛应用,约半数胆道癌患者被发现携带可靶向治疗的分子变异,尤其在肝内胆管癌中比例最高。常见驱动变异包括FGFR2融合/重排、IDH1 R132突变、HER2过表达/ERBB2扩增、BRAF V600E突变等。本文系统回顾了多项关键II/III期临床试验(如FIGHT-202、FOENIX-CCA2、ClarIDHy、HERIZON-BTC-01、DESTINY-PanTumor02等)及真实世界研究数据,评估了针对上述靶点的靶向药物在经治晚期胆道癌患者中的疗效与安全性。
研究结果显示,与FOLFOX相比,靶向治疗在客观缓解率(ORR)和疾病控制率(DCR)方面普遍更优,ORR多数可达40%以上,DCR常超过50%,并能显著延长中位OS,多数药物中位OS超过9个月,部分可达1-2年甚至更长,而FOLFOX为6.2个月。以艾伏尼布为例,疾病控制作用持久,并在OS方面显示出显著优势:在ClarIDHy III期临床试验中,艾伏尼布组的中位OS为10.3个月,而安慰剂组仅为5.1个月(HR=0.49, P<0.0001),进一步证实艾伏尼布在IDH1突变胆道癌患者中的生存获益。安全性方面,靶向药物的3-4级治疗相关不良事件发生率与化疗相当或更低,且多为口服或外周静脉给药,提高了治疗便利性和患者生活质量。真实世界研究亦证实,接受匹配靶向治疗是改善患者总生存期的独立有利预后因素。
专家点评
肿瘤学博士,主任医师,教授
解放军医学院、南开大学博士研究生导师
解放军总医院肿瘤医学部肿瘤内科主任
第六届中央保健委员会会诊专家
第四届中央军委保健委员会会诊专家
2020年第四届国之名医——卓越建树称号获得者
中国研究型医院学会精准医学与肿瘤MDT专业委员会主任委员
中国医师协会结直肠肿瘤专委会副主任委员,MDT专委会主任委员
中华医学会肿瘤学分会结直肠肿瘤学组副主任委员
CSCO理事,胆系肿瘤专委会、胰腺癌专家委员会副主任委员
CSCO智慧医学专委会、结直肠癌专委会常委;胃癌专委会委员
《中华结直肠病电子杂志》副总编辑
近年来,靶向治疗和免疫治疗的快速发展,正在深刻改变胆管癌的治疗格局。FGFR2融合或重排泛亚洲研究为理解亚洲人群FGFR2融合或重排的流行病学和临床特征提供了宝贵数据。3.9%的阳性率略低于西方报道,但与国际多中心研究中的亚洲亚组数据基本吻合,体现了胆管癌分子特征的地区差异性。更重要的是,研究发现FGFR2融合与年轻患者的强相关性,为我们在年轻胆管癌患者中优先进行FGFR2检测提供了理论依据。同时,研究证实FISH与NGS在检测FGFR2融合方面具有良好一致性,考虑到FISH的成本效益和快速出结果的优势,在资源有限的地区仍不失为有效的筛查手段。FGFR2阳性患者TMB显著较低的发现也颇具启发,或许能部分解释该人群对免疫治疗反应不佳的原因,为未来的联合治疗策略提供了思考方向。
LY3410738在晚期实体瘤中的首次人体Ⅰ期研究让我们看到了新一代IDH抑制剂的研发进展。LY3410738作为双IDH1/2抑制剂,其独特价值在于能够克服部分对第一代抑制剂耐药的突变。研究中观察到的良好安全性和持久的D-2-HG抑制效果令人惊喜。LY3410738联合CISGEM在初治患者中达到42.1%的ORR和10.2个月的中位PFS,这一数据甚至优于当前免疫联合化疗的一线标准方案,为IDH突变胆管癌的一线治疗提供了新的可能性。然而,联合度伐利尤单抗未观察到客观缓解的结果也提示,IDH突变肿瘤的免疫微环境可能较为"寒冷",单纯的ICI联合可能不足以逆转这种免疫抑制状态。这些发现为未来研究指明了方向——或许需要探索更多的联合策略来克服耐药。
泽尼达妥单抗的出现标志着胆道癌HER2靶向治疗进入了新的阶段。其独特的双特异性设计带来了卓越的疗效:在HER2 IHC 3+患者中51.6%的ORR和18.1个月的中位OS。更重要的是,其耐受性良好,患者报告的生活质量在应答者中得到改善,体现了精准治疗在提升疗效同时改善患者生活质量的综合价值。泽尼达妥单抗的成功也再次强调了胆道癌分子分型的重要性,特别是在胆囊癌中HER2阳性率较高,应常规进行检测。随着该药物在全球多个国家和地区获批,我们有理由相信它将很快改变HER2阳性胆道癌的治疗标准。
胆道癌精准治疗综述系统梳理了胆道癌精准治疗的最新进展,为我们提供了全面的视角。与传统FOLFOX化疗相比,各靶向药物在ORR、DCR和OS方面展现出显著优势。更重要的是,文章强调了真实世界中接受匹配靶向治疗是改善患者OS的独立有利因素,这从另一个角度印证了精准治疗的价值。然而,我们也应清醒地认识到当前面临的挑战:如何优化检测流程确保不漏掉可靶向的患者、如何克服原发性耐药、如何管理靶向药物不良反应、如何将有效的靶向治疗前移等。未来的研究方向应包括探索更有效的联合治疗策略、开发新一代的靶向药物、建立预测疗效的生物标志物体系等。
综合这些研究,可以清晰地看到胆道癌治疗正在经历从"一刀切"的化疗模式向基于分子分型的精准治疗模式的深刻转变。这种转变不仅改善了患者的生存结局,也提升了治疗的选择性和精准性。作为临床医生,我们应当积极推动胆道癌的常规基因检测,确保每位患者都能获得精准治疗的机会。同时,也期待更多的创新药物和联合策略出现,最终实现将胆道癌转变为慢性可控疾病的愿景。精准治疗的时代已经到来,我们需要做好准备,为患者提供最前沿、最合适的治疗方案。
1. Maruki, Y., Yatabe, Y., Mizoguchi, C., et al. FGFR2 Fusions or Rearrangements in Young Intrahepatic and Perihilar Cholangiocarcinoma Patients: Key Genetic Insights From a Pan-Asian Study. Hepatology Research. https://doi.org/10.1111/hepr.700312.
2. Harding JJ, Oh DY, Mercade TM, et al. Final Results from a First-in-Human Phase 1 Study of the Dual Isocitrate Dehydrogenase (IDH) 1/2 Inhibitor, LY3410738, in Advanced Solid Tumors Harboring IDH1 or IDH2 Mutations. Clin Cancer Res. 2025 Sep 30. doi: 10.1158/1078-0432.CCR-25-0174. Epub ahead of print. PMID: 41026608.
3. Yoon J, Oh DY. An evaluation of zanidatamab, a novel, anti-HER2 biparatopic antibody, for the treatment of biliary tract cancer. Expert Opin Biol Ther. 2025 Sep;25(9):935-946. doi: 10.1080/14712598.2025.2556903. Epub 2025 Sep 6. PMID: 40892073.
4. Tesini G, Ibrahim H, Rimassa L, et al. Evolving Precision: Updates in Targeted Therapy for Cholangiocarcinoma. Hepatology. 2025 Sep 22. doi: 10.1097/HEP.0000000000001541. Epub ahead of print. PMID: 40982790.
本资料的内容仅作为科学信息参考,并仅用于医疗卫生专业人士间的学术交流之目的,请勿转发或用于任何其他用途。
本资料可能会出现某些药品信息,但该药品/适应症可能尚未获得国家药品监督管理局的注册批准。医疗卫生专业人士做出的任何与治疗有关的决定应根据患者的具体情况并应参照国家药品监督管理局批准的药品说明书。对于本资料可能提到的相关诊断、治疗方法,请遵守国家卫生健康委员会以及相关政府部门批准使用的指南或规定。
审批号:M-TIBSO-CN-202511-00014
本文转自:中国医学论坛报今日肿瘤











 苏公网安备32059002004080号
苏公网安备32059002004080号


