2025年欧洲肿瘤内科学会(ESMO)年会于10月17日至21日在德国柏林隆重举行,汇聚了来自世界各地的顶尖专家,共同分享和探讨了肿瘤治疗领域的最新突破。在众多研究中,胆管癌与胰腺癌领域迎来了多项突破性进展,为临床治疗带来了新的曙光。
值此之际,本文特邀中国医学科学院肿瘤医院周爱萍教授围绕胆管癌与胰腺癌在围手术期治疗、晚期系统治疗、靶向治疗等多个关键领域的最新研究成果展开详细解读。
专家简历
内科副主任,博士生导师
中国医学科学院肿瘤医院&国家癌症中心
中国医疗保健国际交流促进会消化肿瘤多学科诊疗学分会主任委员
中国临床肿瘤学会(CSCO)结直肠癌/胃癌专业委员会常务委员
中国临床肿瘤学会(CSCO)尿路上皮癌/肾癌专业委员会副主任委员
中国老年医学学会肿瘤学分会副会长
中国老年学和老年医学学会肿瘤分会副干事长
中国医药教育协会腹部肿瘤结直肠癌分会副主任委员
中华医学会胰腺癌专业委员会委员抗癌协会胃癌专业委员会委员 北京市妇女对外交流协会副理事长
《CSCO结直肠癌诊疗指南》、《中国卫健委结直肠癌诊疗规范》、《CSCO胃癌诊疗指南》、《CSCO肾癌诊疗指南》专家组成员,《CSCO尿路上皮癌诊疗指南》副组长
《中华肝胆外科杂志》、 《中华临床医师杂志》、《中国继续教育杂志》、《肝癌电子杂志》、《中国医刊》编委
胆管癌领域新进展:围术期与靶向治疗的双重突破
围手术期治疗的协同优化
LBA11[1]:II-III期ZSAB-neoGOLP研究证实特瑞普利单抗联合仑伐替尼和吉西他滨/奥沙利铂方案可作为可切除的、高危肝内胆管癌的新辅助治疗选择
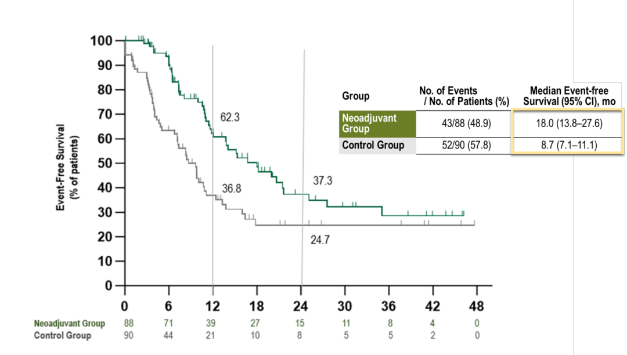
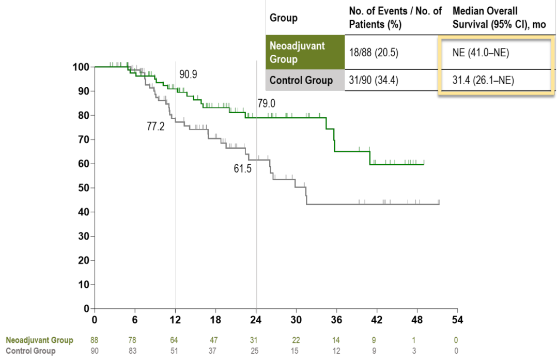
该研究是由复旦大学附属中山医院牵头,作为ESMO大会口头报告展示,首个PD-1抑制剂联合靶向治疗和化疗用于高危肝内胆管癌新辅助治疗的II/III期随机对照研究。截至2025年4月30日,研究纳入178例可切除但具高复发风险的患者,1:1分为两组,GOLP新辅助治疗组(n=88)术前接受3个周期的GEMOX化疗、9周的仑伐替尼(8mg)以及3个剂次的特瑞普利单抗,随后进行手术;对照组(n=90)则直接进行传统手术切除。所有患者术后均予标准化疗卡培他滨辅助治疗8周期。研究的主要终点是无事件生存期(EFS)。
在中位随访16.9个月的中期分析中,新辅助治疗组的中位EFS达到18.0个月,显著优于对照组的8.7个月,疾病复发、进展或死亡风险降低了52%(HR=0.48; 95% CI 0.31-0.74; p=0.0006)。尽管总生存期(OS)数据尚未成熟,但新辅助治疗组已显示出明显的获益趋势(中位OS:未达到 vs. 31.4个月;HR=0.43,p=0.005)。新辅助治疗组患者肿瘤退缩明显,ORR高达54.5%,主要病理缓解(MPR)率为19.3%,pCR率为4.5%。在安全性方面,新辅助治疗阶段≥3级不良反应发生率控制在26.4%。
ZSAB-neoGOLP研究表明,特瑞普利单抗三联方案新辅助治疗可切除、高复发风险的肝内胆管癌患者,可显著延长EFS,并展现出潜在的OS获益趋势,且耐受性良好。
95P[2]:胆道恶性肿瘤(BTC)切除术后辅助S-1或吉西他滨治疗可使患者长期生存获益
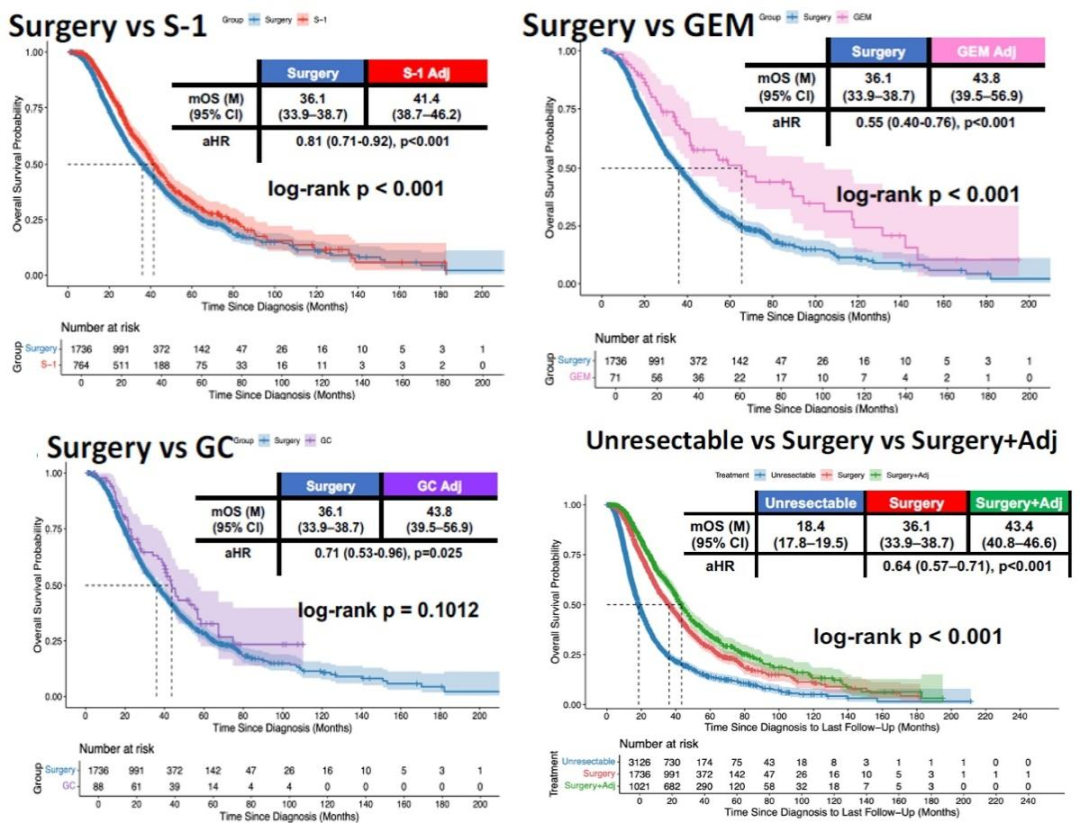
术后辅助治疗的优化同样取得突破。ASCOT试验已证实用S-1辅助治疗可延长总生存,但其远期疗效在真实世界中仍缺定论,该研究是一项日本学者利用全国性数据库进一步探索不同辅助方案的长期价值。研究者回顾性纳入2757例根治术后BTC患者,其中单纯手术组为1736例,术后接受辅助治疗组为1021例,按术后辅助方案(S-1单药n=764、吉西他滨单药n=71、GC n=88或其他n=98)分组。
结果显示:相较于单纯手术,S-1辅助治疗中位生存显著延长(41.4个月vs 36.1个月,p<0.001),降低19%死亡风险(HR=0.81);吉西他滨辅助治疗中位生存显著延长(43.8个月vs 36.1个月,p<0.001),降低45%死亡风险(HR=0.55);而GC组的中位生存延长无统计学差异(43.8个月vs 36.1个月,p=0.1012)。整体辅助治疗组中位OS 43.4个月,较单纯手术36.1个月延长7.3个月(p<0.0001)。
本项大规模真实世界研究证实,术后以S-1或吉西他滨行辅助化疗可为BTC患者带来显著且持久的生存获益,提示将S-1或吉西他滨纳入可切除BTC术后新的标准治疗方案。
晚期系统治疗的精准化探索
107eP[3]:IIIb期ProvIDHe研究揭示真实世界中艾伏尼布治疗IDH1突变胆管癌的疗效和安全性
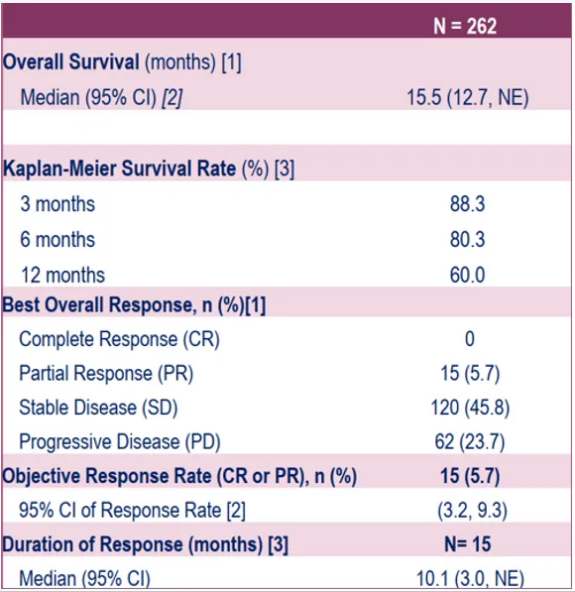
今年ESMO GI大会口头报告了一项探索艾伏尼布用于IDH1突变胆管癌患者的全球多中心IIIb期ProvIDHe研究。首次报告涵盖了在真实世界中接受艾伏尼布治疗mIDH1胆管癌患者的最大队列,重点分析了艾伏尼布的初步疗效。该研究疗效分析纳入来自15个国家的262例患者,结果显示:5.7%的患者达到部分缓解(PR),中位缓解持续时间(DoR)为10.1个月,51.5%的患者达到疾病控制(PR+SD),mPFS为4.7个月以及 mOS为15.5个月[4]。
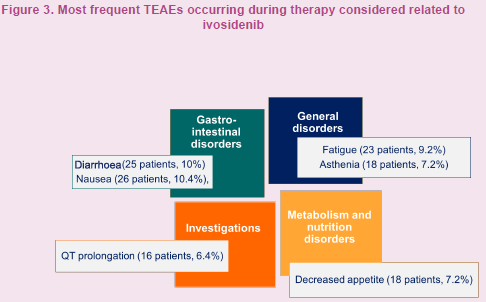
今年EMSO大会更新了ProvIDHe研究的安全性数据,249例患者纳入安全性分析集。结果发现,治疗期间87.1%的患者至少发生1次不良事件(TEAE),其中50.6%与艾伏尼布相关,常见TEAE为恶心、乏力、腹泻;32.9%的患者发生严重TEAE,但仅有4.4%认为与艾伏尼布相关。
ProvIDHe 真实世界数据再次确认艾伏尼布已知安全谱,未发现新的安全信号;研究仍在进行,期待结果的进一步公布,为艾伏尼布的临床应用增添更多循证证据。
基因组标志物的临床转化价值
90P[5]:一项欧洲研究揭示晚期胆道恶性肿瘤患者的双基因变异的临床、病理及生存特征
国内外指南一致推荐BTC患者做基因检测,BTC的分子异质性驱动了预后分层模型的革新。意大利-西班牙多中心研究聚焦于“双基因变异”(DGA)这一独特表型。研究者回顾性筛选2016-2024 年期间的1170例BTC患者,描述最常见的DGA组合,分析其临床-病理特征及与单变异(SGA)相比的生存差异。基因组变异按 ESCAT 分级,并纳入 ATM 突变、MDM2 扩增(TP53 野生型)及 MTAP 缺失等潜在靶点。
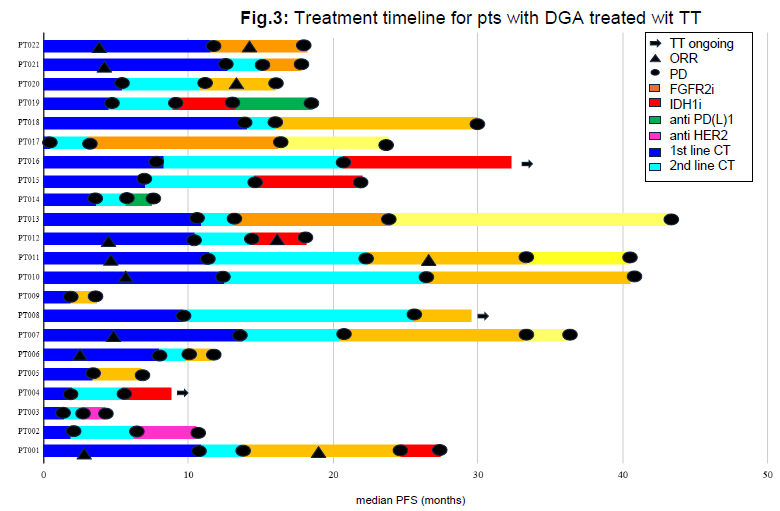
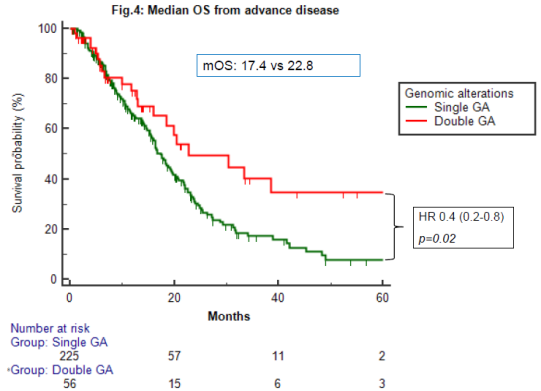
研究者筛选出457例携带可靶向的基因突变,其中 74.8% 为肝内胆管癌,371 例(81.2%)接受一线系统治疗,90 例(19.7%)至少接受一种靶向治疗。其中,19.5%(89例患者)存在DGA,最常见的组合为IDH1突变合并FGFR2融合(8%),其次为IDH1突变合并MDM2扩增(TP53 野生型)(6.7%),IDH1突变合并ERBB2扩增(5.6%)。中位随访 23.3 个月,接受靶向治疗的SGA(n=68)与DGA(n=22)患者,ORR(26.1% vs 14.3%) 与 PFS(6.4个月vs 7.9个月)无差异。值得注意的是,在未接受靶向治疗的患者中,DGA亚群相较单变异者死亡风险降低60%(HR=0.4, p=0.02),DGA是独立预后因素。
研究揭示:DGA可能代表BTC的一个独特生物学亚型,较单变异有更好的预后。因此深入了解BTC的生物学特征,可能为开发双靶联合或序贯靶向策略提供理论依据。
胰腺癌领域新进展:从围手术期到靶向治疗的全面进步
新辅助治疗:术前化疗时长优化
LBA85[6]:III期CASSANDRA研究提示延长术前化疗时间可显著提高可切除/交界可切除(R/BR) PDAC的pCR率及N0切除率,但EFS未显著延长
这是一项由意大利学者开展的CASSANDRA III期试验,探索了可切除/交界可切除(R/BR)PDAC患者术前化疗(CT)的最佳持续时间。患者首先被1:1随机分配接受PAXG方案(顺铂+白蛋白紫杉醇+卡培他滨+吉西他滨)或mFOLFIRINOX方案。治疗4个月后,无疾病进展和不良反应的患者,按既往化疗方案再次分层,第二次随机分为A组患者继续原方案2个月后手术(n=88),B 组患者立即手术(n=82),术后再补2个月原方案。主要终点为从第二次随机化日期起计算的无事件生存期(EFS)。
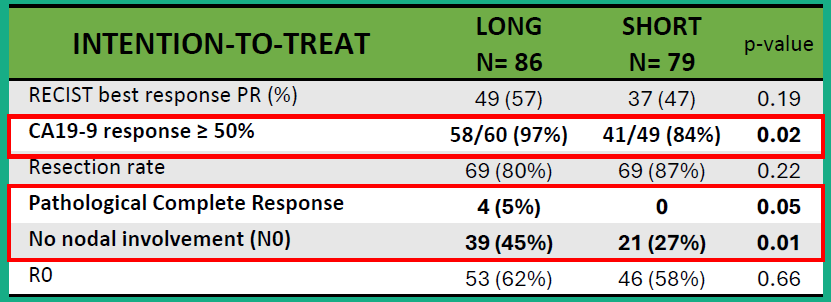
研究结果显示, 意向治疗人群(ITT)中A、B组的中位EFS分别为13.6个月、13.0个月,3年EFS分别为29%、23%,两组差异无统计学意义。A、B组中位OS分别为为36.3个月、32.8个月,3年OS分别为 54%、44%,同样无统计学差异。在手术相关指标方面,A、B组切除率 分别为80%和87%(p=0.22),病理完全缓解率(pCR)分别为5%和0%(p=0.05),N0率(即无区域淋巴结转移率)分别为45%和27%(p=0.01),R0切除率分别为62%和58%(p=0.66)。
研究者认为,延长术前化疗时间可显著提高 R/BR PDAC的pCR率及N0切除率,虽未显著延长 EFS,但趋势可能支持“更长疗程可能更优”。
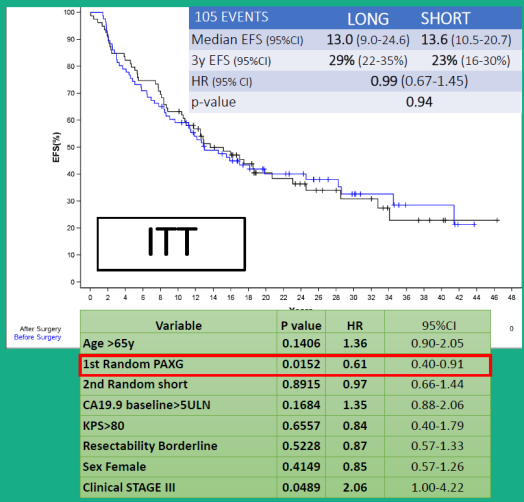
表2 ITT人群中次要研究终点结果
转化治疗:手术转化策略革新
2261eP[7]:NALIRIFOX方案用于局部进展期胰腺癌(LAPC)的转化潜力可期
一项Ⅱ期试验评估了NALIRIFOX方案用于局部进展期(LAPC)胰腺癌的转化疗效,研究纳入未接受治疗的、体能状态良好(ECOG 0-1)的LAPC患者,每2周给予一次NALIRIFOX方案(伊立替康脂质体+奥沙利铂+亚叶酸钙+5-FU)。主要终点为手术转化率
研究共入组20例患者,中位治疗周期4次(2-6次)。20例可评估患者中,1例达到病理完全缓解(pCR),6例部分缓解(PR),8例病情稳定(SD),5例病情进展(PD)。客观缓解率(ORR)为35.0%,疾病控制率(DCR)为75.0%。10例患者接受了手术探查,并成功进行了根治性切除,手术切除率是50%,其中9例患者(90%)实现R0切除。安全性方面,13例(65%)发生≥3级TEAE,4例(20%)需减量。>5%的3-4级TEAE为中性粒细胞减少、淋巴细胞减少等。
研究结论认为NALIRIFOX在LAPC中展现出良好的转化潜力及可管理的毒性。
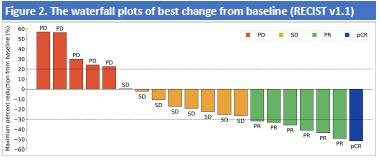
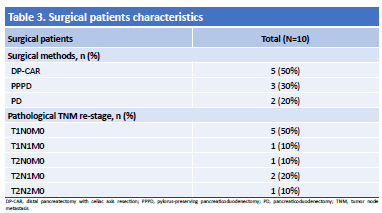
表3 外科手术患者基线特征
一线治疗:序贯给药可能增效
2221P[8]:FOOTPATH研究提示NAPOLI+mFOLFOX6一线治疗序贯方案有带来获益的趋势
FOOTPATH研究是一项随机、开放标签的Ⅱ期研究,对比了NAPOLI方案(伊立替康脂质体+5-FU/亚叶酸)、NAPOLI+mFOLFOX6序贯方案和吉西他滨+白蛋白紫杉醇方案(AG方案)用于初治mPDAC患者的疗效和安全性,主要终点为PFS。
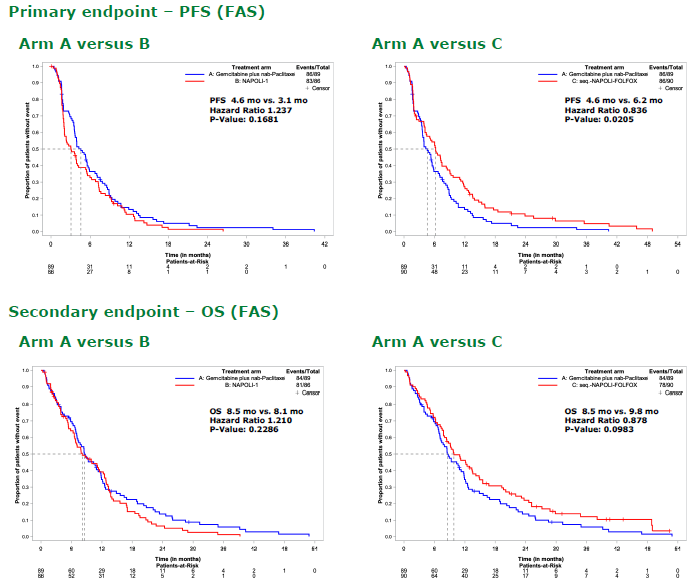
结果显示,在全分析集(FAS;n=265)中,NAPOLI+mFOLFOX6序贯方案mPFS为6.2个月,显著长于AG方案的4.6个月(HR 0.842,p=0.0267)。然而,NAPOLI方案未优于AG(3.1个月 vs 4.6个月;HR 1.237,p=0.1681)。在总生存期方面,NAPOLI+mFOLFOX6序贯方案的mOS为9.8个月,数值高于AG组的8.5个月(HR 0.878,P=0.0983),差异未达统计学意义。NAPOLI方案与AG组OS无差异(8.1个月 vs 8.5个月;HR 1.21;p=0.2286)。
尽管总生存差异未达统计学显著,NAPOLI+mFOLFOX6序贯方案显著改善PFS且OS数值延长,支持该序贯策略可作为mPDAC的有效一线治疗选择。
后线治疗:口服方案提升便捷性
2217P[9]:PC-NaliCap研究提示后线治疗NaliCap方案用于GEM经治mPDAC患者,非劣效于NAPOLI-1方案
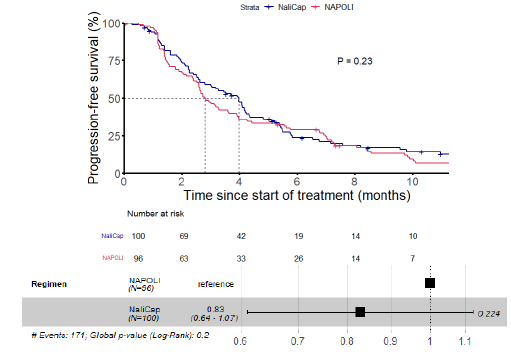
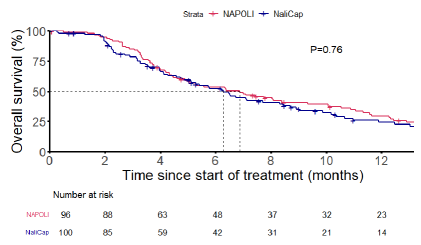
PC-NaliCap 试验一项韩国开放标签、多中心、随机II期研究,评估了伊立替康脂质体/卡培他滨联合方案(NaliCap)较NAPOLI-1在GEM经治mPDAC患者中的非劣效性。研究分为两个阶段:安全性导入(SLI)阶段和随机阶段。在SLI阶段,入组17例患者,确定了NaliCap的推荐II期剂量(RP2D)为nal-IRI 90 mg/m²联合CAP 1000 mg/m²。随机阶段共入组196例患者,其中NAPOLI-1组96例,NaliCap组100例,包括95例二线治疗患者,101例三线及以上治疗患者。主要终点是PFS。
结果显示,NaliCap与NAPOLI-1中位PFS分别为3.97个月和2.8个月,HR 0.83(90%CI 0.64-1.07,p=0.23);OS无显著差异(NaliCap 6.27个月,NAPOLI-1组 6.87个月,HR 0.95,p=0.76)。NaliCap与NAPOLI-1的ORR分别为11%和8.3%(p=0.646)。NaliCap和NAPOLI-1治疗相关3/4级AE发生率分别为28.4%与27.7%,无治疗相关死亡。最常见的3/4级不良事件为中性粒细胞减少(NaliCap 17.9%,NAPOLI-1 24.5%)。
NaliCap方案通过以口服卡培他滨(CAP)替代持续输注的5-FU,在与NAPOLI-1方案的对比中达到了非劣效标准。对于mPDAC患者而言,NaliCap方案不仅在疗效上与NAPOLI-1方案相当,而且通过口服给药的方式,为患者提供了一种更为便捷的治疗选择。
靶向治疗:KRAS G12D抑制剂突破成药壁垒
LBA84[10]:GFH375单药治疗晚期经治KRAS G12D突变型PDAC的疗效与安全性
致癌性KRAS突变在PDAC中最为常见,其中G12D突变最为常见(约40%),且预示着患者预后较差。GFH375是一种口服、强效、高选择性的KRAS G12D抑制剂,在GDP(关闭)和GTP(开启)状态下均有效。本项I/II期研究由我们团队牵头,评估了口服GFH375用于经治KRAS G12D突变型PDAC患者的疗效和安全性。主要终点是客观缓解率 (ORR)。
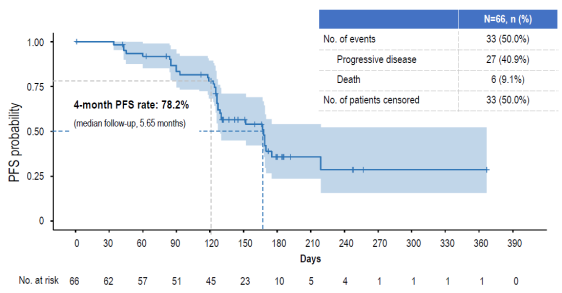
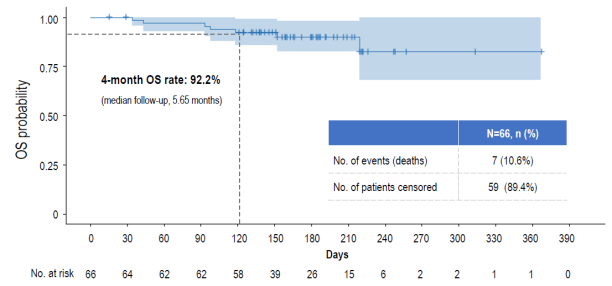
共有66例PDAC患者接受了GFH375治疗(600mg QD),中位暴露持续时间为117天,其中45例(68.2%)患者既往至少接受过两线抗肿瘤治疗。在至少有一次治疗后评估的患者中,ORR为40.7%(24/59),DCR高达97%(57/59)。在中位随访5.65个月的情况下,mPFS为5.52个月,4个月的PFS率为78.2%;mOS未达到,4个月的OS率为92.2%。
安全性方面,20例患者(30。3%)出现了3级TRAE,1名患者(1.5%)出现了4级TRAE。TRAE导致4名患者(6.1%)剂量减少,2名患者(3%)停药。最常见的TRAE包括腹泻、中性粒细胞计数减少、呕吐、恶心、贫血、白细胞计数减少等。
GFH375单药治疗在经治的KRAS G12D突变型PDAC患者中显示出潜在疗效和可管理的安全性,为这一难治性疾病的治疗提供了新的希望。
2215O[11]:HRS-4642联合GA在晚期KRAS G12D突变PDAC患者中的疗效与安全性
HRS-4642是一种高选择性、长效、非共价的KRAS G12D抑制剂。KRAS G12D抑制剂通过阻断MEK/ERK磷酸化,有望进一步提高AG方案在KRAS G12D突变PDAC中的疗效。上海交通大学医学院附属仁济医院王理伟教授牵头开展了一项Ⅰb/Ⅱ期临床研究,旨在评估HRS-4642联合AG方案在晚期KRAS-G12D突变型PDAC患者中的治疗效果。
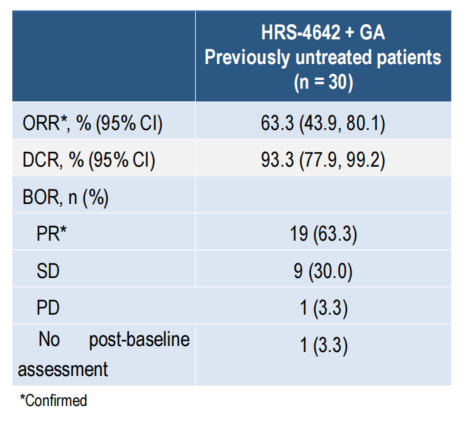
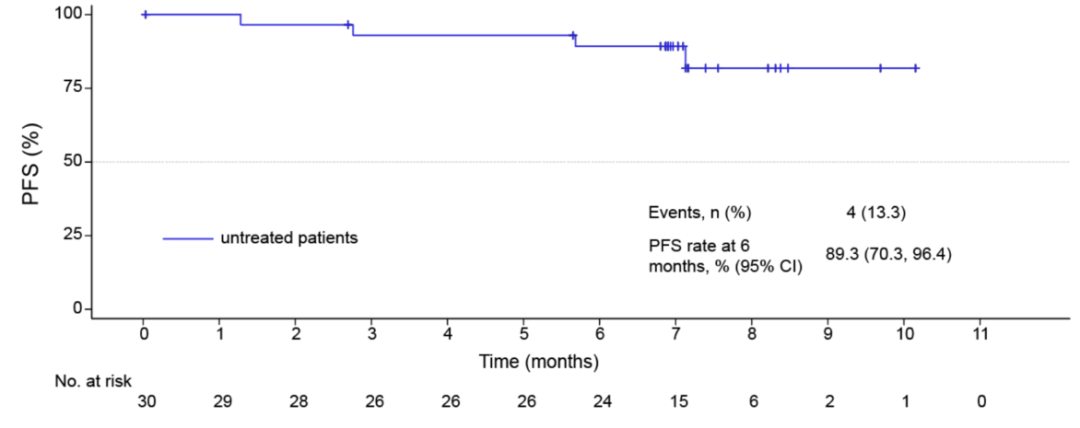
截至2025年7月8日,共有31例患者入组,包括1例经治患者和30例初治患者,接受HRS-4642(第1天500 mg,第8天1200 mg,静脉输注,每三周一次)联合AG方案治疗。中位随访7.5个月,在30例初治患者中,经确认的客观缓解率(ORR)为63.3%(95% CI 43.9%-80.1%)。在19例缓解者中,有18例患者的客观缓解仍在持续,中位缓解持续时间(DoR)尚未成熟。在30例初治患者中,共发生4例疾病进展事(13.3%),6个月的无进展生存期率为89.3%。
在安全性方面,87.1%(27/31)的患者发生了≥3级的治疗相关不良事件(TRAE)。最常见的≥3级TRAEs(发生率≥15%) 包括:中性粒细胞计数降低(90.3%)、白细胞计数降低(87.1%)和贫血(83.9%)。未发生导致治疗终止的TRAE,也无治疗相关死亡事件。
由此可见,HRS-4642联合AG方案在晚期KRAS-G12D突变型PDAC中展现出令人鼓舞的抗肿瘤疗效和可控的安全性特征。
表4 初治患者中HRS-4642联合治疗疗效
915O[12]:HRS-4642治疗KRAS G12D突变晚期实体瘤的I期临床试验
KRAS是实体瘤中最常突变的致癌基因之一,其中KRAS G12D是最主要的突变亚型。同济大学附属东方医院熊安稳教授团队牵头开展了一项多中心、开放标签、首次人体I期研究,旨在评估新型KRAS-G12D抑制剂HRS-4642在标准治疗失败的KRAS G12D突变晚期实体瘤患者中的疗效与安全性。研究采用贝叶斯最优区间设计进行剂量递增(200~500 mg每周一次静脉注射,或800/1200 mg每两周一次,或1200 mg每三周一次),随后进行剂量扩展和适应症扩展。主要终点为安全性、最大耐受剂量和推荐Ⅱ期剂量。
截至2025年3月14日,研究共纳入84例患者接受治疗,包括38例非小细胞肺癌患者和24例胰腺导管腺癌患者,中位既往治疗线数为2线。结果显示,剂量递增阶段18例患者无剂量限制性毒性,最大耐受剂量未达到。
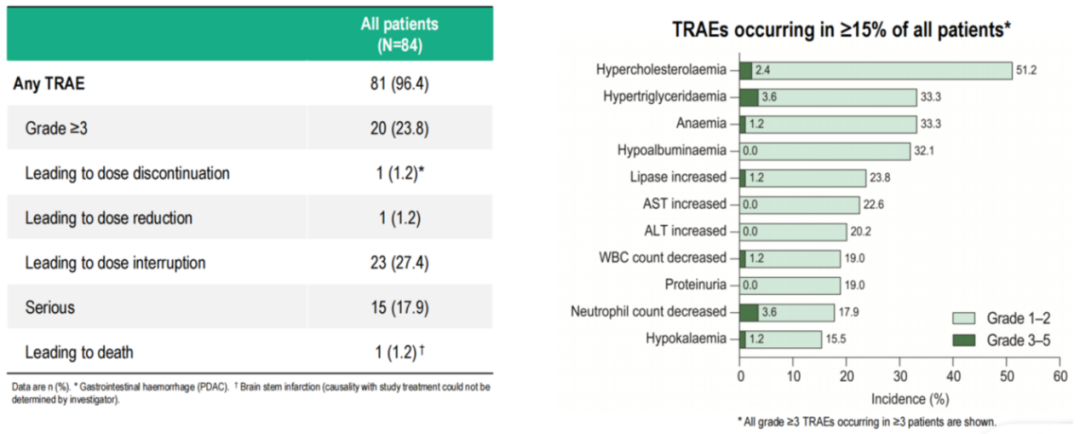
安全性方面,23.8%的患者出现≥3级TRAE,最常见的≥3级TRAE为高甘油三酯血症、中性粒细胞减少和高胆固醇血症,各占3.6%,且仅1例(1.2%)患者因TRAE停药,1例(1.2%)发生治疗相关死亡。
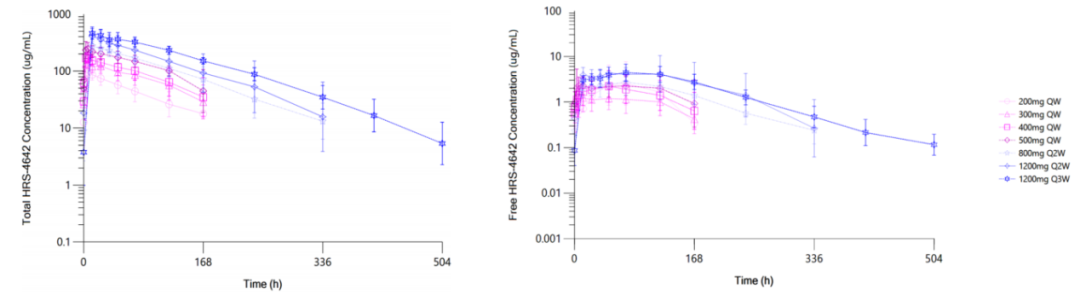
药代动力学方面,HRS-4642的总药物及包封型药物终末半衰期均约为3天,循环游离KRAS G12D的早期变化支持每两周给药方案。
HRS-4642在KRAS G12D突变晚期实体瘤(尤其是非小细胞肺癌和胰腺导管腺癌)中耐受性良好,展现出有前景的活性,为后续联合治疗奠定了重要基础。
结语
随着2025年ESMO年会的圆满落幕,胆管癌与胰腺癌领域的研究新进展如同璀璨星辰,照亮了未来的治疗道路。从围手术期治疗的优化到晚期系统治疗的精准化,从靶向治疗的深入探索到基因组标志物的临床转化,这些研究成果不仅为临床医生提供了新的治疗思路和策略,也为患者带来了新的希望。
1.G. Shi, et al. 2025 ESMO. Abstract LBA11.
2.K. Iida, et al. 2025 ESMO. Abstract 95P.
3.A. Casadei Gardini et al. 2025 ESMO. Abstract 107eP.
4.J.A. Bridgewater, et al. 2025 ESMO GI. Abstract 262MO.
5.V. Genovesi, et al. 2025 ESMO. Abstract 90P.
6.M. Reni, et al. 2025 ESMO. Abstract LBA85.
7.K. Jiang, et al. 2025 ESMO. Abstract 2261eP.
8.T. Gaska, et al. 2025 ESMO. Abstract 2221P.
9.J. Yoon, et al. 2025 ESMO. Abstract 2217P.
10.A. Zhou, et al. 2025 ESMO. Abstract LBA84.
11.L. Wang, et al. 2025 ESMO. Abstract 2215O.
12.A. Xiong, et al. 2025 ESMO. Abstract 915O.
本资料的内容仅作为科学信息参考,仅用于医疗卫生专业人士的学术交流,请勿用于任何其他用途。若您不是医疗卫生专业人士,请勿观看和/或传播此资料。
本资料可能会出现某些药品信息,但该药品/适应症可能尚未获得国家药品监督管理局的注册批准。医疗卫生专业人士做出的任何与治疗有关的决定应根据患者的具体情况并应参照国家药品监督管理局批准的药品说明书。对于本资料可能提到的相关诊断、治疗方法,请遵守国家卫生健康委员会以及相关部门批准使用的指南或规定。
审批号:M-TIBSO-CN-202511-00025
本文转自:中国医学论坛报今日肿瘤











 苏公网安备32059002004080号
苏公网安备32059002004080号


