前列腺癌骨转移是晚期疾病的主要临床表现,在去势抵抗性前列腺癌(mCRPC)患者中发生率高达90%[1],严重影响患者生活质量及生存预后。更为复杂的是,疾病本身及其核心治疗手段(如ADT)均会加剧骨骼损伤,这使得临床管理始终面临控制肿瘤进展与维护骨骼健康的双重挑战。
与此同时,放射治疗技术正经历从姑息止痛向精准治疗的深刻变革,成为应对上述挑战的关键力量。然而,有效的放射治疗手段在杀灭肿瘤的同时,其本身也对骨骼环境存在潜在影响。因此,构建一个融合精准放疗与规范骨保护的综合策略,显得至关重要。
鉴于此,【肿瘤资讯】特邀西南医科大学附属医院罗雨豪教授,就放射治疗在前列腺癌骨转移领域的作用演进、新进展及其与骨保护剂的协同管理策略进行深入解读。
西南医科大学附属医院副主任医师,肿瘤科主任助理
中国肿瘤放射治疗联盟(CRTOG)第一届放射免疫青委会委员
四川省医学科技创新研究会肿瘤免疫治疗分会秘书长、常委
四川省抗癌协会肿瘤内分泌专委会副主任委员
四川省抗癌协会肿瘤支持治疗及全程管理专委会委员
四川省抗癌协会肿瘤心理与健康管理专委会委员
四川省医师协会靶向治疗青委会委员
四川省医师协会肿瘤分会青委会委员
四川省医师协会基因与免疫治疗专委会委员
四川省医师协会放射肿瘤治疗医师分会委员
四川省医促会肿瘤分子靶向专委会委员
四川省生物信息学会智慧免疫分会委员
四川省预防医学会基层肿瘤防治专委会委员
西部放射治疗协会放射免疫专委会青委
专注于结直肠癌、肺癌、神经内分泌肿瘤等多病种精准化全程管理
主持国家自然科学基金青年基金1项,四川省科技厅课题2项,泸州市级课题1项,市校联合课题1项,院级课题2项,教改课题1项。
以第一作者/通讯作者于《Clinical Cancer Research》、《Autophagy》、《Molecular Therapy》、《Cancer Letter》等杂志发表SCI论文12篇,其中IF>5分9篇,单篇最高影响因子16.016,累计影响因子90多分。担任《Frontiers Oncology》、《Frontiers in immunology》、《Cell Death & Disease》、《Current Pharmaceutical Design》等多家SCI杂志审稿人/编委。
前列腺癌具有极高的骨转移倾向,是其晚期阶段的主要表现和致死、致残的主要原因
骨骼是前列腺癌最主要的远处转移靶器官,这一生物学特性决定了晚期患者的预后与生活质量。研究显示,90%的mCRPC患者最终会发展为骨转移[1]。更为复杂的是,前列腺癌的核心治疗手段——雄激素剥夺治疗(ADT),本身也会加剧骨质流失,进一步推高骨折风险(图1)[2,3]。在ADT治疗的第一年内,髋部BMD下降约2%,腰椎BMD下降约3%,并且5年时发生严重骨折的风险为10%~20%[4]。
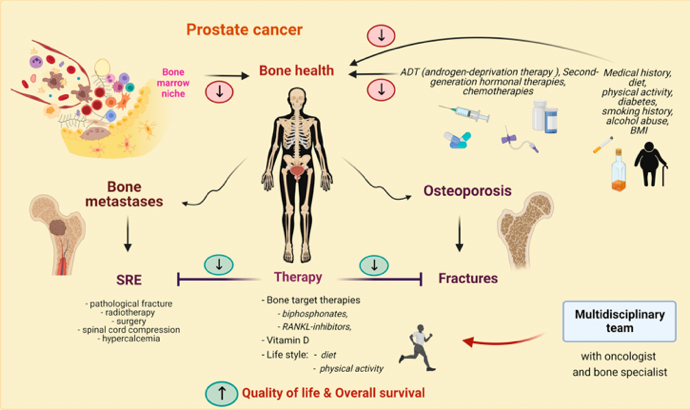
患者一旦发生骨转移,将无法治愈,并会伴有严重的并发症,如高钙血症、病理性骨折和硬膜外脊髓压迫,甚至会造成截瘫和肢体活动障碍等,严重影响患者的生活质量[3],同时也为患者及其家庭带来沉重的经济负担[5]。因此,前列腺癌骨转移的管理面临双重挑战:既要有效控制肿瘤、缓解症状,又必须积极维护骨骼健康,预防SREs。
在此背景下,放射治疗的作用日益凸显,其应用已从传统的姑息治疗,演进为能够改善生存的精准策略。
放射治疗不断发展,已从局部姑息,扩展为兼具全身性疾病控制能力的不可或缺的治疗手段
面对前列腺癌骨转移所带来的严峻挑战与ADT对骨骼的持续损害,临床迫切需要能有效控制病灶、改善预后的强力手段。放射治疗具有直接、高效的杀伤能力占据重要地位,且近年来其技术经历了深刻演进,已形成涵盖局部精准打击、系统性核素靶向乃至肿瘤特异性配体在内的高效方案,为不同阶段患者提供了精准治疗选择。下文将对前列腺癌骨转移放射治疗领域的关键进展进行详尽剖析。
SBRT通过精准清除寡转移灶以改变疾病进程
针对寡转移性前列腺癌,立体定向体部放疗(SBRT)凭借其高精度、高剂量的技术特点,能够对有限的骨转移灶实现精准清除。SBRT通过影像引导实现精准定位,在有效杀灭肿瘤的同时,最大限度地保护周围正常组织[6]。
临床研究显示,对寡转移灶实施SBRT可显著延缓疾病进展。STOMP研究表明,该治疗可将疾病进展时间推迟约8-12个月,同时降低新发病灶的出现频率[7]。从机制上看,SBRT不仅能直接诱导肿瘤细胞死亡,还可重塑肿瘤微环境,可能在一定程度上激活抗肿瘤免疫应答[8]。
在临床实践中,SBRT的优势主要体现在其较短的治疗周期(通常1-5次)和良好的安全性,在有效缓解骨痛的同时,还能显著降低严重不良反应的发生风险[9]。这些特点使其成为寡转移前列腺癌综合治疗中的重要组成部分。
靶向放射性核素疗法已成为mCRPC骨转移患者的重要系统治疗手段
对于发生广泛性骨转移的mCRPC患者,系统性放射性核素治疗展现出独特的治疗优势,其发展历程体现了靶向治疗的持续精进。
β核素如锶-89的应用开启了核素内照射治疗的先河,能有效缓解多发性骨痛,为后续靶向治疗奠定了基础。近年来α核素带来重要突破,其中镭-223作为首个获批的α粒子靶向治疗药物,通过模拟钙离子特性特异性靶向骨转移灶的成骨活跃区域,释放高能α粒子诱导肿瘤细胞DNA双链断裂,同时对周围正常组织损伤极小。基于III期ALSYMPCA研究的证实,镭-223不仅能显著延长mCRPC患者的总生存期,还能有效延迟症状性骨骼事件的发生,实现了从"姑息"到"延长生存期"的重要跨越[10]。目前,镭-223与新型内分泌药物等联合应用正在不断探索中,致力于进一步提升疗效。
当前,肿瘤靶向治疗进一步崛起,177Lu-PSMA-617将放疗从"骨靶向"推向"肿瘤靶向"的新阶段。该药物通过特异性结合前列腺癌细胞高表达的PSMA蛋白,实现对肿瘤病灶(包括骨和内脏)的精准辐射递送。III期VISION研究结果奠定了其在mCRPC治疗中的重要地位,显著改善患者的生存预后[11]。随着研究的深入,新型放射治疗药物仍在不断探索中,包括能量更强、射程更短的225Ac-PSMA和215Bi-PSMA等新型α核素药物正处于临床研究阶段,有望为经多重治疗失败的患者带来新的希望。同时,兼具β治疗和γ成像功能的161Tb-PSMA,以及镭-223与其他α粒子发射体与免疫疗法联合应用的研究也在积极推进[12],尽管目前联合免疫治疗的临床试验结果尚无定论,但这些探索为未来治疗格局的革新提供了新的方向。
放射治疗的疗效依赖于与骨保护剂的协同管理
尽管上述放射治疗策略在控制肿瘤方面成效显著,但它们均会不同程度地扰动骨骼微环境的稳态。外照射放疗可导致照射野内骨坏死和生物力学强度下降;而系统性核素治疗在高效杀灭肿瘤细胞的同时,会破坏局部骨代谢平衡,并启动伴随破骨细胞激活的修复过程,可能引发生物力学强度下降。因此,无论是外照射还是核素治疗,都需要骨保护药物协同治疗。
为什么放射治疗需要骨保护剂协同?
对于SBRT而言,高剂量辐射在精准杀灭寡转移灶的同时,也会不可逆地损伤照射野内的正常骨组织,导致放射性骨坏死、并可能在一段时间内削弱局部骨骼的生物力学强度,增加病理性骨折的风险。
对于靶向放射性核素治疗而言,这类药物的抗肿瘤机制建立在靶向骨转移灶并高效杀灭肿瘤细胞的基础上。然而,肿瘤细胞的死亡会破坏局部已建立的骨代谢平衡,并启动一个涉及炎症反应、破骨细胞激活与骨修复的复杂过程。这一过程可能导致全身多部位骨骼出现暂时的、同步的骨吸收增强,从而潜在地加剧了骨骼的脆弱性,并推高了症状性SREs的整体风险[13]。
地舒单抗通过抑制RANKL成为巩固放疗疗效的基石药物
基于上述机制,完整的骨转移治疗策略必须包含对骨骼本身的保护。地舒单抗通过抑制RANKL通路直接抑制破骨细胞活性,减少骨吸收,从而降低骨骼相关事件的发生风险。研究还发现,地舒单抗可能通过调节骨微环境间接影响免疫应答,RANKL通路的抑制可能影响肿瘤相关巨噬细胞等免疫细胞的功能[14]。值得注意的是,地舒单抗与免疫检查点抑制剂的联合应用可产生协同抗肿瘤效应,为未来联合治疗策略的开发提供了新的思路[14]。
基于现有证据,美国国家综合癌症网络(NCCN)[15]、欧洲泌尿外科学会(EAU)指南[16]、前列腺癌骨转移和骨相关疾病临床诊疗专家共识[17]等多部权威指南一致推荐对前列腺癌骨转移患者尽早使用地舒单抗等骨保护剂,并将其与放射治疗方案联合应用。对于前列腺癌骨转移的患者,这种协同管理模式已成为最大化治疗效益、最小化骨骼相关风险的关键策略。
总结
前列腺癌骨转移的管理需要综合治疗。放射治疗已从传统的姑息手段,演进为一个包含局部SBRT、系统性核素治疗及放射性配体治疗在内的精准治疗体系。然而,必须认识到,有效的抗肿瘤治疗本身可能潜在地增加骨骼的脆弱性。因此,将地舒单抗等骨保护剂作为基础治疗,与放射治疗方案早期联合、协同管理,已成为最大化治疗效益、最小化骨骼相关风险的关键所在,并获国内外权威指南一致推荐。
展望未来,随着新型放射药物的探索及放疗与免疫治疗的联合研究,前列腺癌骨转移的治疗格局将持续革新,其中,以“放射治疗”有力控制病灶,以“规范骨保护”保护骨骼健康,二者并重,将是贯穿始终、改善患者生活质量和生存预后的重要策略。
1. Body JJ, et al. A real-world study assessing the use of bone-targeted agents and their impact on bone metastases in patients with prostate cancer treated in clinical practice in Europe. J Bone Oncol. 2018 Dec 18;14:100212.
2. Lin JK, et al. Bone Health in Prostate Cancer Survivors: Recent Lessons and Opportunities for Improvement. Eur Urol Focus. 2023 May;9(3):422-424.
3. Baldessari C, et al. Bone Metastases and Health in Prostate Cancer: From Pathophysiology to Clinical Implications. Cancers (Basel). 2023 Feb 28;15(5):1518.
4. von Moos R, et al. Pain and analgesic use associated with skeletal-related events in patients with advanced cancer and bone metastases. Support Care Cancer. 2016 Mar;24(3):1327-1337.
5. Body JJ, et al. The economic burden associated with skeletal-related events in patients with bone metastases secondary to solid tumors in Belgium. J Med Econ. 2013;16(4):539-546.
6. Tree AC, et al. Stereotactic body radiotherapy for oligometastases. Lancet Oncol. 2013 Jan;14(1):e28-37.
7. Ost P, et al. Surveillance or Metastasis-Directed Therapy for Oligometastatic Prostate Cancer Recurrence: A Prospective, Randomized, Multicenter Phase II Trial. J Clin Oncol. 2018 Feb 10;36(5):446-453.
8. Weichselbaum RR, et al. Radiotherapy and immunotherapy: a beneficial liaison? Nat Rev Clin Oncol. 2017 Jun;14(6):365-379.
9. Ito K, S et al. Stereotactic body radiotherapy versus conventional radiotherapy for painful bone metastases: a systematic review and meta-analysis of randomised controlled trials. Radiat Oncol. 2022 Sep 13;17(1):156.
10. Sartor O, et al. Effect of radium-223 dichloride on symptomatic skeletal events in patients with castration-resistant prostate cancer and bone metastases: results from a phase 3, double-blind, randomised trial. Lancet Oncol. 2014 Jun;15(7):738-746.
11. Sartor O, et al. Lutetium-177-PSMA-617 for Metastatic Castration-Resistant Prostate Cancer. N Engl J Med. 2021 Sep 16;385(12):1091-1103.
12. Fei X, et al. Current status of radionuclide therapies in metastatic castration-resistant prostate cancer. Ther Adv Med Oncol. 2025 Oct 2;17:17588359251379739.
13. Suominen MI, et al. The Mode-of-Action of Targeted Alpha Therapy Radium-223 as an Enabler for Novel Combinations to Treat Patients with Bone Metastasis. Int J Mol Sci. 2019 Aug 10;20(16):3899.
14. Chang H, et al. Immune Modulation with RANKL Blockade through Denosumab Treatment in Patients with Cancer. Cancer Immunol Res. 2024 Apr 2;12(4):453-461.
15. National Comprehensive Cancer Network. Prostate Cancer (Version 3.2026).
16. European Association of Urology. Guidelines on Prostate Cancer. 2025.
17. 中国抗癌协会泌尿男生殖系统肿瘤专业委员会. 前列腺癌骨转移和骨相关疾病临床诊疗专家共识(2021版).中华肿瘤杂志. 2021;43(10):9.
排版编辑:肿瘤资讯-LBJ











 苏公网安备32059002004080号
苏公网安备32059002004080号


