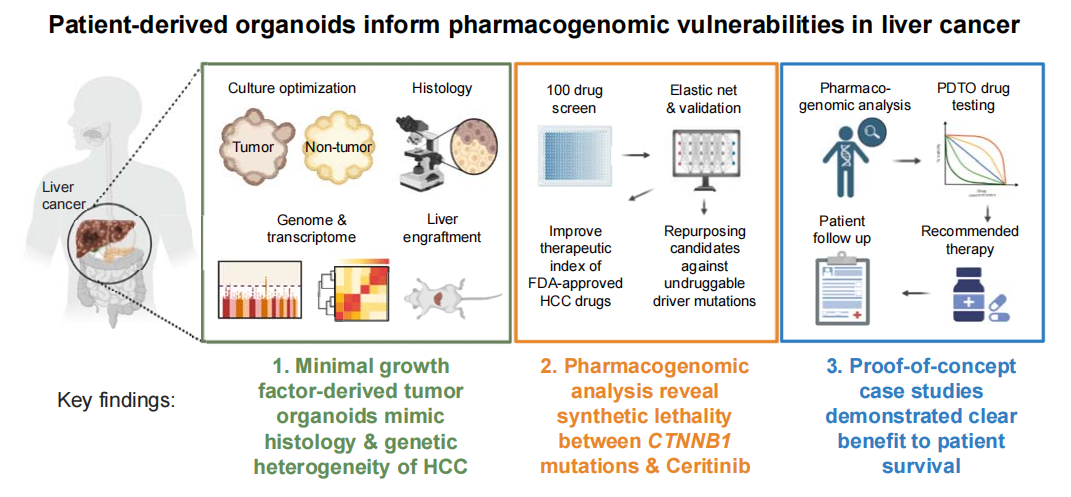
近期,香港中文大学Nathalie Wong教授团队发表一项最新研究——通过患者来源的肿瘤类器官(PDTO)技术,科学家们不仅优化了培养方法,使其更适合临床应用,还发现了新的药物靶点,为肝癌的精准治疗带来了曙光。

题目:患者来源的类器官揭示肝癌的药理遗传学脆弱性
杂志:JHEP Reports
影响因子:7.5
发表时间:2025年6月
研究背景
肝癌(HCC)是全球癌症死亡的主要原因之一,其治疗面临诸多挑战,主要原因包括缺乏可操作的临床变异指标以及主要突变驱动因子(如TP53和CTNNB1)的不可靶向性。因此,重新利用现有药物,针对这些突变背后的合成致死途径,可能是改善治疗结果的一种解决方案。
传统二维细胞培养和动物模型在研究HCC中存在局限性,如培养成功率低、成本高、缺乏标准化以及时间限制等。近年来,患者来源的肿瘤类器官(PDTO)技术逐渐兴起,能够更准确地模拟肿瘤的生物学特性。然而,现有的PDTO培养方法依赖于复杂的生长因子和条件培养基,增加了培养的复杂性和成本。
本研究旨在优化PDTO的培养方法,通过减少生长因子的使用,提高培养的成功率和标准化程度,降低成本,使其更适合临床应用。此外,研究还通过药理遗传学分析,探索了PDTO在精准医疗中的潜力,特别是针对HCC中常见的CTNNB1突变。
通过揭示CTNNB1突变与药物敏感性之间的关系,本研究为HCC的精准治疗提供了新的靶点和策略,有望改善患者的治疗效果和生存率。
研究思路
研究者们优化了PDTO的建立方法,使用生长因子减少的培养基(GF-)来提高培养成功率,并减少环境依赖性。
他们从接受根治性肝切除术的HCC患者中成功建立了23个PDTO,并对其进行了全面分析,包括标志性突变的鉴定、基因组异质性的评估、转录组分析和组织学特征的描述。
此外,研究者们还对这些PDTO进行了100种药物的再利用筛选,以探索肿瘤特异性的药物反应,并进行了药理遗传学分析。
研究结果
1. 患者来源的肝细胞癌类器官的生成
在香港威尔斯亲王医院100例肝癌手术样本中,77例确诊HCC,均携带TP53、CTNNB1或TERT突变。
对这些样本的短期3D培养成功率94.8%,可快速用于药物筛选;30%样本成功建立了长期类器官库(>20代),突变特征与HBV队列一致。
同时,培养了10例非肿瘤/正常肝类器官,并与2D细胞系及ATCC细胞系对比药敏,为精准治疗提供高效平台。
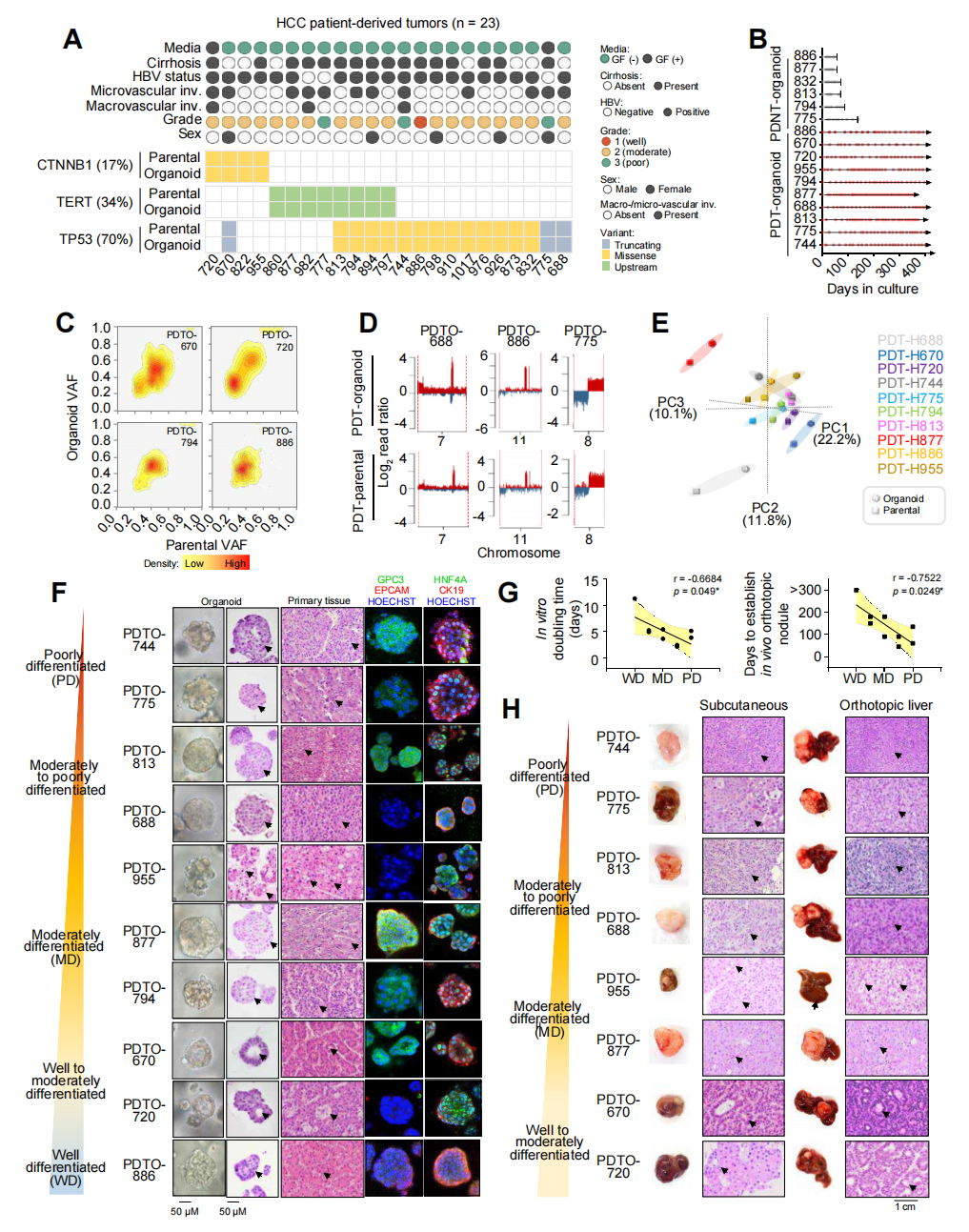
2. PDTO保留了亲代肿瘤的组织病理学和分子特征
为建立符合患者肿瘤生物学的HCC模型,分析了10个覆盖不同病理类型并携带TP53、CTNNB1等关键突变的PDTO。全外显子组测序证实PDTO保留原始致病突变、突变等位基因频率及11q13.3、7q31.2扩增和8p21.1缺失等拷贝数变异;PCA显示转录组与亲代肿瘤高度一致。
PDTO可持续扩增40代以上,并重现实体、假腺泡、小梁等组织学形态,GPC3、CK19等标志表达正确;其倍增时间与病理分级相关,致瘤性在NSG小鼠皮下与肝原位移植均获验证,低分化者植入更快。配对非肿瘤类器官寿命短、呈单层囊状。
综上,该PDTO体系忠实再现亲代HCC,适合后续研究与治疗评估。
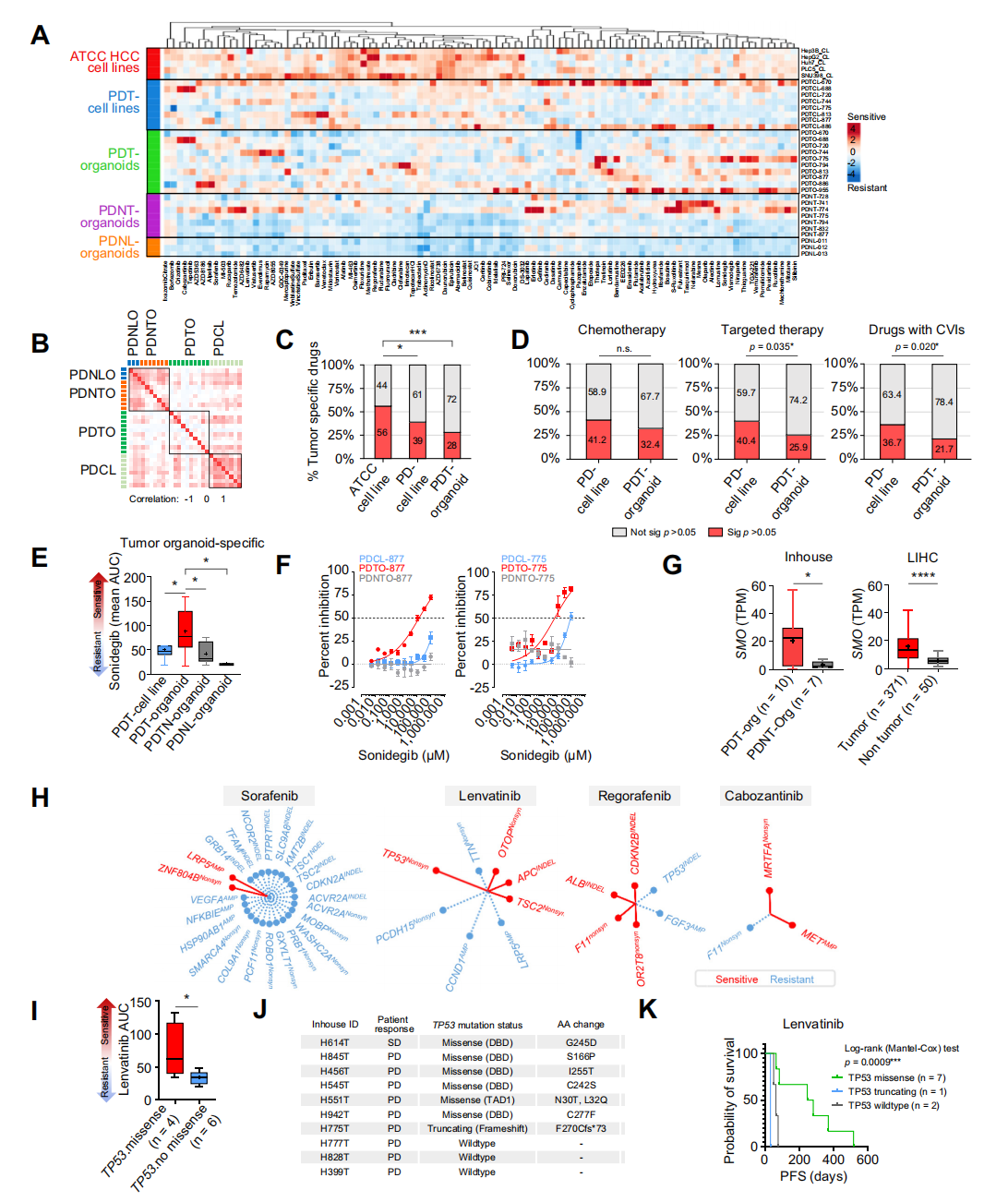
3. 改善治疗指标的药物基因组学指标
在28份患者模型(10个PDTO、8个PDTCL、7个PDNTO、3个PDNLO)和5株ATCC肝癌细胞系中,对100种药物(85种FDA批准+15种管线药物)进行双重复筛,结果显示批次一致性高。
PDNT和PDNL对大多数药物耐药,提示药效具肿瘤特异性;PDTO反应异质性强于PDTCL,后者再低于ATCC细胞系。靶向药(如雷帕霉素、AZD8055)在PDTO中活性显著,化疗组差异不明显。
整合突变与药敏发现:SMO抑制剂sonidegib因SMO上调在PDTO中更敏感;MET扩增、cabozantinib敏感但频率低;TP53错义突变与lenvatinib疗效相关,错义突变患者无进展生存期显著延长(中位262.5天)。
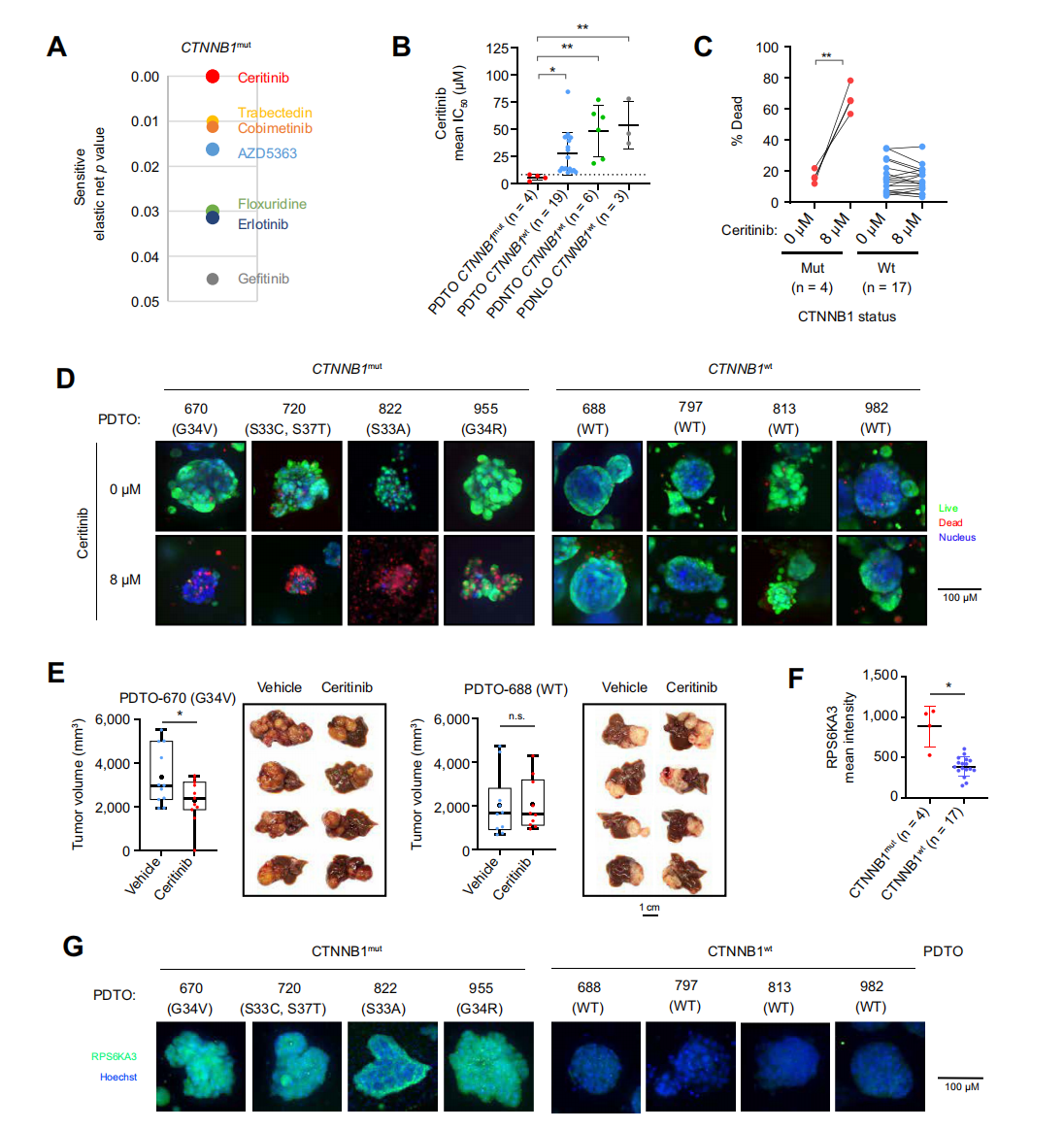
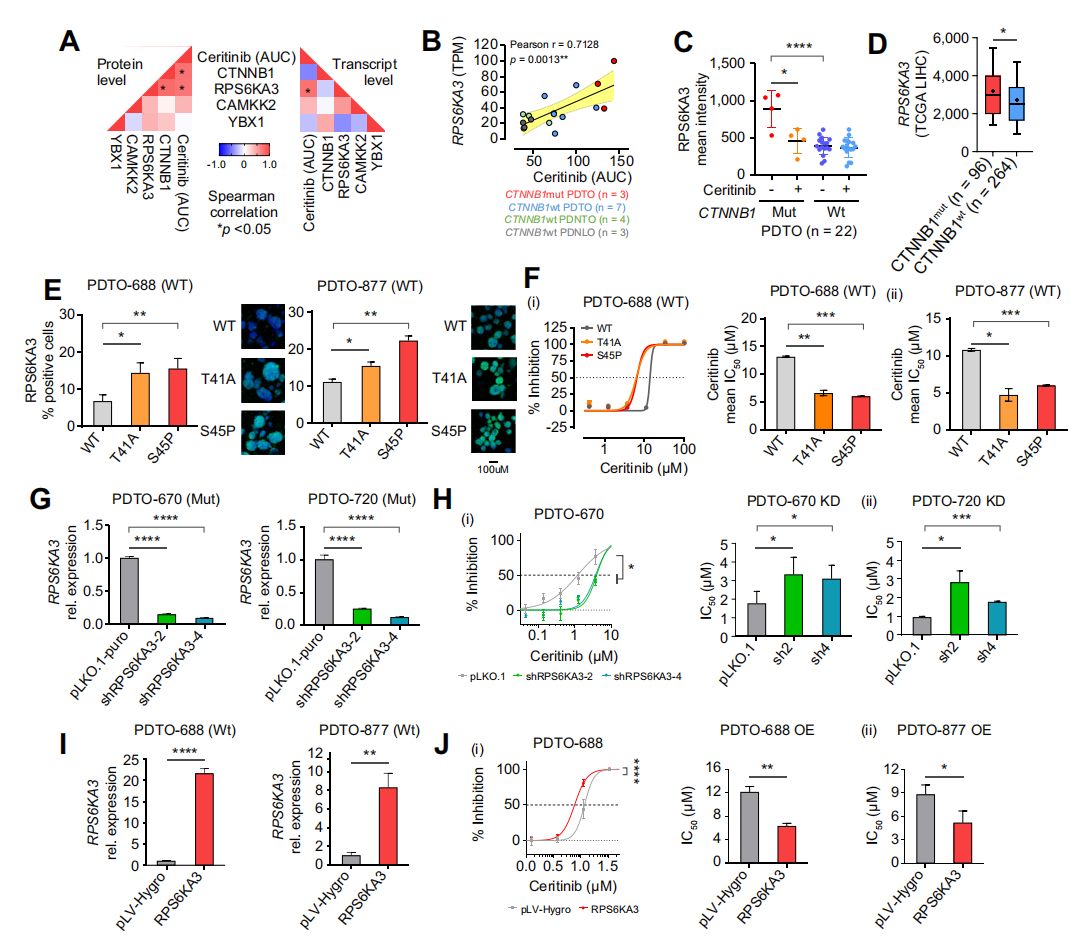
4. CTNNB1突变对ceritinib的敏感性是通过与ALK无关的非经典Wnt信号实现的
CTNNB1突变是HCC的主要驱动因素,发生率为11%–37%。研究发现,CTNNB1突变的PDTO对ceritinib敏感,其IC50显著低于野生型。
Ceritinib在非肿瘤和正常肝类器官中细胞毒性较低,表明其治疗指标良好。在CTNNB1突变的原位体内模型中,ceritinib可导致特异性细胞死亡和肿瘤负荷减轻。
研究还发现,CTNNB1突变的PDTO中RPS6KA3水平显著升高,且与ceritinib应答相关。RPS6KA3的抑制可导致CTNNB1突变的PDTO对ceritinib的耐药性增加,而过表达RPS6KA3可使野生型PDTO对ceritinib敏感。
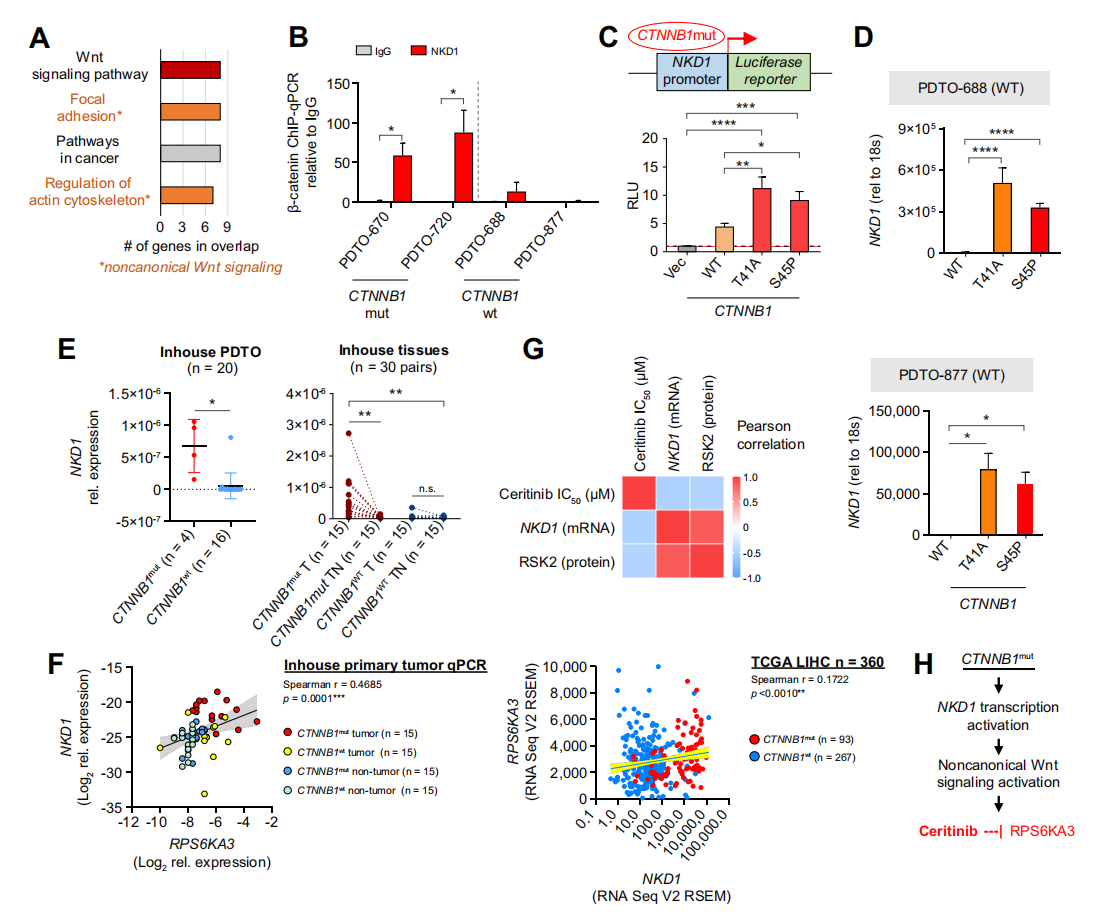
机制研究表明,突变型β-catenin可直接结合NKD1启动子,激活非典型Wnt信号通路,导致RPS6KA3上调。
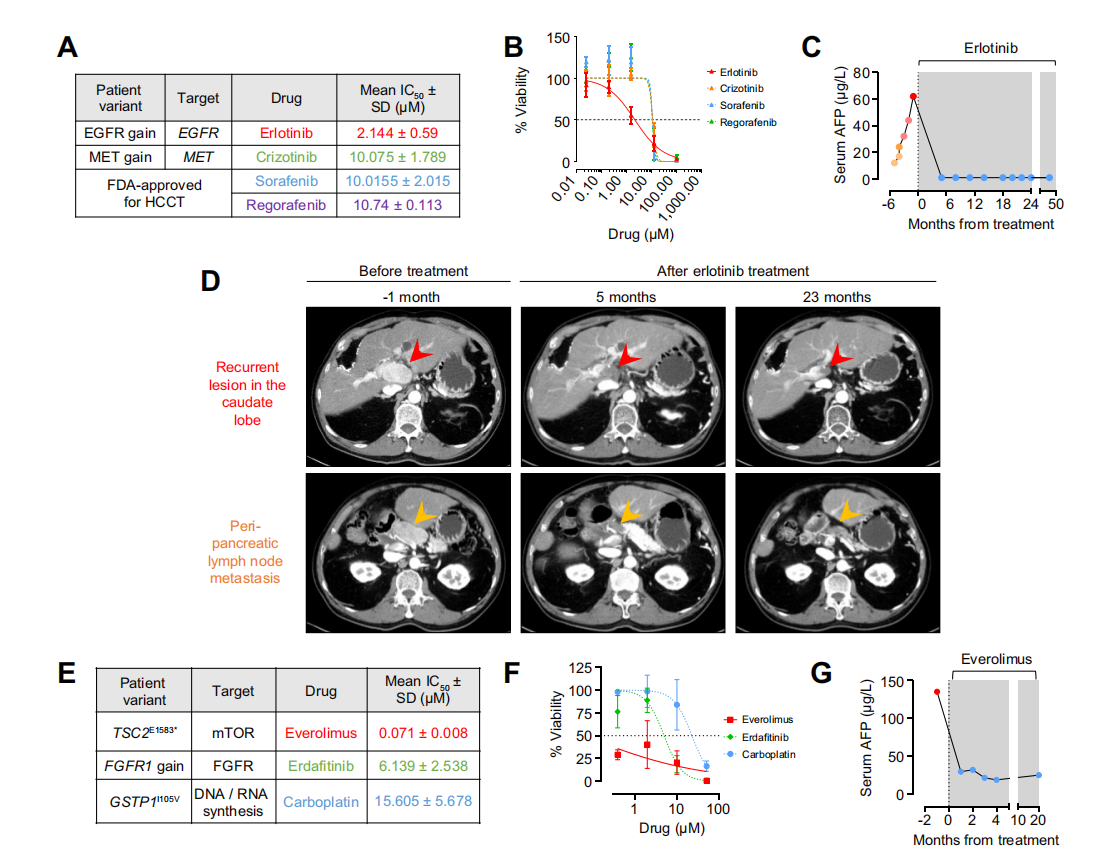
研究通过PDTO培养、下一代测序和基因组引导的药物测试,为两名晚期HCC患者创建个性化治疗方案。
第一位患者,70岁男性,术后复发,接受多种治疗失败后,基于PDTO药物测试结果,开始每日服用厄洛替尼。治疗后5个月,CT扫描显示无存活肿瘤,治疗效果持续48个月,血清AFP水平恢复正常,胰周淋巴结受累程度显著下降,至2024年1月患者仍处于临床完全缓解期。
第二位患者,61岁男性,晚期HCC伴肺转移,接受多种治疗失败后,基于PDTO药物测试结果,接受依维莫司治疗。5个月后血清AFP水平恢复正常,出现部分缓解,至2025年1月患者状况良好,病情稳定,AFP低于参考范围。
小结
本研究通过优化PDTO的培养方法,减少生长因子的使用,显著提高了培养的成功率和标准化程度,降低了成本,使其更适合临床应用。
此外,通过药理遗传学分析,研究揭示了CTNNB1突变与药物敏感性之间的关系,为HCC的精准治疗提供了新的靶点和策略。
这些发现不仅为肝癌的精准医疗带来了新希望,也为未来更多癌症的个性化治疗提供了重要的参考。
Wong AM, Huang H, Wong AM, Leung HHW, Cheung WWY, Lam YK, Ding X, Zhang L, Chu C, Liu Y, Chan CKW, Chan AWH, Ng KKC, Wang X, Chan SL, Wong N. Patient-derived organoids inform pharmacogenomic vulnerabilities in liver cancer. JHEP Rep. 2025 Apr 22;7(7):101426. doi: 10.1016/j.jhepr.2025.101426.
排版编辑:肿瘤资讯-AS











 苏公网安备32059002004080号
苏公网安备32059002004080号


