2025美国临床肿瘤学会胃肠道肿瘤研讨会(2025 ASCO GI)已于1月23日至25日在美国旧金山以线上结合线下的形式举行。在此次大会中公布了多项曲氟尿苷替匹嘧啶(TAS-102)治疗结直肠癌(CRC)的研究结果。TAS-102是一种已经获批用于mCRC治疗的新型口服化疗药物,在晚期mCRC的治疗中发挥了重要作用。为了更好地了解TAS-102的最新研究进展,【肿瘤资讯】特邀宁夏医科大学总医院肿瘤医院陈萍教授分享2025 ASCO GI的精彩内容,以期为临床医生提供更多治疗思路,最终提升结直肠癌患者的生存获益。
宁夏医科大学总医院肿瘤医院 副院长
肿瘤内二科主任 主任医师 教授 研究生导师
中国抗癌协会肿瘤整体评估专委会常委
中国抗癌协会第一届食管肿瘤整合康复专委会常委
中国抗癌协会中西整合神经内分泌肿瘤专委会常委
中国抗癌协会整合肿瘤肾脏病学专委会常委
中国抗癌协会肿瘤热疗专委会肿瘤热化疗灌注专家委员会常委
中国抗癌协会肝脏肿瘤整合康复专委会常委
中国研究型医院学会精准医学与肿瘤MDT专委会消化肿瘤临床研究学组副组长
宁夏抗癌协会临床肿瘤化疗专委会副主委
宁夏抗癌协会肿瘤胃肠病学专委会副主委
宁夏抗癌协会理事会理事
ALTAIR研究证实TAS-102显著改善CRC患者DFS,寡转移Ⅳ期患者获益尤为突出


摘要号:LBA22
英文标题:A randomized, double-blind, phase III study comparing trifluridine/tipiracil (FTD/TPI) versus placebo in patients with molecular residual disease following curative resection of colorectal cancer (CRC): The ALTAIR study.
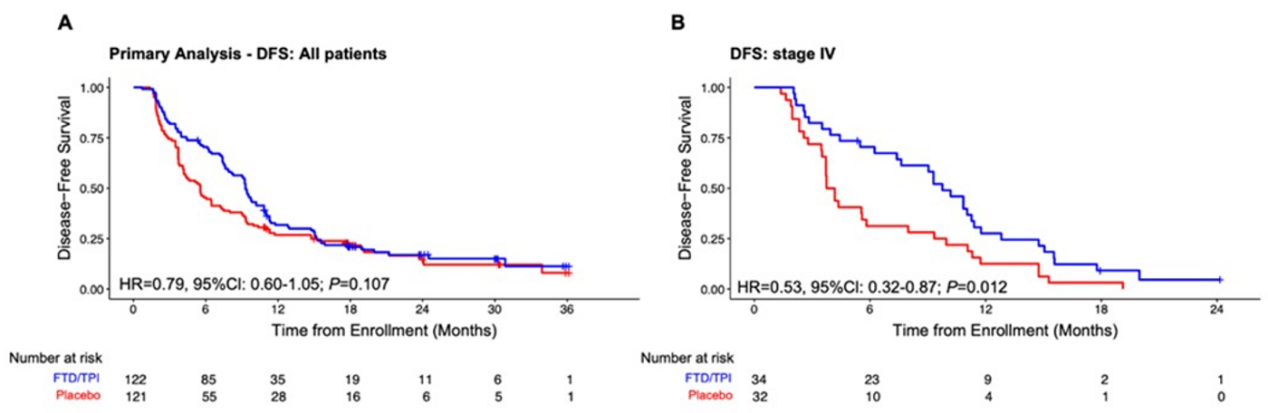
ALTAIR研究是一项随机、双盲的Ⅲ期研究,旨在评估TAS-102对比安慰剂在CRC根治性切除术后有分子残留病灶患者中的疗效。结果显示,TAS-102组与安慰剂组的中位无病生存期(DFS)分别为9.30个月 vs 5.55个月(HR 0.79;P=0.107)(图1 A)。TAS-102在切除的寡转移性Ⅳ期患者中获益非常显著,TAS-102组与安慰剂组的中位DFS分别为9.76个月 vs 3.96个月(HR 0.53;P=0.012)(图1 B)。TAS-102获益显著,平均肿瘤分子(MTM)/mL值越高,获益越显著,在入组时间点,随着MTM/mL值的增加,获益呈线性增加。总生存期(OS)数据仍不成熟。安全性方面,TAS-102可控可管理。
结果表明,TAS-102在切除寡转移性病灶的患者中显示出具有临床意义的DFS获益,并且随着MTM/mL值的增加,DFS获益呈增加趋势。
TAS-102联合贝伐珠单抗显著改善mCRC患者OS,死亡风险降低32%


摘要号:79
英文标题:Real-world clinical outcomes of patients (Pts) with metastatic colorectal cancer (mCRC) who received trifluridine-tipiracil (FTD-TPI) monotherapy or FTD-TPI + bevacizumab (FTD-TPI+bev) combination therapy
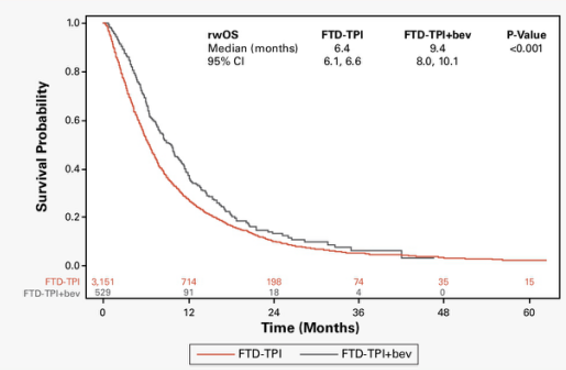
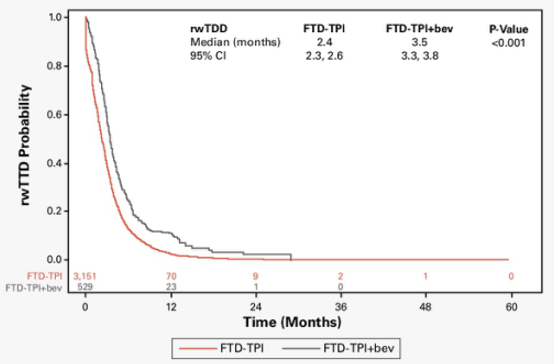
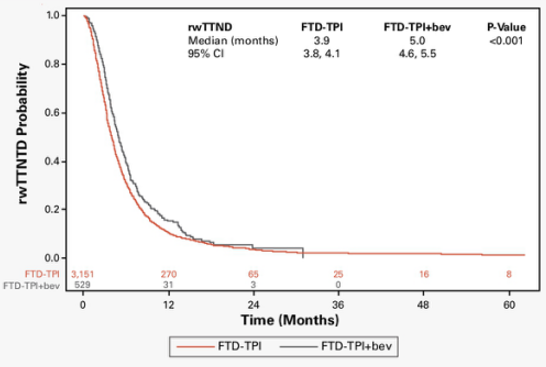
这项研究旨在探索TAS-102单药对比TAS-102+贝伐珠单抗联合方案作为mCRC患者三线治疗的真实临床结果。研究结果显示,TAS-102+贝伐珠单抗组相较于TAS-102单药组显著延长了真实世界OS(rwOS)(9.4个月 vs 6.4个月,P<0.001)(图2),并在调整模型中显著降低了死亡风险(HR 0.68;P<0.001)。在调整患者人口统计学和临床特征后,与TAS-102单药相比,TAS-02+贝伐珠单抗还显著延长了实际停药时间(rwTTD)(中位数:3.5个月 vs 2.4个月;P<0.001)(图3),并降低了停药风险(HR 0.65;P<0.001)。此外,在调整后的模型中,与TAS-102队列相比,TAS-102+贝伐珠单抗队列的至下一次治疗或死亡时间(rwTTNTD)显著更长(中位数:5.0个月 vs 3.9个月;P<0.001)(HR=0.73;p<0.001)(图4)。
研究结果表明,在真实环境中,与接受TAS-102治疗的mCRC患者相比,TAS-102+贝伐珠单抗联合治疗改善了包括rwOS、rwTTD和rwTTNTD在内的临床结果,这些发现与SUNLIGHT研究的结果一致。
TAS-102联合呋喹替尼用于mCRC三线治疗的中位OS达18.4个月且毒性可控,肝/腹膜转移患者疗效一致


摘要号:145
英文标题:Updated analysis of a phase 2 study of fruquintinib plus trifluridine/tipiracil (TAS-102) as third-line treatment in patients with metastatic colorectal adenocarcinoma
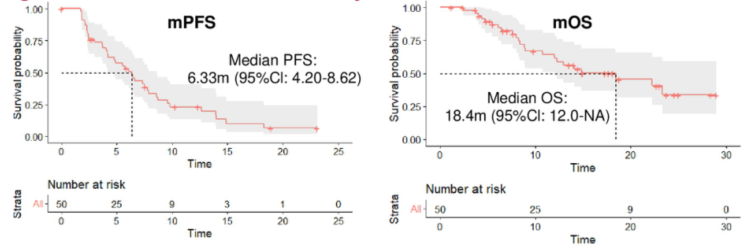
这项开放标签、单组、多中心、Ⅱ期研究旨在评估TAS-102联合呋喹替尼作为mCRC三线治疗的疗效和安全性。结果显示,截至2024年9月3日,客观缓解率(ORR)为10.9%,疾病控制率(DCR)为73.9%。中位无进展生存期(PFS)为6.33个月(图5)。6个月、9个月和12个月的PFS率分别为53.0%、28.3%和23.1%。中位随访时间为17.6个月,中位OS为18.4个月(图5)。6个月、9个月和12个月的OS率分别为87.0%、66.9%和64.3%。肝转移(LM)患者和非LM患者的中位PFS相当(6.33个月 vs 6.46个月,P=0.54)。腹膜转移(PM)患者和非PM患者的结果相似(6.07个月 vs 6.33个月,P=0.95)。RAS基因突变、既往治疗线数≥3、年龄≥65岁、转移部位≥2、PM和右侧转移均未被确定为与PFS或OS显著相关的因素(通过单变量Cox比例风险模型)。最常见的任何级别和≥3级治疗相关不良事件(TRAE)主要为血液学毒性,未观察到与治疗相关的死亡。
研究结果表明,TAS-102联合呋喹替尼作为mCRC患者的三线治疗方案具有令人鼓舞的生存优势,且毒性可接受。该方案可作为此类患者的替代治疗方法。
TAS-102+贝伐珠单抗联合方案在MSI-H/dMMR型mCRC中展现显著OS获益


摘要号:152
英文标题:A retrospective observational study to evaluate the efficacy of trifluridine/tipiracil ± bevacizumab in metastatic colorectal cancer with MSI-high/deficient MMR
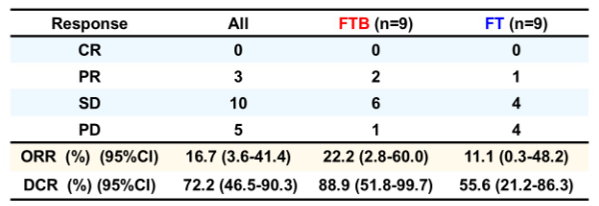
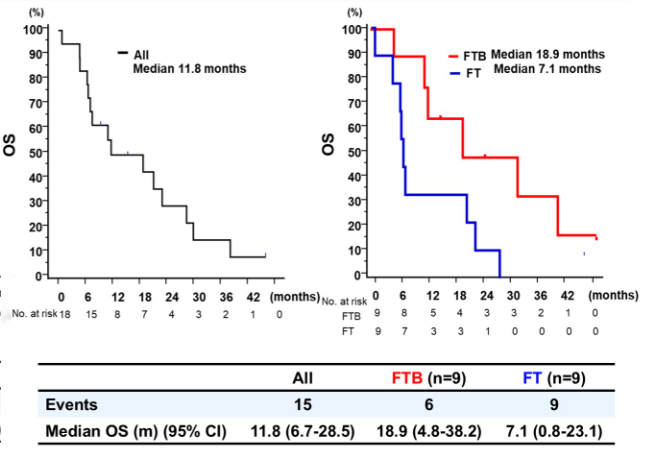
这项回顾性研究旨在评估TAS-102±贝伐珠单抗对MSI-H/dMMR型mCRC二线及以上治疗的疗效。研究结果显示,全人群ORR为16.7%、DCR为72.2%;中位PFS为5.5个月,中位OS为11.8个月。TAS-102+贝伐珠单抗组的ORR、DCR均优于TAS-102组(ORR:22.2% vs 11.1%;DCR:88.9% vs 55.6%)(图6),而两组的中位PFS相似(5.6个月 vs 5.2个月)。TAS-102+贝伐珠单抗组的OS长于TAS-102组(中位OS,18.9个月 vs 7.1个月;HR 0.22;P=0.03)(图7)。安全性方面,各组中最常见的≥3级不良事件是中性粒细胞减少症、贫血。
研究结果表明,TAS-102±贝伐珠单抗显示出良好的疗效和良好的安全性。虽然这是一项样本量较小的回顾性研究,但TAS-102±贝伐珠单抗疗法对MSI-H/dMMR型mCRC的疗效可能优于先前前瞻性研究中对MSS/pMMR型mCRC的疗效。
TAS-102联合伊立替康及贝伐珠单抗二线治疗mCRC实现1年OS率92%且毒性可控


摘要号:155
英文标题:Phase II study of trifluridine/tipiracil (TAS-102) plus irinotecan in combination with bevacizumab as a second‐line therapy for patients with metastatic colorectal cancer
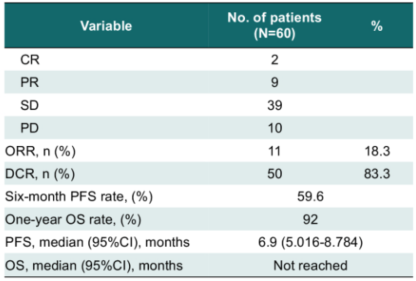
这项多中心、单组Ⅱ期研究旨在评估TAS-102、伊立替康和贝伐珠单抗联合方案在mCRC患者二线治疗中的安全性和有效性。研究结果显示,截至2024年8月31日,所有60例患者均评估了疗效,ORR为18.3%[2例完全缓解(CR),9例部分缓解(PR),39例病情稳定(SD)]。39例SD患者中,29例肿瘤缩小。DCR为83.3%。中位随访时间为8.6个月。6个月PFS率为59.6%。中位PFS为6.9个月,中位OS未达到(图8)。1年OS率为92%。所有患者均可进行安全性评估。最常见的TRAE是恶心(100%)、中性粒细胞减少症(86.7%)和贫血(83.3%)。未发生治疗相关死亡。
研究结果表明,TAS-102、伊立替康和贝伐珠单抗方案作为二线治疗,初步证明对mCRC患者具有良好疗效且毒性可耐受。该方案值得在难治性mCRC患者中进一步探索。
mCRC三线治疗新策略:TAS-102联合呋喹替尼间歇给药的探索性研究


摘要号:174
英文标题:Exploratory study of TAS-102 combined with intermittent administration of fruquintinib in the treatment of third-line metastatic colorectal cancer
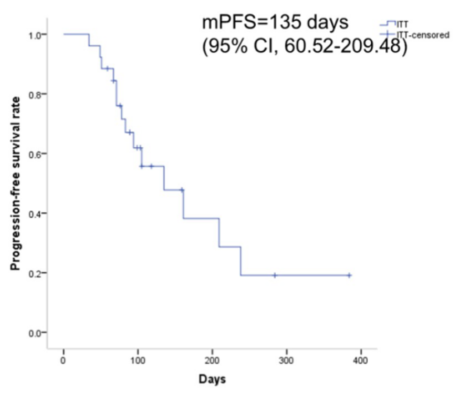
这项开放标签、单组、单中心、探索性临床研究旨在评估TAS-102联合呋喹替尼间歇性给药作为mCRC患者三线治疗的疗效和安全性。研究结果显示,18.2%(4/22)的患者获得PR,50%(11/22)的患者最佳缓解为SD。中位PFS为135天(图9)。RAS突变型和RAS野生型患者的中位PFS分别为161天和135天,ORR分别为25%和12.5%。LM和非LM患者的中位PFS分别为135天和161天,ORR分别为14.3%和25%。多发转移患者的中位PFS为135天,ORR为17.6%。中位OS尚未成熟。TRAE总体上可控且可耐受,未观察到与治疗相关的死亡。
研究结果表明,间歇性使用TAS-102与呋喹替尼联合方案作为mCRC患者的三线治疗,可降低血液学毒性,耐受性良好,临床效果令人鼓舞。
TAS-102+贝伐珠单抗治疗mCRC真实世界研究:有效性和安全性良好


摘要号:204
英文标题:Efficacy and safety of trifluridine/tipiracil and bevacizumab (FTD/TPI+BEV) in patients with metastatic colorectal cancer (mCRC) in real-world practice.
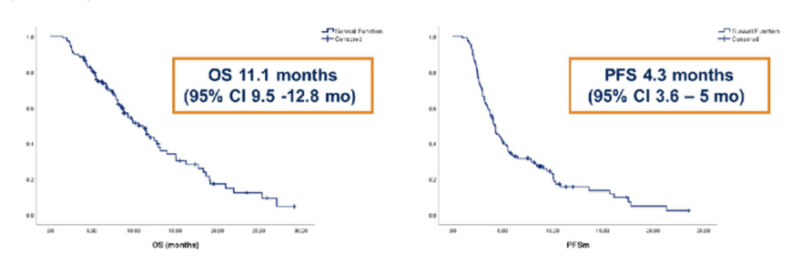
这项回顾性、观察性、多中心研究旨在评估TAS-102+贝伐珠单抗联合治疗mCRC在真实世界中的有效性和安全性。研究结果显示,ORR为4.6%,DCR为50%。中位PFS为4.9个月,中位OS为11.1个月(图10)。最常见的3~4级毒性包括中性粒细胞减少症(41.8%)、乏力(7.2%)和肝毒性(5.5%)。未报告与治疗相关的死亡。
研究结果表明,TAS-02+贝伐珠单抗联合方案治疗mCRC在常规临床实践中具有良好的有效性和安全性,即使在预后不良和有大量既往治疗史的人群中也是如此。
AREG可作为TAS-102治疗mCRC预后指标,TAS-102联合贝伐珠单抗显著延长OS至14.4个月


摘要号:230
英文标题:Preclinical analysis and clinical validation to identify biomarkers for trifluridine/tipiracil (FTD/TPI) efficacy with or without bevacizumab in patients with metastatic colorectal cancer
这项研究旨在评估了候选的生物标志物在mCRC患者接受TAS-102+贝伐珠单抗或单独使用TAS-102的中的临床意义。研究结果显示,与TAS-02组相比,TAS-102+贝伐珠单抗组的中位OS明显更长(14.4个月 vs 6.2 个月,HR 0.53)且DCR更高(58.8% vs 34.4%,P=0.047)。在单变量分析中,第2次IL-8或AREG升高和疾病进展(PD)时IFI16升高与较差的临床结果相关。≥3级中性粒细胞减少症(NEU)与两个组的更好生存率相关。多变量分析发现AREG降低和≥3级NEU是PFS和OS的更好标志。当IL-8在第2次升高时,TAS-102+贝伐珠单抗组的OS显著长于TAS-102组(12.8个月 vs 5.8 个月,HR 0.43)。当EREG(12.8个月 vs 6.2 个月,HR 0.27)或AREG(14.2个月 vs 9.7 个月,HR 0.40)在第2次降低时,A组的OS也长于B组。该方案和生物标志物(IL-8、EREG 和 AREG)对OS没有显著的相互作用。
研究结果表明,AREG可作为TAS-02疗效的预后指标。IL-8、EREG和AREG的变化可能有助于延长TAS-02+贝伐珠单抗联合治疗的生存期。
总结
2025年ASCO GI会议上公布了关于CRC治疗药物TAS-102的多项研究结果,通过以上研究,TAS-102在CRC治疗中的应用前景得到了进一步证实,尤其是在特定患者群体中显示出显著的生存获益。同时,TAS-102与贝伐珠单抗的联合使用在真实世界中也显示出较好的疗效和安全性。这些研究为CRC的治疗提供了新的思路和方法。
排版编辑:肿瘤资讯-jyy
版权声明











 苏公网安备32059002004080号
苏公网安备32059002004080号


