国家癌症中心/中国医学科学院肿瘤医院放射治疗科 医师
北京协和医学院肿瘤学博士
主要从事胸部肿瘤放疗与生物标志物临床转化研究;
目前以第一作者(含并列)身份在Mol Cancer、Signal Transduct Target Ther、J Hematol Oncol、Int J Surg、Clin Transl Med等国际知名学术期刊发表SCI论文10余篇,累计总影响因子超过180分;
获批授权发明专利10余项;
主持国家自然科学基金青年项目、中国医学科学院肿瘤医院合作基金,作为课题骨干参与多项国家级、省部级课题研究;
北京慢性病防治与健康教育研究会 会员
GCOG抗癌协作组青年委员会 会员
荣获博士研究生国家奖学金,北京协和医学院校长奖,北京市优秀毕业生、北京协和医学院优秀毕业生等称号;
ASCO解读文献
Abstract 8012
The preliminary results of a randomized phase II trial evaluating induction toripalimab plus chemotherapy followed by concurrent chemoradiotherapy and consolidation toripalimab in bulky unresectable stage III non-small-cell lung cancer (InTRist / GCOG0074)
一项评估特瑞普利单抗联合诱导化疗,随后同步放化疗及特瑞普利单抗巩固治疗用于巨大不可切除的Ⅲ期非小细胞肺癌的随机II期试验的初步结果
研究解读
肺癌在中国肿瘤谱中高居首位,非小细胞肺癌(NSCLC)约占肺癌的80%–85%,其中近三分之一患者确诊时已为Ⅲ期/局部晚期[1]。Ⅲ期NSCLC具有高度异质性,既存在是否可手术切除的争议,也面临放疗耐药与潜在转移的双重风险,使治疗道路险峻难行[2]。尽管免疫检查点抑制剂(ICIs)已变革局部晚期NSCLC的治疗格局,但其疗效高度异质。尽管PACIFIC研究在不可切除的III期NSCLC领域确立了同步放化疗后巩固PD-L1抑制剂的新标准[3],但对于巨块病变而言,传统放化疗靶场过大、肿瘤缺氧、肺毒风险高等难题仍未解决。如何突破这一困局,使免疫疗法惠及“巨无霸”病灶,是亟待破解的时代命题。
岁月更迭,前路几何
长期以来,多学科团队对Ⅲ期NSCLC的探索从未止步。与Ⅳ期不同,Ⅲ期NSCLC是一种高度异质性疾病,尽管其总体预后较差(5年生存率约13–36%),但因无远处转移,仍具有根治性治疗的可能。部分ⅢA病灶通过外科及新辅助策略可望治愈,而较晚期或淋巴结广泛累及的ⅢB/C则可依赖根治性放化疗,通过积极的多学科联合治疗提高疗效[4, 5]。在过去的十余年里,随着化疗方案和放疗技术进展,一批潜在可切除的患者获得了手术机会;但生存获益有限。进入免疫时代后,靶向疗法和免疫疗法的出现正逐步重塑可切可不切的疆界,让更多Ⅲ期患者带来了新的治疗曙光。但同样也引发争鸣:究竟哪些患者能从免疫疗法中受益?传统的“放化疗后巩固免疫”路径是否进一步完善?尤其对于肿瘤负荷极高的巨块型患者,巨大靶区和肿瘤部位缺氧等因素,往往导致传统放疗的局部控制率下降,同时也提升了放射性肺炎等毒性风险[6]。在这样的挑战下,如何突破现有治疗瓶颈成为燃眉之急。
风雨渐歇,曙光初现
针对如此难题,研究者注意到,在可切除NSCLC的新辅助研究中,Ⅲ期患者从免疫治疗中获益尤为显著[6],提示将免疫治疗前置可能带来额外优势。CheckMate-816研究显示,免疫联合组显著提高病理完全缓解率(24.0% vs 2.2%,P<0.001),并延长事件无进展生存期(EFS,31.6 vs 20.8个月,HR=0.63),从根本上重塑了可切NSCLC围术期治疗模式;更值得注意的是,亚组分析中,ⅢA期患者的获益尤为显著,提示免疫治疗在“负荷较大”或局部进展期患者中可能具有更强的生物学效应[7]。同时,通过研究者前期的回顾性研究发现,给予巨块不可切除Ⅲ期患者2个疗程的诱导期PD-1抑制剂联合化疗,可显著缩小肿瘤体积,有利于后续放疗方案的设计[1, 6]。
基于此种理论和临床启示,InTRist研究(GCOG0074)应运而生,旨在探索将诱导期特瑞普利单抗联合化疗纳入不可切除、肿瘤体积巨大的III期NSCLC治疗序列的可行性和价值。
InTRist研究是一项国内首项面向巨块期III期NSCLC患者的随机、单中心、II期临床研究,纳入无EGFR/ALK突变的巨块型不可切除的III期NSCLC患者,巨块型定义为原发肿瘤最大径≥5cm或转移淋巴结最短径≥2cm。符合标准的患者,随机1∶1分配至特瑞普利单抗(每3周 240mg)联合铂类双药化疗诱导治疗组(特瑞普利单抗组)或单纯诱导化疗组(对照组),均进行2个周期治疗,随后接受根治性同步放化疗(cCRT)。所有在cCRT后无疾病进展或未发生≥3级肺炎的患者,接受特瑞普利单抗(每3周 240mg)巩固治疗,最长12个月,或因疾病进展或严重不良事件提前停药。主要研究终点是从随机分组至无进展生存期(PFS),次要终点包括总生存(OS)、客观缓解率(ORR)、疾病控制率(DCR)以及缓解持续时间(DoR)、缓解至出现时间(TTR)及不良事件发生率。InTRist研究是首例在大肿块Ⅲ期NSCLC中将诱导PD-1抑制剂与后续放化疗整合的随机Ⅱ期临床研究,通过将免疫治疗前置到放化疗之前这一“独辟蹊径”的策略,为研究免疫疗法与放疗的协同效应提供了前瞻性平台。
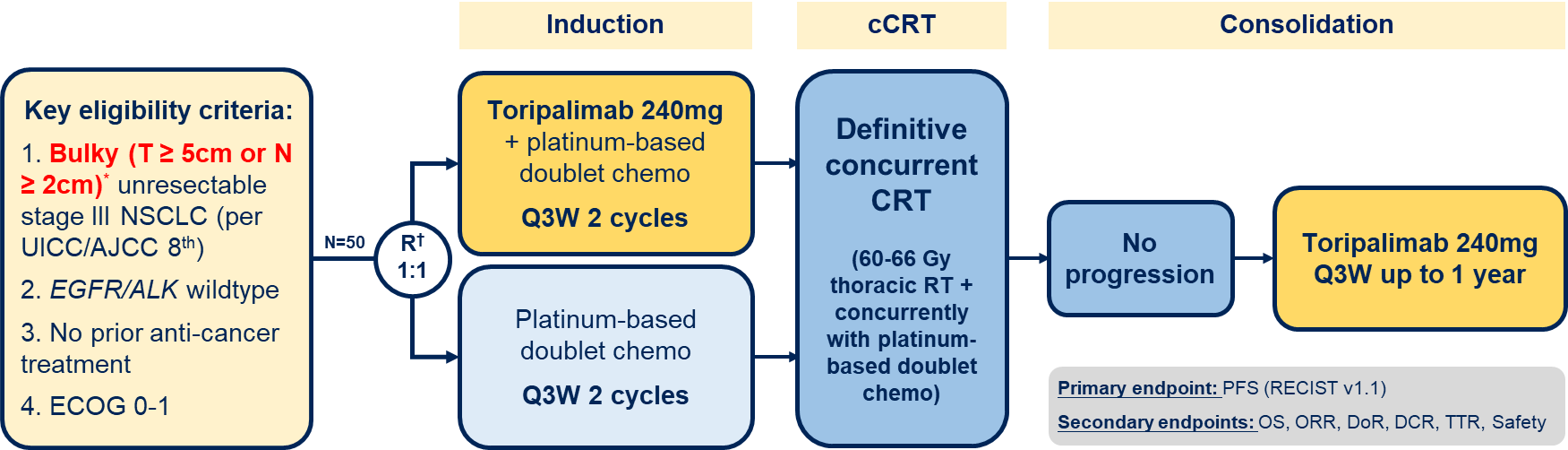 图1. 研究设计图
图1. 研究设计图山河可移,效益可期
InTRist的初步结果可谓春风化雨、硕果累累。研究在2023年1月20日至2024年10月8日期间,共计52例患者纳入分析。其中,特瑞普利单抗组n=27,对照组n=25。截至数据截止日期(2025年3月6日),中位随访时间为14.7个月。
诱导期加入特瑞普利单抗组的无进展生存明显优于对照组。具体而言,试验组患者尚未观察到中位PFS(置信区间未达),而对照组中位PFS为12.4个月。1年PFS率达85.6%对比对照组的54.5%,两者之间风险比(HR)为0.26(95% CI 0.08–0.81,P=0.012),意味着特瑞普利单抗诱导组使疾病进展或死亡风险下降了74%;ORR由对照组的40.0%跃升至77.8%,显示诱导免疫组在诱导后显著提高了肿瘤缩小。疾病控制率也维持在96% vs 92%。值得注意的是,诱导后肿瘤明显退缩的中位比例也显著增加,为32% vs 21%,为后续放疗创造了良好条件。综合来看,在目前数据成熟度下,联合免疫治疗组的疗效显著优于传统方案,验证了“放疗前先免疫”策略能够重新塑造治疗格局。
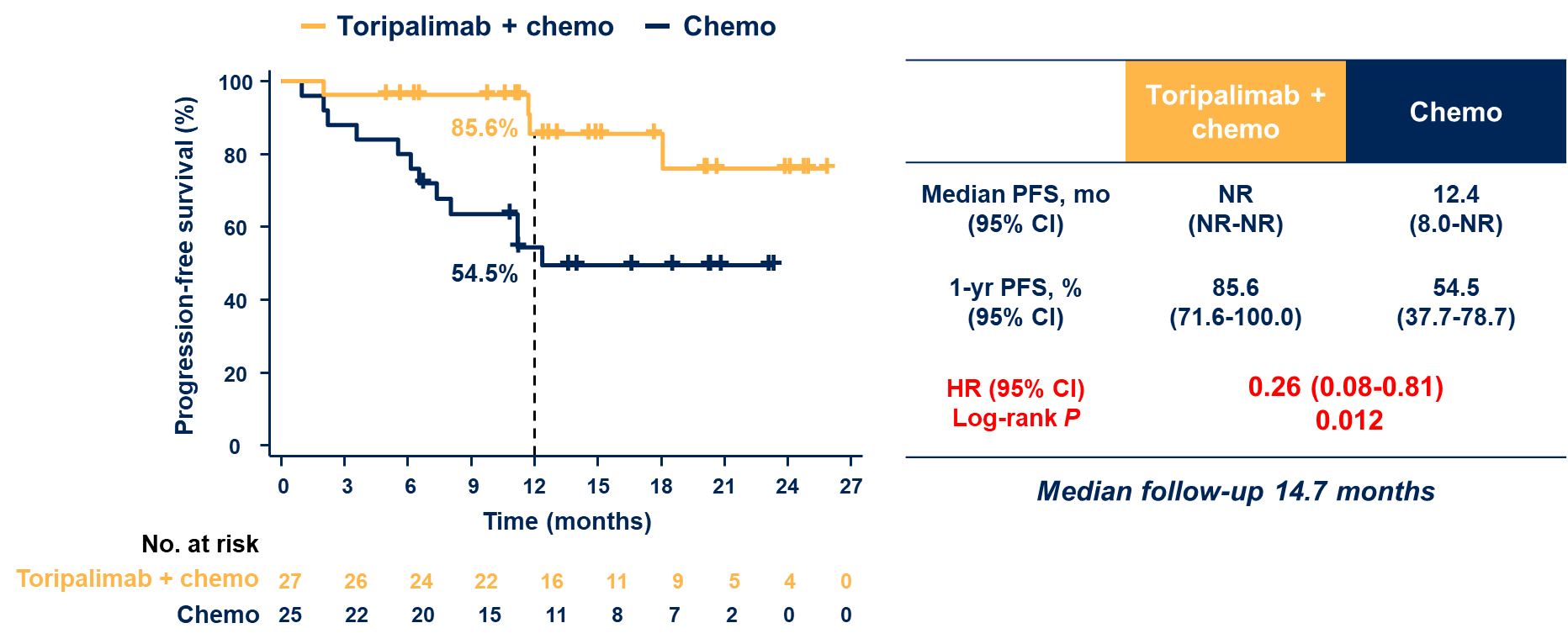 图2. 两组PFS
图2. 两组PFS 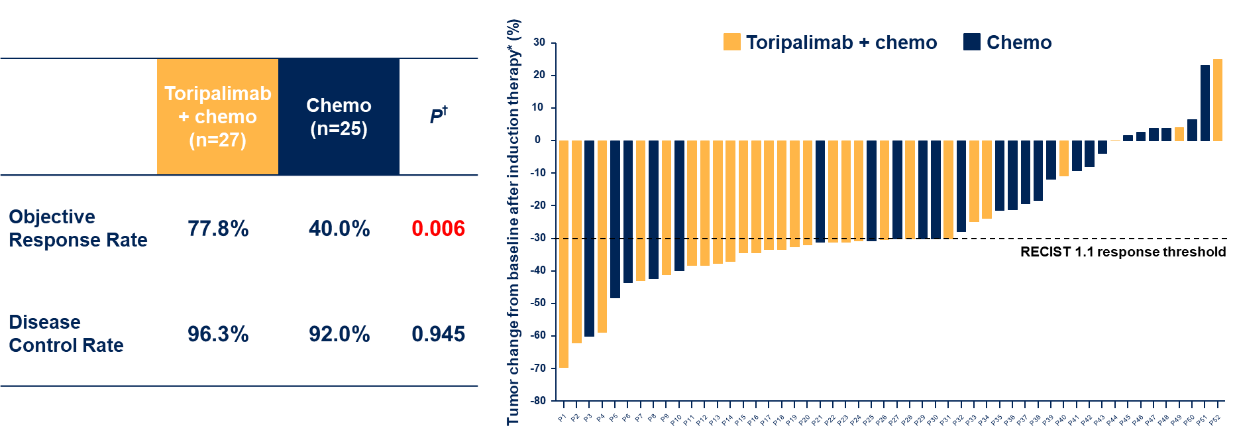 图3. 两组的肿瘤缓解表现
图3. 两组的肿瘤缓解表现微瑕不掩熊光
疗效提升的同时,安全性亦不容忽视。InTRist研究中,两组均未发生4–5级放射性肺炎,但1/2级放肺炎在试验组和对照组分别为37.0%和48.0%,3级肺炎分别为11.1%和4.0%。虽试验组轻中度肺炎发生率略高,但总体可控,无新增安全信号。免疫相关副作用以轻度甲状腺功能减退(7.4%)为主,偶见皮疹或肌炎等可处理的免疫反应。总体而言,毒性谱与既往研究相符,绝大多数患者能够耐受全程治疗。正如一句古语所言,“微光不掩风浪”——在疗效如潮的背后,我们仍需谨慎评估放疗协同免疫的肺毒和全身免疫负担,持续进行风险监控和优化治疗。
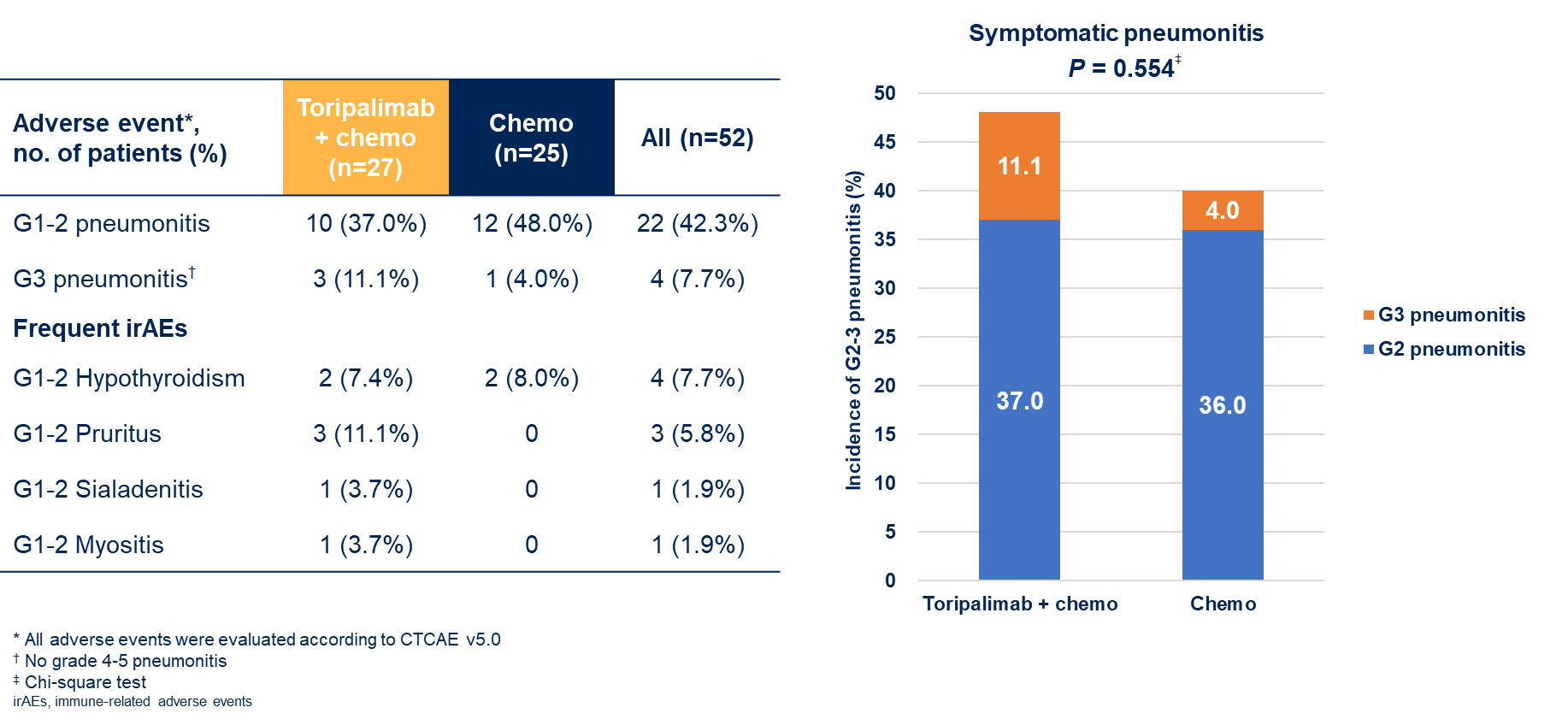 图4. 两组安全性
图4. 两组安全性综上,诱导加入特瑞普利单抗的组别在肿瘤缓解和PFS上均表现出显著优势,而毒性并未出现不可接受的急剧上升。这一结果表明诱导免疫疗法有潜力延长早期无进展期,为巨块期III期患者带来新的生存希望。
去留之间,唯精准不负
与既往研究强调“并发叠加”的免疫推进路径不同,InTRist研究另辟蹊径,选择了“诱导前移、时序解耦”的免疫联合化疗模式,试图在疗效与安全之间寻找更优解。PACIFIC-2试验(Concurrent Durvalumab+cCRT)和CheckMate-73L试验(Nivolumab+cCRT)均验证了与同步放疗同时给予ICIs并不能显著改善PFS或OS。PACIFIC-2显示并用Durvalumab组中位PFS仅略高于安慰剂组(13.8 vs 9.4个月,HR=0.85,P=NS),未达到统计学意义[8];CheckMate-73L也未见nivolumab组在PFS上战胜传统Durvalumab巩固组(16.7 vs 15.6个月,HR=0.95,P=0.646)[9],而三线治疗相关毒性反而增多。积累的经验表明,单纯在放化疗过程中叠加免疫并非出路。相较之下,InTRist选取了高危“巨块”亚群作为精准靶点,通过诱导疗法先打消肿瘤体积并激活免疫,为后续放化疗铺平道路。这种策略与基于肿瘤负荷的分层治疗思路不谋而合。进一步来看,晚期或Ⅲ期患者对新辅助免疫受益更大,提示临床需要进一步精准识别哪些患者真正需要“放疗前免疫”的新路径。
欲穷千里目,更上一层楼
InTRist研究的初步结果为Ⅲ期大体积NSCLC患者开启了新的希望之窗。初步数据显示,通过短期诱导免疫加化疗序贯传统CRT,患者的PFS和肿瘤缓解率均有显著提高,这一“以退为进“的治疗序列,可能为局部晚期肺癌患者提供一种打破治疗僵局的新路径。后续更多随访和更大样本的研究将进一步验证这一路径的长期获益。未来,伴随生物标志物和精准医学工具的不断成熟,研究者有望为每位Ⅲ期NSCLC患者找到“量身定制”的最佳方案。“登高望远”,只有不断迭代治疗策略,方能在变化的肿瘤战场上,一次次跨越新的制高点。
毕楠教授—中国医学科学院肿瘤医院
InTRist研究突破性地提出以巨块型肿瘤(原发肿瘤最大径≥5cm或转移淋巴结最短径≥2cm)为筛选标准,精准锁定潜在获益患者,彰显个体化免疫诱导治疗的新方向。基于坚实的回顾性数据支持,我们的研究首次验证了免疫联合化疗诱导治疗在III期NSCLC中显著改善无进展生存期(PFS)和肿瘤缓解率,同时未增加高危肺炎风险。InTRist不仅为复杂异质性III期NSCLC提供了更具针对性的治疗策略,也为免疫治疗安全性与疗效平衡开辟了新路径,具有重要临床指导价值。
1. Zhao, J., et al., A retrospective comparison of induction chemoimmunotherapy versus chemotherapy followed by concurrent chemoradiotherapy and consolidation immunotherapy in stage III non-small cell lung cancer. Front Oncol, 2024. 14: p. 1432954.
2. Riely, G.J., et al., Non-Small Cell Lung Cancer, Version 4.2024, NCCN Clinical Practice Guidelines in Oncology. J Natl Compr Canc Netw, 2024. 22(4): p. 249-274.
3. Spigel, D.R., et al., Five-Year Survival Outcomes From the PACIFIC Trial: Durvalumab After Chemoradiotherapy in Stage III Non-Small-Cell Lung Cancer. J Clin Oncol, 2022. 40(12): p. 1301-1311.
4. Evison, M., The current treatment landscape in the UK for stage III NSCLC. Br J Cancer, 2020. 123(Suppl 1): p. 3-9.
5. Petrella, F., et al., Stage III Non-Small-Cell Lung Cancer: An Overview of Treatment Options. Curr Oncol, 2023. 30(3): p. 3160-3175.
6. Wang, Y., et al., Induction PD-1 inhibitor toripalimab plus chemotherapy followed by concurrent chemoradiotherapy and consolidation toripalimab for bulky locally advanced non-small-cell lung cancer: protocol for a randomized phase II trial (InTRist study). Front Immunol, 2023. 14: p. 1341584.
7. Forde, P.M., et al., Neoadjuvant Nivolumab plus Chemotherapy in Resectable Lung Cancer. N Engl J Med, 2022. 386(21): p. 1973-1985.
8. Driessen, R.S., et al., Functional stress imaging to predict abnormal coronary fractional flow reserve: the PACIFIC 2 study. Eur Heart J, 2022. 43(33): p. 3118-3128.
9. De Ruysscher, D., et al., CheckMate 73L: A Phase 3 Study Comparing Nivolumab Plus Concurrent Chemoradiotherapy Followed by Nivolumab With or Without Ipilimumab Versus Concurrent Chemoradiotherapy Followed by Durvalumab for Previously Untreated, Locally Advanced Stage III Non-Small-Cell Lung Cancer. Clin Lung Cancer, 2022. 23(3): p. e264-e268.
【温馨提示】:如果您觉得张志慧医生解读的好,请在下方为她点赞并将文章分享给更多的同道!当然,您也可以在下方留下您的个人见解哦!











 苏公网安备32059002004080号
苏公网安备32059002004080号


