结直肠癌作为我国高发的恶性肿瘤之一,近年来其发病率明显上升。TAS-102作为一种新型口服化疗药物,用于治疗转移性结直肠癌,因其良好的疗效和安全性,在该领域的治疗中显示出广阔的应用潜力。本文通过分析三例病例,深入研究了TAS-102联合方案在晚期结直肠癌治疗中的临床效果,为晚期结直肠癌的治疗提供新的临床参考。
病例一
病例汇报:
张文慧教授 包头市肿瘤医院
病例点评:
高洪生教授 河北医科大学第四医院
李宁宁教授 北京协和医院
内蒙古抗癌协会淋巴瘤专业委员会委员
内蒙古抗癌协会胃癌专业委员会委员
内蒙古自治区医学会肿瘤内科学委员
内蒙古医师协会肿瘤内科学委员,CSCO会员
患者基本情况
一般资料:男性,68岁。
现病史:
患者于2017年7月无明显诱因出现血便,外院行肠镜检查后提示直肠腺癌。
既往史与家族史:无特殊。
诊疗经过
手术治疗
患者于2017年8月行“腹腔镜下腹会阴联合直肠癌根治术”。术后病理:直肠中分化腺癌,肿瘤大小3*2.5*1.2cm,累及肠外壁下层并侵犯齿状线,肠周淋巴结见癌转移(1/15)。
基因检测:MSS型,PD-L1(CPS>10),KRAS:野生型。
目前诊断:直肠中分化腺癌(MSS型,PD-L1 CPS>10,KRAS野生型)。
辅助治疗
患者术后予以xelox方案化疗1周期,后行局部放疗,放疗期间联合卡培他滨单药同步化疗两周期。放疗结束后,再次予以xelox方案化疗3周期。
2019年7月,复查胸部CT提示,左肺上叶出现大小约1.4*3.4cm的空洞型肿块,肝脏S4段见约1.7*1.8cm的异常强化结节(图1)。
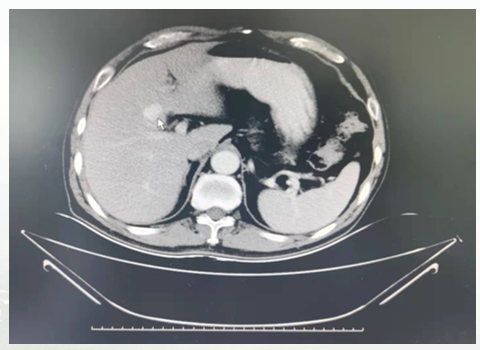
一线治疗
患者于2019年7月予以瑞戈非尼治疗。期间定期复查。
2020年12月10日复查:
实验室检查提示,总胆红素36.4umol/L,谷草转氨酶216U/L,谷丙转氨酶32U/L。
胸部CT提示,左肺上叶空洞型肿块较前增大,现约6.4*3.8cm,空洞壁不规则增厚较前增加,约1.5cm(图2)。
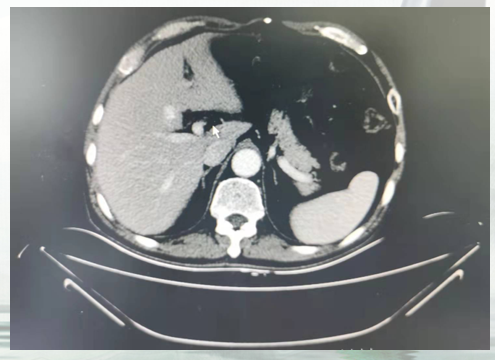
二线治疗
患者及家属拒绝穿刺活检及化疗,遂于2021年1月予以PD-1抑制剂+呋喹替尼治疗。
复查CT显示,左肺上叶空洞型肿块较前缩小,现约3.9*2.4cm,其内空洞较前增大,增强扫描后实性部分不均匀强化;肝脏结节大小相仿。
疗效评估为部分缓解(PR)。
2022年6月,患者因心前区疼痛就诊,诊断为急性心肌梗死,行冠状动脉药物球囊扩张术,抗肿瘤治疗暂停。
2022年9月7日,复查CT示左肺肿块再次增大至4.2*3.1cm。遂继续PD-抑制剂+呋喹替尼方案治疗至2024年6月12日。
2023年12月,因骨病变穿刺,病理结合免疫组化结果倾向于肠道来源的转移性腺癌。
2024年6月,复查CT示左肺肿块进一步增大至7.5*4.8cm,双肺结节增多、增大,腹膜后淋巴结亦增大。
三线治疗
患者于2024年6月12日予以TAS-102+呋喹替尼+地舒单抗。
2024年8月复查,疗效评估为疾病稳定(SD)+。
病例小结
该患者为一名68岁男性,直肠癌术后7年,经历多次复发转移。在多线治疗中,依次使用了瑞戈非尼、PD-1抑制剂联合呋喹替尼等方案,期间因急性心肌梗死而中断治疗。近期因骨转移及肺部病灶再次进展,应用TAS-102联合呋喹替尼及地舒单抗治疗。该病例充分体现了晚期直肠癌治疗的长期性、复杂性以及真实世界中个体化决策的重要性。
病例二
病例汇报:
李群教授 河南省肿瘤医院
病例点评:
李云峰教授 吉林大学第二医院
魏孝礼教授 哈尔滨医科大学附属肿瘤医院
医学博士
河南省预防医学会循证医学专业委员会委员
河南省抗癌协会食管癌专业青年委员会委员
河南省抗癌协会肿瘤化疗专业青年委员会委员
河南省抗癌协会胃肠肿瘤专业委员会委员
郑州市抗癌协会癌症康复与姑息治疗专业委员会
患者基本情况
一般资料:男性,34岁。
现病史:
2022年11月因腹胀、腹痛就诊。CT提示腹盆腔大量积液,腹水病理考虑腺癌。
辅助检查:
肿瘤标记物:CEA:8.14ng/ml,CA125:51.29U/ml,CA724:165.7U/ml。
2022年12月6日行腹部CT检查,提示结肠肝曲及横结肠管壁增厚,腹膜、肠系膜及大网膜多发转移(图3)。
肠镜见升结肠隆起性肿物阻塞肠腔。活检病理为结肠低分化腺癌,伴神经内分泌表达。免疫组化:CK20+,CK8/18+,SATB2+,CDX-2+,P53+,Ki-67 70%,SyN+,CgA-。基因检测:全RAS野生型,MSS型。
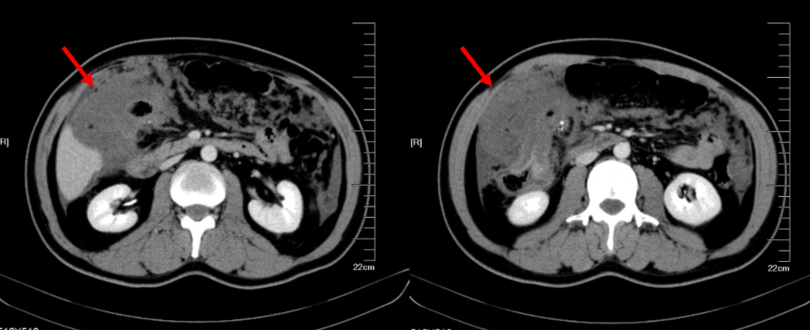
图3.腹部CT检查(2022年12月6日)
初步诊断:
右半结肠腺癌伴网膜转移(cT4N+M1 Ⅳ期),全RAS野生型 BRAF野生型 MSS型。
诊疗经过
一线治疗
患者于2022年12月予以FOLFOX+贝伐珠单抗治疗,并予“5-FU”腹腔灌注控制腹水。
1周期治疗后诉间断腹胀、腹痛,行平扫CT检查,提示结肠肝曲及横结肠管壁增厚,较前相仿,其旁少量积气,可疑穿孔,腹腔肠管内少许高密度对比剂;腹盆腹膜、肠系膜及大网膜多发软组织密度灶,转移可能。
患者于2023年1月5日在全麻下行“回肠造瘘加腹腔脓肿冲洗引流加肠粘连松解术”。
术中所见:腹腔广泛严重粘连,黄色浑浊液,约2000ml,大网膜、小肠及其系膜、盆腔可见大量黄色脓苔,无法探及肠壁瘘口,双侧膈肌、腹腔、盆腔、肠系膜、大网膜见大量转移灶,肿瘤位于右侧腹腔,与大网膜、肝脏关系密切,直径约18cm,质硬,活动度差。
术后予以mFOLFOX6+贝伐珠单抗方案治疗8周期,至2023年6月。
期间定期复查,影像学检查提示疗效评价为SD。
后续予以卡培他滨+贝伐珠单抗维持治疗3周期。
2023年8月,腹部CT检查提示结肠肝曲及横结肠管壁增厚,较前大致相仿;腹盆腔积液,较前增多;腹盆腔腹膜、肠系膜及大网膜转移,较前范围稍大腹水增多,腹膜转移范围增大。疗效评价为PD。
二线治疗
患者于2023年8月29日至2023年12月18日予以伊立替康+贝伐珠单抗方案治疗9周期,期间给予5-FU+雷替曲塞腹腔灌注治疗控制腹水。
期间定期复查,影像学检查提示结肠肝曲及横结肠管壁增厚,较前大致相仿,腹盆腔积液,较前减少。疗效评价为SD。
患者于2024年1月1日予以TAS-102+贝伐珠单抗(双周方案)维持治疗,治疗至今已21周期。期间定期复查,病情持续SD。无进展生存期(PFS)已超过15个月。
病例小结
该患者为一名年轻的右半结肠癌Ⅳ期患者,伴有大量腹水及腹膜转移,病理类型差,预后不佳。一线治疗期间出现肠穿孔,经手术干预后继续全身治疗。在一线治疗进展后,二线采用伊立替康联合贝伐珠单抗获得疾病稳定,并创新性地采用TAS-102联合贝伐珠单抗进行长期维持治疗,取得了超过15个月的PFS,且患者耐受性良好。
病例三
病例汇报:
胡志云教授 唐山市人民医院
病例点评:
王冬慧教授 运城市中心医院
张帅教授 天津市人民医院
唐山市医学会第一届肿瘤免疫学分会青年委员
河北省健康学会老年肿瘤防治管理分会委员
擅长肺癌、结直肠癌、胃癌、肝癌等实体肿瘤的放化疗,靶向及免疫等治疗
患者基本情况
一般资料:男性,69岁。
现病史:
2022年2月因便血,肠镜示直肠距肛缘7-11cm处可见隆起型病变,表面糜烂,覆鲜血及污苔,累及近全周,活检,质脆易出血。咬检病理示直肠中分化腺癌。
辅助检查:
实验室检查:CEA 0.51ng/ml、CA242 0.68IU/ml、CA724 0.56U/ml,血常规、肝肾功能等未见明显异常。
影像学检查:2022年3月15日行胸腹盆腔CT检查,示双肺散在多发小结节,直径均小于0.3cm,左下腹造瘘术后改变,吻合口无增厚。
初步诊断:
直肠中分化腺癌T3N1M0Ⅲ期。
诊疗经过
手术治疗
患者于2022年2月14日直肠癌根治术,术后病理示直肠溃疡型中分化腺癌,癌组织穿透肌层及浆膜下层,肿瘤体积4.8*3*0.8cm,无明确脉管内癌栓及神经侵犯,环周切缘未见癌。
术后辅助治疗
患者于2022年3月17日至8月16日,予以XELOX方案化疗6周期。期间于6月至7月行盆腔野放疗。
2023年12月12日复查胸部CT示双肺多发结节(图4),PET-CT提示为转移瘤。
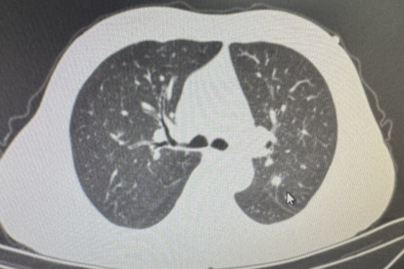
目前诊断:直肠癌术后复发 ypT3N1M1a(Ⅳ期),肺转移。
一线治疗
患者基因检测提示:KRAS、HRAS、NRAS和 BRAF 均为野生型。遂于2024年1月17日予以XELOX+西妥昔单抗,但因奥沙利铂过敏性休克,调整为mXELIRI+西妥昔单抗方案,共治疗6周期,疗效评价为SD。
后续予以卡培他滨+西妥昔单抗维持治疗6周期,至2024年12月18日,病情持续SD。
2025年1月22日复查CT提示双肺结节较前增大,肿瘤标志物CA72-4升高,疾病进展。
二线治疗
患者于2025年1月22日予以TAS-102+贝伐珠单抗方案治疗。
治疗期间定期复查至2025年6月,影像学检查显示病情持续SD。
病例小结
该患者为一名69岁男性,直肠癌术后接受标准辅助治疗后,出现肺部复发转移。一线采用西妥昔单抗联合化疗(因过敏调整为mXELIRI)及后续维持治疗。进展后,二线选择TAS-102联合贝伐珠单抗治疗,目前疾病稳定。该病例展示了对于RAS/BRAF野生型患者,从抗EGFR到抗VEGF药物的跨线治疗策略,以及TAS-102联合方案在后线治疗中的重要价值。
总结
晚期结直肠癌的治疗充满挑战,尤其是面对多线治疗后的患者。综合上述病例可以看出,在真实世界的临床实践中,个体化治疗策略尤为重要。对于不同患者,需结合其病理类型、基因状态、身体状况及个人意愿制定方案。例如,病例一中的老年男性患者,因依从性问题未遵循标准治疗路径,但通过多线联合用药仍实现了较长时间的疾病控制;病例二中的年轻患者则在伴有腹膜转移的情况下,通过创新性地采用TAS-102联合贝伐珠单抗方案,取得了超过15个月的PFS;而病例三展示了从抗EGFR到抗VEGF药物的跨线治疗思路,以及TAS-102联合方案在后线治疗中的显著价值。这些病例不仅体现了晚期结直肠癌治疗的复杂性,也反映了精准医学和多学科协作的重要性。未来,随着更多临床研究的开展,TAS-102在晚期结直肠癌治疗中的地位和应用前景将更加广阔,有望为更多患者带来生存希望和生活质量的改善。
排版编辑:肿瘤资讯-jyy











 苏公网安备32059002004080号
苏公网安备32059002004080号


