乳腺癌是我国女性最常见的恶性肿瘤之一,严重威胁着女性生命健康。近年来,随着治疗方案的日趋成熟和新型药物的不断问世,乳腺癌5年生存率逐年升高。然而在乳腺癌的治疗过程中,肿瘤治疗所致血小板减少症(CTIT)是导致抗肿瘤治疗减量、延迟或终止的常见不良反应之一,影响患者的生存和预后。因此,积极应对CTIT成为乳腺癌患者的重要管理手段之一。
本期特邀苏州大学附属第一医院周好医师、周思颖医师分享乳腺癌抗肿瘤治疗期间经历CTIT的诊疗经过,苏州大学附属第一医院过兆基教授就患者抗CTIT过程予以精彩点评,探索CTIT治疗新思路。
病例分享者简介
2012年毕业于上海交通大学附属瑞金医院
现就职苏州大学附属第一医院(甲乳外科)
从事甲状腺、乳腺疾病的相关手术治疗
曾在天津市肿瘤医院进修乳房再造相关技术
系苏州市抗癌协会第一届乳腺癌专业委员会青年委员
工作至今,主持并完成苏州市课题项目1项
参与并完成国家自然科学基金项目2项
以第一作者等发表SCI论文及核心论文数十篇
苏州大学附属第一医院甲乳外科
近年来以第一作者及通讯作者身份发表SCI论文13篇,第一作者身份发表Medline论文1篇,中文核心2篇。
主持江苏省自然科学基金1项。
病例介绍
病历资料:
基本情况:女,44岁
我院初次就诊日期:2021年2月18日
主诉:发现左乳肿物六月余。
现病史:患者六月前发现左乳肿物,肿瘤固定,局部皮肤呈橘皮样改变。近期自觉肿物增大,行乳腺超声示左乳结节性病灶,大小约34×8mm,4C类。
专科查体:左乳外下象限局部皮肤呈橘皮样改变,无红肿,无破溃,乳头稍凹陷,无溢血,局部可及范围约5cm*4cm肿块,质硬,表面欠光滑,边界欠清楚,与胸壁固定,活动度差。左腋下未及明显肿大淋巴结。右乳及腋下未及明显异常。
辅助检查:
乳腺超声:左侧乳腺占位性病灶,拟US-BI-RADS 4C类,建议穿刺活检。右侧乳腺未见明显肿块,拟US-BI-RADS 1类。双侧腋下未见明显肿大淋巴结。
颈部及锁骨上淋巴结超声:未见肿大淋巴结。
乳腺MRI:左乳中央区非肿块样强化伴左侧乳头内陷及皮肤增厚,考虑恶性可能性大,BI-RADS 4C;双侧腋下数枚小淋巴结。
左乳肿物穿刺:浸润性导管癌II级。免疫组化:癌细胞E-cadherin(+),Ki-67(+10%),ER(40%,2+),PR(10%,1+),Her2(3+),建议FISH检测,AR(+40%,2+),P53(+60%),CK5/6(-),Calponin(-)。
PET-CT:左乳腺癌确诊后:左乳腺体弥漫性葡萄糖代谢增高,左乳皮肤稍增厚伴葡萄糖代谢增高,结合病理考虑乳腺癌。右乳放射性分布欠均。左腋窝多发小淋巴结,未见明显葡萄糖代谢增高。胰尾脾门部软组织密度灶伴环形钙化。
临床诊断:左乳癌(T4N0M0,IIIB期,HER2阳性(HR+)型)。
诊疗经过:
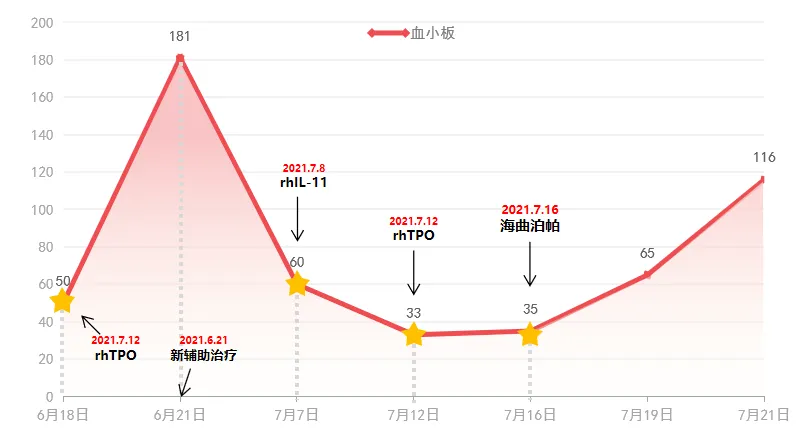
患者确诊为乳腺癌IIIB期,肿块较大且HER-2阳性,为降低期别、争取手术机会,改善预后,根据指南建议拟行新辅助化疗6周期联合靶向治疗,方案为多西他赛120 mg+卡铂0.6 g +曲妥珠单抗首剂490 mg、维持370 mg +吡咯替尼400 mg(TCbH+Py)。前5周期患者耐受良好,治疗如期进行。在第6周期化疗前,患者血小板降低至50×109/L,发生II度骨髓抑制,考虑诊断为CTIT,予重组人血小板生成素注射液15000 U,皮下注射,4天,复查血小板升至181×109/L,遂行第6周期化疗。

结束新辅助化疗联合靶向治疗后,患者复查结果显示病灶缩小,已具备手术指征,但术前检查发现血小板再次下降至60×109/L,首先予注射用重组人白介素-11 1.5 mg,皮下注射,5天,血小板不升反降,低至33×109/L;更换rhTPO使用5天后复查血小板35×109/L,无明显升高。为尽早手术,再次为患者更改升板方案,予海曲泊帕 5 mg/d口服6天,复查血小板116×109/L。两天后,患者行左乳癌改良根治术,手术顺利。因术前穿刺结果提示激素受体ER、PR以及HER2均为阳性,术后患者将继续靶向治疗联合内分泌治疗,预防术后复发。
诊疗思考
世界卫生组织国际癌症研究机构(IARC)发布数据显示,乳腺癌已成为全球患病率最高的癌症[1]。目前,乳腺癌的治疗手段众多,临床医生需全面评估患者情况,制定个体化治疗方案,并全程密切检测治疗相关不良反应,方可使患者获益最大化。
本例患者完成肿瘤相关评估,结合检查结果及病理诊断为左乳腺癌,T4N0M0 IIIB期,HER2(+),根据《CSCO乳腺癌诊疗指南(2021年版)》[2]给予新辅助治疗后行手术治疗,方可为患者带来最大获益。PHEDRA研究显示,吡咯替尼联合曲妥珠单抗和多西他赛用于乳腺癌新辅助治疗的tpCR率为41%,可为HER2阳性乳腺癌患者带来获益[3]。
综合考量,给予患者6周期新辅助化疗联合靶向治疗TCbH+Py方案(多西他赛120 mg+卡铂0.6 g+曲妥珠单抗490 mg+吡咯替尼400 mg qd)。前5周期患者治疗顺利,在第6周期化疗前出现CTIT,根据《肿瘤化疗所致血小板减少症诊疗中国专家共识(2018版)》[4]推荐首选rhTPO或rhIL-11治疗。本例首先选择rhTPO升板,患者反应良好,血小板4天后恢复正常,保证了第六周期化疗顺利进行。
新辅助治疗结束后,待患者血常规、肝肾功能、心功能等重要指标恢复正常,应尽早手术。既往研究表明[5],新辅助治疗结束后21天内接受手术患者获益最大。本例患者术前检查时再次出现血小板减少,为确保手术顺利完成,先后使用rhIL-11和rhTPO均效果欠佳,更换为口服促血小板生成素受体激动剂(TPO-RA)海曲泊帕。患者接受海曲泊帕5mg qd口服治疗后,不仅快速有效地提升血小板、降低了出血风险,且保障手术及时进行,确保患者获益最大化。
无独有偶,在本科室就诊的另一乳腺癌患者(pT2N0M0;ⅡA期;HER2阳性且HR阳性),抗肿瘤治疗方案为乳腺癌术后辅助化疗(化疗方案:盐酸多柔比星脂质体50mg+环磷酰胺0.9g, ivgtt d1;Q3W×4周期),在第3次化疗结束后出现骨髓抑制,血小板计数低至42*109/L。综合考量下,给予海曲泊帕7.5mg qd口服治疗,9天后复查血常规提示血小板计数 105*109/L,达到治疗预期,患者得以顺利进行第4周期的化疗方案。
海曲泊帕是恒瑞自主研发的1类新药,作为中国首个自主研发的口服非肽类小分子促血小板生成素受体激动剂(TPO-RA),海曲泊帕具有更好的疗效和更优的安全性,多中心随机双盲对照Ⅱ期临床研究[6]结果显示,与安慰剂相比,海曲泊帕(起始剂量7.5mg/d)可显著提升实体瘤患者的治疗有效率(60.7% vs 12.9%;OR:10.4)。在本病例中也成功展示了其治疗CTIT的疗效,尤其在传统药物如rhTPO和rhIL-11疗效不佳的情况下,给CTIT治疗提供了新的诊疗思路和方法。
病例点评专家简介
苏州大学附属第一医院甲乳外科
苏州市抗癌协会乳腺癌专业委员会主任委员
江苏省妇幼保健协会乳腺疾病分会苏南乳腺疾病协作组第一届委员会组长
上海市科学技术普及志愿者协会健康科普分会乳腺健康管理与科普专委会苏南分会顾问
江苏省社会办医疗协会甲状腺乳腺专委会常委兼秘书长
江苏省医师协会外科医师分会第三届委员会乳腺外科学组委员
江苏省中西医结合学会乳腺分会委员
苏州市生物治疗学会副秘书长
病例点评
Q1:肿瘤治疗所致的血小板减少症是临床上常见的不良反应,请您谈一谈血小板减少症会给肿瘤患者带来哪些危害?
过兆基教授:CTIT是肿瘤治疗常见的血液学毒性之一,它的出现会给抗肿瘤治疗带来多种影响,如抗肿瘤治疗延迟或剂量降低。一项回顾性研究[7]分析了609例实体瘤或淋巴瘤患者共计1262个化疗周期,其中因血小板减少导致的化疗延迟以及化疗剂量减少所占比例分别达8%和17%。化疗方案的剂量以及疗程是疗效的重要保障,因此,CTIT影响着患者治疗的正常进行,降低抗肿瘤疗效,延长患者住院时间,对患者预后产生严重不良影响。
与此同时,血小板减少是颅内出血的关键因素,严重血小板减少还会导致患者颅内出血并增加死亡风险。相关研究显示[7],PLT<20×109/L时,患者出血发生率翻倍,而当PLT<10×109/L时可能危及患者生命。由此可见CTIT的早期积极干预尤为重要。
除此之外,血小板减少还可能增加手术出血风险,并导致手术推迟。目前,乳腺癌新辅助治疗完成后的至手术时间(TTS)尚无明确推荐。但有研究表明[5],TTS是总生存和无复发生存的独立预后因素。新辅助治疗后TTS可能影响患者生存预后,新辅助治疗结束后的21天内接受手术的患者获益最大。因此,新辅助治疗结束后,在患者身体条件允许的情况下应尽早手术,从而最大限度提高治疗效果。
Q2:本例患者接受新辅助化疗联合靶向治疗后出现血小板减少,治疗后术前评估再次出现重度血小板减少,您认为其血小板减少症的原因是什么?乳腺癌新辅助治疗CTIT发生率如何?
过兆基教授:本例患者新辅助治疗方案为化疗联合靶向治疗,其中,化疗与靶向治疗均可能导致肿瘤患者血小板减少。不同抗肿瘤治疗手段导致血小板减少症的发生机制各不相同,作用于血小板生成、分布、凋亡和破坏等各个环节[8]。卡铂、吉西他滨、紫杉醇等常用化疗药物在杀伤肿瘤细胞的同时对造血干细胞和原始巨核细胞也无选择性地杀伤,抑制造血干细胞的增殖分化、巨核细胞的增殖成熟,破坏成熟的血小板,从而导致血小板减少[9]。靶向治疗药物引起的血小板减少症机制研究较少,已有研究表明,导致血小板减少症的机制因药物结构不同而不尽相同,包括免疫因素、骨髓抑制等[8]。
不同化疗方案引起血小板减少症的发生率存在差异,其中基于吉西他滨和铂类治疗方案的发生率最高[10]。相关研究显示,以铂类为基础的治疗方案3级和4级CTIT发生率为6.5%和4.1%[8],多西他赛3-4级CTIT发生率为1.9%。曲妥珠单抗单药治疗的血液学毒性并不常见,但在曲妥珠单抗联合化疗时,CTIT发生率显著上升。此外,随着化疗周期增加,血小板减少发生率逐步增加,严重程度也逐步增加。
对于HER2阳性的乳腺癌患者,常见新辅助治疗方案为TcbHP或THP。KRISINE研究显示,血小板减少是TCbHP方案(紫杉类+卡铂+曲妥珠单抗+帕妥珠单抗)治疗中常见≥3级不良反应,其发生率约为5%,而所有级别的血小板减少发生率则高达12%[11]。
Q3:本例患者在治疗CTIT时,先后使用rhTPO、rhIL-11及TPO-RA类药物,您如何评价本例患者升血小板的治疗过程?您认为新一代TPO-RA药物海曲泊帕在CTIT治疗中有哪些优势?
过兆基教授:本例患者诊断为乳腺癌患者,接受TCbH+Py方案新辅助治疗,方案为多西他赛120 mg+卡铂0.6 g+曲妥珠单抗490 mg+吡咯替尼400 mg qd。《CSCO乳腺癌诊疗指南(2021年版)》[2]强调,HER2阳性新辅助治疗应该完成预先计划的治疗周期,完整的新辅助治疗周期是提高手术pCR率的关键,可使患者获益最大化。
本例患者在第6周期化疗前出现CTIT,给予rhTPO升板治疗,患者反应良好,血小板迅速恢复正常。患者完成6周期新辅助治疗后,再次出现CTIT。因考虑经济因素,患者改为使用rhIL-11治疗,但疗效欠佳。另外,rhIL-11的不良反应发生率较高,在首次给药或多次给药后,均可能发生过敏或超敏反应,同时有水钠潴留、房性心律失常等不良反应[12]。随后患者转用rhTPO,rhTPO作为大分子药物,存在免疫原性,有内源性TPO抗体形成风险,且患者使用后再次出现疗效不佳的情况。
在先后使用rhIL-11和rhTPO治疗10天后,本例患者血小板计数仍处于较低水平(35×109/L ),对于需接受限期手术的乳腺癌患者而言,血小板减低面临极高出血风险,当血小板计数<50×109/L时,患者不能进行手术和侵袭性检查操作[8]。为尽早手术,争取最佳治疗效果,予患者海曲泊帕5mg qd口服治疗,患者血小板较前显著上升,保证手术及时、顺利且安全完成。
在本例中,海曲泊帕展示出了卓越的升板效果。作为新一代TPO-RA类药物,海曲泊帕可与TPO受体(TPO-R)的跨膜区结合,刺激TPO-R依赖的STATPI3K、ERK等信号通路,刺激巨核细胞增殖和分化,促进血小板生成,同时不影响内源性TPO与TPO受体胞外区的结合,具理论上具有协同效应。另外,海曲泊帕的小分子、非肽类化学结构也决定了其不具有肽类TPO⁃RA(如罗米司亭)的免疫原性。多项临床研究均显示出海曲泊帕在CTIT治疗中的巨大潜力。海曲泊帕多中心随机双盲对照Ⅱ期临床研究[6]结果显示,与安慰剂相比,海曲泊帕(起始剂量7.5mg/d)治疗CTIT有效率显著高于安慰剂组(60.7% vs 12.9%;OR:10.4),同时可更快恢复血小板至正常水平(7.5天 vs 13.0天)。
针对上一周期出现过CTIT患者,海曲泊帕预防用药也展示出了很好的潜力。在一项评估海曲泊帕一级预防CTIT的前瞻性研究[13]中,预防组患者在海曲泊帕治疗10天后均未出现血小板减少或血小板计数过高。在临床实践中,我们也发现,使用T-DM1或TCb方案的乳腺癌患者,如上一周期发生过CTIT,在下一治疗周期开始前5天使用海曲泊帕进行预防,能够很好的控制血小板计数,避免再次发生CTIT。
海曲泊帕口服用药,更为简便,方便进行院外管理且能提高患者的依从性。在临床实践中也表现出良好的安全性,日治疗费用可控,兼具有良好的经济性。
总体而言,应用新一代TPO-RA海曲泊帕治疗CTIT可保障抗肿瘤治疗的顺利进行,与传统药物rhTPO和rhIL-11相比,疗效更可靠,安全性更优,口服治疗更方便,且日治疗费用可控,性价比高。在CSCO《肿瘤治疗所致血小板减少症指南(2023)》中,海曲泊帕也作为唯一一个TPO-RA药物获治疗和预防Ⅱ级推荐,相信海曲泊帕未来能够为广大CTIT患者带来更多临床获益。
1. https://gco.iarc.fr/
2. 中国临床肿瘤学会指南工作委员会.中国临床肿瘤学会(CSCO)乳腺癌诊疗指南2021[M].北京:人民卫生出版社,2021.
3. 2021 SABCS. Abstract PD8-08.
4. 中国临床肿瘤学会肿瘤化疗所致血小板减少症共识专家委员会. 肿瘤化疗所致血小板减少症诊疗中国专家共识(2018版) [J] . 中华肿瘤杂志,2018,40 (9): 714-720.
5. Eur J Surg Oncol. 2017 Apr;43(4):613-618.
6. 2023 ECIM abstract 2360.
7. Elting LS, et al. J Clin Oncol. 2001 Feb 15;19(4):1137-46.
8. 中国临床肿瘤学会指南工作委员会.中国临床肿瘤学会(CSCO)肿瘤治疗所致血小板减少症指南2023[M].北京:人民卫生出版社,2023.
9. 欧阳锡林,等.化疗致血小板减少症的预防、治疗和出血风险评估研究进展[J].中国输血杂志,2010,23(04):319-321.
10. Semin Hematol,2009,46 (1 Suppl 2): S26-S32.
11.Sara A Hurvitz, et al. J Clin Oncol. 2019 Sep 1;37(25):2206-2216.
12. 注射用重组人白介素-11(1mg;1.5mg;3mg)产品说明书.批准日期2021年8月16日.
13. 2022 ESMO Asia poster 563.
排版编辑:肿瘤资讯-邓文普











 苏公网安备32059002004080号
苏公网安备32059002004080号


