
胃癌是全球范围内常见的恶性肿瘤之一,其发病率和死亡率均高居不下。SPOTLIGHT研究和GLOW研究一致地证实了Claudin18.2作为胃癌新兴靶向治疗靶标的潜力,其规范化检测也成为临床上备受关注的话题。
近日,病理学权威期刊Modern Pathology杂志发表一篇名为Claudin18.2 Immunohistochemical Evaluation in Gastric and Gastroesophageal Junction Adenocarcinomas to Direct Targeted Therapy: A Practical Approach[1]的文章,系统地介绍了Claudin18.2的表达、检测及相关经验。本期【肿瘤资讯】有幸邀请到中南大学湘雅二医院范松青教授详细解读这篇综述实践篇的内容,特整理成文,以飨读者。
本期特邀专家——范松青 教授
中南大学湘雅二医院病理科主任
医学博士 美国Emory大学博士后 一级主任医师 二级教授 博士生导师 博士后导师
湖南省高层次卫生人才“225”工程首批学科骨干人才
湖南省医师协会病理科医师分会会长
中国医师协会病理科医师分会常务委员
中国老年医学学会病理专业委员会常务委员
中国实验医学病理专家委员会常务委员
中国医学装备协会病理装备协分会常务委员/诊断部副部长
中华病理学会科研工作者委员委员
中华消化内镜学会病理协作组委员/中华消化病学会炎症性肠病学组病理俱乐部委员
湖南省抗癌协会病理专业委副主委/鼻咽癌标志专家委员会副主委
湖南省病理专业委员会副主委
湖南省病理质控中心副主任
湖南省病理生理学会肿瘤专业委员会副主委
湖南省健康管理学会病理专业委员会副会长
湖南省抗癌协会肺癌专业常委/皮肤病理专业
肿瘤精准治疗专业委员会委员
主持7项国家自然科学基金,发表SCI论文(第一和通讯作者)100多篇
全国病理学国际论文学术影响力百强(排名35专家)专家,培养毕业博士和硕士研究生共25人
Claudin18.2免疫组化染色评估的实践经验
1. 样本的管理及免疫组化染色
Claudin18.2检测应遵循免疫组化常规的福尔马林固定、石蜡包埋流程[2],厚度约4μm(3~5μm)的组织切片放于带正电的载玻片上,切片于干燥的室温(30±5℃)中保存。
由于组织切片的抗原稳定性可能会降低,建议从组织块上切片后立即进行检测。在未染色的组织切片上抗原的稳定性能至少保持45天,每个实验室应在各自环境中验证超45天稳定性,置于4°C冰箱中保存更佳。
在染色过程中需确保脱蜡完全,否则易出现非特异性染色或导致背景增强。
2. 阳性对照和阴性对照
在预测性生物标志物常规检测过程中,强烈建议常规采用阳性和阴性组织/细胞作为对照,这些对照应采用与检测样本相同的固定和包埋流程。
在检测Claudin18.2的实际操作中,待测样本上的非肿瘤性胃组织可作为内部阳性对照[3]:通常正常胃黏膜上皮细胞为强的膜染色、化生区域为弱到中度膜染色、固有层(淋巴细胞、巨噬细胞、平滑肌细胞、血管和周围神经等)为完全无染色。
3. 样本的选择是否影响Claudin18.2的检测结果?
手术样本和活检样本都可以用于Claudin18.2的检测,由于活检样本通常能够更及时和充分的固定,因此能获得理想的检测结果。
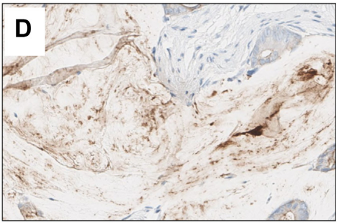
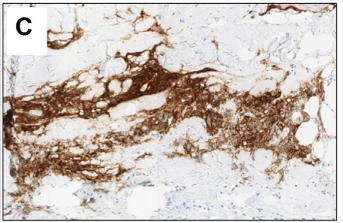
与CerbB-2的检测一样,Claudin18.2表达也呈现高度的瘤内异质性(图1),大型回顾性研究表明胃腺癌和胃食管结合部腺癌的Claudin18.2表达的瘤内异质性分别高达40%和33%[4]。因此Claudin18.2检测最好在充足数量的活检标本上进行,最理想的活检标本数量为6~8个。如有肿瘤样本不充足的情况,该患者所有可及样本都需进行染色,以更好地评估Claudin18.2的表达情况。

(A和B)两个呈现明显瘤内异质性的胃腺癌病例;其中Claudin18.2高表达区域与阴性区域共存;
(C和D)腺体内部Claudin18.2异质性的代表性病例
4. 原发灶和转移灶哪个更适合检测?
多项研究表明[4-5],Claudin18.2的表达在原发灶和同时性/匹配的淋巴结或远处转移灶间的一致性很高(>80%),二者均可用于Claudin18.2的检测。目前尚没有研究数据表明特定转移部位(如肝、腹膜)的Claudin18.2表达存在差异,以及Claudin18.2表达在肿瘤进展以及新辅助/辅助治疗过程中是否改变。由于恶性肿瘤细胞数量较少,评估来自转移灶的活检样本中Claudin18.2表达是有挑战性的(尤其腹膜转移样本)。为充分评估Claudin18.2的表达,至少需要50个活的肿瘤细胞,而更佳的定量评估阈值为100个活的肿瘤细胞[6]。
5. 组织学类型与Claudin18.2表达
有报道表明Claudin18.2在低粘附性癌/弥漫型胃癌中表达更高,在印戒细胞癌中相关性更明显[4,7]。一项纳入4507例样本的研究分析表明,低粘附性癌/弥漫型胃癌中Claudin18.2的阳性率为48.3%,高于肠型(38.8%)和混合型胃癌(42.9%)[8]。
评估低粘附性癌的Claudin18.2表达需要谨慎,因为表达阴性的肿瘤细胞容易被忽视,或被误认为炎症或基质细胞,进而影响最终的评分计算,建议匹配对应的HE染色切片来准确评估肿瘤细胞区域。
在评估混合型(肠型和弥漫型)胃癌时,应选择最具代表性的肿瘤进行Claudin18.2的检测,报告时需综合评估两种成分的表达情况。腺鳞癌是食管和胃食管交界处癌的少见类型,鳞癌成分通常不表达Claudin18.2。胃高分化神经内分泌肿瘤和肠嗜铬细胞样增生通常Claudin18.2中度至强的染色,因此在评估混有该成分胃癌时,应仅对腺癌成分评估。
6. Claudin18.2评估的潜在“陷阱”
细胞质或和染色:Claudin18.2评估的核心是仅肿瘤细胞上可见的、确切的线性膜染色才能被评估为阳性,细胞质或核染色不能记为阳性(图2)。
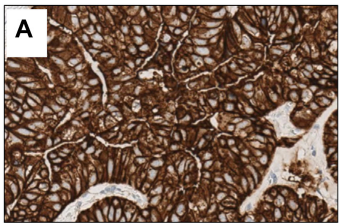 图2 Claudin18.2阳性腺癌中的细胞质广泛染色使膜染色的评估变得困难
图2 Claudin18.2阳性腺癌中的细胞质广泛染色使膜染色的评估变得困难
与CerbB-2的染色一样,印戒细胞由于细胞质边缘的非特异性染色可能会导致误判[9]。细胞质颗粒状阳性和清晰的线性膜染色不易辨别,当存在模糊染色时,应谨慎判读。当存在明显的与细胞质染色相关的伪影时,该样本应被定义为“不适合Claudin18.2评估”以避免假阴性或假阳性的结果。如果肿瘤的一部分可评估,而另一部分有明显的伪影,则应仅在适合评估的部分进行评分(图3)。
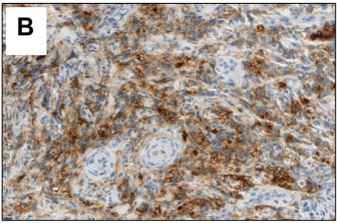 图3 以颗粒状细胞质免疫染色为特征的胃癌
图3 以颗粒状细胞质免疫染色为特征的胃癌
不典型增生:胃食管不典型增生病变(低级别和高级别)的Claudin18.2表达与侵袭性腺癌相似,不应在评估Claudin18.2表达时考虑[3](图4和图5)。
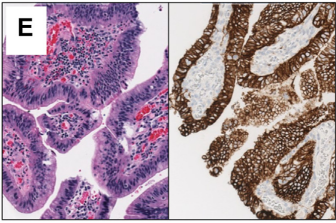
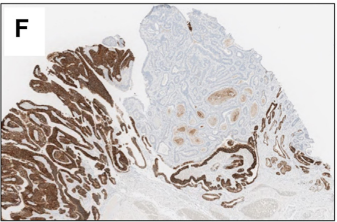
图5 呈现异质性染色模式的低级别和高级别不典型增生
异常阳性:极少数病例中的炎性细胞或其他非类型肿瘤细胞会出现异常的细胞质染色,评分时不应计入,多数是由于检测前的因素导致,应在其他可及样本中重复检测。在黏液腺癌或坏死细胞中可观察到黏蛋白的中度到强的异常染色,评估时应谨慎仔细(图6)。
检测前伪影:检测前阶段是生物标志物分析常见且重要的误差来源。经电灼的组织(特别是黏膜/黏膜下切片)表现为撕裂和凝固。在这些样品中,抗原保存可能受损,有热伪影的区域应排除在Claudin18.2评估之外。固定不足也可能不利于抗原维持,并可能导致边缘效应和非特异性细胞质染色的假阴性染色(图7)。
7. Claudin18.2病理报告建议
病理报告和生物标志物判读的标准化是精准抗肿瘤治疗至关重要的一环。病理报告应清晰、简洁地呈现检测结果,以指导临床专家为患者选择最佳的治疗方案。理想的Claudin18.2表达报告应包含以下信息:
用于分析的样本类型(活检/手术)和样本部位(原发灶/转移灶需表明具体的转移部位)
组织固定时间
样本充分性,如不充分,需说明不充分的原因(如缺乏肿瘤细胞,电灼/固定伪影,<6个检测样本等)
检测所用的Claudin18.2一抗的克隆号、免疫组化染色试剂和检测设备
中度和强(2+和3+)的膜染色肿瘤细胞的百分比
检测结果阴性或阳性,可以参考中度和强的膜染色肿瘤细胞≥75%为标准判读
其他分析和临床注释内容(如实验室资质或参考书目等),如需要
结语
本篇综述的前半部分为基础篇,系统地阐述了Claudin18.2的生物学特性、成药机制及免疫组化检测要点。后半部分从实践的角度,深入探讨Claudin18.2免疫组化评估的实用方法和经验。准确地进行生物标志物的评估是精准医学的基础,病理专家在治疗策略选择方面发挥至关重要的作用。希望通过本篇综述的解读,为Claudin18.2检测的普及化和规范化助力。
1. Fassan M, Kuwata T, Matkowskyj KA, et al. Claudin-18.2 Immunohistochemical Evaluation in Gastric and Gastroesophageal Junction Adenocarcinomas to Direct Targeted Therapy: A Practical Approach. Mod Pathol. 2024 Nov;37(11):100589.
2. Compton CC, Robb JA, Anderson MW, et al. Preanalytics and Precision Pathology: Pathology Practices to Ensure Molecular Integrity of Cancer Patient Biospecimens for Precision Medicine. Arch Pathol Lab Med. 2019 Nov;143(11):1346-1363.
3. Wong, Mary T., et al. Claudin-18: Patterns of Expression in the Upper Gastrointestinal Tract and Utility as a Marker of Gastric Origin in Neuroendocrine Tumors. Archives of Pathology & Laboratory Medicine, vol. 147, no. 5, May 2023, pp. 559+.
4. Coati I, Lotz G, Fanelli GN, et al. Claudin-18 expression in oesophagogastric adenocarcinomas: a tissue microarray study of 523 molecularly profiled cases. Br J Cancer. 2019 Jul;121(3):257-263.
5. Dai J, Zheng H, Jin J, et al. Claudin18.2 expression and clinicopathological features in cytology effusion specimens from gastric adenocarcinoma: A comparative study with tissue specimens. Cancer Cytopathol. 2023 Jun;131(6):365-372.
6. Angerilli V, Fassan M, Parente P, et al. A practical approach for PD-L1 evaluation in gastroesophageal cancer. Pathologica. 2023 Apr;115(2):57-70.
7. Rohde C, Yamaguchi R, Mukhina S, et al. Comparison of Claudin 18.2 expression in primary tumors and lymph node metastases in Japanese patients with gastric adenocarcinoma. Jpn J Clin Oncol. 2019 Sep 1;49(9):870-876.
8. Kohei Shitara et al. Global prevalence of CLDN18.2 in patients with locally advanced (LA) unresectable or metastatic gastric or gastroesophageal junction (mG/GEJ) adenocarcinoma: Biomarker analysis of two zolbetuximab phase 3 studies (SPOTLIGHT and GLOW).. JCO 41, 4035-4035(2023).
9. Woo CG, Ho WJ, Park YS, et al. A potential pitfall in evaluating HER2 immunohistochemistry for gastric signet ring cell carcinomas. Pathology. 2017 Jan;49(1):38-43.
仅供医疗卫生等专业人士参考
审批编号:MAT-CN-VYL-2025-00041
审批时间:2025-3-24
材料有效期:2026-3-24
排版编辑:肿瘤资讯-jj
往期回顾
FM18.2系列:
FM18.2丨侯英勇教授:从隐匿到闪耀,Claudin18.2的奇妙探索之旅
FM18.2丨于国华教授:胃/胃食管结合部腺癌中Claudin18.2免疫组化评估之理论篇
FM18.2丨周炜洵教授:从国内外指南的更迭,看胃癌Claudin18.2检测的当下和未来
Around18.2系列:
Around18.2 | 大咖论道:病理专家视角下的胃癌精准诊疗新格局
Around18.2 | 大咖论道:新标志物出现时病理科如何化挑战为机遇
Around18.2丨大咖论道:胃癌生物标志物检测的全景解析与未来展望
Around18.2丨大咖论道:加强临床病理交流合作,推动Claudin18.2检测规范化











 苏公网安备32059002004080号
苏公网安备32059002004080号


