急性白血病具有高度异质性,总体预后欠佳。目前,化疗和造血干细胞移植是其主要治疗手段。盐酸米托蒽醌脂质体注射液是一种新型蒽醌类药物脂质体制剂,于2022年1月获得中国国家药品监督管理局上市批准,适用于既往至少接受过一线标准治疗的复发或难治外周T细胞淋巴瘤成年患者。已有多项临床研究显示含盐酸米托蒽醌脂质体方案治疗急性白血病具有一定的效果,但由于上市时间尚短,目前临床应用经验较少。为进一步规范盐酸米托蒽醌脂质体在急性白血病患者中的临床应用,专家组成员结合盐酸米托蒽醌脂质体应用现状及相关循证医学证据,制定了盐酸米托蒽醌脂质体注射液治疗急性白血病临床应用指导原则,旨在为我国临床医师用药提供参考。
ALL多发于儿童,发病高峰在3~7岁,在过去30年中,儿童ALL的5年OS率已从50%提高到80%以上,预后得到明显改善;成年ALL患者长期生存率仅为30%~50%,总体复发率高,预后较差 。费城染色体(Ph)阴性ALL的治疗仍以多药联合的化疗方案为主,Ph阳性ALL的治疗原则是在化疗基础上联合酪氨酸激酶抑制剂(TKI)。复发难治ALL的治疗目前尚无统一意见,指南推荐可以选择挽救化疗、免疫靶向治疗或临床试验,挽救治疗获完全缓解(CR)后考虑allo-HSCT 。
米托蒽醌是一种蒽醌类抗肿瘤药物,常用于AL的临床治疗。盐酸米托蒽醌脂质体是传统米托蒽醌剂型的改良和升级,于2022年1月获得中国国家药品监督管理局(NMPA)上市批准,适用于既往至少接受过一线标准治疗的复发或难治外周T细胞淋巴瘤(PTCL)成年患者。基于米托蒽醌的作用机制及其在AL中的应用前景,盐酸米托蒽醌脂质体自上市以来,也在AL中得到一定的应用,并显示出较好的疗效。为进一步提高临床应用盐酸米托蒽醌脂质体注射液治疗AL的规范性和合理性,专家组成员结合盐酸米托蒽醌脂质体的应用现状及相关临床研究数据,制定了本指导原则,供广大临床医师参考。
1 米托蒽醌概述
米托蒽醌作为一种传统蒽醌类抗肿瘤药,通过干扰DNA、RNA以及抑制拓扑异构酶Ⅱ发挥抗肿瘤作用,属于细胞周期非特异性药物,既往在AL中应用较多且相关诊疗指南有推荐。在2024年版中国临床肿瘤学会(CSCO)恶性血液病诊疗指南中,AML诱导、巩固和复发难治治疗均有含米托蒽醌方案推荐,ALL诱导治疗阶段以VDP(长春碱类、蒽环类药物联合糖皮质激素)为基础的方案中米托蒽醌为可选择的蒽环/蒽醌类药物之一 ;2024年第1版美国国家综合癌症网络(NCCN)肿瘤临床实践指南中,复发难治ALL治疗也有含米托蒽醌方案推荐 。
米托蒽醌在AL治疗领域有多篇研究报道。一项关于米托蒽醌联合阿糖胞苷对比柔红霉素联合阿糖胞苷治疗初治AML的荟萃分析结果显示,米托蒽醌可显著改善所有年龄段患者的CR和无病生存(DFS);关于CLAG(克拉屈滨+阿糖胞苷+粒细胞集落刺激因子)联合米托蒽醌、MAE(米托蒽醌+阿糖胞苷+依托泊苷)等含米托蒽醌方案治疗复发难治AML的研究显示,CR率可达50%以上;FLAM(氟达拉滨+阿糖胞苷+米托蒽醌)、MEC(米托蒽醌+依托泊苷+异环磷酰胺)、MAE等含米托蒽醌方案在复发难治ALL中也显示出一定的疗效 。
相关研究显示,米托蒽醌和其他蒽环类药物没有完全交叉耐药性,对于既往一线使用蒽环类药物治疗后复发的患者仍然有效。但由于严重的骨髓抑制和心脏不良反应,使米托蒽醌在临床应用中受到了限制。
2 盐酸米托蒽醌脂质体概述
2.1 作用机制
盐酸米托蒽醌脂质体是普通米托蒽醌剂型的改良和升级,其活性成分为米托蒽醌,脂质体包裹并没有改变米托蒽醌固有的作用机制。经脂质体包裹后,改变了米托蒽醌在体内的药代动力学特征和组织分布。该脂质体具有的60 nm粒径使其不易透过正常血管间隙,能够被动靶向肿瘤部位;表面经甲氧基聚乙二醇修饰,使其免受网状内皮系统识别,延长了血液循环时间;其在血液中包封稳定,游离药物占总药量比例恒定在1%左右,使药物在到达肿瘤组织前保持脂质体完整性,不产生药理、毒理活性。较小的体积及较长的血液循环时间保证了盐酸米托蒽醌脂质体给药后能够有效地在肿瘤组织中聚集,在肿瘤微环境和DNA快速扩增下触发药物释放,进而发挥抗肿瘤活性。
2.2 药代动力学
盐酸米托蒽醌脂质体治疗复发难治淋巴瘤单次给药后的药代动力学研究结果显示,在12~20 mg/m 2剂量范围内,血浆总米托蒽醌的消除半衰期(t 1/2)范围为67.69~84.00h。此外,在12、16、20 mg/m 2剂量下,游离米托蒽醌与总米托蒽醌的0时至无限时间点的血药浓度曲线下面积(AUC 0~∞)比值为1%左右。给药后0~672 h,游离米托蒽醌与总米托蒽醌浓度比值为0.50%~2.00%。目前尚未评估米托蒽醌脂质体在人体内的代谢和排泄情况。非脂质体剂型米托蒽醌研究数据显示,米托蒽醌以原形或无活性代谢产物的形式经尿液和粪便排泄,在给药后5 d内分别有11%和25%的剂量在尿液和粪便中被回收。在尿液回收的物质中,65%为原形药物,其余35%包括单羧酸和二羧酸衍生物及其葡萄糖醛酸结合物。
盐酸米托蒽醌脂质体联合阿糖胞苷治疗儿童初治AML单次给药后,其药代动力学特征相比单药没有改变。30 mg/m 2盐酸米托蒽醌脂质体给药后,游离米托蒽醌与总米托蒽醌的0时至下次给药前最后可测量时间点的血药浓度曲线下面积(AUC 0~t)比值为(1.83±0.55)%,总米托蒽醌的平均t 1/2为(60.20±9.35)h。由此可见,盐酸米托蒽醌脂质体具有良好的药代动力学特征,且与阿糖胞苷联用后药代动力学特征不受影响。
3 盐酸米托蒽醌脂质体在AL中的临床应用
3.1 临床研究
盐酸米托蒽醌脂质体自上市以来,在AML和ALL中已有一些临床研究结果。初步数据显示盐酸米托蒽醌脂质体联合方案在AL中有一定疗效,且不良反应可控。
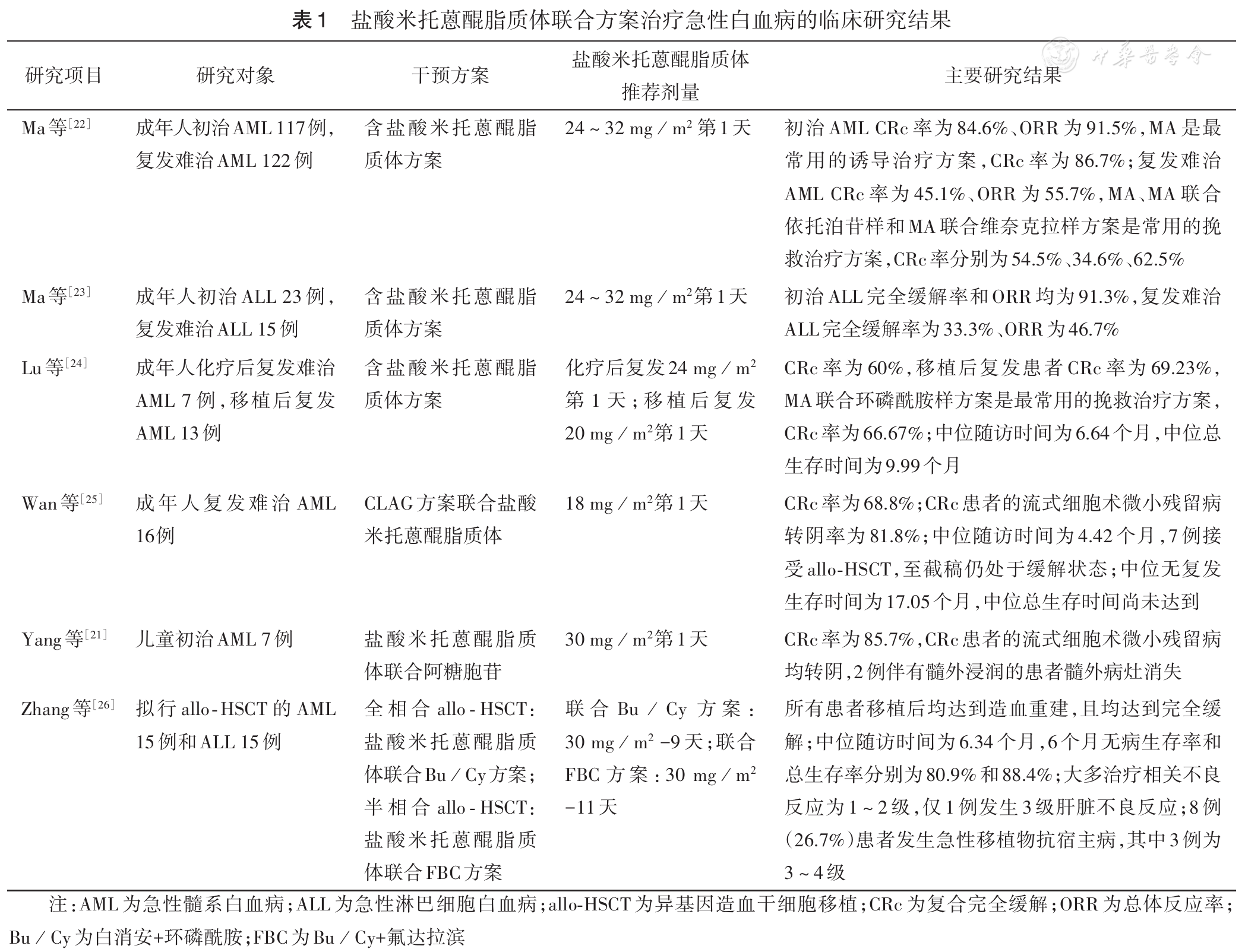
盐酸米托蒽醌脂质体在AL中的临床研究结果见表1 。一项真实世界研究纳入239例AML患者和38例ALL患者,经含盐酸米托蒽醌脂质体方案治疗后,初治和复发难治AML的复合完全缓解(CRc)率分别为84.6%和45.1%,初治和复发难治ALL的CR率分别为91.3%和33.3%。Lu等开展的盐酸米托蒽醌脂质体联合方案用于化疗后复发难治或移植后复发AML的Ⅱ期研究结果显示,总体及移植后复发患者的CRc率分别为60%和69.23%,中位OS时间为9.99个月。Wan等回顾了16例接受盐酸米托蒽醌脂质体联合CLAG方案治疗的复发难治AML患者,CRc率为68.8%,中位无复发生存(RFS)时间为17.05个月。Yang等的研究结果显示,初治AML儿童患者接受MA(盐酸米托蒽醌脂质体+阿糖胞苷)方案治疗的CRc率可达85.7%,且缓解患者流式细胞术检测微小残留病(MRD)均转阴。Zhang等回顾了30例拟行allo-HSCT的成年AL患者,采用盐酸米托蒽醌脂质体联合白消安(Bu)/环磷酰胺(Cy)样方案行移植预处理,结果显示所有患者移植后均达到造血重建且不良反应可控。
此外,初治和复发难治AML领域有多项关于盐酸米托蒽醌脂质体的临床研究正在开展(表2 )。在初治AML中,MA方案±维奈克拉或高三尖杉酯碱治疗年轻AML患者、MA方案联合依托泊苷治疗年轻AML患者、改良盐酸米托蒽醌脂质体+阿糖胞苷+维奈克拉(MAV)方案治疗老年AML患者、MA方案治疗继发AML患者、MA方案治疗儿童初治AML患者等临床研究均正在进行中;在复发难治AML中,CLAG方案联合盐酸米托蒽醌脂质体、MAV方案、VAM(维奈克拉+阿扎胞苷+盐酸米托蒽醌脂质体)方案治疗复发难治AML等临床研究正在进行中。

3.2 指南推荐
2024年版CSCO恶性血液病诊疗指南中将盐酸米托蒽醌脂质体联合方案纳入复发难治AML推荐治疗方案 。对于适合强化疗且早期(<12个月)复发的患者,盐酸米托蒽醌脂质体+阿糖胞苷+依托泊苷为一种可选择方案,后续可行allo-HSCT;对于适合强化疗且晚期(>12个月)复发的患者,盐酸米托蒽醌脂质体+阿糖胞苷或盐酸米托蒽醌脂质体+阿糖胞苷+依托泊苷也可作为推荐方案(Ⅲ级推荐),后续可行allo-HSCT;盐酸米托蒽醌脂质体的推荐剂量为24~32 mg/m 2第1天。
4 盐酸米托蒽醌脂质体在AL中的用药建议
盐酸米托蒽醌脂质体在AML和ALL治疗中的用药建议见表3 。

对于髓系肉瘤或髓外浸润AML,一篇多发脏器侵犯的孤立性髓系肉瘤病例报道显示,使用MA方案治疗后,眼眶平扫+增强磁共振成像(MRI)检查显示病灶较前整体缩小,提示治疗有效,且不良反应轻微;同时,在一项儿童AML的临床研究中,2例伴髓外浸润AML患儿接受MA方案治疗后髓外病灶消失。推荐在此类患者中尝试应用盐酸米托蒽醌脂质体方案。
对于初治AML和ALL,关于盐酸米托蒽醌脂质体治疗的真实世界研究纳入117例初治AML和23例初治ALL患者,显示出一定的治疗效果;对于拟行allo-HSCT且需要接受强化预处理方案治疗的AML或ALL患者,可在专科医生指导下尝试使用盐酸米托蒽醌脂质体联合Bu/Cy样方案。
以上推荐方案和用药剂量均可由临床医生结合患者临床特点进行适当的个体化调整,或建议患者参加临床试验。
5 盐酸米托蒽醌脂质体安全性与不良反应管理
盐酸米托蒽醌脂质体的安全性数据来自目前已开展的13项临床试验,共有307例患者接受至少1次盐酸米托蒽醌脂质体治疗,其中223例(72.6%)接受的剂量>20 mg/m 2。162例(52.8%)患者发生过至少1次≥3级不良反应,常见的≥3级不良反应包括中性粒细胞计数降低(38.8%)、白细胞计数降低(38.8%)、血小板计数降低(11.4%)、贫血(8.1%)、肺炎(6.2%),其他非血液学不良反应均为1~2级。关于心脏安全性,在一项盐酸米托蒽醌脂质体与米托蒽醌对比的Ⅱ期研究中,60例患者按1∶1分配至接受盐酸米托蒽醌脂质体20 mg/m 2治疗组和米托蒽醌14 mg/m 2治疗组,结果显示,盐酸米托蒽醌脂质体组心肌损伤标志物肌钙蛋白T升高的发生率低于米托蒽醌组(3.3%比36.7%),整体心脏安全性良好。盐酸米托蒽醌脂质体在AML和ALL中的已发表研究数据及临床实践显示,其不良反应仍以血液学不良反应为主。
盐酸米托蒽醌脂质体需要特别关注的不良反应处理方法如下。
(1)血细胞减少症:治疗期间应密切监测中性粒细胞、血小板、血红蛋白水平。发生治疗相关的血细胞减少时,应根据临床实践指南,通过应用造血细胞生长因子或输血进行对症治疗,必要时后续治疗周期应降低给药剂量。
(2)色素沉着障碍:临床表现主要为皮肤蓝染,多发生在颜面部及四肢远端的皮肤,巩膜未见蓝染发生;多出现在第3次用药后,程度均较轻,无需处理,可自行恢复,平均恢复时间为3~4个月。色素沉着障碍不会增加溃烂、感染等其他皮肤不良反应,未造成停药、死亡等严重不良后果。
(3)心脏不良反应:对于射血分数值40%~50%或较基线值降低10%~19%或心力衰竭2级的患者,仅当治疗的潜在获益超过风险时,才能继续用药进行治疗;射血分数值<40%或较基线值降低>20%或心力衰竭≥3级时需停止用药,给予积极心功能维护治疗;一旦患者出现心力衰竭的症状,建议参考相应的指南进行心功能维护治疗;用药过程中若检出心肌酶升高,建议予以依那普利治疗1年,结束用药后1年内至少每3个月复查1次超声心动图。
(4)感染:对于用药前有严重感染的患者,需在感染得到有效控制后才能开始使用盐酸米托蒽醌脂质体治疗;在治疗期间应监测和评估患者是否出现发热或其他感染相关症状和体征,并给予相应治疗。
(5)肝损害:由于肝功能不全会减少米托蒽醌的代谢,建议肝功能不全患者在用药时密切监测肝功能,用药最初2个月内至少每2周监测1次;一旦出现肝损害,应积极予以保肝治疗,每周监测1次肝功能,直至恢复至基线水平,并在后续治疗中进行剂量调整。
(6)输液相关反应:多发生在用药后5~30 min,常发生于首次用药期间,偶有患者在后续用药周期中出现。通常表现为潮红、呼吸急促、面部肿胀、头痛、寒战、胸痛、背痛、胸部和咽喉发紧、发热、心动过速、瘙痒、皮疹、发绀、晕厥、支气管痉挛、哮喘、呼吸暂停和低血压。
用药期间应密切监测患者临床症状及生命体征(包括心率、血压、血氧饱和度等),一旦出现输液相关反应,应积极予以处理。2~3级输液相关反应处理原则包括降低输注速率或暂停输注;给予对症支持治疗,可选择不同的物理、药物处理方式,如低热时采用擦浴等方式物理降温,高热时给予解热镇痛药;给予糖皮质激素或抗组胺药物减轻过敏反应等;若经过上述处理,患者仍无法耐受,须停止用药。如发生4级输液相关反应,须立即停止用药,积极抢救治疗。
此外,对于其他可能发生的不良反应,建议参考相应临床实践指南进行处理。
剂量调整:在使用盐酸米托蒽醌脂质体过程中应密切监测不良反应,并根据不良反应情况进行用药调整,包括延迟用药、降低剂量或永久停药。采用盐酸米托蒽醌脂质体联合化疗方案治疗时,要注意不良反应的叠加作用。如需调整盐酸米托蒽醌脂质体剂量,可参考盐酸米托蒽醌脂质体单药的剂量调整原则进行;如需调整其他化疗药物剂量,则依据医疗实践常规进行。如出现非血液学不良反应,需综合具体情况对各药物与不良反应的相关性进行判断,从而调整药物剂量。
6 总结
盐酸米托蒽醌脂质体作为新型的蒽醌类脂质体药物,在AML和ALL中显示出一定的治疗效果,且不良反应可控,为AL临床治疗提供了新的选择。随着盐酸米托蒽醌脂质体在我国上市后临床医生用药经验不断丰富以及更多研究成果的呈现,将为盐酸米托蒽醌脂质体的临床应用提供更多的有益参考。本指导原则为盐酸米托蒽醌脂质体注射液临床合理用药提供指导意见,实际应用中可结合患者临床特点制订适合不同患者的个体化治疗方案。
中国临床肿瘤学会(CSCO)白血病专家委员会. 盐酸米托蒽醌脂质体注射液治疗急性白血病临床应用指导原则(2024年版)[J]. 白血病·淋巴瘤,2024,33(12):705-711. DOI:10.3760/cma.j.cn115356-20240805-00122











 苏公网安备32059002004080号
苏公网安备32059002004080号


