医路曼话,百家畅谈。2024年9月03日17:00良医汇【肿瘤资讯】携手大连医科大学附属第二医院乳腺肿瘤科李曼教授开展的系列乳腺癌线上培训课程——“半月曼谈”第五十七期如约举行。

本期9月03日17:00的精品云课堂名家齐聚,特邀中国医科大学附属第一医院MDT团队肿瘤内科滕月娥教授、乳腺外科于鑫淼教授与胸外科李文雅教授参与,同大连医科大学附属第二医院乳腺肿瘤科李曼教授率领的MDT团队,包括乳腺肿瘤科徐岭植教授与影像科孙传恕教授,针对人表皮生长因子受体2(HER2)阳性晚期乳腺癌病例展开讨论。


课程伊始,乳腺肿瘤科李曼教授首先进行了讲话,阐述了自“半月曼谈”开播两年以来,主要针对乳腺癌疑难病例进行了深入的探讨。我们发现乳腺癌这一疾病出现了多发转移后的治疗涉及多个科室,包括乳腺内科、乳腺外科、病理科、影像科、放射科以及核医学科等。我们关注乳腺癌疑难病例,通过多学科团队(MDT)的合作,共同探讨并提出宝贵的意见,以节省患者时间。本期我们非常荣幸地邀请到中国医科大学附属第一医院滕月娥教授及其MDT团队。中国医科大学附属第一医院在乳腺肿瘤MDT开展方面处于全国领先水平,也推动了辽宁地区MDT的发展。

畅叙医情——病例分享
在“畅叙医情”环节,大连医科大学附属第二医院乳腺肿瘤科徐岭植教授分享了一例HER2阳性晚期乳腺癌病例。多学科专家们围绕该例患者的后续治疗方案进行了探讨。

病例资料
基本情况
患者,女,68岁,绝经后女性,既往史及家族史无特殊。
现病史:
2016.7因“发现左乳肿物3月余”为主诉首次就诊。3月余前无意间触及左乳肿物1枚,时约鸡蛋黄大小,无特殊不适未在意,后肿物渐进性增大,遂就诊。
查体:左乳外下象限4点钟方向触及肿物1枚,范围约6cm*5cm,质硬,活动度差,边界不清晰,形态不规则,无触痛,局部皮肤无异常,同侧乳头挤压无溢液,左侧腋窝触及多枚质韧淋巴结,大者长径约1cm,无触痛,未融合。余查体未见异常。
乳腺超声:双乳扫查:右乳腺腺体层不厚,回声均匀,未见占位性病变,未见异常血流信号。左乳3-4点钟位腺体层内见一低回声光团,大小6.1*2.9*4.5cm,边界不清,形态不规则,周边见毛刺征,内回声不均匀,内未见钙化斑,周边及内部见丰富血流信号,并可探及动脉频谱,呈高阻型,峰值速度11.6cm/s;RI 0.83(BI-RADS 4C级)。ABVS:肿物周边未见“汇聚征”象。右侧腋下扫查未见肿大淋巴结。左侧腋下见多个低回声,最大1.2*0.6cm,边界清,形态规则,淋巴门偏心,未见血流信号。
超声引导下穿刺活检:左乳肿物(穿刺活检):倾向腺癌。
免疫组化:肿瘤细胞 ER(<1%弱阳性),PR(-),Her2(3+),Ki-67指数20%。左腋下淋巴结(穿刺活检):反应性增生。
骨ECT和肋骨CT重建:核素骨扫描(骨ECT)提示左后第8肋存在非常明显的的核素浓聚。进一步完善该部位的CT重建,可以看到该处肋骨存在骨质密度不均匀,考虑是恶性肿瘤骨质受累的情况。

图1. 骨ECT和肋骨CT重建
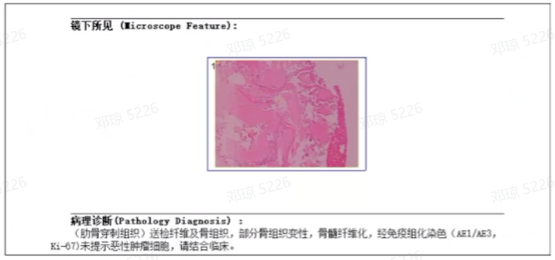
CT引导下穿刺活检:左后第8肋(穿刺活检):(肋骨穿刺组织)送检纤维及骨组织,部分骨组织变性,骨髓纤维化,免疫组化染色(AE1/AE3,Ki-67)未提示恶性肿瘤细胞。
病史特点及治疗方案:
诊断:左乳腺浸润性癌cT3N0Mx左后第8肋骨转移?HR阴性HER2阳性。
治疗方案:结合外院会诊意见,自2016.8行EC-TH方案治疗,具体用药:表柔比星联合环磷酰胺共4周期,序贯多西他赛联合曲妥珠单抗4周期,期间疗效评价:部分缓解(PR)。
手术:2017.3行左乳腺癌改良根治手术。
术后病理:(左乳房)非特殊型浸润性乳腺癌(2级),大小3*2*2.5cm,可见脉管内癌栓,未见神经侵犯(MP分级不详);左腋窝淋巴结无癌转移(0/19)。手术标本免疫组化未做。
术后:放疗未行,结合外院会诊意见,自2017.3继续曲妥珠单抗靶向治疗(至2019.6停用,时长约3年),联合口服卡培他滨(d1-d14,q21d)(持续用药至今),并联合双膦酸盐治疗。
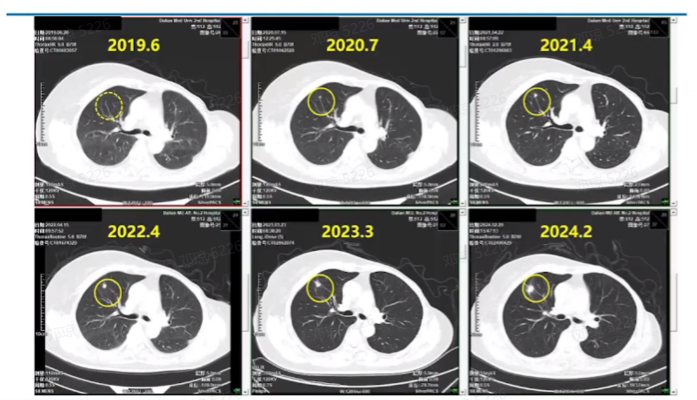
2020.7胸部CT:检查发现右肺上叶单发结节(此时距离停用曲妥珠单抗约1年),予定期监测,渐进性增大,恶性可能性不除外。
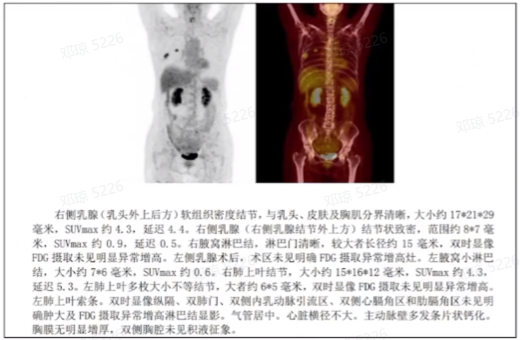
2024.8 全身PET-CT:右侧乳腺(乳头外上后方)软组织密度结节,与乳头、皮肤及胸肌分界清晰,大小约17*21*29mm,SUV max约4.3,延迟4.4。右侧乳腺(右侧乳腺结节外上方)结节状致密,范围约8*7mm,SUV max约0.9,延迟0.5。右腋窝淋巴结,淋巴门清晰,较大者长径约15mm,双时显像FDG摄取未见明显异常增高。左侧乳腺术后,术区未见明确FDG摄取异常增高灶。左腋窝小淋巴结,大小约7*6mm,SUV max约0.6。右肺上叶结节,大小约15*16*12mm,SUV max约4.3,延迟5.3。左肺上叶多枚大小不等结节,大者约6*5mm,双时显像FDG摄取未见明显异常增高,左肺上叶索条。双时显像纵隔、双肺门、双侧内乳动脉引流区、双侧心膈角区和肋膈角区未见明确肿大及FDG摄取异常增高淋巴结显影。气管居中。心脏横径不大。主动脉壁多发条片状钙化。胸膜无明显增厚,双侧胸腔未见积液征象。
骶椎MRI:骨质未见异常。
超声引导下右乳肿物穿刺活检:右乳腺原位癌。(右乳)穿刺组织:导管上皮非典型增生,结合免疫组化考虑中等核级导管原位癌,穿刺组织有限,是否伴有浸润请结合临床。
免疫组化结果:Calponin(肌上皮+),ER(90%强+),CK5/6(-)。
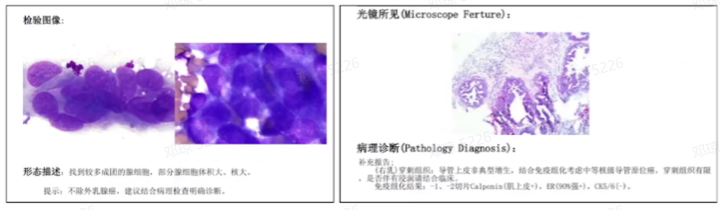
CT引导下右肺上叶肿物穿刺活检:(肺穿刺)癌,结合病史,符合乳腺癌来源。
免疫组化结果:TTF-1(-),NapsinA(-),CK7(+),P40(-),GATA3(部分+),ER(-),PR(-),HER2(3+),Ki-67(+,约20%)。
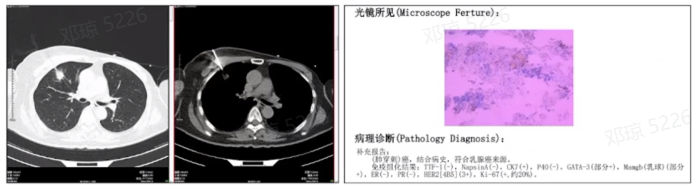
疾病诊断:1、左乳腺浸润性癌术后 肺转移 骨转移?,HR阴性HER2阳性 2、右乳腺原位癌。
集思广医—多学科专家各抒己见
在讨论环节中,中国医科大学附属第一医院MDT团队滕月娥教授、于鑫淼教授、李文雅教授分别以多学科视角针对该病例的诊疗策略分享了看法,大连医科大学附属第二医院MDT团队李曼教授、徐岭植教授、孙传恕教授也基于临床经验分享了诊疗建议。
问题讨论:
1、骨病灶穿刺结果解读
孙传恕教授:在乳腺癌治疗中,肋骨转移是常见的现象,通常表现为多发性骨破坏,以溶骨性破坏为主,也可能伴有混合性或成骨性改变。影像科医生在评估时需非常谨慎,因为这些变化可能仅表现为局部骨密度的降低或混合性密度。在临床实践中,我们发现有些患者可能并非转移,而是其他原发性病变,如骨髓异常增生症或良性骨病。此外,乳腺癌患者放疗后可能导致骨损伤,早期表现为骨密度降低,随后可能出现坏死和骨密度增高,最终可能导致骨折。

2、后续治疗方案?
于鑫淼教授:影像学分析对于判断乳腺癌患者的骨转移至关重要,尤其是在M1与M0的诊断不明确时,这将直接影响治疗策略。如果患者处于根治状态,通常只需完成1年的曲妥珠单抗靶向治疗。由于患者ER、PR阴性,无内分泌治疗指征,单一靶向治疗可能已足够。然而,若存在骨转移风险,可能需延长靶向治疗。决策时需考虑患者的不良反应、耐受性、基础疾病、经济条件及药物可行性,以确定最适宜的维持治疗方案。这是基于患者整体状况的综合考量,旨在实现最佳治疗效果。

滕月娥教授:这个病例的关键在于分期和是否存在肋骨转移。尽管进行了穿刺检查,但由于肋骨的特性,阳性率不高。目前病理结果未显示阳性,转移阴性的可能性较大,但不能排除转移。在这种情况下,我们可以考虑按照早期处理方案进行治疗,如术前化疗EC-TH,到单药靶向治疗是一个标准治疗方案。术后,需密切观察肋骨变化,通过定期复查来确定是否有成骨性或溶骨性病变,以帮助确定转移可能性。
如果不能完全排除转移的可能,患者可能需要长期单药靶向治疗,或考虑联合卡培他滨治疗。由于患者的ER和PR为阴性,内分泌治疗不适用,药物选择有限。在这种情况下,单药靶向治疗可能是一个合理的选择。这是一个需要综合考虑病理、影像学和临床症状的复杂病例,治疗决策应基于对患者整体状况的评估。

3、(1)局部方案:右乳腺原位癌干预时机?右肺中叶寡病灶干预时机及方式?(2)全身治疗方案?
李文雅教授:肺结节已明确诊断为左乳癌转移到右肺上叶前段的转移癌。结节从小尺寸逐渐增长至1.6cm,确认为转移性。是否进行手术需从全身状况考虑,需要评估是否为寡转移,并考虑患者的生存期。全身PET-CT显示仅右肺有转移,符合寡转移特征,且经过4年观察,肿瘤生长相对惰性。有案例表明乳腺癌寡转移患者可能有较好的疗效,5年生存率可达50%-60%。
关于骨病灶的改变,可能是转移或骨纤维异常增殖症。对比PET-CT检查结果,如果骨形态有明显成骨或溶骨改变,可能是治疗后转移的表现。如果形态无太大改变,则可能是良性病变。对于这个病例,我个人更倾向于进行局部干预手术,如手术切除或立体定向放疗(SBRT)等,作为科学治疗方案之一。

孙传恕教授:在乳腺癌治疗中,影像学评估对于病灶的诊断至关重要。对于胸部影像,我们团队在MDT讨论中对原发肿瘤与转移的鉴别有过深入讨论。穿刺活检证实了转移性病变,但影像学上与原发性肺癌的区分可能具有挑战性。局部治疗的选择包括手术、SBRT和消融术,如冷消融和热消融。这些方法的适应症需要仔细评估。对于寡转移的情况,通常需要内科治疗稳定6个月以上,才考虑局部治疗。因此,建议在完成内科治疗后重新评估,如果病情稳定,可以考虑进行消融、手术或SBRT等局部治疗。
于鑫淼教授:新发病灶在乳腺癌治疗中的意义重大,它可能标志着疾病进展,尤其是在晚期治疗中,代表全身治疗控制不足,需要根据新病灶的分子分型变化调整治疗方案。本病例中,新发病灶为原位癌,可能代表一个相对独立的事件,而非直接提示乳腺癌进展。结合肺部明确的转移情况,新发病灶佐证了全身治疗的不足。对于治疗策略,不建议仅因原位癌而急于手术。如果分子分型仍是HER2阳性,可能需要内科治疗。在疾病控制良好且患者耐受性良好的情况下,才考虑手术切除新发病灶。对于肺部转移灶的切除,建议在综合治疗有效且病情稳定一段时间后才考虑局部治疗干预。
徐岭植教授:对于这位患者,我们的首要任务是控制全身病情,尤其是考虑到肺部转移与患者初诊时左乳的分子分型一致。全身治疗应优先考虑,鉴于患者病情进展相对惰性和缓慢,且对曲妥珠单抗治疗敏感,建议采用以曲妥珠单抗为基础的靶向治疗联合策略。如果药物可及且经济条件允许,联合曲帕双靶治疗是一个更优选择。
在化疗药物选择上,由于患者术前治疗期间使用过紫杉类药物并显示出疗效,且停药时间已接近6-8年。若患者耐受性好,可以考虑再次使用紫杉类药物联合曲帕双靶的方案。在全身病情控制有效后,可考虑对局部转移病灶进行手术或消融治疗。同时,对右侧乳腺病变也应适时处理。

滕月娥教授:对于乳腺癌寡转移患者,预后通常相对较好。在全身治疗有效的前提下,对寡转移进行局部干预,可以延长患者的无病生存期,甚至带来生存获益。对于右乳腺新发的病灶,活检为中级别导管原位癌,应仔细评估是否为双原发癌或新发乳腺癌。建议进行乳腺钼靶或磁共振成像检查,以确定是否存在弥漫性钙化或其他异常组织。
对于肺部病变,经过术后多年观察,若肺部病变为孤立性转移,可以考虑局部干预,但仍应在全身治疗有效的基础上进行。如果曲妥珠单抗作为一线治疗,那么在停药一年后,可以考虑联合其他HER2靶向药物如帕妥珠单抗或吡咯替尼。在选择治疗方案时,还需要考虑患者的年龄和体能状态。对于年龄较大的患者,可能需要选择耐受性更好的化疗方案,如长春瑞滨联合双靶的方案。
总结
本次云课堂以一例HER2阳性晚期乳腺癌患者的治疗进行了深入讨论。患者经过新辅助治疗后,虽然达到了部分缓解,但后续出现了肺和乳腺的转移。专家们从多学科角度出发,讨论了在不确定骨转移的情况下,如何平衡全身治疗与局部治疗的策略。专家们一致认为,在全身治疗有效的基础上,应考虑对局部转移病灶进行干预,以提高患者的生存质量和生存期。此次讨论不仅为该患者提供了治疗方向,也为类似病例的临床决策提供了宝贵的参考。感谢MDT团队的专家提供指导,并对参与云课堂的大家表示感谢。相信本次课程也让大家对该类乳腺癌的规范化诊治有了更深入的了解。“半月曼谈”更多精品课程将继续呈现,精彩不断,欢迎持续关注!
排版编辑:肿瘤资讯-G











 苏公网安备32059002004080号
苏公网安备32059002004080号


